导读
该试剂盒至多30分钟就可得到检测结果,目前仅被批准凭处方购买,普通人无法自己购买,且FDA提示,该试剂盒检测出的阴性结果并不能排除感染风险,有症状患者还需与医护人员进一步确认。该试剂盒明年春季初才会大规模进入全美市场
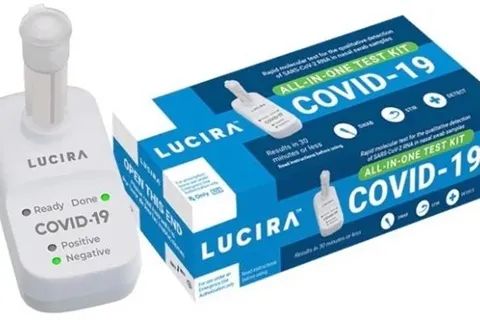
该试剂盒由加州制造商LuciraHealth生产,LuciraHealth官网显示,该试剂盒包含拭子、样品瓶、便携式检测装置等一体化套件。图片来源于网络。

文丨实习记者 王伯文 记者 马丹萌
秋冬疫情反弹明显,居家自检需求或上升。FDA(美国食品药品监督管理局)近期批准了全美首个新冠家用自检试剂盒的紧急使用授权,至多30分钟就可得到检测结果。据财新记者了解,中国清华大学学者研发的一款同类试剂盒也正在报批过程当中,但是否开放居家检测仍须监管部门进一步考量。
FDA批注上市的上述试剂盒目前仅允许凭处方购买,普通人无法自己购买。且FDA提示,该试剂盒检测出的阴性结果并不能排除感染风险,有症状患者还需与医护人员确认。
该试剂盒由加州制造商LuciraHealth生产,LuciraHealth官网显示,该试剂盒包含拭子、样品瓶、便携式检测装置等一体化套件。受测者自取鼻拭子后,只需将拭子与样品瓶中的溶液搅拌,再将样本瓶插入检测装置,即可等待显示屏闪烁——查看结果,整个检测过程可居家完成。而此前市面上一些居家检测试剂盒的消费者在家中收集样本后,仍需以邮寄的方式向实验室送检。
根据LuciraHealth披露的数据,阳性结果可在11分钟内获得,阴性结果则至多需等待30分钟。此次获批的LuciraCOVID-19一体化检测试剂盒是一次性的分子检测设备,采用实时环介导等温扩增(LAMP)技术,让用于扩增病毒RNA的聚合酶链式扩增(PCR)反应能够在恒温状态下进行。
相比于常规PCR,LAMP检测成本低、速度快,在保证灵敏度的同时可以大大增加检测的可及性与及时性,是目前核酸快检的主要技术路线之一。
上月28日,香港国际机场也展开了RT-LAMP核酸快检技术的测试,大约15-30分钟即可获得结果。(详见财新网《新加坡本地疫情平息将开放中国内地旅客入境》)Lucira一体化检测试剂盒的准确性暂未获FDA透露。
LuciraHealth在其官网宣称,以FDA最可靠的高灵敏度核酸检测方法作为基准:该检测确认阳性样本的准确率为94.1%,如果排除病毒水平极低(37.5Ct或以下)的样本可达100%,确认阴性样本的准确率为98.0%。
FDA在公告中提示,检测结果阴性但出现新冠感染症状的受检者,应与医护人员联系进一步确认。
目前,该试剂盒仅被批准按处方药方式购买,所有检测结果都需按照地方、州、联邦的要求,向相关卫生部门报告。14岁以上的疑似新冠感染者获得处方后,可以申请此试剂盒在家中自采鼻拭子样本进行检测,年龄小于14岁的采检对象,则须由医护人员现场执行采检作业。
……
(本文来自新闻原创付费网站“财新网”,点击文末阅读全文,关注财新网服务号即可阅读全篇文章,阅读更多精彩文章可直接订阅。)
解药|美批准再生元新冠中和抗体紧急使用 全球多个仍在研 [2020-11-23]
当地时间11月21日,美国再生元公司(NASDAQ:REGN)的新冠病毒中和抗体鸡尾酒疗法得到了美国食品药品监督管理局(FDA)的紧急使用授权(EUA),这是美国第二个获批紧急使用的新冠中和抗体。
鸡尾酒疗法指两个或多个药物联合使用。再生元的新冠中和抗体鸡尾酒疗法包括casirivimab和imdevimab两个药物,获批用于治疗病毒检测为阳性、并且有发展到重度或住院风险的轻度至中度COVID-19成人和(12岁及以上、体重不低于40公斤的)未成年患者。在使用中,两种抗体必须同时使用,且禁止对住院患者、接受吸氧治疗的患者,或需要增加基线氧流速的成人或儿童患者使用。这一紧急使用会在美国政府有关部门的全程监控下进行。
Casirivimab和imdevimab是针对新冠病毒棘突蛋白中受体结合域的人源IgG1中和性单克隆抗体。它们通过和新冠病毒结合,让病毒失去进入和侵染人体细胞的能力,从而缓解新冠病毒感染的症状。在9月29日和10月28日,再生元公司分别发布了这一疗法的无缝I/II/III期实验的第一次描述性分析和最终结果,在分别对275名和另外524名患者中展开的用药试验结果表明,这一疗法能显著降低患者体内的病毒载量,从而改善临床结果。
解药|美首个新冠疫苗申请紧急使用 高危群体最快12月接种 [2020-11-21]
当地时间11月20日,辉瑞公司(NYSE:PFE)和BioNTech公司(NASDAQ:BNTX)宣布,将于当日向美国食品药品监督管理局(FDA)申请新冠信使核酸(mRNA)疫苗的候选疫苗BNT162b2的紧急使用授权。如果这一申请得到批准,美国国内的高危群体将可于12月中下旬开始接种疫苗。
利好消息带动两公司股票上涨。截至财新记者发稿,辉瑞股价报36.75美元/股,涨1.53%;BioNTech报99.96美元/股,涨5.3%。另一mRNA疫苗研发公司Moderna(Nasdaq:MRNA)的股票报96.84美元/股,涨4.4%。
这一申请是基于11月19日辉瑞和BioNTech公司宣布的疫苗III期临床试验结果。数据显示,截至接种者出现第170例病例(其中安慰机组162例,疫苗组8例)为止,在接种第二针疫苗7天后,BNT162b2疫苗对接种人群达到了95%的保护率。
解药|FDA紧急授权首个新冠联合治疗方案,药物之一由AI发现 [2020-11-20]
FDA再度紧急批准新冠疗法。11月19日,美国食品药品监督管理局(FDA)授予巴瑞替尼(Baricitinib)与瑞德西韦联用疗法紧急使用授权(EUA),用于治疗需使用吸氧、有创呼吸机或体外膜肺氧合(ECMO)的确诊或疑似患者。巴瑞替尼用于治疗新冠肺炎,最初由人工智能(AI)发现。
巴瑞替尼原是一种用于治疗中度和重度类风湿关节炎的JAK*制剂抑**,最早于2017年在欧洲获批,目前已在超过70个国家上市。其最初由因塞特医疗(INCY.NASDAQ)研发,礼来随后获得授权推广。
巴瑞替尼与瑞德西韦联用已完成一项名为ACTT-2的随机双盲对照临床III期试验,其数据于10月公布。礼来和因塞特方面称,巴瑞替尼瑞德西韦联用使患者恢复时间缩短。相比仅使用瑞德西韦的患者,巴瑞替尼瑞德西韦联用患者恢复时间的中位数由8日缩短为7日。该实验将“恢复”(recovery)定义为不再需要吸氧或医疗看护,或在第29日出院。
责编|任波
版面|赵今朝 王伯文
本文首发于财新网
我们坚持并尊重原创版权,未经授权请勿转载
转载授权、投稿及爆料请联络财新健康管理员
邮箱:denghuiliu@caixin.com
恰询:caixinhealth@caixin.com