前段时间,中华消化病与影像杂志编辑部邀请我写一篇关于手术与细胞治疗肝病的述评,现已正式发表,这篇文章把肝硬化的发病机制和各种治疗方法以及治疗原理、适应证等,说的比较详尽,我摘出来全文给大家汇报分享,文章字数较多,如能阅读下来,将十分有用。

肝硬化的手术与细胞治疗
上海市公共卫生临床中心普外科 刘保池
摘要: 肝硬化是由一种或多种病因长期或反复作用形成的弥漫性肝损害。肝移植是治疗失代偿期肝硬化的有效的方法,但是由于肝源紧张等因素,多数肝硬化患者因上消化道出血、肝性脑病、继发感染、癌变等并发症危及生命。干细胞治疗可以改善肝硬化,自体骨髓经门静脉移植到肝脏,更有利于干细胞在肝内的存活和增殖。对150 多例失代偿期肝硬化患者做自体骨髓经门静脉移植,结果肝功能好转, 肝脏体积增大,弹性超生检查提示肝脏硬度减低。
关键词: 肝硬化,干细胞,自体骨髓,肝功能,肝移植
Operation and cell therapy for liver Cirrhosis
Liu Baochi Department of Surgery, Shanghai publical health center affiliated to Fudan University
Abstract: Cirrhosis is a diffuse liver injury caused by long-term or repeated action of one or more etiologies. Liver transplantation is an effective treatment for decompensated cirrhosis. However, due to liver source tension and other factors, most patients with cirrhosis are at risk of life due to complications such as upper gastrointestinal bleeding, hepatic encephalopathy, secondary infection and cancer. Stem cell therapy can improve cirrhosis of the liver. Transplantation of autologous bone marrow into the liver via portal vein is more beneficial to the survival and proliferation of stem cells in the liver. More than 150 patients with decompensated liver cirrhosis underwent autologous bone marrow transplantation via portal vein, Results the liver function was improved, the liver volume was increased, and the hardness of liver was decreased
Key words: liver cirrhosis, stem cells, autologous bone marrow, liver function, liver transplantation
肝硬化是临床常见的慢性进行性肝病,由一种或多种病因长期或反复作用形成的弥漫性肝损害。在我国大多数为肝炎后肝硬化,另外还有酒精性肝硬化,血吸虫性肝硬化,瘀胆性肝硬化等等。其主要病变有肝细胞呈弥漫性变性、坏死、凋亡,残存细胞再生,形成再生结节,结缔组织弥漫性增生形成纤维隔,最终分割及破坏正常肝小叶结构,代之以硬化性结节或假小叶为特征的病理性改变。肝脏逐渐变形、变硬而发展为肝硬化。早期由于肝脏代偿功能较强可无明显症状,后期则以肝功能损害和门脉高压为主要表现,并有多系统受累,晚期常出现上消化道出血、肝性脑病、继发感染、脾功能亢进、腹水、癌变等并发症[1-2]。
一. 肝脏的损伤与修复
正常情况下,肝脏的实质细胞和细胞外基质保持着动态平衡,从而保证肝脏的各种生理功能。肝脏受损伤后,典型的修复过程包括两个方面:一方面是肝细胞再生,即新生的肝细胞替代受损、坏死的肝细胞发挥作用。另一方面则是纤维组织增生,纤维结缔组织代替了肝正常的实质组织,逐渐形成肝硬化。
新生肝细胞来源包括:(1) 成熟肝细胞,通过有限的有丝分裂补充肝细胞的数量,其增殖能力及修复作用有限;(2) 肝前体细胞(肝卵圆细胞、肝干细胞),肝脏受损时可定向增殖分化为肝细胞或胆管上皮细胞参与肝脏修复,能起到一定的代偿修复作用,但肝内所含数量有限,在增殖分化能力上弱于多能干细胞;(3) 非肝源性多能干细胞,如骨髓间充质干细胞等,此类细胞具有强大的增殖分化能力,在肝损害的微环境下可以增殖分化出较多的肝细胞,因此是理想的肝脏修复细胞来源。
阻断或逆转肝纤维化发展进程及促进肝细胞再生是修复肝损伤和治疗肝硬化的主要方法。
二. 肝硬化的一般治疗
1. 去除病因 阻断对肝细胞进一步损坏的因素是对肝硬化的基本治疗。对不同肝炎病毒引起的肝硬化有不同的抗病毒药物,用核苷类药物如恩替卡韦,替诺福韦等抗乙肝病毒药物治疗可以控制乙型肝炎病毒的大量复制,但是不能清除乙肝病毒,所有需要长期抗病毒治疗。索菲布韦和达卡他韦等抗丙肝病毒药物治疗3到6个月可以清除丙型肝炎病毒,停止酗酒是治疗酒精性肝硬化的基础。
2. 保护肝细胞 常用的药物如肝泰乐、维丙肝、肝宁、益肝灵(水飞蓟素片)、肌苷等。补充维生素C、E及B族维生素有改善肝细胞代谢,防止脂肪性变和保护肝细胞的作用,亦可服用酵母片。酌情补充维生素K、B12和叶酸。
3. 中药:祖国医学对慢性肝病的诊治有独特的见解,中西医结合治疗,往往能收到较好的效果。我国传统医学家认为肝硬化由湿热所致,肝气郁积,影响脾胃,致血行不畅、脉络阻塞,造成积聚或症癜,后期则出现水蛊。辨证多属肝郁脾滞或水积鼓胀型,前者可用柴胡疏肝汤(散)、复肝汤等;后者可用五苓散或五皮饮。
目前对肝硬化无特效药,不宜滥用药物,否则将加重肝脏负担而适得其反。
三.肝硬化门脉高压的手术治疗
门静脉是肝脏入口处的一个大的静脉,门静脉收集食管下段,胃,肠,胰腺,胆囊,脾脏的静脉回流血液,输送到肝实质内。血液到了肝脏,进行“来料加工”,其中的营养成分得到吸收。门静脉血流丰富,每分钟达到1升左右。当肝硬化发生时,肝小叶纤维化,肝实质变硬,肝内阻力增加,门静脉收集的静脉血液流入肝脏受阻,淤滞在门静脉系统内,形成门静脉高压症。门静脉属支压力增高,胃冠状静脉,食管下段和胃底静脉曲张,容易发生破裂出血。消化道出血和肝性脑病是引起肝硬化死亡的主要原因。脾静脉是门静脉属支,门静脉高压导致脾脏肿大,脾功能亢进。针对肝硬化门静脉高压和脾功能亢进,做脾切除可以缓解脾功能亢进,预防和治疗消化道出血的手术方式可以分为分流和断流两类。如果要彻底解决肝硬化问题需要肝脏移植手术。
1.分流手术
将门静脉血液分流到腔静脉系统。目的是降低门静脉压力,减少食管下段静脉曲张破裂出血的可能性。常用的手术方式有脾静脉肾静脉分流,门静脉下腔静脉分流,肠系膜上静脉下腔静脉分流,以及通过介入手术的经颈静脉途径肝内门体分流术(Transjugular intrahepatic portosystemic stent shunt, TIPSS)。其原理是经颈内静脉途径,在肝静脉/下腔静脉与门静脉之间建立一条有效的分流通道,使一部分门脉血直接进入体循环,达到降低门静脉压力、控制和防止食管胃底静脉曲张破裂出血和促进腹水吸收的目的[3-4]。这些手术的目的都是通过分流门静脉血液进入下腔静脉系统,降低门静脉压力,减少上消化道曲张的血管破裂出血。但是门静脉血分流到腔静脉,一些有毒物质没有经过肝脏代谢直接进入体循环系统而引起肝性脑病是最常见的并发症[5]。此外分流道狭窄与闭塞也是影响对门静脉压力降低的因素。
2.断流手术
作贲门周围血管离断,阻断门静脉血通过胃冠状静脉,贲门周围静脉,奇静脉到上腔静脉的分流[6]。由于15%左右的血流可以通过胃黏膜下静脉进入食管下段静脉,也有的手术进行胃底切断再吻合,彻底阻断门静脉经过食管下段静脉进入奇静脉的血流,以期防治食管下段静脉曲张破裂引起的消化道出血。但是这种手术方法仅仅阻断了肝硬化患者病理状况下建立起来的门静脉经过奇静脉到上腔静脉的分流,断流以后使门静脉压力增加,不久会在食管周围形成新的侧枝重建,仍然还会发生食管下段静脉曲张破裂出血。而且断流手术往往因为也切断了迷走神经,引起手术后的胃肠功能障碍。
3.肝脏移植手术
20世纪80年代以前,即使采用多种一般药物治疗和手术治疗方法, 肝硬化一旦发展到失代偿期,5年存活机会仅有约20%。20世纪80年代以后, 肝移植技术的成熟及更有效的抑制排异药物的临床应用, 肝移植后患者5年生存率可以达到75%~80%。所以肝移植成为治疗失代偿期肝硬化的最有效的方法[7]。但是由于肝源紧张和昂贵的医疗费用,限制了肝移植的普及开展。
四.肝硬化的干细胞移植
干细胞作为一种具有横向分化能力的多能干细胞,近年来大量研究表明在合适的培养条件下其在体内外均可以向肝细胞分化[7-17]。2000年,日本学者使用大鼠骨髓干细胞,加入不同浓度的HGF(肝细胞生长因子)进行体外诱导培养之后,发现了骨髓干细胞可以分化为肝样细胞。
间充质干细胞(mesenchymal stem cell, MSC)移植治疗肝硬化正在成为一种损伤小、并发症少、疗效明显的治疗手段。MSC具有向肝实质细胞分化的潜能。MSC 是一类具有自我增殖和多向分化潜能的多能干细胞。大量研究表明MSC能向多种细胞分化,具有强大的可塑性。在一定的微环境中MSC可被诱导分化为肝细胞、成骨细胞、软骨细胞、脂肪细胞、骨骼肌细胞等。已经在骨髓、胎盘、脐带、脂肪等许多组织中分离出了MSC。
MSC的作用机制:目前对于移植的骨髓干细胞或MSC发挥治疗作用的具体机制有了初步的了解,机制可能包括:
(1) 直接分化:在肝脏损伤微环境的影响下定植、增殖,并分化成为肝细胞发挥作用;
(2) 旁分泌途径: 在肝损伤环境中MSC可以分泌不同水平的细胞因子相互影响,表现出抗炎症反应的作用,并可能激活肝内的干细胞,促进肝细胞再生;
(3) 细胞融合: MSC可能直接与肝细胞融合,进而启动细胞的增殖过程;
(4) MSC通过高表达基质金属蛋白酶降解细胞外基质,直接降解肝内过量沉积的细胞外基质,减轻肝纤维化;
(5) MSC不仅能分化为肝细胞,而且在体内具有免疫调节的功能,减轻肝脏炎症反应和损伤。
笔者根据目前的医学知识,骨髓中包含有间充质干细胞,造血干细胞,血管始祖细胞和细胞间质。如果将骨髓整体移植到门静脉,应该是将间充质干细胞和其周围的微环境一起移植到肝脏,可能更有利于干细胞在肝内的存活和增殖。从2009 年4月至2015年5月,对12例艾滋病合并失代偿期肝硬化患者进行脾脏切除手术加自体骨髓经门静脉输注治疗,结果患者在手术后3 个月由原来的肝功能Child-Pugh分级从C级或者B级全部恢复到*级A**。1 例手术后第3 年死于吸毒引起的癫痫发作,其余11例至今肝功能维持在*级A**,全身情况明显好转。自体骨髓经门静脉输注1 年后复查肝脏体积增大,弹性超生检查提示肝脏硬度减低[18]。另外有7例艾滋病合并失代偿期肝硬化患者因为担心手术风险,不同意手术治疗,仅用抗病毒治疗和保肝利尿等一般治疗,结果3 年内全部死于肝脏衰竭。
我们将这种方法应用到150 多例没有艾滋病病毒感染的一般肝硬化患者,结果收到更好疗效[19-20]。例如1例患者男,56 岁,失代偿肝硬化大量腹水合并脐疝(图1)。 CT检查提示肝脏明显萎缩,肝脏体积1302 ml,大量腹水, 脾脏肿大(图2)。我们对患者进行脾切除加脐疝修补,自体骨髓经门静脉输注治疗。手术后3 个月,肝功能Child-Pugh分级从C级转成*级A**,手术后1 年,肝功能正常,腹部伤口愈合良好(图3)。CT检查提示肝脏明显增大,体积1796 ml,腹水基本消失(图4)。对于肝功能C级的患者手术风险比较高,围手术期输注白蛋白,凝血酶原复合物,纤维蛋白原,改善肝脏功能,手术中经胃网膜右静脉插管埋置骨髓输注装置,输注自体骨髓。随着自体骨髓干细胞在肝内发生复杂的变化,肝硬化组织中的胶原纤维被降解和吸收,肝脏组织的增生和体积增大,肝功能好转,门静脉压力会逐渐降低。但是在手术和自体骨髓经门静脉输注后1到2 年内,仍然有可能随时发生上消化道出血,需要经胃镜检查,套扎食管黏膜下明显曲张的静脉血管。这样脾脏切除解除脾功能亢进,不做贲门周围血管离断,减少了手术损伤。食管黏膜下静脉曲张用胃镜下套扎治疗。待肝硬化的逐渐逆转,食管黏膜下静脉曲张程度将会逐渐减轻。
肝硬化门静脉高压症是临床上常见的可以致命的严重疾病,该疾病的发生机制、演变有复杂的病理变化,治疗过程中有很多已知或未知的因素难以掌握,围手术期治疗又颇为复杂。精细的围手术期治疗加自体骨髓经门静脉输注,有可能使失代偿期肝硬化患者逆转回健康状态。
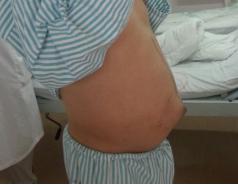
图1.代偿肝硬化大量腹水合并脐疝患者手术前照片
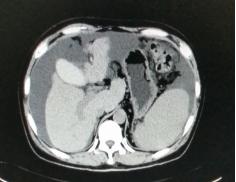
图2.术前腹部CT断层照片

图3.切除加自体骨髓输注后1 年患者照片
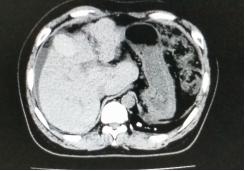
图4.1年后对比手术前同一部位CT断层照片
参考文献
1.南月敏.肝硬化并发症诊治现状及展望[J]《中华肝脏病杂志》.2017,25(04):241-245.
2.Pantham G, Mullen KD. Practical Issues in the Management of Overt Hepatic Encephalopathy[J] Gastroenterol Hepatol. 2017; 13(11): 659–665.
3.Bannas P, Roldán-Alzate A, Johnson KM, Longitudinal Monitoring of Hepatic Blood Flow before and after TIPS by Using 4D-Flow MR Imaging[J].Radiology. 2016;281(2):574-582.
4. Cavași A, Mercea V, Anton O, et al.Therapeutic Challenges for Symptomatic Portal Cavernoma Cholangiopathy[J].J Gastrointestin Liver Dis. 2016;25(3):395-9.
5. Owen JM, Gaba RC.Transjugular Intrahepatic Portosystemic Shunt Dysfunction: Concordance of Clinical Findings, Doppler Ultrasound Examination, and Shunt Venography[J]. J Clin Imaging Sci. 2016 Jul 18;6:29. doi: 10.4103/2156-7514.186510.
6. Zhang YB, Lu Y, Wu WD,at al.Indocyanine green retention is a potential prognostic indicator after splenectomy and pericardial devascularization for cirrhotic patients[J].Hepatobiliary Pancreat Dis Int, 2016, 15(4): 386-390.
7. Pan HC, Chen YJ, Lin JP,at al. Proteinuria can predict prognosis after liver transplantation[J]. BMC Surg, 2016, 16(1): 63. doi: 10.1186/s12893-016-0176-8
8.Takami T, Terai S, Sakaida I.Stem cell therapy in chronic liver disease[J].Curr Opin Gastroenterol, 2012,28(3):203-208.
9. Nicolas CT, Hickey RD, Chen HS, Mao SA, Lopera Higuita M, Wang Y, Nyberg SL. Concise Review: Liver Regenerative Medicine: From Hepatocyte Transplantation to Bioartificial Livers and Bioengineered Grafts[J]Stem Cells. 2017; 35(1):42-50. doi: 10.1002/stem.2500.
10. Kim JK, Kim SJ, Kim Y, Chung YE, Park YN, Kim HO, et al. Long-Term Follow-Up of Patients After Autologous Bone Marrow Cell Infusion for Decompensated Liver Cirrhosis[J]. CELL TRANSPLANT. 2017;26: 1059-66.
11. Nicolas CT, Wang Y, Nyberg SL. Cell therapy in chronic liver disease[J].Curr Opin Gastroenterol. 2016 May; 32(3):189-94. doi: 10.1097/MOG.0000000000000262
12. Cantz T., Sharma A.D., Ott M. Concise review: Cell therapies for hereditary metabolic liver diseases-concepts, clinical results, and future developments[J]. Stem Cells. 2015;33:1055–1062. doi: 10.1002/stem.1920.
13. Borhofen SM, Gerner C, Lehmann J, et al. The Royal Free Hospital-Nutritional Prioritizing Tool is an independent predictor of deterioration of liver function and survival in cirrhosis[J]Dig Dis Sci. 2016;61(6):1735–1743.
14. Mullen KD, Sanyal AJ, Bass NM, et al. Rifaximin is safe and well tolerated for long-term maintenance of remission from overt hepatic encephalopathy[J]Clin Gastroenterol Hepatol. 2014;12(8):1390–1397.e2.
15. Pan XN, Zheng LQ, Lai XH. Bone marrow-derived mesenchymal stem cell therapy for decompensated liver cirrhosis: a meta-analysis[J]. World J Gastroenterol. 2014;20: 14051-7.
16. Levine P, McDaniel K, Francis H, Kennedy L, Alpini G, Meng F. Molecular mechanisms of stem cell therapy in alcoholic liver disease[J]. Dig Liver Dis. 2014;46: 391-7.
17. 刘保池.肝炎后失代偿期肝硬化的治疗与手术技巧[J] 国际外科学杂志,2017,44(1)35-37
18. Baochi Liu ,Xiaodong Chen , Yufang Shi.Curative Effect of Hepatic Portal Venous Administration of Autologous Bone Marrow in AIDS Patients with Decompensated Liver Cirrhosis[J] Cell Death & Disease (2013).4, e739; doi:10.1038/cddis.2013.261
19. 刘保池,李垒,司炎辉,等. 失代偿肝硬化合并胆囊结石的自体骨髓肝内输注治疗[J]. 肝胆胰外科杂志, 2016, 28(1): 10-12
20. 刘保池,冯铁男,李垒. 自体骨髓对失代偿期肝硬化合并小肝癌的治疗[J] 肝胆胰外科杂志, 2017, 29(3): 188-191

作者简介:
刘保池,主任医师。医学博士,博士生导师。教授。专长肝胆外科的手术与细胞治疗。
学术任职:全国卫生产业企业管理学会外科技术创新与推广分会理事,手术与细胞治疗学术委员会主任委员;中国研究型医院学会卫生应急专业委员会常务委员,感染与特殊感染学组组长
作者单位:上海市公共卫生临床中心
单位地址:上海市金山区漕廊公路2901号 邮编:201508
基金资助: 申康医院发展中心资助课题“自体骨髓肝内输注促进肝硬化的肝功能重建研究”(项目编号 SHDC12016129)