以下文章来源于天津市药物临床研究技术创新中心 ,作者创新中心
创新中心/报道
滤泡性淋巴瘤的定义
滤泡性淋巴瘤(follicular lymphoma,FL)是一类惰性病程的淋巴肿瘤,来源于生发中心B细胞,呈结节性或滤泡样分布,是一组包括小有裂滤泡中心细胞(中心细胞)和大无裂滤泡中心细胞(中心母细胞)的恶性淋巴细胞的增生性疾病[1-2]。
流行病学
在美国,FL约占成人非霍奇金淋巴瘤(non-Hodgkin lymphomas , NHLs)的20%-25 %,每年约有14 000例新发病例。FL最常见于北美和西欧,而东欧、亚洲、非洲、非洲裔的美国人中较少见。诊断时的中位年龄为59岁,男女比例为1 : 17 。该病在20岁以下的青年中罕见,儿利病例似乎代表一种独立的疾病,通常为局部病变,不伴t ( 14 ; 18)易位和BCL2表达,预后好。
临床表现
FL患者常表现为无痛性弥漫性淋巴结肿大,较少见的有腹部不适,包括疼痛、早饱、腹围增加,后者可能由于巨大的腹部包块或肝脾肿大引起。大约有10%的患者伴B症状(发热、盗汗或体重减轻10 %)。该病通常诊断时已为弥漫性,累及多个淋巴结、肝脏和脾脏。40%-70%患者发生骨髓累及。FL较常见的原发病灶还包括皮肤、胃肠道、眼附属器,以及乳房,但中枢神经系统累及罕见,除非组织学转变为弥漫大B细胞淋巴瘤。
滤泡性淋巴瘤的分型、分级和分期
FL在Rappaport分型中称为“结节性淋巴瘤”,在工作分类中称为“滤泡中心细胞淋巴瘤”。现在的世界卫生组织(World Health organization,WHO)分型将之命名为“滤泡性淋巴瘤”, 在镜下FL 有时可合并弥漫性成分出现,根据滤泡成分和弥漫成分所占的比例不同可以将FL分为:①滤泡为主型(滤泡比例>75%);②滤泡和弥漫混合型(滤泡比例25%-75%);③局灶滤泡型(滤泡比例<25%)。根据WHO淋巴瘤分类方法即基于高倍镜视野下中心母细胞的数量,FL进一步可以分为1-3 级。FL的分期一般参考英国Cotswords修订的Ann Arbor分期标准,该标准主要考虑受累部位情况,将FL分为Ⅰ-Ⅳ期。
滤泡性淋巴瘤的靶向治疗
据文献报道,FL 的临床病程长,8%-70%的FL 患者在整个疾病发展过程中可以转化为其他更具侵袭性的淋巴瘤,其中以DLBCL 最为常见,年发生率为2%-3%,持续至少15 年,之后转化风险逐渐下降。转化后的患者预后差,中位生存时间为10-18个月。如何提高FL患者的无病生存期,抑制FL向DLBCL转化成为改善FL患者生存质量的关键因素而目前对于转化性FL患者尚无标准的治疗措施,经典的治疗方案难以达到该目的。FL作为药物研发热门适应症之一,新药特别是新的靶向治疗的出现则给FL的治疗提供了更多的选择和机会(详见下表)[3]:
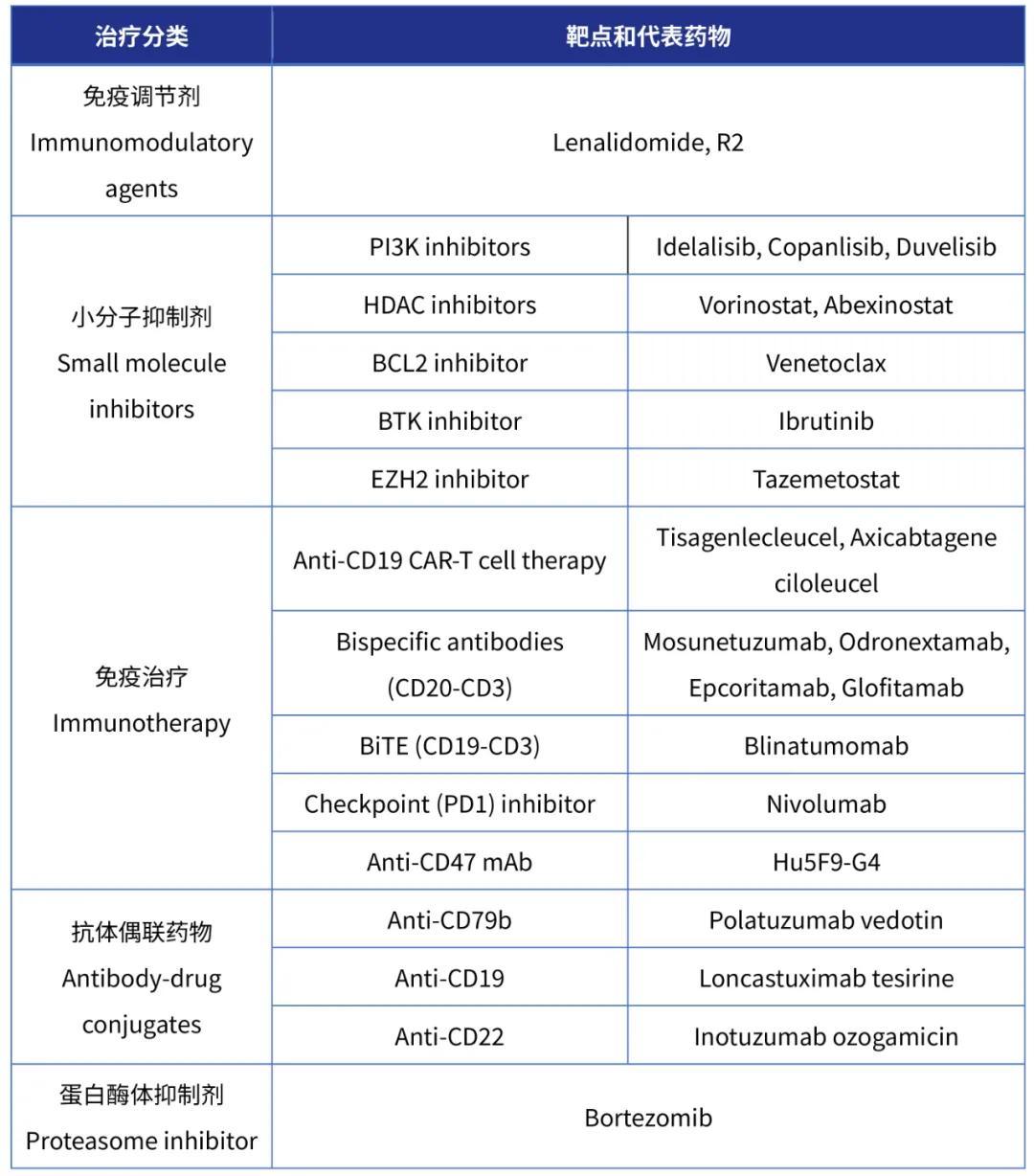
免疫调节剂
来那度胺是一种口服免疫调节剂(IMiD),具有直接和间接抗肿瘤活性。来那度胺的作用机制尚未完全清楚。来那度胺以肿瘤细胞中的cereblon为靶点,具有降低干扰素调节因子4和抑制增殖活性的下游效应,同时来那度胺增加NK细胞介导的细胞毒性和ADCC,增强细胞毒性T细胞和树突状细胞活性,改善T细胞至恶性B细胞突触的形成,减少促炎细胞因子,并通过与微环境、内皮细胞和血管内皮生长因子的相互作用抑制血管生成[4-6]。来那度胺与抗CD20单克隆抗体结合具有协同效应,已被批准与利妥昔单抗(Rituximab,R)联合治疗R/R FL患者。这项批准基于AUGMENT研究的结果。这项III期研究将R/R FL患者随机分为利妥昔单抗+来那度胺组(R2组)和利妥昔单抗+安慰剂组(R+安慰剂组)。共有358名患者被随机分配到R2组(n=178)或R+安慰剂组(n=180)。两组ORR分别为78%和53%,CR分别为34%和18%。R2组的PFS为39.4个月,R+安慰剂组为14.1个月,HR 0.46(95%CI,0.34-0.62;P<0.001)[7]。
小分子*制剂抑**
PI3K*制剂抑**
Idelalisib是一种口服PI3K*制剂抑**,每天口服两次。在一项单臂开放标签2期临床试验中,纳入了125名患者,其中包括72名FL患者,平均接受过4线治疗(线数范围2-12),患者每天口服两次Idelalisib,直至进展或不耐受。FL患者的ORR为57%,CR为6%,DOR为12.5个月。27%的患者出现3级中性粒细胞减少[8]。72例FL患者的事后亚组分析结果显示ORR为 56%,CR为14%, DCR为87%[9]。
Duvelisib也是一种口服PI3K*制剂抑**,每天口服两次。除δ异构体外,该制剂还抑制γ异构体。FDA批准其用于FL是基于一项II期研究(DYNAMO)结果,该研究报告Duvelisib 治疗FL患者的平均DOR为10个月,PFS为9.5个月,ORR为42%[10]。
Copanlisib是一种注射使用PI3K制剂,可抑制α和δ异构体。与Idelalisib或Duvelisib相比,Copanlisib表现出更好的安全性。Copanlisib每4周为1个周期(给药3周内休息1周)。在一项2期研究(CRONOS-1)中,共纳入142名≥2线经治的R/R惰性NHL患者,其中包括104名FL患者,FL亚组的ORR为59%,CR为14%,中位DOR为12个月。Copanlisib的不良事件主要包括腹泻、结肠炎、皮疹、全身炎症、感染、高血压和高血糖。后两种不良事件具体归因于α异构体的抑制[11]。
BTK*制剂抑**和BCL2*制剂抑**
破坏B细胞受体信号通路的药物,包括BTK*制剂抑**伊布替尼和BCL2*制剂抑**venetoclax,这类药物已在包括FL在内的一系列B细胞恶性肿瘤中显示出活性。伊布替尼的两项项针对R/R FL患者的单臂II期研究结果已经发表,第一项研究的ORR为20.9%,中位PFS为4.6个月,在第二项研究中,ORR为20.5%,中位PFS为14个月,PFS的差异可能是因为前者中利妥昔单抗和烷化剂难治性患者的比例更高[12,13]。
HDAC*制剂抑**
HDAC*制剂抑**(HDACi)是基于表观遗传学理论发现的一类新型药物。
Vorinostat是一种口服HDAC*制剂抑**。在以R/R iNHL为研究对象的2期研究中,共纳入37名患者,其中包括17名FL患者。21天为一个周期(治疗14天,休息7天),获得缓解的患者持续治疗至疾病进展。达到CR的患者在获得CR后再进行2个周期后停止治疗,但如果在6个月内复发,可以重新开始治疗。所有患者的ORR为29%,FL患者的ORR为47%(CR为10.8%),中位PFS为15.4个月[14]。在另一项2期试验中,iNHL患者在至少1线治疗,使用Vorinostat直到疾病进展或达到停药标准。对于FL患者,ORR为49%,中位PFS为20个月[15]。上述两项研究中大多数3-4级不良事件是血液学不良事件[14,15]。在一项Vorinostat与利妥昔单抗联合治疗研究中,纳入初治/经治的iNHL患者28例,其中22例为FL患者。对于FL患者,ORR为41%,CR率为27%,2年PFS为61%。达到CR患者被允许停止治疗,并在病情进展时重新开始治疗,4例疾病进展重新开始治疗的患者中有2例再次获得CR[16]。
Abexinostat也是一种口服泛HDAC*制剂抑**,每日服用两次,已发表两项2期研究结果。第一项研究纳入R/R FL和R/R MCL患者。对于FL患者,ORR为56.3%,1名患者达到CR,中位PFS为20.5个月[17]。在第二项研究中,患有R/R NH或CLL的患者接受Abexinostat治疗,直至疾病进展或因其他原因退出治疗。100名患者中有18名患有FL,对于FL患者,ORR为56%,中位DOR为16个月[18]。在这两项研究中,大多数3-4级毒性都是血液学毒性,虽然HDACis包括QT间期延长的心*毒脏**性值得关注,但在每项研究中都只有1名患者出现这种情况[17,19]。
EZH2 *制剂抑**
Tazemetostat是首个批准上市的口服使用,靶向突变型或野生型EZH2选择性*制剂抑**,EZH2也是基于表观遗传学理论发现的新型药物。其FL适应症获批主要基于一项开放标签2期研究,该研究共纳入45例EZH2突变(EZH2MT)和54例野生型(EZH2WT)R/R FL患者,患者接受Tazemetostat治疗至满2年、直到疾病进展、无法耐受毒性或停药。49%的EZH2MT和59%的EZH2WT患者为含利妥昔单抗方案难治性患者。两组的ORR分别为69%和35%(CR率分别为13%和4%),中位PFS分别为13.8个月和11.1个月,总体上治疗耐受性良好[20]。
免疫治疗
利用患者免疫系统治疗FL的疗法显示出巨大的前景。目前针对FL适应症的免疫治疗的开发主要包括针对新靶点的单克隆抗体,双特异性抗体,免疫检查点*制剂抑**及CAR-T治疗。
CAR-T治疗
在单臂2期试验中,两种已批准的CAR-T细胞产品在高级别B细胞淋巴瘤(包括转化后的滤泡淋巴瘤。tFL)中证明了该治疗组合带来明显持久的缓解和高CR率,FL中也报告了有希望的结果。一项针对FL中CD19导向的CAR-T细胞的I/II期研究包括8例R/R FL患者和13例tFL患者。FL和tFL的CR率分别为88%和46%,所有FL患者在治疗后24个月的随访仍保持缓解。细胞因子释放综合征(CRS)和神经毒性均发生在约50%的FL患者中,且在FL患者中更常见[21]。在宾夕法尼亚大学的另一项研究中,14例FL患者用CD19 CAR-T细胞治疗,其中8例为利妥昔单抗和烷化剂难治性患者。研究结果ORR为79%,6个月时CR率为71%,中位PFS未达到,中位随访时间为28.6个月时,70%无进展[22]。中期分析:ZUMA-5研究报告80例FL患者的ORR为95%,CR率为80%。在整个iNHL队列中,分别有19%和11%的患者发生≥3 级CRS和神经毒性安全性事件[23-25]。
BiTE
BiTE (bispecific T cell engager)是一种以T细胞作为效应细胞的双特异性单链抗体,它具有两个抗原结合部位,可以同时结合T细胞及病变细胞表面的抗原分子,从而有效的激活静止的T细胞,达到*伤杀**病变细胞的目的。在包括28名FL患者的1期剂量递增研究中,探索了CD19-CD3 Blinotumab治疗R/R NHL的疗效和安全性,在以目标剂量治疗的15名患者中,12名获得客观缓解,6名获得CR/CRu[26]。全长CD3-CD20双特异性抗体目前正在研制中。BiTE的优点包括输液时间短,半衰期长,神经毒性明显降低。目前至少有4种药物正在研发中(Mosunetuzumab,Odronextamab,Epcoritamab和Glofitamab)。以摘要形式发布的阶段性数据表明,Mosunetuzumab为多线经治的B细胞非霍奇金淋巴瘤患者(包括FL患者)带来高缓解率。最大的队列包括69名接受Mosenutuzumab治疗的iNHL患者,其中反应可评估患者的ORR和CR率分别为64.1%和42.2%,先前系统治疗的线数的中位数为3[27]。在另一项研究中,14名R/R FL等级为1-3A的患者在使用≥ 5 mg剂量Odronextamab治疗时,ORR和CR率分别为93%和71.4%[28]。主要毒性是CRS,提示具有剂量依赖性,与肿瘤负荷亦有关系,通过逐步递增给药策略和恰当治疗可以控制。
免疫检查点*制剂抑**
免疫检查点*制剂抑**已在包括经典霍奇金淋巴瘤在内的其他恶性肿瘤中显示出应用前景,但是在B细胞NHL中单药活性有限。其可能通过与其他药物联合使用发挥作用。相关制剂在FL适应症发表文献较少。在一项包括40名R/R FL患者的1/2期研究中,PD-1*制剂抑**nivolumab与BTK*制剂抑**伊布替尼联合使用,治疗持续至患者疾病进展。ORR为33%,CR率为10%[29]。在另一项研究中,至少经过两线治疗FL患者使用nivolumab进行治疗,至少随访12个月,ORR仅为4%,PFS中位数为2.2个月[30]。
新型单克隆抗体
CD47是一种广泛表达于多种细胞表面的跨膜糖蛋白,通过一系列复杂过程,对免疫系统发挥着重要的调节作用。对于恶性肿瘤细胞,其细胞表面CD47则发挥作用帮助肿瘤细胞抗吞噬。Hu5F9-G4单克隆抗体可阻断CD47,从而实现对恶性细胞的吞噬作用,与利妥昔单抗合用可增强其效果。在Hu5F9-G4+R的Ib期研究中,22名患者的队列包括7名FL患者,所有患者均为利妥昔单抗难治性患者, 5名患者获得客观缓解,3位患者达到CR[31]。
抗体偶联药物(ADC)
Polatuzumab vedotin(Pola)是一种针对CD79b的抗体偶联药物,其负载为甲基澳瑞他汀(monomethyl auristatin)。与治疗相关的主要不良事件神经病变主要与其负载有关。目前已批准与苯达莫司汀-利妥昔单抗联合治疗弥漫性大B细胞淋巴瘤(DLBCL)。最初在几项早期研究中对其进行了研究,最后在ROMULUS研究中与Pinatuzumab进行了比较。在这项研究中,Pola以2.4 mg/kg的剂量给药,患者接受治疗直到疾病进展或无法耐受。该研究纳入了FL和DLBCL患者,在本研究中,20名FL患者服用了Pola。20名患者中有14名获得客观缓解,9名达到完全缓解。本研究的缓解持续时间(DOR)为9.4个月,无进展生存期(PFS)为15.3个月。36%的Pola组患者出现神经病变,均为1-2级。23%的出现周围感觉神经病变,其中8%的患者高于2级。由于不良事件,Pola的剂量降低至1.8 mg/kg,持续时间限制为6-8个周期[32]。
Loncastuximab tesirine(ADCT-402)为首款CD19靶向抗体偶联药物,由靶向CD19的人源化单克隆抗体通过连接子与吡咯并苯并二氮杂䓬(pyrrolobenzodiazepine,PBD)二聚体负载偶联而成。Lotis-1(NCT02669017)是一项开放、单臂、国际多中心的1期临床试验。作为ADCT-402的首次人体试验,Lotis-1目标人群为R/R B-NHL患者。研究分为两个部分:剂量递增阶段和剂量扩展阶段。该研究纳入了14例R/R FL患者,结果显示,经ADCT-402治疗的FL患者的ORR达到78.6%(CR 64,3%,PR 14.3%)[33]。因为早期研究样本量的限制,ADCT-402治疗的R/R FL患者的潜力,有必要在更大的人群中进行证明。针对R/R FL患者而开展2期试验Lotis-6(NCT04699461)的设计初衷应该就是为了达到此项目的。Lotis-6在2021年第二季度开始患者入组,共招募150名受试者,进行随机平行分配。研究计划对比ADCT-402和PI3K*制剂抑**Idelalisib治疗R/R FL患者的疗效和安全性,纳入人群必须是经历了两种或两种以上治疗方案的R/R FL患者,且在既往治疗中至少有一种必须包含抗CD20的治疗。研究选取CR作为主要终点指标,ORR作为次要终点指标。
蛋白酶体*制剂抑**
一项随机3期研究评估了蛋白酶体*制剂抑**硼替佐米与利妥昔单抗联合应用治疗复发FL患者的有效性和安全性,该研究中未观察到因联合应用硼替佐米而对PFS起到改善作用,但单独报告了联用可以对FLPI评分≥ 3的高危亚组和高肿瘤负担患者带来益处[34.35]。
代表*药性**物治疗R/R FL的疗效比较
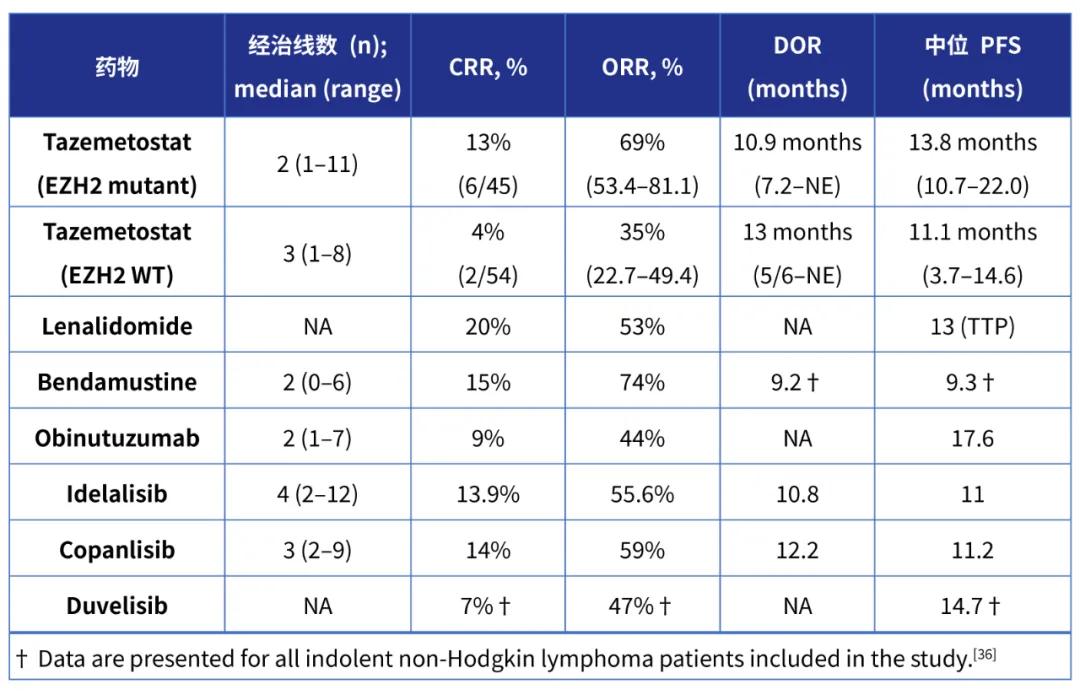
结语
FL 的发病机制目前仍未完全探明,很多靶点理论上可行,但由于体内生理反应的复杂性,必须通过大量临床试验来验证。这些高效药物可能会在未来几年改变FL治疗格局,需要设计良好的随机对照试验来充分证明其疗效和安全性。同时,也有联合用药的初探,证明药物联用带来的突破性疗效提升,联用机制以及安全性和疗效性的确认也尚需在更大规模的临床研究中进一步探讨。期待FL 机制的进一步阐明,新药的有效性得到进一步验证,为FL 患者带来福音。
参考文献
1. Williams Hematology_9 edition
2. 黄慧强. 中国滤泡性淋巴瘤诊断与治疗指南(2020年版)[J]. 中华血液学杂志, 2020(7):537-544.
3. Northend Michael,Townsend William,Novel Therapy Approaches to Follicular Lymphoma.[J] .Drugs, 2021, 81: 453-469.
4. Gribben John G,Fowler Nathan,Morschhauser Franck,Mechanisms of Action of Lenalidomide in B-Cell Non-Hodgkin Lymphoma.[J] .J Clin Oncol, 2015, 33: 2803-11.
5. Garciaz Sylvain,Coso Diane,Schiano de Colella Jean-Marc et al. Lenalidomide for the treatment of B-cell lymphoma.[J] .Expert Opin Investig Drugs, 2016, 25: 1103-16.
6. Ramsay Alan G,Gribben John G,Immune dysfunction in chronic lymphocytic leukemia T cells and lenalidomide as an immunomodulatory drug.[J] .Haematologica, 2009, 94: 1198-202.
7. Leonard John P, Trneny Marek, Izutsu Koji et al. AUGMENT: A Phase III Study of Lenalidomide Plus Rituximab Versus Placebo Plus Rituximab in Relapsed or Refractory Indolent Lymphoma. [J] .J Clin Oncol, 2019, 37: 1188-1199.
8. Salles G, Schuster SJ, de Vos S,Wagner-Johnston ND, Viardot A, Blum KA, et al. Efficacy and safety of idelalisib in patients with relapsed, rituximab- and alkylating agent-refractory follicular lymphoma: a subgroup analysis of a phase 2 study. Haematologica. 2017;102(4):e156–9.
9. Gopal AK, Kahl BS, Flowers C,Martin P, Link BK, Ansell S, et al. Activity of idelalisib in high-risk follicular lymphoma with early relapse following front line immunochemotherapy. [J] .Blood. 2015 Dec;126(23):2744.
10. Swarup S, Quick DP, Sultan A, et al. Incidence of serious adverse events, pneumonitis, infection and sepsis in patients with relapsed and refractory chronic lymphocytic leukemia/small lymphocytic lymphoma treated with phosphatidylinositol 3-Kinase (PI3K) inhibitors. Oral presentation at: 61st ASH Annual Meeting & Exposition; December 7-10, 2019; Orlando, FL. Abstract 798.
11. Dreyling M, Santoro A, Mollica L, et al. Phosphatidylinositol 3-kinase inhibition by copanlisib in relapsed or refractory indolent lymphoma. [J] . J Clin Oncol. 2017;35(35):3898–905.
12. Gopal AK, Schuster SJ, Fowler NH, Trotman J, Hess G, Hou J-Z, et al. Ibrutinib as treatment for patients with relapsed/refractory follicular lymphoma: results from the open-label, multicenter, Phase II DAWN study. [J] . J Clin Oncol. 2018;36:2405–12.
13. Bartlett NL, Costello BA, LaPlant BR, Ansell SM, Kuruvilla JG, Reeder CB, et al. Single-agent ibrutinib in relapsed or refractory follicular lymphoma: a phase 2 consortium trial. [J] .Blood. 2018;131:182–90.
14. Kirschbaum M, Frankel P, Popplewell L, Zain J, Delioukina M, Pullarkat V, et al. Phase II study of vorinostat for treatment of relapsed or refractory indolent non-Hodgkin’s lymphoma and mantle cell lymphoma. [J] . J Clin Oncol. 2011;29:1198–203.
15. Ogura M, Ando K, Suzuki T, Ishizawa K, Oh SY, Itoh K, et al. A multicentre phase II study of vorinostat in patients with relapsed or refractory indolent B-cell non-Hodgkin lymphoma and mantle cell lymphoma. [J] .Br J Haematol. 2014;165:768–76.
16. Chen R, Frankel P, Popplewell L, Siddiqi T, Ruel N, Rotter A, et al. A phase II study of vorinostat and rituximab for treatment of newly diagnosed and relapsed/refractory indolent non-Hodgkin lymphoma. [J] .Haematologica. 2015;100:357–62.
17. Evens AM, Balasubramanian S, Vose JM, Harb W, Gordon LI,Langdon R, et al. A Phase I/II multicenter, open-label study of the oral histone deacetylase inhibitor abexinostat in relapsed/refractory lymphoma. [J] .Clin Cancer Res. 2016;22:1059–66.
18. Michot J-M, Bouabdallah R, Vitolo U, Doorduijn JK, Salles G,Chiappella A, et al. Avadomide plus obinutuzumab in patients with relapsed or refractory B-cell non-Hodgkin lymphoma (CC-122-NHL-001): a multicentre, dose escalation and expansion phase 1 study. [J] . Lancet Haematol. 2020;7:e649–59.
19. Ribrag, Kim WS, Bouabdallah R, Lim ST, Coiffier B, Illes A, et al. Safety and efficacy of abexinostat, a pan-histone deacetylase inhibitor, in non-Hodgkin lymphoma and chronic lymphocytic leukemia: results of a phase II study. [J]. Haematologica. 2017;102:903–9.
20. Morschhauser F, Tilly H, Chaidos A, McKay P, Phillips T, Assouline S, et al. Tazemetostat for patients with relapsed or refractory follicular lymphoma: an open-label, single-arm, multicentre, phase 2 trial. [J] .Lancet Oncol. 2020;21:1433–42.
21. Hirayama AV, Gauthier J, Hay KA, Voutsinas JM, Wu Q, Pender BS, et al. High rate of durable complete remission in follicular lymphoma after CD19 CAR-T cell immunotherapy. [J].Blood. 2019;134:636–40.
22. Schuster SJ, Svoboda J, Chong EA, Nasta SD, Mato AR, Anak Ö, et al. Chimeric antigen receptor T cells in refractory B-cell lymphomas. [J].N Engl J Med. 2017;377:2545–54.
23. Bishop MR. The case for CAR T-cell therapy in follicular lymphomas. Blood. 2019;134:577–8.
24. Dickinson M, Popplewell L, Kolstad A, Ho J, Teshima T, Dreyling MH, et al. ELARA: a phase II, single-arm, multicenter, open-label trial investigating the efficacy and safety of Tisagenlecleucel in adult patients with refractory/relapsed follicular lymphoma (r/r FL). [J].J Clin Oncol. 2019;37:TPS7573.
25. Jacobson CA, Chavez JC, Sehgal AR, William BM, Munoz J, Salles GA, et al. Interim analysis of ZUMA-5: a phase II study of axicabtagene ciloleucel (axi-cel) in patients (pts) with relapsed/ refractory indolent non-Hodgkin lymphoma (R/R iNHL). [J]. J Clin Oncol. 2020;38:8008.
26. Goebeler M-E, Knop S, Viardot A, Kufer P, Topp MS, Einsele H, et al. Bispecific T-cell engager (BiTE) antibody construct blinatumomab for the treatment of patients with relapsed/refractory non-hodgkin lymphoma: final results from a Phase I study. [J]. J Clin Oncol. 2016;34:1104–11.
27. Schuster SJ, Bartlett NL, Assouline S, Yoon S-S, Bosch F, Sehn LH, et al. Mosunetuzumab induces complete remissions in poor prognosis non-hodgkin lymphoma patients, including those who are resistant to or relapsing after chimeric antigen receptor T-cell (CAR-T) therapies, and is active in treatment through multiple lines. [J]. Blood. 2019;134:6.
28. Bannerji R, Allan JN, Arnason JE, Brown JR, Advani RH, Barnes JA, et al. Clinical activity of REGN1979, a bispecific human, anti-CD20 x anti-CD3 antibody, in patients with relapsed/refractory (R/R) B-cell non-hodgkin lymphoma (B-NHL). [J]. Blood. 2019;134:762.
29. Younes A, Brody J, Carpio C, Lopez-Guillermo A, Ben-Yehuda D, Ferhanoglu B, et al. Safety and activity of ibrutinib in combination with nivolumab in patients with relapsed non-Hodgkin lymphoma or chronic lymphocytic leukaemia: a phase 1/2a study. Lancet Haematol. 2019;6:e67-78.
30. Armand Philippe,Janssens Ann,Gritti Giuseppe et al. Efficacy and safety results from CheckMate 140, a phase 2 study of nivolumab for relapsed/refractory follicular lymphoma.[J].Blood, 2021, 137: 637-645.
31. Advani R, Flinn I, Popplewell L, Forero A, Bartlett NL, Ghosh N, et al. CD47 Blockade by Hu5F9-G4 and rituximab in non-hodgkin’s lymphoma. [J].N engl J Med United States. 2018;379:1711–21.
32. Morschhauser F, Flinn IW, Advani R, Sehn LH, Diefenbach C, Kolibaba K, et al. Polatuzumab vedotin or pinatuzumab vedotin plus rituximab in patients with relapsed or refractory non-Hodgkin lymphoma: final results from a phase 2 randomised study (ROMULUS). [J].Lancet Haematol. 2019;6(5):e254–65.
33. Hamadani M, Radford J, Carlo-Stella C, et al. Final results of a phase 1 study of loncastuximab tesirine in relapsed/refractory B-cell non-Hodgkin lymphoma. [J]. Blood. 2021 May 13;137(19):2634-2645.
34. Coiffier B, Osmanov EA, Hong X, Scheliga A, Mayer J, Offner F, et al. Bortezomib plus rituximab versus rituximab alone in patients with relapsed, rituximab-naive or rituximab-sensitive, follicular lymphoma: a randomised phase 3 trial. [J].Lancet Oncol.2011;12:773–84.
35. Zinzani PL, Khuageva NK, Wang H, Garicochea B, Walewski J, Van Hoof A, et al. Bortezomib plus rituximab versus rituximab in patients with high-risk, relapsed, rituximab-naïve or rituximab-sensitive follicular lymphoma: subgroup analysis of a randomized phase 3 trial. [J]. J Hematol Oncol. 2012;5:67.
36. Julia Edith,Salles Gilles,EZH2 inhibition by tazemetostat: mechanisms of action, safety and efficacy in relapsed/refractory follicular lymphoma.[J].Future Oncol, 2021, 17: 2127-2140
