
作者:蓝鲸晓虎
本文为作者授权医脉通发布,未经授权请勿转载。
 异基因造血干细胞移植(allo-HSCT)通常是各种血液病患者唯一的治愈希望,尤其是侵袭性或晚期血液恶性肿瘤患者。急性移植物抗宿主病(aGVHD)是allo-HSCT后的常见并发症。人类白细胞抗原(HLA)全相合的allo-HSCT中aGVHD的发生率约为30%-50%。aGVHD在单倍体相合和匹配的非亲缘供者移植中也很常见。
异基因造血干细胞移植(allo-HSCT)通常是各种血液病患者唯一的治愈希望,尤其是侵袭性或晚期血液恶性肿瘤患者。急性移植物抗宿主病(aGVHD)是allo-HSCT后的常见并发症。人类白细胞抗原(HLA)全相合的allo-HSCT中aGVHD的发生率约为30%-50%。aGVHD在单倍体相合和匹配的非亲缘供者移植中也很常见。
aGVHD的发生机制
1966年,Billingham将GVHD发病的生物学过程分为三个阶段:
a)移植物/供体含有具有免疫活性的细胞;
b)受体/宿主具有供体细胞中不表达的组织抗原;
c)受体无法产生免疫应答以有效消除供体细胞。
因此,在allo-HSCT期间,对受者进行预处理后,组织抗原表达至供体T细胞,导致供体T细胞活化、表达和对宿主的免疫应答增强,即发生aGVHD。
aGVHD中组织损伤的潜在机制是大量炎性细胞因子分泌,可观察到促炎细胞因子肿瘤坏死因子(TNF)-α、白细胞介素(IL)-1β和IL-6及抗原呈递细胞上模式识别受体的表达增加。


GVHD发病机制的三个环节(APC,抗原呈递细胞;DC,树突状细胞;LPS,脂多糖;TCR,T细胞受体)
GVHD的临床表现
为简便起见,临床上可以100天为临界将GVHD分类为“急性”和“慢性”。
值得注意的是,对于接受降低强度预处理(RIC)的allo-HSCT或供体淋巴细胞输注(DLI)后的患者,在数月后仍可发生aGVHD。因此美国国立卫生研究院(NIH)共识标准将GVHD分为4个亚类(表1):
表1 GVHD的4个亚类(根据NIH共识标准)

根据改良Glucksberg标准,将急性GVHD的严重程度分为I-IV级(表2):
表2 aGVHD的临床表现、分期和分级

GVHD的风险因素
-
供体-受体的主要组织相容性复合体(MHC)位点匹配,如HLA I类(HLA-A、-B和-C)和II类(HLA-DR、-DP和-DQ)。HLA-A、-B、-C或-DRB1(以及可能的-DQ和-DP)的错配增加了GVHD的风险并影响其严重程度,并对生存期产生负面影响;
-
供者干细胞来源:与骨髓干细胞相比,外周血干细胞(PBSCs)具有更高的GVHD风险,而脐带血细胞可能降低风险;
-
T细胞剂量:与T细胞补充移植物相比,移植物中CD3+ T细胞减少2-3个对数级可有效降低急性GVHD发生率。然而,T细胞耗竭增加移植物衰竭、机会性感染和疾病复发的风险,因此目前不支持泛T细胞耗竭治疗。
-
其他风险因素包括:供体和受体年龄、性别不匹配、供者捐赠次数、受者疾病分期和预处理强度。
aGVHD的预防
GVHD预防对于接受allo-HSCT的患者至关重要,最重要的环节是通过供体选择和预处理方案将风险因素降至最低。欧洲血液和骨髓移植工作组提出了GVHD预防指南。
钙调磷酸酶*制剂抑**和甲氨蝶呤是预防性治疗的主要支柱。经典的GVHD预防手段是环孢素+短疗程甲氨蝶呤联合治疗,与单用任一药物相比显示生存期改善。环孢素和他克莫司均可降低T淋巴细胞的增殖。在降低aGVHD风险方面,他克莫司+甲氨蝶呤优于环孢素+甲氨蝶呤,尤其是在非亲缘HSCT中。上述两种方案均被认为是大多数GVHD预防策略的基石。
预防方案1 钙调磷酸酶*制剂抑**+甲氨蝶呤
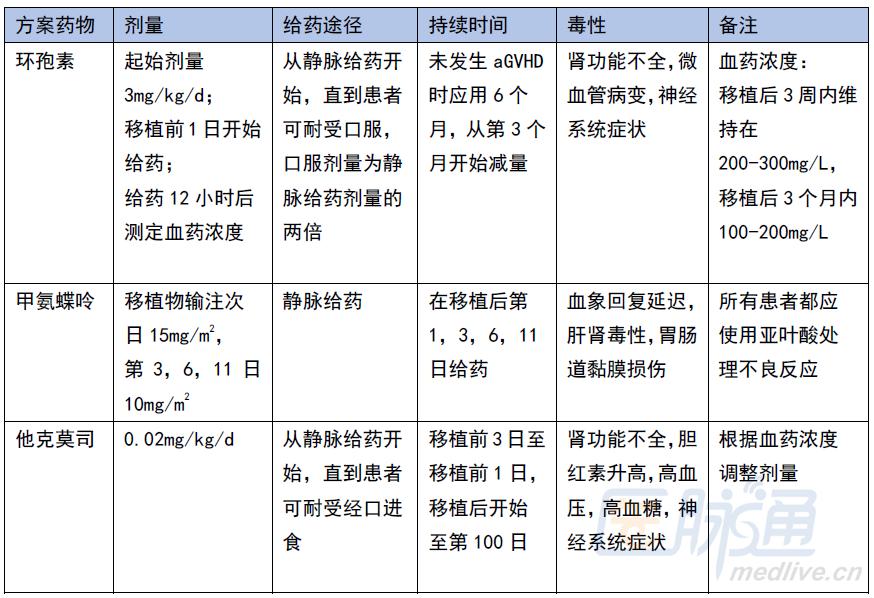
预防方案2 吗替麦考酚酯+钙调磷酸酶*制剂抑**

aGVHD的治疗
aGVHD的治疗选择取决于受累器官、症状的严重程度和移植前的预防方案。
外用激素是I级aGVHD针对皮肤表现的最常见治疗,也可给予抗组胺药。
II-IV级aGVHD的初始治疗包括高剂量糖皮质激素。激素治疗对约半数的患者有效,通常以1-2mg/kg/d的泼尼松当量开始治疗,在GVHD症状和体征减轻后逐渐减量。使用激素前5日无应答患者的移植相关死亡率较高。
对于其他抗排异药物,麦考酚酯与依那西普等联合激素获得了最佳完全缓解率。JAK1/2*制剂抑**芦可替尼在激素难治性aGVHD中取得了相当大的成功,被美国食品药品监督管理局批准用于aGVHD的治疗。
体外光分离术(ECP)、吗替麦考酚酯、西罗莫司、依维莫司、利妥昔单抗和伊布替尼是cGVHD的二线治疗选择。ECP被推荐用于治疗激素抵抗型aGVHD,总缓解率为50%-65%。
下表简要总结了目前激素难治性aGVHD的新型二线疗法。
表3 当前aGVHD的部分新型二线治疗策略汇总

参考文献
1. Aladağ E, Kelkitli E, Göker H. Acute Graft-Versus-Host Disease: A Brief Review. Turk J Haematol. 2020 Feb 20;37(1):1-4.
2. Nassereddine S, Rafei H, Elbahesh E, Tabbara I. Acute Graft Versus Host Disease: A Comprehensive Review. Anticancer Res. 2017 Apr;37(4):1547-1555.
3. Mistrik M, Bojtarova E, Sopko L, Masakova L, Roziakova L, Martinka J, Batorova A. Graft-versus-host disease management. Bratisl Lek Listy. 2016;117(7):388-96.
4. Appelbaum FR. Maintenance therapy after allogeneic hematopoietic cell transplantation for acute myeloid leukemia. Best Pract Res Clin Haematol. 2019 Dec;32(4):101109.
5. Baron F, Mohty M, Blaise D, Socié G, Labopin M, Esteve J, Ciceri F, Giebel S, Gorin NC, Savani BN, Schmid C, Nagler A. Anti-thymocyte globulin as graft-versus-host disease prevention in the setting of allogeneic peripheral blood stem cell transplantation: a review from the Acute Leukemia Working Party of the European Society for Blood and Marrow Transplantation. Haematologica. 2017 Feb;102(2):224-234.
6. Bittenbring J, Reichrath J. Extracorporeal Photopheresis for Non-skin GVHD. Anticancer Res. 2016 Mar;36(3):1395-6.
