
2019年10月19-23日,第27届欧洲消化疾病周(UEW week)在西班牙巴塞罗那隆重召开。
这场一年一度的学术会议,是由欧洲胃肠病*联学**合组织(UEG)主办,是欧洲最有影响力的综合性消化病学会议,近年参会者约1.3万人。
UEGW会议内容广泛,涉及多种消化系统疾病,大量最新的临床研究的结果在此次会议公布。
在炎症性肠病(IBD)领域,公布了三项维多珠单抗治疗治疗克罗恩病(CD)和溃疡性结肠炎(UC)大型多中心研究结果,引起广泛关注和讨论。

摘要一:维多珠单抗可能不影响后续抗-TNF药物治疗炎症性肠病的疗效
摘要编号:P1091

研究背景:对于溃疡性结肠炎(UC)或克罗恩病(CD)患者,一线使用维多珠单抗 (Vedolizumab)治疗后,是否会影响后续再使用抗-TNF药物的疗效,需要真实世界数据来回答这个问题。
研究目的:在UC或CD患者中,比较一线使用维多珠单抗之后再二线使用抗-TNF药物的疗效,与一线使用抗-TNF药物是否有区别。
研究方法:这是一项成年(≥18岁)UC和CD患者的真实世界、多国回顾性研究,由加拿大、希腊和美国多个医疗中心合作完成。
在2014年5月-2018年3月,接受抗-TNF药物一线治疗的患者,或一线使用维多珠单抗治疗但由于任何原因停用后接受抗-TNF药物二线治疗的患者,纳入此研究。
抗TNF药物包括:阿达木单抗、英夫利西单抗、戈利木单抗和塞妥珠单抗。
分析一线抗-TNF启动/维多珠单抗治疗后二线抗-TNF药物启动,随访6个月的临床有效性数据。
使用Kaplan-Meier方法,评估UC和CD患者一线或二线使用抗-TNF药物超过6个月累积临床应答和临床缓解率。
通过预设分层,评估临床应答和临床缓解的累积率。使用对数秩检验生成P值。
研究结果:该研究纳入了36家医院的579名接受抗-TNF药物治疗的患者。
其中497例患者一线使用抗-TNF药物(UC 224例; CD 273例); 82例患者在维多珠单抗停药后二线使用抗-TNF药物(UC 58例; CD 24例)。
不同抗-TNF药物在两个队列(1线和2线)中的占比如下
-
阿达木单抗(1线:41.4%;2线:19.5%)
-
英夫利西单抗(1线:52.7%;2线:79.3%)
-
戈利木单抗(1线:4.8%;2线:1.2%)
-
赛妥珠单抗(1线:0.8%;2线:0.0%)
抗-TNF药物1线和2线队列,患者人口学和病史特征如下:
-
平均年龄:1线39.6岁;2线49.4岁
-
男性占比:1线49.9%;2线61.0%
-
中位病程:1线2.0年;2线3.7年
在1线或2线抗-TNF药物开始治疗6个月时,两组患者的疗效数据如下:
-
持续治疗率(1线:83.9%; 2线:83.6%)
-
临床应答率(1线:49.5%; 2线:65.6%)
-
临床缓解率(1线:29.5%; 2线:31.4%)
因此,CD和UC患者1线接受抗-TNF药物治疗,和维多珠单抗停药后2线使用抗-TNF药物,6个月的疗效相似(见下表)。
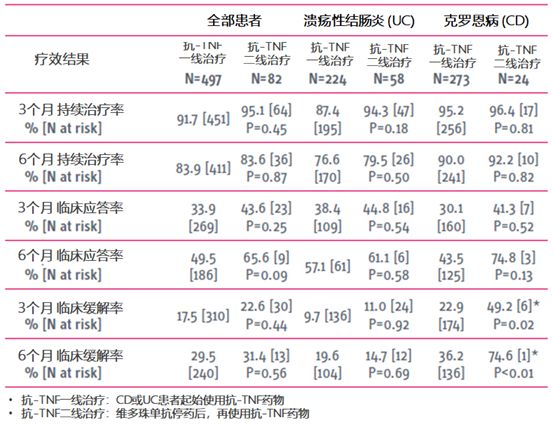
当进一步分层分析UC和CD患者时,尽管样本量较小,仍得到相同的结果。
研究结论:
IBD患者一线使用维多珠单抗停药后转为二线抗-TNF药物治疗,6个月的持续治疗率、临床应答和临床缓解率,与一线直接使用抗-TNF药物疗效相当。
这表明在真实世界中, CD和UC患者一线使用维多珠单抗可能不会影响后续抗-TNF药物的有效性 。

摘要二:真实世界生物制剂初治IBD患者使用维多珠单抗和抗-TNF药物的安全性比较
摘要编号:OP005

研究背景:GEMINI系列III期临床试验表明,维多珠单抗(VDZ)在治疗中度至重度活动性溃疡性结肠炎(UC)和克罗恩病(CD)的患者具有良好的安全性。
在真实世界中,需要比较维多珠单抗和抗-肿瘤坏死因子(anti-TNF)药物的安全性。
研究目的:在真实世界中,对于之前未使用过任何生物制剂的UC或CD患者,比较维多珠单抗和抗-TNF药物的安全性。
研究方法:这是一项多国多中心回顾性研究,纳入2014年5月至2018年3月之间接受维多珠单抗或抗-TNF药物 (阿达木单抗、英夫利西单抗、戈利木单抗、赛妥珠单抗)治疗,且之前未接受过任何生物制剂治疗的CD和UC成年患者,随访≥6个月。
收集开始维多珠单抗或抗-TNF药物开始治疗后,发生的严重不良事件(SAE)和严重感染(SI)事件。
严重不良事件定义为:威胁生命、需要入院、导致严重的残疾/失能,或在医疗记录中的重要的医疗事件。
分析患者严重不良事件(SAE)和严重感染(SI)的发生率(每100患者-年[PYs])。
根据患者基线特征,使用校正的Cox比例风险模型来比较维多珠单抗和抗-TNF药物队列之间,SAE和SI的发生率。并报告了校正后的风险比(HR)。
研究结果:这项研究纳入42家医院的1,095例患者,其中接受维多珠单抗治疗的患者598例 (UC 380例; CD 218例);接受抗-TNF药物治疗的患者497例 (UC 224例; CD 273例)。
患者基线特征显示,与抗-TNF药物患者相比,维多珠单抗的患者:
-
平均年龄更大(47.9岁 vs 39.6岁, p<0.01)
-
男性比例更高(56.9% vs 49.9%, p=0.02)
-
中位病程较长(5.0年 vs 2.0年, p<0.01)
患者中位随访时间,维多珠单抗患者随访15.3月,抗-TNF药物患者随访16.3月。
随访期间,患者严重不良事件(SAE)的发生率 (每100患者-年):维多珠单抗为4.6 [3.5-6.8],抗-TNF药物为10.3 [9.5-14.9]
严重感染的发生率 (每100患者-年)::维多珠单抗为2.6 [1.9-4.4],抗-TNF药物为7.0 [5.9-10.2]
Cox比例风险模型,维多珠单抗严重不良事件和严重感染的发生风险,显着低于抗-TNF药物(校正后HR: SAE=0.42 [0.27-0.66],SI=0.33 [0.18-0.58])。
分别对UC和CD患者进行分层分析,也显示出相似的趋势。
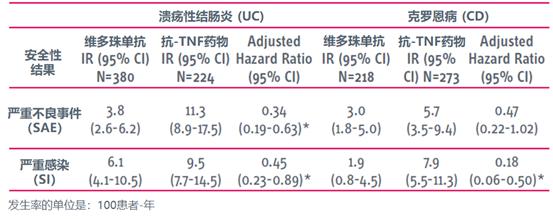
此外,抗-TNF药物的胃肠道(GI)感染患者比例,也显著高于V维多珠单抗(4.4% vs 1.5%,p<0.01)。
研究结论:
与抗-TNF药物相比,之前未使用过生物制剂的CD和UC患者, 使用维多珠单抗发生严重不良事件和严重感染(包括胃肠道感染)的可能性要低得多。
这些数据支持在现实世界的临床实践中,维多珠单抗在生物制剂初治的IBD患者中比抗-TNF药物具有更好的安全性。

摘要三:炎症性肠病患者妊娠期间使用维多珠单抗或乌司奴单抗没有发生严重新生儿和产妇并发症
摘要编号:OP010

研究背景:炎症性肠病(IBD)在育龄期的发病率很高。
维多珠单抗(Vedolizumab)和乌司奴单抗(Ustekinumab)是目前用于IBD治疗的新型生物制剂,其在怀孕期间使用的安全性数据较少。
研究目的:GETAID研究联盟中进行了一项回顾性多中心研究,收集了IBD女性病例资料,这些女性在怀孕期间或受孕前的最后两个月,至少接受过一次维多珠单抗或乌司奴单抗治疗。
研究目的:1. 评估妊娠期间接受维多珠单抗或乌司奴单抗的IBD女性患者,妊娠和新生儿结局;2. 观察维多珠单抗或乌司奴单抗停药,对怀孕期间和产后IBD疾病活动的影响
研究结果:GETAID研究联盟的19个中心参与这项研究,纳入62名IBD女性的67次妊娠数据,其中克罗恩病患者43例,溃疡性结肠炎患者19例,中位年龄29岁
接受乌司奴单抗期间按发生了25例怀孕,7例受孕前最后2个月内用药,11例怀孕后接受了1剂,7例在第二孕期前停药。
所有25例怀孕患者中,22例(88%)活产,1例选择性妊娠终止,2例自然流产。有2例患者出现妊娠并发症(1例妊娠糖尿病、1例早产征兆)。
胎儿和新生儿方面,3例发生胎儿妊娠并发症(子宫内生长受限),4例新生儿出现非严重新生儿并发症(3例早产,1例出生低体重)和1例法洛四联症(TOF)。
接受维多珠单抗治疗期间发生怀孕42次:15例受孕前最后2个月内用药,16例受孕后接受了1剂,11例在孕期停止(6例第二孕期,5例第三孕期)。
所有42例怀孕患者中,36例(86%)活产,1例选择性妊娠终止(唐氏综合征),5例(12%)自然流产。5名产妇出现并发症(1例胆汁淤积,4例先兆子痫)。
胎儿和新生儿方面,1名发生胎儿并发症(子宫内生长受限),13例新生儿出现非严重并发症(6例早产,6例出生低体重、1例先天性胼胝体发育不全)。
关于孕/产妇的IBD疾病活动,有65%的妇女在受孕时已缓解,只有2例患者在怀孕期间复发。
研究结论:
在维多珠单抗或乌司奴单抗暴露下的67例妊娠女性IBD患者中,没有发生严重的新生儿和产妇并发症(不包括心脏畸形)。
对于直接暴露于维多珠单抗或乌司奴单抗女性患者的妊娠结局,还需要更多前瞻性安全性评估。
