本文来自微信公众号:X-MOLNews副标题:烯烃与脂肪族胺的分子间不对称烯丙基C-H键胺化
脂肪胺普遍存在于天然产物、药物分子和其它生物活性分子中,其中烯丙基胺是一种特别有吸引力的合成目标(图1A)。近些年来,科学家开发了许多构建脂肪族烯丙基胺的方法,例如:1)预*能官**团化烯烃的亲核取代反应(图1B,左上),但通常会伴随双烯丙基化等问题;2)Pd催化的Tsuji-Trost反应(图1B,左下);3)钯催化的烯丙基C-H键胺化反应(图1B,右上);4)光催化和电催化的烯丙基C-H键胺化反应。尽管如此,但因选择性、亲核试剂的种类以及烯烃空间位阻等多方面的因素严重阻碍了脂肪族烯丙基胺的构建,尤其是脂肪族伯/仲胺以及医药上有价值的杂环(如:哌啶和哌嗪)作为亲核试剂,因此直接实现不同取代型烯烃的烯丙基胺化反应仍然是一个重大挑战。
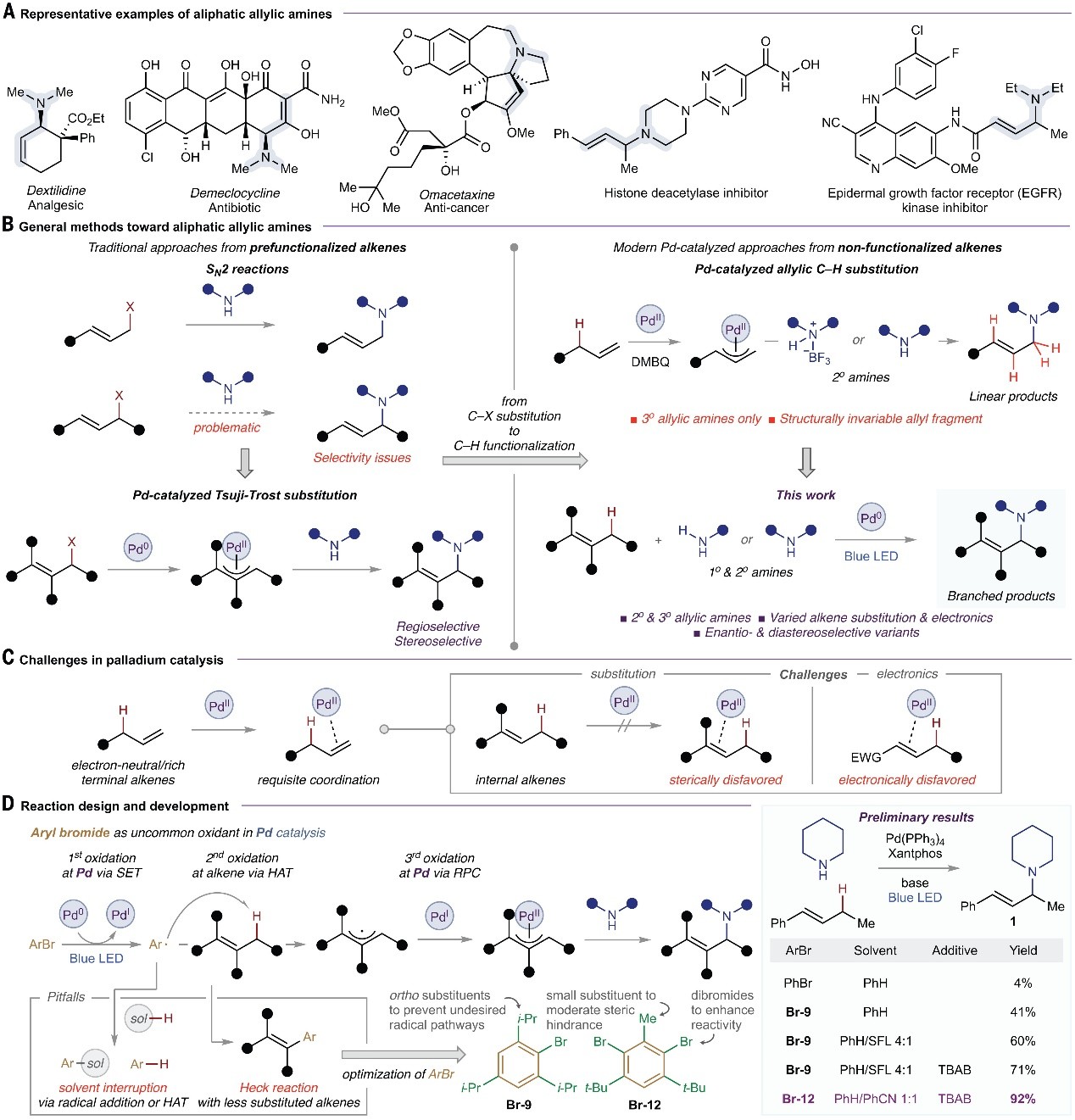
图1. 反应设计和发展。图片来源: Science
为了解决上述局限性,美国 德克萨斯大学达拉斯分校 的 Vladimir Gevorgyan 教授课题组重新审视了经典的Pd(II/0)催化过程(图1C),发现其主要挑战均来源于Pd(II)催化剂,具体而言:1)Pd(II)与内部烯烃的配位效率低,钯催化仅适用于位阻较小的单取代烯烃;2)Pd(II)盐易与Lewis碱性脂肪族胺(特别是伯胺)结合导致催化剂失活。鉴于Gevorgyan课题组在2016年利用光催化生成的杂芳基Pd(I)自由基实现了脂肪族C( sp 3)-H位点的分子内氢原子转移过程( J. Am. Chem. Soc ., 2016 , 138 , 6340-6343),并且芳基和脂肪族C-H键之间存在巨大的键解离焓(BDE)能量差,在热力学上有利,因此作者试图利用上述驱动力来实现烯丙基C-H键断裂的均裂模式,进而替代Pd(II)-烯烃配位作用的异裂模式。近日,他们 在温和芳基溴化物的体系中,利用光诱导电子转移形成多功能Pd(I)中间体的策略,开发了一种用于不同取代的烯烃与伯/仲脂肪族胺的分子间烯丙基C-H键胺化的光催化通用平台 (图1B,右下), 而且还成功地实现了多种烯烃的对映和非对映选择性烯丙基C-H键胺化。 其具体过程如下(图1D):首先,第一次氧化是在金属中心进行的光诱导单电子氧化过程(Pd0→PdI),随后通过分子间HAT过程氧化烯烃(第二次氧化),所形成的烯丙基-Pd(I)自由基中间体通过自由基-极*交性**叉在Pd上进行第三次氧化并形成经典的闭壳π-烯丙基Pd(II)配合物,再与脂肪族胺进行反应便可得到所需的C-H键胺化产物,同时将钯催化剂恢复到其原始氧化态进而完成催化循环。需要指出的是,Pd(0/I/II)循环在该反应中起了重要作用,并且Pd(I)中间体减弱了Lewis酸度,从而最大限度地减少了烯烃的异构化和与脂肪胺的相互作用。相关成果发表于 Science 上。
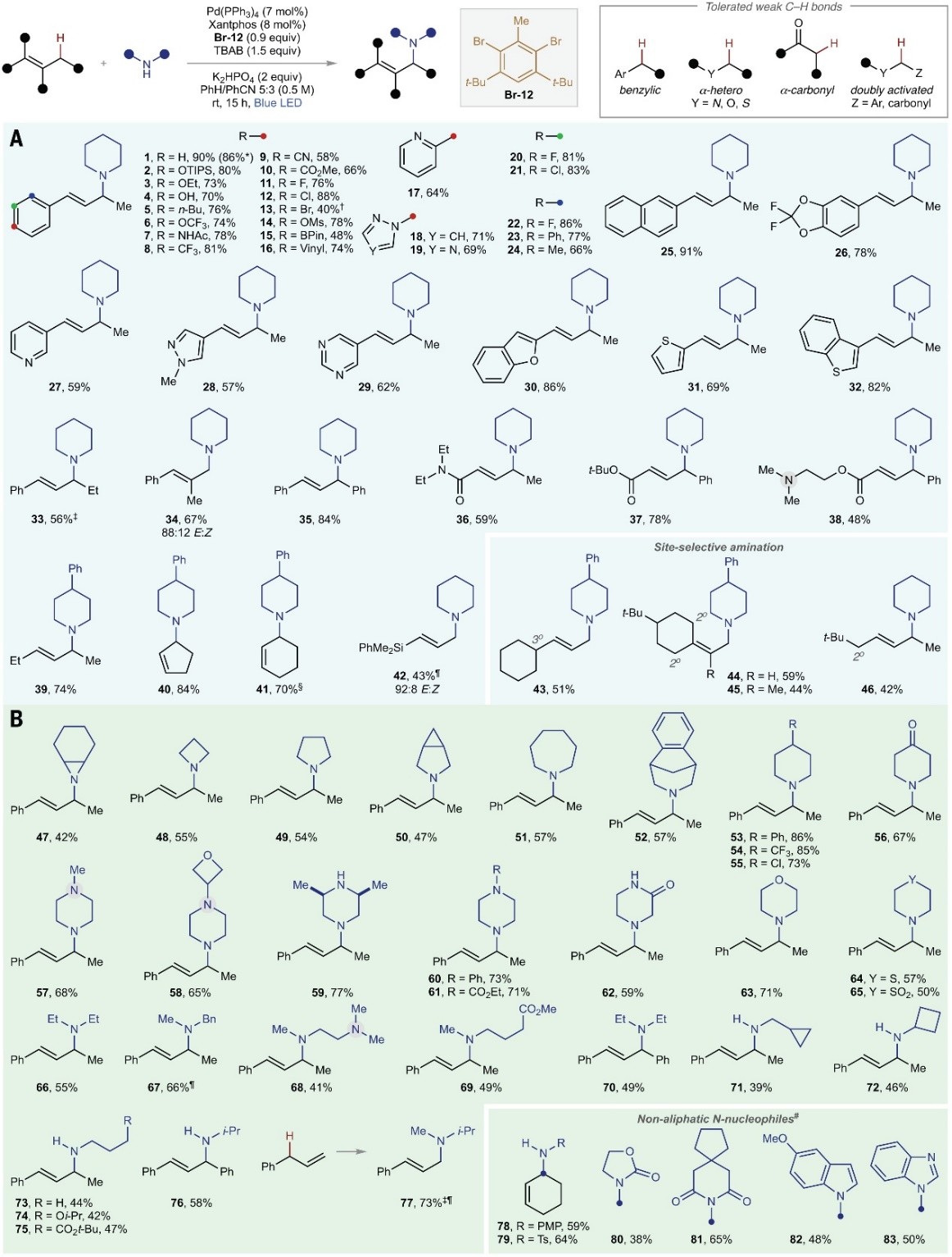
图2. 底物拓展。图片来源: Science
首先,作者选择( E )-β-乙基苯乙烯和哌啶为模型底物对反应条件进行了优化(图1D),初步研究表明在(PPh3)4/Xantphos、溴苯和碳酸铯的条件下用蓝色LED照射15 h后,能以4%的产率获得烯丙基胺 1 以及联苯和Heck副产物。为此,作者对芳基溴化物进行筛选并发现 Br-9 可将产率提高至41%,并且采用极性介质以及四丁基溴化铵(TBAB)作为添加剂后可以71%的产率获得产物。进一步研究发现 Br-12 (可由市售1,3-二叔丁基-5-甲基苯的Friedel-Crafts溴化一步获得)是最有效的芳基溴化物,这是由于其中一个较大位阻的烷基被较小的甲基取代来补偿由空间位阻增加导致降低的反应性,并且 Br-12 骨架中两个溴原子提高了反应性和原子经济性。此外,对反应条件进行微调后可以90%的分离产率获得烯丙基胺 1 ,并且对照实验证明钯催化剂和可见光是必不可少的。值得注意的是,异构体β-乙基苯乙烯(2.8:1 E/Z )同样能以立体收敛的方式获得产物 1 。另外,作者并没有检测到哌啶的α-C-H键活化副产物,进而表明HAT过程主导了分子间化学选择性。
在最优条件下,作者对烯烃的底物反应进行了探索(图2A),结果显示苯环上带有不同取代基的烯烃( 2-26 )、杂芳基烯烃类似物( 27-32 )、其它烯烃变体(如:延伸烷基链( 33 )、甲基重排( 34 )、苯基取代( 35 )、Michael受体( 36-37 )、侧链带有叔脂肪胺( 38 ))甚至脂肪族烯烃( 39-42 )均能兼容该反应,以良好的产率获得相应产物,特别是 Br-12 的空间位阻阻碍了自由基添加至末端双键,进而有效地合成了苯乙烯衍生物 16 。对于含有不同烯丙基C-H位点的脂肪族烯烃而言( 43-45 ),该方法能够在更强的伯C-H键进行位点选择性胺化而非较弱但不易接近的叔/仲位点,相反,大多数分子间HAT反应优先针对较弱的C-H键。类似地,当底物中存在多个仲C-H位点且位阻不同时,在位阻较小的位置发生选择性胺化( 46 )。其次,作者对脂肪族胺的兼容性进行了探索(图2B),结果显示不同尺寸的环状胺( 47-62 ,包括:氮杂环丙烷、氮杂环丁烷、吡咯烷、氮杂环庚烷、哌啶、哌嗪及其衍生物)、吗啉( 63 )、硫代吗啉( 64-65 )、非环状仲胺( 66-70 )甚至伯胺( 71-76 )均可有效地进行选择性胺化反应,并以中等至较好的产率获得所需产物。类似地,各种非脂肪族氮亲核试剂( 78-83 ,例如:苯胺、磺胺、氨基甲酸酯、酰亚胺以及芳香族氮杂环)均是有效的亲核试剂。此外,该方法对于末端烯烃( 77 )同样有效,并且其是经典Pd(II/0)催化循环下烯丙基C-H键胺化的唯一底物。
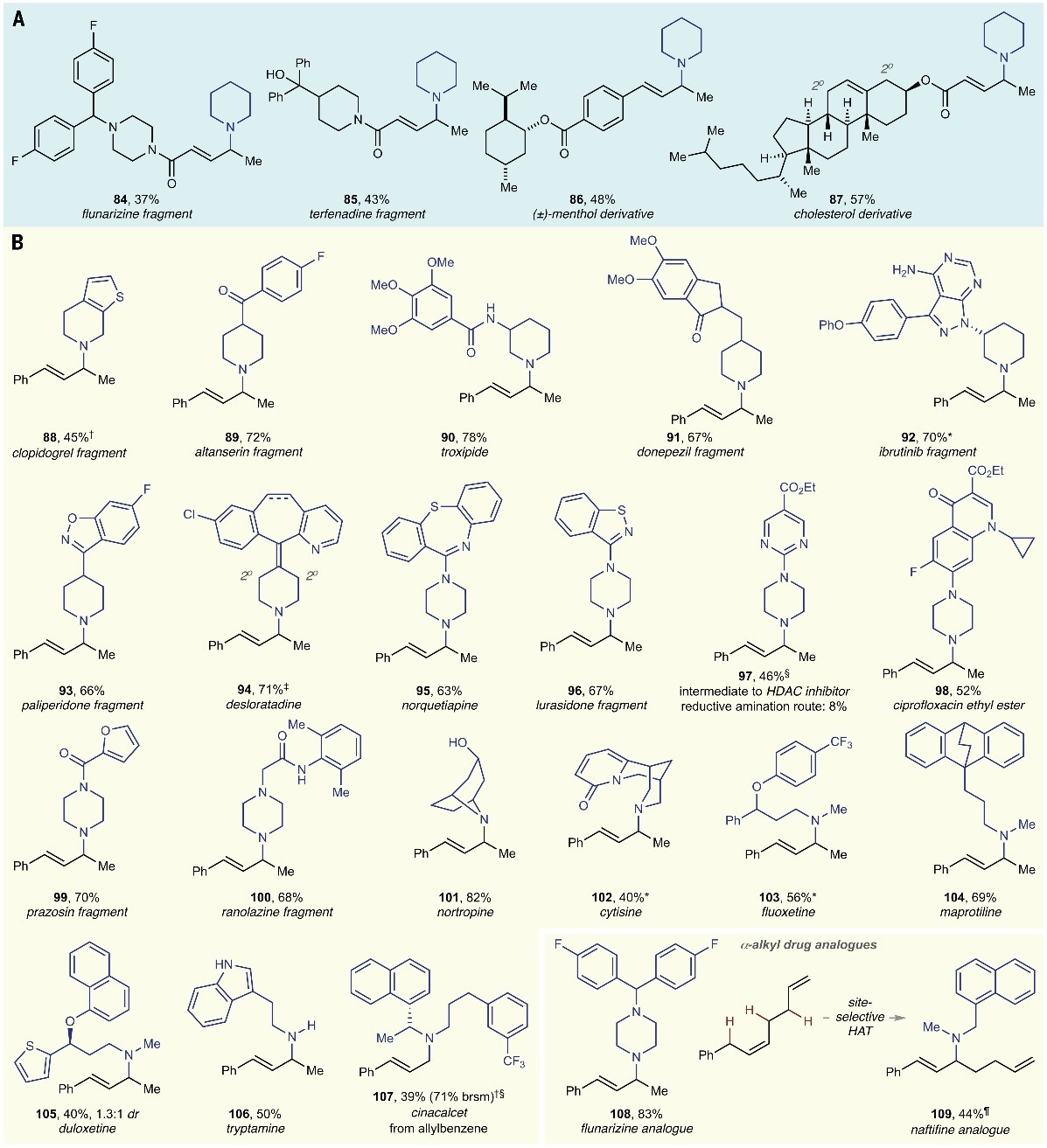
图3. 复杂胺类药物及其衍生物的合成。图片来源: Science
随后,作者利用该方法对复杂分子及其天然产物的后期修饰进行了探索。如图3A所示,多种药物片段和天然产物的衍生物均可顺利反应并获得相应的胺化产物( 84-87 )。鉴于哌啶和哌嗪骨架在医药领域具有广泛的应用,因此作者考察了一系列含有哌啶和哌嗪骨架的药物或其片段( 88-100 )作为亲核试剂发生烯丙基C-H键胺化反应,特别是组蛋白去乙酰化酶*制剂抑**的关键中间体 97 能以46%的产率合成,而传统还原胺化方法的产率仅为8%。进一步研究发现各种环状( 101-102 )和非环状活性胺( 103-107 )均能实现这一转化,同时还可获得药物制剂的α-取代类似物,例如:氟桂利嗪( 108 )和萘替芬( 109 ),其中后者是通过具有三个不同仲烯丙基C-H键的烯烃的位点选择性HAT获得的。
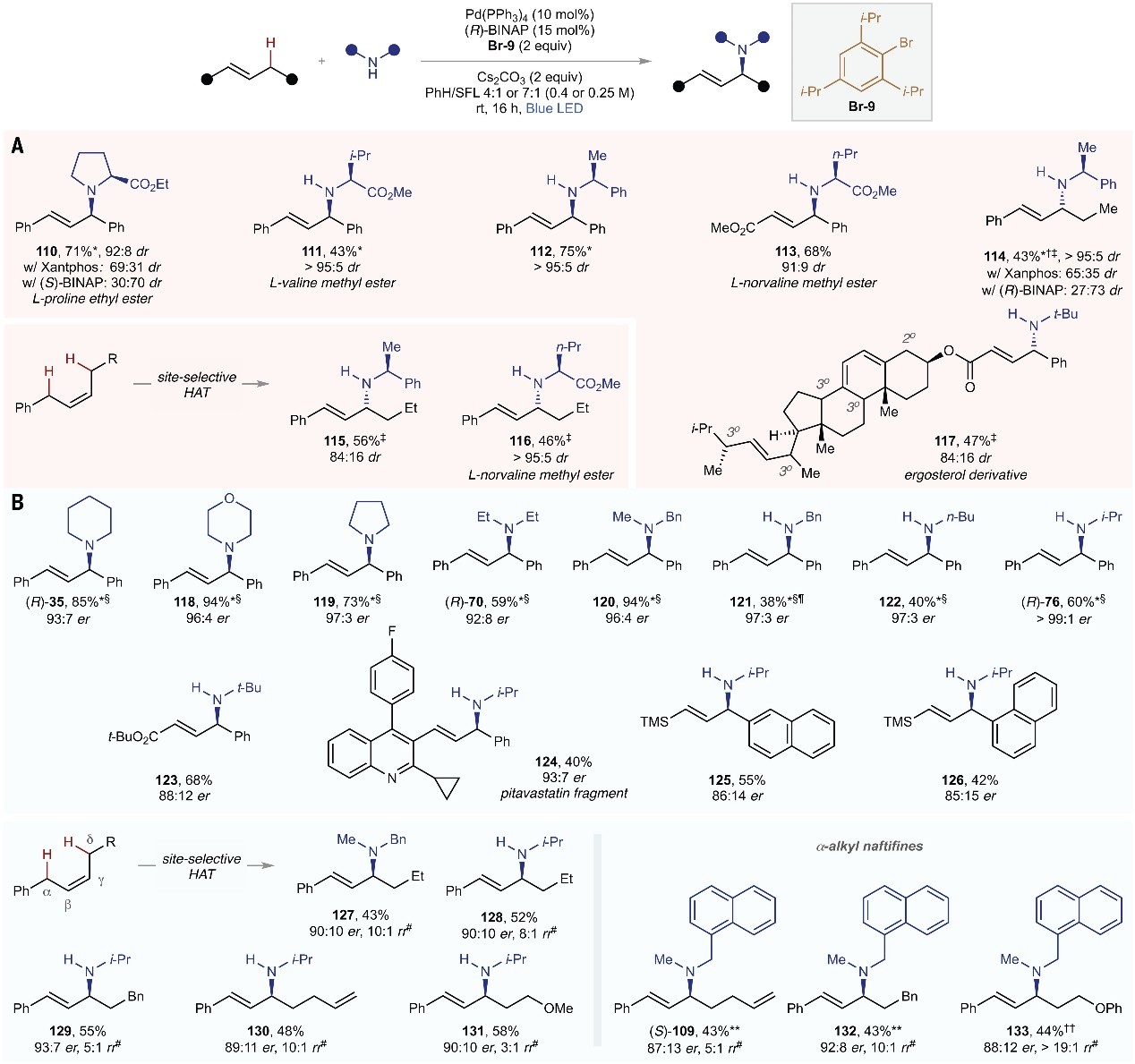
图4. 立体对映选择性的烯丙基C-H键胺化。图片来源: Science
最后,作者对该方法的手性版本进行了探索。对于非对映选择性反应而言,1,3-二苯基丙烯与手性脯氨酸酯在非手性Xantphos配体存在下可以较低的非对映选择性获得胺化产物 110 (图4A),而在Pd/( R )-BINAP催化体系下则能显著提高非对映选择性,并且( S )-BINAP可以较低的选择性获得另一个非对映体。此外,其它手性胺( 111-112 )对该体系同样有效。同时,在更具挑战性的情况下,π-烯丙基钯(II)中间体( 113 )也获得了良好的立体选择性,特别是这些产物( 110-113 )氮原子的α-位均具有芳基,并且类似的烷基取代产物 114 也可通过该方法获得。值得一提的是,该方法还可以实现含有多个烯丙基C-H键的烯烃底物的位点和非对映选择性胺化反应( 115-116 ),并且麦角甾醇衍生物( 117 )也可通过该方法来获得。另一方面,作者研究发现对称取代的烯丙基底物可以优异的对映选择性获得手性烯丙基胺(如:( R )- 35 , ( R )- 70 , ( R )- 76 , 118-122 ),而非对称的烯丙基底物(如:酯基- ( 123 )、多取代杂芳基- ( 124 ) 和硅基 ( 125-126 ) 取代的底物)同样具有良好的对映选择性。除此之外,含有多个烯丙基C-H键位点的底物也可在烯烃的α-C-H键位点发生位点特异性HAT过程,并以高的对映选择性和良好的区域选择性获得相应的手性胺( 127-133 、( S )- 109 )。总之,上述结果证实了用单一催化剂将激发态自由基化学与基态不对称过程相结合的可行性。
总结
Vladimir Gevorgyan教授课题组在利用光诱导电子转移形成多功能 Pd(I)中间体的策略,开发了一种用于不同取代的烯烃与伯/仲脂肪族胺的分子间烯丙基C-H键胺化的光催化通用平台,还成功地实现了多种烯烃的对映和非对映选择性烯丙基C-H键胺化。该方法不仅条件温和、底物范围广、*能官**团耐受性好,而且对药物分子、天然产物及其衍生物的合成以及后期修饰均有很好的效果。
Asymmetric intermolecular allylic C-H amination of alkenes with aliphatic amines
Kelvin Pak Shing Cheung, Jian Fang, Kallol Mukherjee, Andranik Mihranyan, Vladimir Gevorgyan
Science , 2022 , 378 , 1207-1213. DOI: 10.1126/science.abq1274
(本文由 吡哆醛 供稿)