
9月8日到12日,欧洲肿瘤内科学会(ESMO)2017年会在西班牙首都马德里盛大召开。在这场一年一度的肿瘤领域盛宴上,新型口服多激酶*制剂抑**瑞戈非尼相关研究收获颇丰。今年5月,瑞戈非尼在中国正式上市,用于治疗既往接受过以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗VEGF治疗、抗EGFR治疗(RAS野生型)的转移性结直肠癌(mCRC)。也正因为如此,我国临床医生对瑞戈非尼在肠癌治疗上的最新进展极为关注。本文汇总了ESMO 2017上公布的瑞戈非尼肠癌相关的研究结果。
基础研究数据显示:瑞戈非尼联合抗PD1单抗有望用于CRC治疗(摘要号:1198P)
瑞戈非尼为作用于多靶点小分子酪氨酸激酶*制剂抑**(TKI),可干预肿瘤生长、血管生成及肿瘤免疫等过程。有研究数据显示,瑞戈非尼可延长肝癌、结直肠癌(CRC)患者的总生存期。目前,关于免疫治疗的探索性研究开展的如火如荼,本研究旨在通过基础研究手段评价瑞戈非尼单药或联合抗PD1抗体对CRC的疗效。
研究采用小鼠结肠癌细胞系CT26和MC38细胞,体外评估肿瘤细胞生长情况及免疫状态。
研究结果显示,瑞戈非尼和抗PD1抗体均可抑制MC38细胞的生长,当二者联合使用或先给予抗PD1抗体、后给予瑞戈非尼均可进一步显著提高药效。此外,瑞戈非尼可剂量依赖性的降低MC38和CT26细胞中肿瘤浸润巨噬细胞比例。
上述研究结果提示,瑞戈非尼联合抗PD1单抗用于CRC治疗值得进一步探索和研究。
II期临床研究结果:联合DCE-MRI和ctDNA可预测瑞戈非尼抗血管生成的疗效和作用持续时间(摘要号:116P)
瑞戈非尼对初治mCRC患者的疗效已被证实,但在临床实践中,亟需开展具有疗效预测性的生物标志物检测,以更好的对目标患者进行筛选。
该项II期临床研究对象为RAS 野生型mCRC患者。基线进行6~12针活检,如疾病稳定或进展2个月后再次活检。治疗前和治疗后15天行磁共振动态对比增强(DCE-MRI)。使用循环肿瘤DNA(ctDNA)评价容量转运常数(Ktrans)、EF和KEF(Ktrans*EF/100),数字PCR检测RAS克隆突变。
共有27例mCRC患者接受了MRI评价,每个患者选择1处靶病灶(其中肝脏25处、盆腔2处)。结果显示治疗后中位KEF下降58.2%,在23例可分析患者中(4例因毒性治疗≤1周期),70% (8/27)以上患者的KEF下降与2个月评价为疾病控制(DCR)相关。KEF下降与中位无进展生存期(PFS)(HR=0.24,p=0.03)和总生存期(OS)(HR ,p=0.02)、6个月PFS(43.8% VS 0%)相关。
在所有DCR患者中,PFS 5.6个月对比 4.2个月[HR 0.30, p=0.140],OS15.2个月对比5.8个月(HR 0.11, p=0.057)。KEF下降与再次活检组织中CD31下降有关(P=0.04)。8周后在ctDNA种RAS突变衰减与更好PFS(HR 0.21, p=0.01)和OS(HR 0.28, p=0.06)相关。瑞戈非尼疗效与低肿瘤fBV (4.5个月对比 10.6个月, p=0.03)和更低CD31标记微血管密度有关(4.3个月对比 8.9个月,P=0.02)。
该研究结论提示联合DCE-MRI和ctDNA可预测瑞戈非尼抗血管生成的疗效和作用持续时间。
CORRECT研究亚组分析结果:mCRC患者MSI状态与瑞戈非尼疗效不相关(摘要号:534P)
有研究证实,微卫星高度不稳定(MSI-H)的CRC患者预后相对较理想,然而越来越多的证据显示,晚期CRC 伴有MSI-H时患者对化疗的反应较差。本次更新的CORRECT III期临床研究亚组分析评价了瑞戈非尼用于mCRC的疗效与基线MSI状态的关系。
CORRECT研究为国际多中心、安慰剂对照III期临床研究,纳入既往标准治疗失败的mCRC患者760例,2:1随机分为瑞戈非尼160 mg/天组(用药3周停药1周)和安慰剂组。研究采用Cox比例风险模型和卡普兰-迈耶分析评估了不同MSI状态下mCRC患者OS和PFS及其与治疗之间的潜在相互作用。
在760例患者*共中**有229例接受了肿瘤组织标本检测,其中MSI-H患者42例(18%);非MSI-H患者187例(82%),男性占62%,ECOG评分为0和1的患者分别占57%和43%,58%的患者伴有KRAS基因突变,3%的患者伴有BRAF基因突变。
研究结果显示,虽然MSI-H亚组临床获益较少,但总体上MSI-H亚组和非MSI-H亚组OS和PFS无差异(P=0.15)。
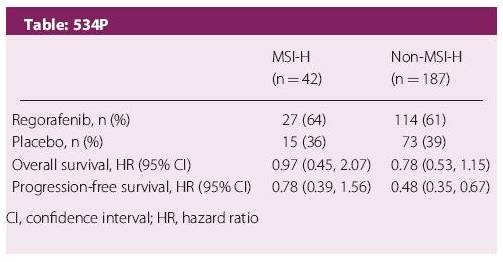
该项在CORRECT研究中部分mCRC患者中进行的分析结果显示,该亚组患者中MSI-H发生率15%~20%,MSI状态对瑞戈非尼疗效无影响。由于纳入的样本数较少,未来还需更多研究数据以进一步确定MSI状态与瑞戈非尼临床疗效的关系。
1b期临床研究结果:瑞戈非尼联合西妥昔单抗治疗晚期实体瘤未出现不可预期毒性(摘要号:380P)
瑞戈非尼联合西妥昔单抗可克服EGFR敏感和耐药肿瘤的原发和获得性耐药。该项1b期临床研究旨在评价瑞戈非尼联合标准剂量西妥昔单抗(开始剂量400mg/m2,后每周250 mg/m2)的安全性、药代动力学(PK)、最大耐受剂量(MTD)和初步疗效。本次报道展示了瑞戈非尼(用3周停1周)剂量组结果。
本研究为开放标签、剂量递增(3+3)设计,研究对象为标准治疗失败的局部晚期或转移性实体瘤患者。瑞戈非尼起始剂量为120 mg/天,用药3周停药1周,共4周期。如患者可耐受,剂量上调为160 mg/天;如不能耐受剂量下调为80 mg/天。治疗1周期后评价剂量限制性毒性(DLTs)。根据NCI-CTCAE 4.03版评价AEs,根据RECIST v1.1评价疗效。
截至2017年1月31日,共分析患者数据31例,其中瑞戈非尼120 mg组8例、160 mg组23例。在6例可评价的120 mg组患者中,1例出现DLTs(3级手足综合征);在160 mg剂量组未出现DLTs。MTD为瑞戈非尼标准剂量160 mg/天(用药3周停药1周)联合西妥昔单抗。
最常见AEs(不论与研究药物是否有关),包括低磷血症(42%)、乏力(39%)、恶心(39%)。瑞戈非尼相关≥3级AEs包括低磷血症(23%)、乏力(10%)。
瑞戈非尼AUC (0–tlast) 在160 mg剂量组为29.1 mg·h/L;在120 mg剂量组为17.4 mg·h/L。
西妥昔单抗对瑞戈非尼PK参数无影响。疗效评价结果显示PR 1例(120 mg组);SD 8例(160 mg组 6例,占29%;120 mg组2例,占25%)。
该研究结论指出,瑞戈非尼160 mg/天(用药3周停药1周)联合标准剂量西妥昔单抗未出现不可预期毒性。观察到的AEs与瑞戈非尼和西妥昔单抗既往报道基本一致。
Ⅱ期临床研究设计:瑞戈非尼120 mg/天用于标准治疗失败、不可切除mCRC的疗效和安全性(摘要号:613Tip)
为CRC患者制定合理治疗方案是世界性的研究课题。CORRECT研究纳入了包括日本在内的17个国家,结果显示瑞戈非尼较安慰剂显著延长OS。CORRECT研究共纳入760例患者,其中,日本患者100例。研究中采用的瑞戈非尼标准剂量为160 mg/天,并未根据患者身高、体重和种族等因素调整剂量。
为评价瑞戈非尼初始剂量120 mg/天用于mCRC患者的疗效和安全性,开展了此项多中心、单臂设计Ⅱ期临床研究。研究对象纳入标准为年龄≥20岁、伴有远端转移或局部晚期手术无法切除、标准治疗失败或标准治疗结束3个月之内出现疾病进展的CRC患者。标准化疗方案可包括氟尿嘧啶、奥沙利铂、伊立替康,贝伐珠单抗和抗EGFR单抗(如果RAS为野生型),患者应未接受过TAS-102治疗。瑞戈非尼剂量为120 mg/天,餐后使用,用药3周停药1周,4周为一周期,治疗直至疾病进展。
主要研究终点为DCR(≥6周);次要研究终点包括OS、PFS、ORR、安全性和治疗依从性。
Ⅱ期临床研究设计:不同瑞戈非尼诱导剂量(第一周期)治疗mCRC的安全性及治疗依从性(摘要号:610Tip)
瑞戈非尼为广谱多靶点TKI,具有抗血管生长、抗基质和抗增殖作用。在临床实践中,由于瑞戈非尼耐受性问题,可能导致减量或治疗中断,影响药物剂量强度和依从性。在CORRECT试验中,瑞戈非尼治疗相关毒性常发生在治疗前2周期。在1期剂量爬坡研究中,瑞戈非尼120 mg/天(用药3周停药1周),7例患者未出现剂量限制性毒性。另外一项瑞戈非尼与化疗联合CPRDIAL试验中,瑞戈非尼方案为160 mg/天用药一周停药一周。
本II期研究为评估瑞戈非尼剂量递增方案用于标准治疗失败mCRC患者的安全性及治疗依从性。患者1:1:1随机分组,组A:给予标准剂量的瑞戈非尼;组B:第一周期给予瑞戈非尼120 mg/天,用药3周停1周;组C:瑞戈非尼160 mg/天用药一周停药一周。组A和组B患者第1周期无毒性出现后瑞戈非尼剂量递增到标准剂量。
主要研究终点为不同剂量组的安全性。次要终点包括按计划完成患者的比例,治疗前2周期及整个治疗期间的剂量强度,DCR、PFS、治疗失败时间、OS。目前研究正在进行中,计划入组患者295例,截至2017年3月,已入组患者160例。