在《非酒精性脂肪肝: 饮食调整不一定减肥,运动不一定带氧》中,介绍了减肥可以改善脂肪肝,但不一定是先决条件;无论带氧运动还是阻力训练都可以改善脂肪肝,尽管体重可以不变。 调整宏量营养的比例,减少碳水特别是精制碳水对改善脂肪肝的效果最明显。
有人说我减肥了但脂肪肝还在,锻炼也见到减重效果,但脂肪肝没有离开,这些我都经历过。减肥和运动有效果的,只是可能不足以逆转冰封三尺的脂肪肝….. 这一篇会更为细致介绍:
1. 同样是碳水化合物,果糖对脂肪肝的影响更直接快速;
2. 但同样含果糖的水果,对脂肪肝却有改善作用;
3. 含抗性淀粉的全谷类跟精制碳水不一样,对改善脂肪肝有帮助;
4. 脂肪对脂肪肝的影响取决于是什么脂肪,饱和脂肪和欧米茄6脂肪加剧脂肪肝;
5. 欧米茄3和含多酚的橄榄油改善脂肪肝。
总之,饮食对健康的影响,不是碳水究竟50%好还是低于10%更健康,也不是生酮还是低脂肪对炎症更友好…. 因为devil is in details! 魔鬼在细节中!饮食的“质量”比宏量营养的比例,对健康的影响更大。
对研究细节不感兴趣的,对脂肪肝有帮助的饮食在总结有精简的建议。但魔鬼的确在细节里,你可能连体重没有改变的情况下,脂肪在肝脏都在快速积累……..
但一切从肠道先说起。
肠道菌群
肠道菌群影响脂肪肝的形成。 肠道细菌的代谢物,包括LPS等通过膳食脂肪,乳糜微粒等会运送到肝脏,造成肝脏的慢性炎症。而益生菌代谢产生的短链脂肪酸却可以减少肝脏分泌的致炎症细胞因子。[1]
肠漏也可能是NAFLD的风险因素,研究发现显示肠漏严重程度的连蛋白(Zonulin)跟NAFLD也存在正关系。[2]
首都医科大学等医院和研究机构2019年在《细胞》子刊发表的一项研究。[3] 研究学者从一个病例中发现有脂肪性肝炎患者出现自动酿酒综合征(Auto-brewery syndrome),也就是不喝酒但都出现喝酒后的症状,研究人员从患者的肠道中发现肺炎克雷白杆菌(Klebsiella pneumoniae,检测Kp), Kp是可以代谢碳水发酵酒精的细菌。研究人员之后分析了32名NASH患者的粪便,发现21名也有Kp细菌。研究通过移植Kp细菌到小鼠,证明Kp是可以导致脂肪肝的形成,效果跟酒精导致脂肪肝的发病机制类似。克雷伯菌对炎症的影响在《强直性脊柱炎: 基因与细菌共舞》也有介绍,有兴趣多了解的可以参考。
肠道细菌对肝脏造成类似酒精性影响可能只是脂肪肝发病机制的其中一个路径,肠道菌群对脂肪肝的影响在未来的研究中可能还会不断的新发现。这就不难理解为什么同样的宏量营养比例,因为对肠道菌群的影响不一样,对脂肪肝造成的压力也就不一样。
果糖和白糖加剧脂肪肝
高碳水饮食类的饮食对脂肪肝最不友好的,但当中的果糖可能对肝脏脂肪积累压力最大。 碳水化合物消化后会变成葡萄糖和其他单糖,葡萄糖会被吸收进入循环系统为我们提供能量,胰岛素负责调节血糖的高低,同时协助葡萄糖进入细胞作为能量的原料。果糖的代谢跟葡萄糖完全不一样,果糖不受胰岛素的调节,所以人体摄入果糖后胰岛素不会分泌,摄入果糖(少量在小肠和肾脏代谢)直接到达肝脏,经过磷酸果糖激酶代谢,但由于没有胰岛素的控制,磷化过程过度迅速,摄入的果糖很快便变成三脂甘油和脂肪储存在肝脏,引起脂肪肝和其他代谢有关疾病。
下面是哈佛大学和波士顿儿童医院在2016年发表的研究,[4]发现果糖比高脂肪饮食更容易造成脂肪肝,原理同样指向脂质新生。 汽水等含糖饮料的甜味来自果糖,含糖饮料是最容易造成脂肪肝的。

2015年另一项研究[5],8位受试者在18天试验当中,9天摄取大量的果糖,另外9天摄取的能量不变但用其他碳水化合物取代果糖。 喝果糖饮料的9天,受试者出现脂质新生反应,肝脏把多余的能量转化为脂肪储存。该项试验证明尽管摄入的热量和碳水化合物不变,果糖的摄入会引致脂肪肝的形成。
增加果糖加剧脂肪肝,减少果糖可以逆转脂肪肝。2017年发表的研究[6] ,41位8-18岁平日大量摄取果糖的肥胖(当中63%肝脏脂肪过多)儿童,在9天试验中被限制果糖摄取量(能量所需的4%),减少的卡路里用淀粉类食物取代,所以能量和总碳水化合物的摄取量没有变化。9天后受试者的肝脏脂肪减少,体脂也减少了,胰岛素抵抗降低,各项健康指标都有所改善。研究人员的结论是该项研究支持减少糖的摄取量。
2019年加州大学圣地亚哥分校的一项对照组临床研究,[7] 发现不需要改变整体饮食结构,只需要剔除含糖(白糖和果糖)的饮食和饮料(包括果汁)到>3% 卡路里,8周后受试的青少年的NAFLD都显著改善。
添加的糖,特别是果糖,比一般淀粉类饮食对脂肪肝的影响更大。戒糖和含糖饮料是最有效简单改善脂肪肝的方法。
水果改善脂肪肝
果糖对脂肪肝不友好,但水果却有助改善脂肪肝。2020年韩国的流行病学研究,[8] 分析了2130个NAFLD病例,发现水果和蔬菜可以减少NAFLD的风险约25%。分开计算,水果减少风险23% 而蔬菜减少29%。
2020年美国南加州大学的队列研究,[9] 也发现食用水果跟NAFLD有显著的反向关系,水果可以降低NAFLD的风险。
2017年西班牙发表的研究,[10] 70名肥胖的NAFLD受试者分成两组的卡路里限制(CR)饮食组接受试验,6个月干预后的结果显示,两组在宏量营养上类似,但膳食中较多水果的一组脂肪肝改善更为明显,研究解析含有丰富膳食纤维的水果可以显著改善肝功能。研究的结论是对于肥胖的NAFLD患者,设计卡路里限制饮食中考虑增加含膳食纤维的水果可能更有效果。下图发现水果的纤维越多,肝功能改善越大。
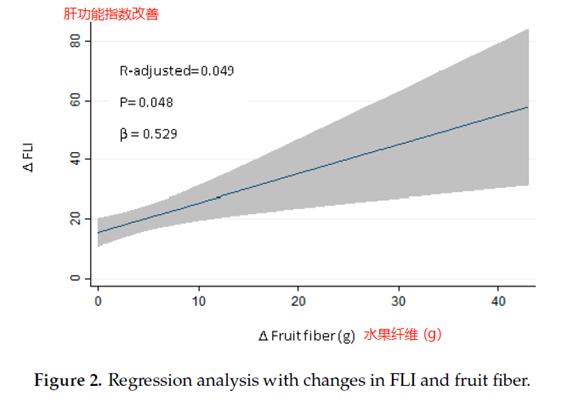
果糖不利脂肪肝,但水果却对脂肪肝有改善作用,因为水果含有膳食纤维和多酚类抗氧化物,这些对健康有益的物质,证明饮食的“质量”比简单化的宏量营养比例可能对脂肪肝更重要。
抗性淀粉改善脂肪肝
动物实验发现抗性淀粉可以减轻饮食对肝脏造成的脂肪积累压力,减少体重增加,逆转脂肪性肝炎。[11] 增加抗性淀粉促使动物增加缓解炎症的短链脂肪酸,减少肝脏甘油三酯。
天津科技大学在2019年对NAFLD的一项动物实验,[12] 发现肥胖的小鼠喂食不同份量的抗性淀粉,对改善身体代谢压力,包括NAFLD的效果更剂量有很大关系。 抗性淀粉显著减少肝脏重量和减少肝脏脂肪的积累,但只有中和大剂量的抗性淀粉能明显启动抗炎症细胞信号AMPK,也只有中等和大剂量的抗性淀粉可以改变肠道菌群的比例,有效改善肠道环境。从这个动物实验可以这样理解,抗性淀粉对NAFLD和肠道健康跟剂量有关,只有足够多的抗性淀粉才能产生明显效果。
2014年的对照组病例研究,[13]发现精制谷物碳水增加NAFLD风险,全谷物降低NAFLD风险。
2020年发表的临床研究,[14]112名肥胖的脂肪肝患者连续12周用全谷类食物取代一半的谷类淀粉食物,结果显示肝炎和肝酶都同样改善。研究解析全谷物对改善肝脏功能的作用起码部分应该来至改善肠道菌群包括增加短链脂肪酸(益生菌代谢物)而产生的。
2018年的临床研究也发现,[15] 增加膳食纤维,改善NAFLD患者的肝功能。32名NAFLD受试者连续6个月增加全麦面包、糙米饭和其他含膳食纤维饮食,从每天19g增加到每天29g,结果显示肝细胞损害的敏感指标:血清丙氨酸转氨酶(aspartate aminotransferase,ALT)和天冬氨酸转氨酶(aspartate aminotransferase,AST)等都显著下降,显示肝功能改善。研究解析,膳食纤维通过改善肠漏改善肝功能。
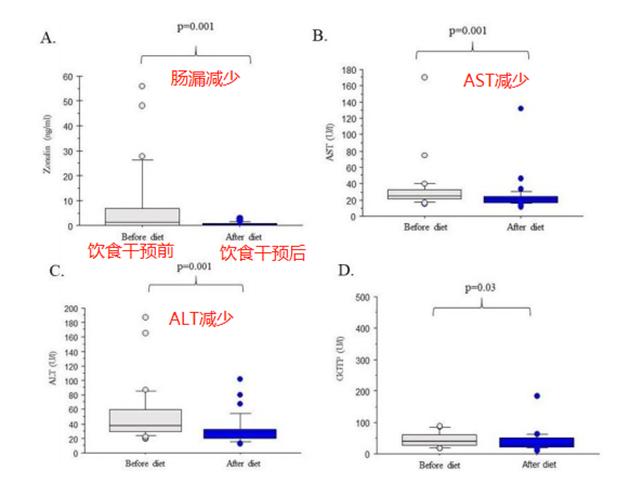
同样是主食类的淀粉食物,含抗性淀粉的全谷类可以改善脂肪肝,但当然不能过量,过多的卡路里无论什么食物,对脂肪肝都有害无益。用粗粮取代精粮是健康的做法。
脂肪的质量
饱和脂肪
2018年芬兰发表的一项临床试验,[16] 比较了增加膳食中的饱和脂肪,不饱和脂肪和碳水饮食对脂肪肝的影响。 38名肥胖的受试者连续3周每天增加进食1000卡路里的不同食物,1组增加饱和脂肪(30g椰子油,40g黄油和100g的芝士),2组增加不饱和脂肪(36g橄榄油,26g的松子油,54g的坚果,20g黄油),3组增加糖类的碳水化合物。结果显示,3组受试者在过量进食下,增加的体重大概都在1.2kg左右,不算太多。但无论什么饮食,增加卡路里都导致肝脏脂肪的增加,但饱和脂肪组增加的肝脏甘油三酯最多,大概55%,其次是糖类增加了33%,而不饱和脂肪增加了肝脏甘油三酯15%。
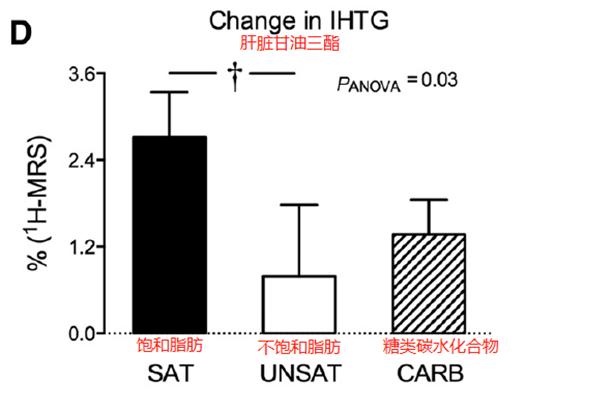
研究进一步分析,发现糖类对肝脏脂肪的影响正如之前的研究发现一样,是通过增加脂质新生活动,导致肝脏脂肪的产生和积累。
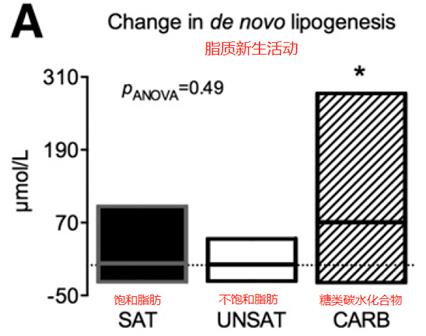
脂解作用(lipolysis)指脂脂肪从脂肪细胞组织外溢,脂肪细胞释放游离脂肪酸和甘油到血液中,在上一篇我们已经看到同位素跟踪发现脂肪外溢是导致脂肪肝的主要原因。 研究早就发现胰岛素抵抗是导致脂解作用活动增加的主要原因,正常情况下,胰岛素会压抑脂解作用,但当细胞的胰岛素敏感度下降,脂解作用便增加,血液中的游离脂肪酸也增加,导致肝脏脂肪积累。[17]
回到上述临床研究,发现增加饱和脂肪的摄入,同时增加致炎症细胞因子,脂解作用活动增加,血液中的游离脂肪酸同样增加,HOMA-IR胰岛素抵抗指数增加了23%。饱和脂肪通过增加炎症细胞因子,导致脂解作用的增加,释放游离脂肪酸到血液,最终导致肝脏脂肪的剂量。但该研究发现不饱和脂肪减少脂解作用活动。
2019年的一项双盲对照组临床试验,[18] 同样证实过多的饱和脂肪造成脂肪肝,受试者分为饱和脂肪组(SFA)和不饱和脂肪组(PUFA),连续8周增加脂肪食物,SFA组和PUFA组的体重分别增加了2.31kg和2.01kg,分别不大,但PUFA组的肝脏脂肪没有明显增加,但SFA组却增加了。之后4周的卡路里限制饮食可以逆转有关的代谢性指标。
饱和脂肪不利脂肪肝。
橄榄油不只是MUFA
橄榄油可以改善脂肪肝。[19][20] 特级初榨橄榄油(EVOO)中含有多种抗氧化物,但有部分多酚类抗氧化物是EVOO独有的,例如羟基酪醇(Hydroxytyrosol)和橄榄苦苷(oleuropein)。 [21] 动物实验发比较了普通橄榄油(MUFA)和含多酚橄榄油(EVOO)在NAFLD小鼠模型的作用,[22] 无论是普通的MUFA,还是含多酚类抗氧化的EVOO都可以减少肝脏脂肪的积累和一定程度改善血糖耐量和胰岛素抵抗,但EVOO在改善胰岛素抵抗的效果更明显,只有EVOO可以抗炎症和减少致炎症细胞因子,而MUFA效果却不明显。 炎症因子(TNF-A, IL-1,IL-6)导致胰岛素敏感度降低,增加内脏脂肪的积累。研究也发现EVOO可以增加脂肪氧化活动,减少ROS(减少H2O2产生)和有助线粒体电子传送链的解耦(decoupling)从而减少线粒体产生ATP过程中出现的ROS。上述作用只有含多酚的EVOO有,普通MUFA没有。
2019年的一项双盲对照组临床研,[23] 66名NAFLD患者接受试验,干预组服用每天20g的橄榄油,对照组服用葵花籽油,两组受试者都被建议每天饮食中减少500卡路里。12周后两组受试者的腰围、脂肪肝和血液都有改善,但只有橄榄油组显著改善了脂肪肝和体脂。 研究的结论是橄榄油无论是否改善心血管指标,都可能可以改善脂肪肝。
2018年的一项临床研究,[24] 同样发现12周使用EVOO配合限制卡路里饮食(CR),比单单进行CR更能改善AST和ALT等脂肪肝指标。
2014年的临床研究,[25] 干预时间更长,6个月使用橄榄油显著改善脂肪肝,减少BMI,改善胰岛素敏感度,HOMA-IR,减低三脂甘油。研究把受试者的NAFLD严重程度分3级,结果轻度的1级从73.3%减少到23.3%,次严重的2级,从20%减少到10%,而最严重的3级则从6.7%变为0。
2019年关于橄榄油的随机对照组临床研究可能最有指导意义,[26] 100名NAFLD受试者接受3年的地中海饮食干预试验。 同样是地中海饮食,包括每天60ml的EVOO橄榄油,相对减少脂肪补充坚果,和普通地中海饮食的2组,橄榄油组显著改善NAFLD,脂肪性肝炎比例只有8.8%,而普通地中海饮食组,和坚果低脂组的脂肪性肝炎比例都是33.3%。可圈可点的地方,该研究并没有限制受试者的卡路里摄入也没有增加运动量。
欧米茄3 vs 欧米茄6
n-3脂肪酸可以阻止脂肪在肝脏的积累,[27] 而膳食中缺乏n-3脂肪或n-6/n-3比例过高,都容易导致NAFDL。
多不饱和脂肪n-3和n-6都可以抑制Acetyl-CoA的载体CIC,多不饱和脂肪可以降低CIC的表达和活动,减少Acetyl-CoA从线粒体进入细胞,也就是可以减少脂质新生的活动,减少肝脏脂肪的积累。饱和脂肪和单不饱和脂肪都不具备有关的作用。[27]
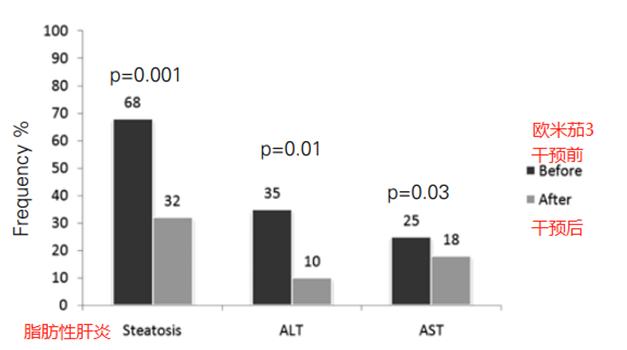
欧米茄3鱼油对改善儿童的脂肪肝有帮助,2015年的一项双盲对照组临床研究,[28] 108名平均年龄在13.8岁的肥胖青少年接受试验,干预组连续12个月每天1克的鱼油配合减少卡路里饮食和锻炼,对照组只进行限制卡路里饮食和锻炼,结果两组都改善了肝炎和脂肪肝,但鱼油组的改善比对照组显著。干预组中67.8%受试者的脂肪性肝炎改善, NAFLD指标ALT升高频率从39.2%降低到14.2%,而AST从25%降低到17.8%。
2020年中国台湾发表的荟萃分析,[29] 包括了22个临床研究一共1366名受试者,发现补充欧米茄3鱼油显著改善肝脏脂肪,同时改善胆固醇,BMI等代谢性指标。
2020年芬兰赫尔辛基大学发表的一项有趣的横断研究,[30] 分析了50对年龄在23-36岁的同卵双胞胎受试者,当中10对受试者的肝脏脂肪有显著分别,进一步分析这些受试者,发现肝脂肪高的受试者的n-6/n-3脂肪比例更高,6.6对3.2,研究的结论是调整饮食中n-6/n-3比例可能可以改善脂肪肝。这个研究可能告诉我们不要埋怨基因问题,更多是饮食和生活习惯问题。
意大利2018年发表的一项对照组临床研究,[31] 发现低GI的地中海饮食配合运动,可以改善人体细胞膜的n-6/n-3比例(AA/EPA), 142名NAFLD患者接受90天试验,分了不同组别,结果证明带氧运动和阻力训练加上地中海饮食在90天后都可以改善n-6/n-3比例,效果相当。
总结
除了饮食和运动之外,适当补充抗氧化物对改善脂肪肝也有好处,但既然通过改变生活习惯和增加饮食调整已经足以很大程度改善脂肪肝,我觉得没有必要把重点放在补充抗氧化物上,所以这里不作详细的介绍。
从最新的临床研究我们可以得出下面的结论:
1. 肠道健康对脂肪肝的影响深远,饮食以减少有害细菌增加益生菌为重要任务,同样的淀粉、脂肪和蛋白质的比例,“质量”差的饮食只会不利肠道菌群平衡,最终加剧脂肪肝的形成,而且在你可能连体重都没有改变的情况下,脂肪已经在肝脏积累;
2. 饮食中的糖类和精制碳水容易加剧脂肪肝,含糖饮料差不多直接导致肝脏脂肪的积累,戒糖和含糖饮料是改善脂肪肝最简单的办法;
3. 水果虽然含果糖但可以改善脂肪肝,水果和蔬菜含大量的膳食纤维,改善肠道环境,对改善脂肪肝有好处,但千万别只喝果汁,果汁含大量果糖却没有膳食纤维的;
4. 含有抗性淀粉的全谷类,粗粮等饮食则可以改善脂肪肝。粗粮含有大量的膳食纤维对改善肠道和减少肝脏脂肪积累都有帮助;
5. 饱和脂肪过多导致炎症和脂解,增加肝脏脂肪积累,所以NAFLD患者需要控制饮食中的饱和脂肪不能过多;
6. 含多酚的橄榄油抗炎症好改善脂肪肝,橄榄油的作用不只因为它是MUFA单不饱和脂肪,所以其他同样含有单不饱和脂肪的食用油,并不含有橄榄油EVOO的多酚类物质,对改善脂肪肝起码需要打折;
7. 增加欧米茄3的食物对改善脂肪肝有好处。
免责声明:
本文内容仅作为科普知识提供,不能代替医生的治疗诊断和建议。文章内容中涉及医学的部分均来源于参考文献。
参考:
[1] Ni, Yinhua & Ni, Liyang & Zhuge, Fen & Fu, Zhengwei. (2020). The Gut Microbiota and Its Metabolites, Novel Targets for Treating and Preventing Non-Alcoholic Fatty Liver Disease. Molecular Nutrition & Food Research. 64. 10.1002/mnfr.202000375.
[2] Ji, Yun & Yin, Yue & Sun, Lijun & Zhang, Wei-Zhen. (2020). The Molecular and Mechanistic Insights Based on Gut–Liver Axis: Nutritional Target for Non-Alcoholic Fatty Liver Disease (NAFLD) Improvement. International Journal of Molecular Sciences. 21. 3066. 10.3390/ijms21093066.
[3] Yuan, Jing & Chen, Chen & Cui, Jinghua & Lu, Jing & Yan, Chao & Wei, Xiao & Zhao, Xiangna & Li, NanNan & Li, Shaoli & Xue, Guanhua & Cheng, Weiwei & Li, Boxing & Li, Huan & Lin, Weishi & Tian, Changyu & Zhao, Jiangtao & Han, Juqiang & An, Daizhi & Zhang, Qiong & Liu, Di. (2019). Fatty Liver Disease Caused by High-Alcohol-Producing Klebsiella pneumoniae. Cell Metabolism. 30. 1172. 10.1016/j.cmet.2019.11.006.
[4] Softic, S., Cohen, D. E., & Kahn, C. R. (2016). Role of Dietary Fructose and Hepatic De Novo Lipogenesis in Fatty Liver Disease. Digestive diseases and sciences, 61(5), 1282–1293. https://doi.org/10.1007/s10620-016-4054-0
[5] Schwarz JM, Noworolski SM, Wen MJ, et al. Effect of a High-Fructose Weight-Maintaining Diet on Lipogenesis and Liver Fat. J Clin Endocrinol Metab. 2015;100(6):2434–2442. doi:10.1210/jc.2014-3678
[6] Schwarz, Jean-Marc et al., Effects of Dietary Fructose Restriction on Liver Fat, De Novo Lipogenesis, and Insulin Kinetics in Children With Obesity , Gastroenterology, 2017. Volume 153, Issue 3, 743 – 752
[7] Schwimmer, J. B., Ugalde-Nicalo, P., Welsh, J. A., Angeles, J. E., Cordero, M., Harlow, K. E., Alazraki, A., Durelle, J., Knight-Scott, J., Newton, K. P., Cleeton, R., Knott, C., Konomi, J., Middleton, M. S., Travers, C., Sirlin, C. B., Hernandez, A., Sekkarie, A., McCracken, C., & Vos, M. B. (2019). Effect of a Low Free Sugar Diet vs Usual Diet on Nonalcoholic Fatty Liver Disease in Adolescent Boys: A Randomized Clinical Trial. JAMA, 321(3), 256–265. https://doi.org/10.1001/jama.2018.20579
[8] Kim, S. A., & Shin, S. (2020). Fruit and vegetable consumption and non-alcoholic fatty liver disease among Korean adults: a prospective cohort study. Journal of epidemiology and community health, 74(12), 1035–1042. https://doi.org/10.1136/jech-2020-214568
[9] Noureddin, M., Zelber-Sagi, S., Wilkens, L. R., Porcel, J., Boushey, C. J., Le Marchand, L., Rosen, H. R., & Setiawan, V. W. (2020). Diet Associations With Nonalcoholic Fatty Liver Disease in an Ethnically Diverse Population: The Multiethnic Cohort. Hepatology (Baltimore, Md.), 71(6), 1940–1952. https://doi.org/10.1002/hep.30967
[10] Cantero, I., Abete, I., Monreal, J. I., Martinez, J. A., & Zulet, M. A. (2017). Fruit Fiber Consumption Specifically Improves Liver Health Status in Obese Subjects under Energy Restriction. Nutrients, 9(7), 667. https://doi.org/10.3390/nu9070667
[11] Rosado, C. P., Rosa, V., Martins, B. C., Soares, A. C., Santos, I. B., Monteiro, E. B., Moura-Nunes, N., da Costa, C. A., Mulder, A., & Daleprane, J. B. (2020). Resistant starch from green banana (Musa sp.) attenuates non-alcoholic fat liver accumulation and increases short-chain fatty acids production in high-fat diet-induced obesity in mice. International journal of biological macromolecules, 145, 1066–1072. https://doi.org/10.1016/j.ijbiomac.2019.09.199
[12] Wang, A., , Liu, M., , Shang, W., , Liu, J., , Dai, Z., , Strappe, P., , & Zhou, Z., (2019). Attenuation of metabolic syndrome in the ob/ob mouse model by resistant starch intervention is dose dependent. Food & function, 10(12), 7940–7951. https://doi.org/10.1039/c9fo01771b
[13] Georgoulis, M., Kontogianni, M. D., Tileli, N., Margariti, A., Fragopoulou, E., Tiniakos, D., Zafiropoulou, R., & Papatheodoridis, G. (2014). The impact of cereal grain consumption on the development and severity of non-alcoholic fatty liver disease. European journal of nutrition, 53(8), 1727–1735. https://doi.org/10.1007/s00394-014-0679-y
[14] Dorosti, M., Jafary Heidarloo, A., Bakhshimoghaddam, F., & Alizadeh, M. (2020). Whole-grain consumption and its effects on hepatic steatosis and liver enzymes in patients with non-alcoholic fatty liver disease: a randomised controlled clinical trial. The British journal of nutrition, 123(3), 328–336. https://doi.org/10.1017/S0007114519002769
[15] Krawczyk, M., Maciejewska, D., Ryterska, K., Czerwińka-Rogowska, M., Jamioł-Milc, D., Skonieczna-Żydecka, K., Milkiewicz, P., Raszeja-Wyszomirska, J., & Stachowska, E. (2018). Gut Permeability Might be Improved by Dietary Fiber in Individuals with Nonalcoholic Fatty Liver Disease (NAFLD) Undergoing Weight Reduction. Nutrients, 10(11), 1793. https://doi.org/10.3390/nu10111793
[16] Luukkonen, Panu & Sädevirta, Sanja & Zhou, You & Kayser, Brandon & Ahonen, Linda & Lallukka-Brück, Susanna & Pelloux, Véronique & Gaggini, Melania & Jian, Ching & Hakkarainen, Antti & Lundbom, Nina & Gylling, Helena & Salonen, Anne & Oresic, Matej & Hyotylainen, Tuulia & Orho-Melander, Marju & Rissanen, Aila & Gastaldelli, Amalia & Yki-Järvinen, Hannele. (2018). Saturated Fat Is More Metabolically Harmful for the Human Liver Than Unsaturated Fat or Simple Sugars. Diabetes Care. 41. dc180071. 10.2337/dc18-0071.
[17] Bugianesi, Elisabetta & Moscatiello, S & Ciaravella, M.F. & Marchesini, Giulio. (2010). Insulin Resistance in Nonalcoholic Fatty Liver Disease. Current pharmaceutical design. 16. 1941-51. 10.2174/138161210791208875.
[18] Rosqvist, F., Kullberg, J., Ståhlman, M., Cedernaes, J., Heurling, K., Johansson, H. E., Iggman, D., Wilking, H., Larsson, A., Eriksson, O., Johansson, L., Straniero, S., Rudling, M., Antoni, G., Lubberink, M., Orho-Melander, M., Borén, J., Ahlström, H., & Risérus, U. (2019). Overeating Saturated Fat Promotes Fatty Liver and Ceramides Compared With Polyunsaturated Fat: A Randomized Trial. The Journal of clinical endocrinology and metabolism, 104(12), 6207–6219. https://doi.org/10.1210/jc.2019-00160
[19] Soriguer, Federico & Morcillo, Sonsoles & Cardona, Fernando & Rojo-Martinez, Gemma & Almaraz, Maria & Adana, María & Olveira, Gabriel & Tinahones, Francisco & Esteva, Isabel. (2006). Pro12Ala Polymorphism of the PPARG2 Gene Is Associated with Type 2 Diabetes Mellitus and Peripheral Insulin Sensitivity in a Population with a High Intake of Oleic Acid. The Journal of nutrition. 136. 2325-30. 10.1093/jn/136.9.2325.
[20] Assy, Nimer & Nassar, Faris & Nasser, Gattas & Grozovski, M.. (2009). Olive oil consumption and non-alcoholic fatty liver disease. World journal of gastroenterology : WJG. 15. 1809-15. 10.3748/wjg.15.1809.
[21] Abenavoli, L., Milanović, M., Milić, N., Luzza, F., & Giuffrè, A. M. (2019). Olive oil antioxidants and non-alcoholic fatty liver disease. Expert review of gastroenterology & hepatology, 13(8), 739–749. https://doi.org/10.1080/17474124.2019.1634544
[22] Lama, Adriano & Pirozzi, Claudio & Mollica, Maria & Trinchese, Giovanna & Di Guida, Francesca & Cavaliere, Gina & Calignano, Antonio & Mattace Raso, Giuseppina & Berni Canani, Roberto & Meli, Rosaria. (2017). Polyphenol-rich virgin olive oil reduces insulin resistance and liver inflammation and improves mitochondrial dysfunction in high fat diet fed rats.
[23] Rezaei, S., Akhlaghi, M., Sasani, M. R., & Barati Boldaji, R. (2019). Olive oil lessened fatty liver severity independent of cardiometabolic correction in patients with non-alcoholic fatty liver disease: A randomized clinical trial. Nutrition (Burbank, Los Angeles County, Calif.), 57, 154–161. https://doi.org/10.1016/j.nut.2018.02.021
[24] Shidfar, F., Bahrololumi, S. S., Doaei, S., Mohammadzadeh, A., Gholamalizadeh, M., & Mohammadimanesh, A. (2018). The Effects of Extra Virgin Olive Oil on Alanine Aminotransferase, Aspartate Aminotransferase, and Ultrasonographic Indices of Hepatic Steatosis in Nonalcoholic Fatty Liver Disease Patients Undergoing Low Calorie Diet. Canadian journal of gastroenterology & hepatology, 2018, 1053710. https://doi.org/10.1155/2018/1053710
[25] Nigam, P., Bhatt, S., Misra, A., Chadha, D. S., Vaidya, M., Dasgupta, J., & Pasha, Q. M. (2014). Effect of a 6-month intervention with cooking oils containing a high concentration of monounsaturated fatty acids (olive and canola oils) compared with control oil in male Asian Indians with nonalcoholic fatty liver disease. Diabetes technology & therapeutics, 16(4), 255–261. https://doi.org/10.1089/dia.2013.0178
[26] Pinto, Xavier & Fanlo, Marta & Corbella, Emili & Corbella, Xavier & Mitjavila, M & Moreno, Juan & Casas, Rosa & Estruch, Ramon & Corella, Dolores & Bulló, Mónica & Ruiz-Canela, Miguel & Castañer, Olga & Alfredo, Martinez & Ros, Emilio. (2019). A Mediterranean Diet Rich in Extra-Virgin Olive Oil Is Associated with a Reduced Prevalence of Nonalcoholic Fatty Liver Disease in Older Individuals at High Cardiovascular Risk. The Journal of nutrition. 149. 10.1093/jn/nxz147.
[27] Ferramosca, Alessandra & Zara, Vincenzo. (2014). Modulation of hepatic steatosis by dietary fatty acids. World journal of gastroenterology : WJG. 20. 1746-1755. 10.3748/wjg.v20.i7.1746.
[28] Boyraz, M., Pirgon, Ö., Dündar, B., Çekmez, F., & Hatipoğlu, N. (2015). Long-Term Treatment with n-3 Polyunsaturated Fatty Acids as a Monotherapy in Children with Nonalcoholic Fatty Liver Disease. Journal of clinical research in pediatric endocrinology, 7(2), 121–127. https://doi.org/10.4274/jcrpe.1749
[29] Lee, C. H., Fu, Y., Yang, S. J., & Chi, C. C. (2020). Effects of Omega-3 Polyunsaturated Fatty Acid Supplementation on Non-Alcoholic Fatty Liver: A Systematic Review and Meta-Analysis. Nutrients, 12(9), 2769. https://doi.org/10.3390/nu12092769
[30] Bogl, L. H., Kaprio, J., & Pietiläinen, K. H. (2020). Dietary n-6 to n-3 fatty acid ratio is related to liver fat content independent of genetic effects: Evidence from the monozygotic co-twin control design. Clinical nutrition (Edinburgh, Scotland), 39(7), 2311–2314. https://doi.org/10.1016/j.clnu.2019.10.011
[31] Tutino, V., De Nunzio, V., Caruso, M. G., Bonfiglio, C., Franco, I., Mirizzi, A., De Leonardis, G., Cozzolongo, R., Giannuzzi, V., Giannelli, G., Notarnicola, M., & Osella, A. R. (2018). Aerobic Physical Activity and a Low Glycemic Diet Reduce the AA/EPA Ratio in Red Blood Cell Membranes of Patients with NAFLD. Nutrients, 10(9), 1299. https://doi.org/10.3390/nu10091299