opdivo
PD-1/PD-L1免疫疗法(immunotherapy)是当前全世界备受瞩目、广为研究的新一类抗癌免疫疗法,旨在充分利用人体自身的免疫系统抵御、抗击癌症,通过阻断PD-1/PD-L1信号通路使癌细胞死亡,具有治疗多种类型肿瘤的潜力,实质性改善患者总生存期。今天,全球肿瘤医生网将两大PD-1药物其中之一--opdivo至今获批的适应症临床数据总结如下,供癌症患者参考。
2014年12月22日
不可切除或转移性黑色素瘤及ipilimumab治疗后病情进展的BRAF V600E突变患者
Opdivo 的有效性在 120 名患有不可切除或转移性黑色素瘤患者参与的临床试验中得到证实。结果显示,32% 的接受 Opdivo 治疗的受试者其肿瘤出现缩小(客观有效率)。这种效果在大约三分之一的经历肿瘤缩小的受试者中会持续 6 个多月。
2015年3月4日
铂类化疗后进展的转移性非小细胞鳞癌
一项国际随机开放临床试验证明了Opdivo治疗晚期NSCLC的安全性与有效性。该试验入组了582名在铂类化疗和适当生物治疗期间或治疗后出现疾病进展的晚期NSCLC患者,他们在试验中接受Opdivo治疗或多西他赛治疗。平均而言,Opdivo治疗组患者的总生存期是12.2个月,而多西他赛治疗组患者的总生存期只有9.4个月。此外,Opdivo治疗组有19%的患者达到了肿瘤完全或部分缩小,其疗效平均持续了17个月;相比之下,多西他赛治疗组只有12%的患者达到了肿瘤完全或部分缩小,其疗效平均持续了6个月。
2015年11月23日
既往接受过抗血管生成疗法的进展期肾细胞癌
Opdivo晚期肾细胞癌适应症的获批,是基于开放标签随机III期研究CheckMate-025的积极顶线数据,该研究在既往曾接受过抗血管生成疗法的晚期肾细胞癌(RCC)患者中开展,一项既定的中期分析数据显示,与诺华抗癌药Afinitor(everolimus,依维莫司)相比,Opdivo显著延长了患者的总生存期(中位OS:25个月 vs 19.6个月),且OS收益独立于PD-L1的表达状态。除了延长总生存期,Opdivo在总缓解率(ORR:21.5% vs 3.9%)、缓解持续时间(中位DOR:23.0个月 vs 13.7个月)也表现出了相对于Afinitor的显著优越性。该研究中,Opdivo的安全性与此前的研究一致。
2016年5月17日
自体干细胞移植和本妥昔单抗治疗或三线及以上系统治疗后出现复发获进展的经典型霍奇金淋巴瘤
此次加速批准,是基于对II期CheckMate-205研究和I期CheckMate-039研究的总缓解率数据的合并分析。根据这一分析(n=95),Opdivo治疗实现了非常高的缓解率,客观缓解率(ORR)达65%(CI 95%: 55-75;62/95患者),完全缓解率为7%(CI 95%: 3-15; 7/95患者),部分缓解率为58%(CI 95%: 47-68; 55/95患者)。实现缓解的患者中,缓解持续中位时间为8.7个月(CI 95%: 6.8-NE; 范围:0.0+,23.1+)。
2016年11月10日
治疗含铂化疗后出现局部进展的复发或转移性头颈鳞状细胞癌(HNSCC)
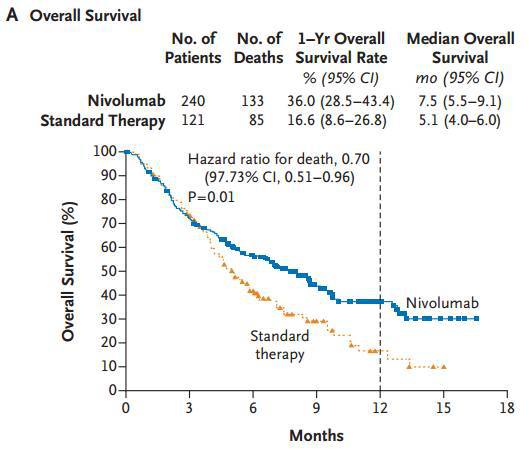
该适应症的批准是基于一项名为CheckMate-141的III期临床研究结果。该研究结果显示,Opdivo组的OS显著优于对照组(研究者选择的甲氨喋呤、多西他赛或西妥昔单抗),组间差异具有统计学意义与临床意义,Opdivo降低死亡风险30%(HR=0.70 [95% CI: 0.53-0.92; p=0.0101]),Opdivo组中位OS为7.5个月(95%CI: 5.5-9.1),对照组(研究者选择疗法)的中位OS为5.1个月(95%CI: 4.0-6.0)。
2017年2月2日
含铂化疗期间或含铂辅助化疗、新辅助化疗一年内出现疾病进展的局部晚期或转移性尿路上皮癌
Opdivo治疗转移性尿路上皮癌(mUC)新适应症的获批,是基于一项II期临床研究CheckMate-275的数据。数据显示,患者接受Opdivo治疗后,确认的客观缓解率(ORR)为19.6%(95% CI:15.1-24.9,n=53/270)、完全缓解率(CRR)为2.6%(n=7)、部分缓解率(PRR)为17%(n=46)。
2017年7月31日
氟尿嘧啶,奥沙利铂和伊立替康治疗后出现进展的MSI-H或dMMR转移性结直肠癌(成人或≥12岁儿童)
该批准基于研究CA209142(CHECKMATE 142; NCT 02060188)的数据,在单药组全组中,ORR为32%(24/74; 95%CI, 22-44),2名患者达CR(完全缓解),22名患者PR。中位缓解持续时间(DoR)终点尚未达到。53名患者既往接受过5-FU、奥沙利铂和伊立替康的治疗。该亚组中的ORR为28%(n=15; 95%CI, 17-42)。该组的CR率为1.9%,PR率为26%。mDoR终点尚未达到。
2017年9月22日
接受过索拉菲尼(多吉美)治疗后的肝细胞癌患者
CheckMate-040研究是一项1/2期开放、多中心、单臂研究,评估Nivolumab在索拉非尼治疗后进展或不耐受的HCC患者中的作用。14.3%的患者在Nivolumab治疗后缓解。91%的患者缓解时间达6个月或更长,55%的患者缓解时间达12个月或更长。
TIPS
上文常见数据:
完全缓解(CR, complete response)所有靶病灶消失,无新病灶出现,且肿瘤标志物正常,至少维持4周部分缓解(PR, partial response)靶病灶最大径之和减少≥30%,至少维持4周疾病稳定(SD, stable disease)靶病灶最大径之和缩小未达PR,或增大未达PD疾病进展(PD, progressive disease)靶病灶最大径之和至少增加≥20%,或出现新病灶总生存期(OS,overall survival)从随机化开始至因任何原因引起死亡的时间。总缓解期(Duration of overall response)从第一次出现CR或PR,到第一次诊断PD或复发的时间。疾病稳定期(duration of stable disease)是指从治疗开始到评价为疾病进展时的这段时间。无病生存期(DFS, Disease-free survival)或者无疾病生存时间,是从随机入组开始到第一次复发或死亡的时间。无进展生存期(PFS,progression-free survival)从入组开始到肿瘤进展或死亡之间的时间。疾病控制率(DCR,disease control rate):CR+PR+SD。客观缓解率(ORR,Objective Response Rate)指肿瘤缩小达到一定量并且保持一定时间的病人的比例,包括CR+PR的病例。总缓解率 (ORR,overall response rate)经过治疗CR+PR病人总数占对于总的可评价病例数的比例。缓解率(RR, response rate)达到CR、PR的病人占同期病人总数的百分比。