
“月光倾泻铺满信笺,我把欣喜凝在笔尖;一词一句绘尽流年,一段一篇诉说期待”
亲爱的阿替利珠单抗:
你好~~窗外月色如水,摊开信纸之前,我还沉浸在朋友圈刷屏的消息里:“小细胞肺癌(SCLC)获得新疗法了!”“ 国家药品监督管理局(NMPA)批准阿替利珠单抗一线治疗广泛期小细胞肺癌(ES-SCLC)的适应证”“等待20年,SCLC终于等到一线治疗新选择”“刚刚!我国首个一线治疗SCLC的免疫疗法获批!”……大家纷纷用一个又一个兴奋而欣喜的文字祝贺你的到来,庆贺我们的成绩。非常荣幸能与你一起见证SCLC治疗史上的里程碑时刻,而作为SCLC一线战场的老将,我也有很多话想对你说。
阿替利珠单抗,知道吗,是你的出现终结了SCLC一线治疗的“药荒时代”,这么说一点也不夸张。几十年来SCLC一直气焰嚣张,我们化疗家族曾经有雄心把他打败。但经历了屡战屡败,屡败屡战,似乎也没能够成功。
山穷水尽疑无路 ——SCLC治疗探索举步维艰
SCLC是一种高侵袭性肿瘤,占所有肺癌发病率的15%左右。SCLC疾病进展快,易发生早期转移,60%患者确诊时已经是ES-SCLC。SCLC的发生与长期吸烟有着密切关系。SCLC具有较高突变负荷,但是绝大多数基因突变缺乏有效的靶向药物,这一点和非小细胞肺癌(NSCLC)有霄壤之别。
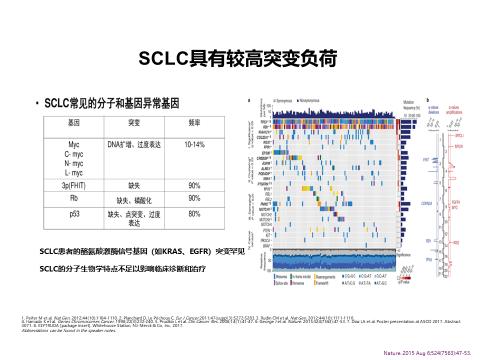
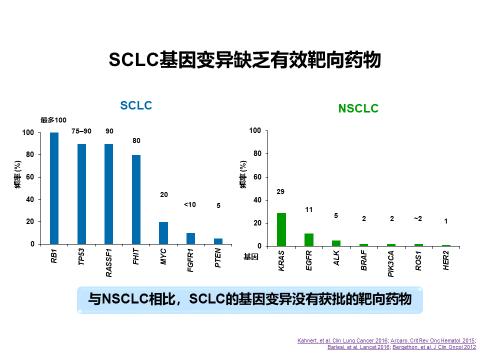
过去数十年里,不断涌现的靶向新药显著改善了NSCLC患者的生存,但SCLC尤其是ES-SCLC的治疗方式除了化疗/放疗外,几乎没有进展。SCLC虽然初始对我们化疗家族高度敏感,但大多数患者容易出现复发,中位总生存(OS)仅8-11个月,5年生存率不足5%。我们尝试找更多的盟友一起并肩战斗,但过去二十年乏善可陈的研究进展和窘迫的治疗现状让我们的梦想被现实一点点吞噬。
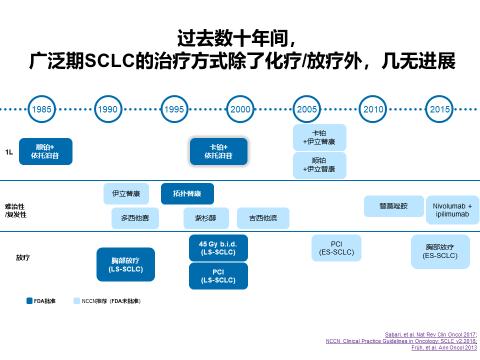
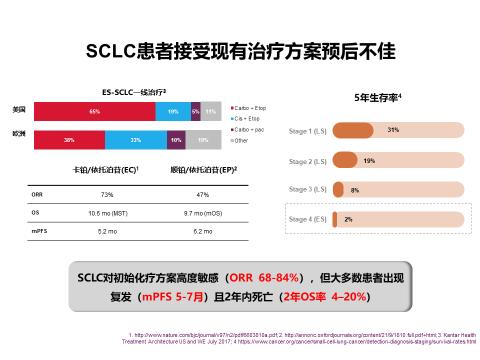
柳暗花明又一村 ——重磅IMpower133研究一鸣惊人
随着免疫治疗研究的大热,PD-1/PD-L1*制剂抑**在NSCLC开拓了广阔疆土,SCLC患者对免疫药物也是翘首以盼。PD-L1*制剂抑**阿替利珠单抗的出现让SCLC患者看到了希望和曙光。然而阿替利珠单抗在SCLC领域的探索并非一蹴而就,在介绍重磅的IMpower133研究前,允许我们先回顾一下阿替利珠单抗在前期做的研究探索。
PCD4989g是一项小样本量Ⅰ期单臂临床研究,旨在探索阿替利珠单抗用于多种晚期或转移性实体瘤和血液恶性肿瘤的剂量和安全性。其中,SCLC患者共有17例,PCD4989g的初步疗效和安全性结果为阿替利珠单抗治疗ES-SCLC提供了前期证据。同时该研究和阿替利珠单抗非临床研究数据为IMpower133选用阿替利珠单抗1200 mg固定剂量方案提供了参考依据。
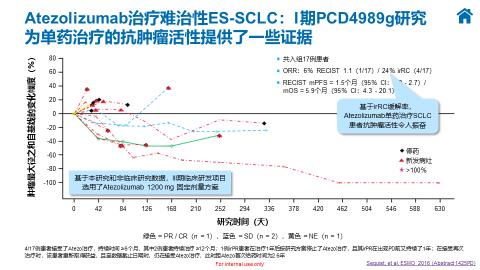
而IMpower133研究则算得上是SCLC领域的一个开拓者。
IMpower133是一项多中心、随机、双盲、安慰剂对照的III期临床研究,旨在评估阿替利珠单抗+化疗(卡铂+依托泊苷,EC)相比较于化疗对初治ES-SCLC的疗效和安全性。研究将403例患者1:1随机分组,分别接受阿替利珠单抗+化疗(试验组),或安慰剂+化疗(对照组);诱导治疗4周期(21天/周期)后阿替利珠单抗或安慰剂维持治疗,直至疾病进展。
2018年世界肺癌大会(WCLC)上,Dr. Liu带来了重磅的IMpower133研究,研究结果显示阿替利珠单抗联合EC方案对比安慰剂+EC方案,显著改善了ES-SCLC一线治疗的OS和无进展生存(PFS)。2019年欧洲肿瘤内科学会(ESMO)年会上进一步公布了IMpower133研究中位随访22.9个月时的结果。
研究结果显示,卡铂+依托泊苷联合阿替利珠单抗可以较单纯化疗显著提高病人的PFS(5.2个月 vs 4.3个月, 进展或死亡风险降低23%, P=0.02)和OS(12.3个月 vs 10.3个月)[ HR 0.76 (0.60, 0.95),p=0.0154)] ,降低了24%的死亡风险。18个月OS率的结果显示,阿替利珠单抗组为34%,显著优于对照组的21%。
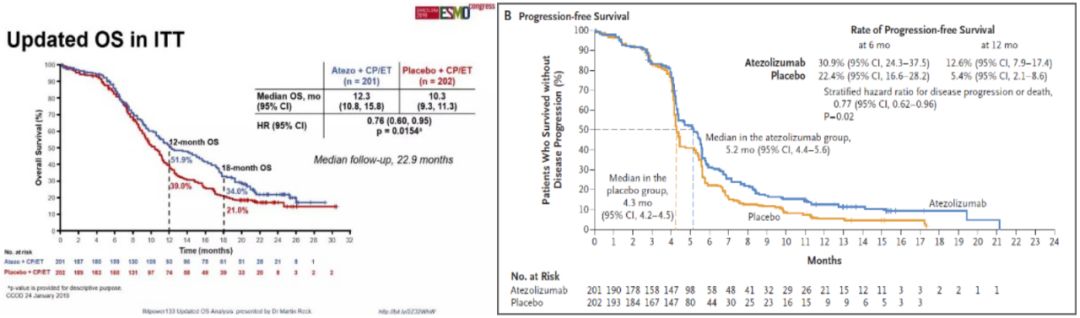
EP方案化疗联合阿替利珠单抗可以较单纯化疗显著提高病人的OS(左)和PFS(右)
此外,总体上,患者的不良反应事件比例在两组之间并无统计学差异,阿替利珠单抗联合化疗安全性与既往报道一致,未发现新的毒性。
▍ IMpower133日本亚组与全球人群的疗效及安全性一致
由于亚裔和白人患者群体之间在身高和体重方面等遗传和生理差异可能会改变治疗相关不良事件的疗效和发生率。近日,IMpower133研究的日本亚组结果发表在《Clinical Lung Cancer》上,并进一步分析了阿替利珠单抗在日本亚群中的有效性和安全性。

研究截图
在IMpower133试验纳入的403名患者中,有42名来自日本研究中心。其中,20名患者被随机分配到阿替利珠单抗组,22名患者被随机分为安慰剂组。在日本患者中,阿替利珠单抗组的中位随访时间为16.5个月(范围5.3-17.8个月),安慰剂组为15.3个月(范围0.5-16.6个月)。
日本亚组研究结果显示,亚洲人群较总体人群的OS获益有了进一步的增加:在ITT人群的日本患者中,阿替利珠单抗组的中位OS为14.6个月,而安慰剂组的中位OS为11.9个月 (HR 0.72;95% CI 0.31-1.67),降低了28%的死亡风险。阿替利珠单抗组的中位PFS也高于安慰剂组(4.5个月 vs 4.0个月)[HR 0.473 (0.234, 0.956)]。值得注意的是,虽然日本亚组样本量较小,但是阿替利珠单抗组的OS曲线始终在安慰剂组的上方,早期便显示出差异,后续长期治疗的优势将进一步拉大。
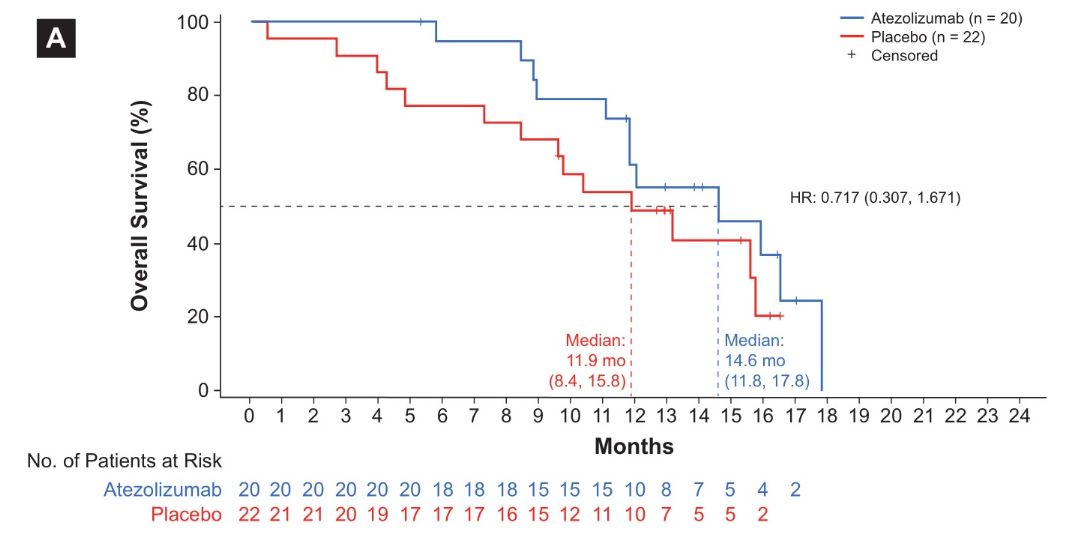
日本亚组OS结果
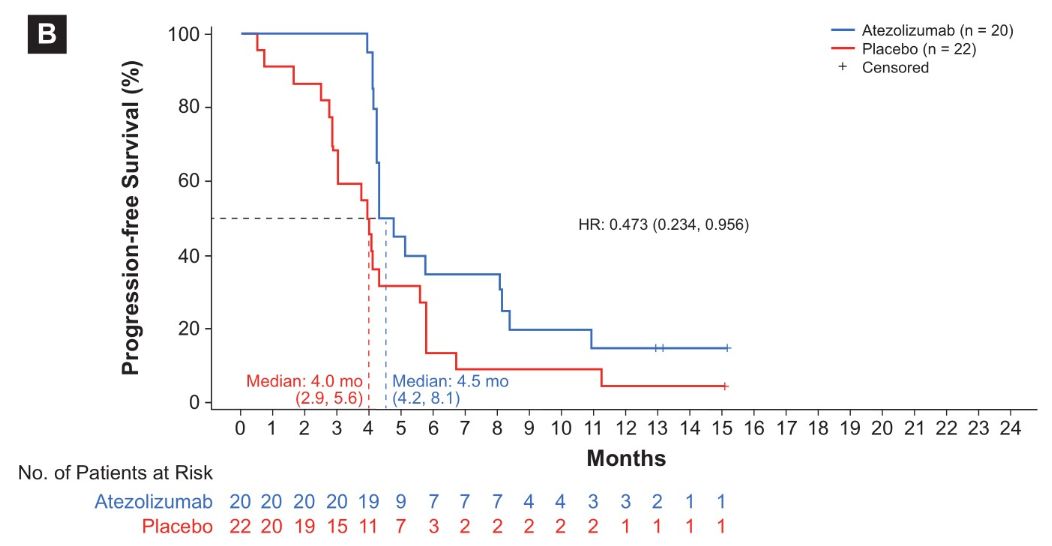
日本亚组PFS结果
在IMpower133日本亚组中,阿替利珠单抗组的客观缓解率(ORR)达到75%,高于安慰剂组的50%;数据截止时,阿替利珠单抗组的持续缓解的患者比例也高于安慰剂组(20% vs 9.1%)。
在安全性方面,尽管IMpower133研究中日本人群中全因和治疗相关的3/4级不良反应事件(AEs)的发生率高于非日本人群,但严重AEs的发生率仍是较低的,而日本人群和非日本人群的AEs发生率的差异也可能是由于前者的体重较轻导致的。另外,不论是在日本人群还是非日本人群中,所有原因AEs、治疗相关AEs、所有原因3/4级AEs、治疗相关3/4级AEs、严重AEs等,阿替利珠单抗组都与安慰剂组相当。
表1:日本和非日本患者的AEs
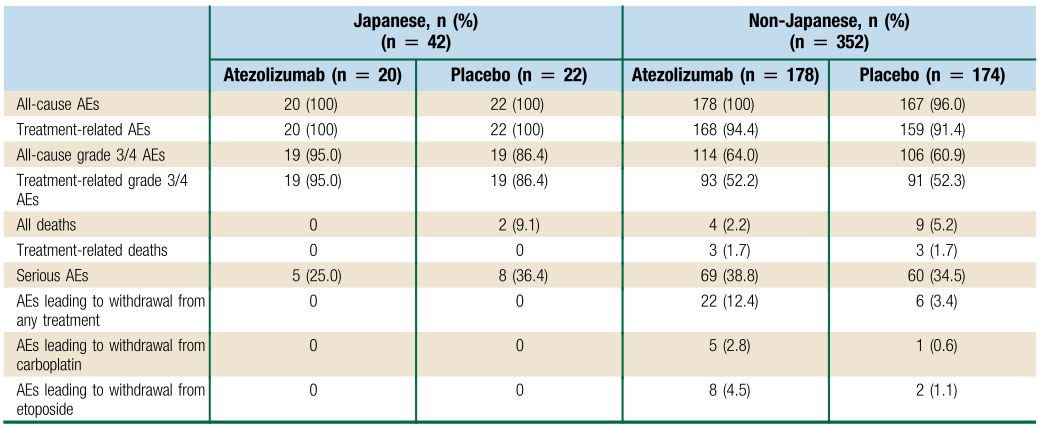
总的来说,从IMpower133日本亚组分析来看:相比安慰剂组,接受阿替利珠单抗治疗的日本患者获得了更长的OS;此外,与IMpower133中接受阿替利珠单抗治疗的总体人群相比,接受阿替利珠单抗治疗的日本亚群的OS数值还要更长。整体安全性方面,阿替利珠单抗的耐受性良好,没有治疗相关死亡。
IMpower133研究见证了免疫治疗与化疗在ES-SCLC的完美配合。我促进肿瘤抗原释放,你通过T细胞加强免疫*击狙**,带来更深、更持久的缓解。灯光、掌声、鲜花、赞美,我有幸与你携手站在2018年WCLC,有幸与你并肩亮相在《新英格兰医学杂志》(NEJM)的主刊,美国国立综合癌症网络(NCCN)指南一类优选、FDA加速审批通过、在中国获批上市……我们的IMpower133给SCLC重新定义了一个时代!只恨自己才疏学浅,没有更多的词语来描述与你合作的完美。



正如罗氏公司的首席医疗官和全球产品开发主管Sandra Horning博士所说:“阿替利珠单抗是首个被批准的一线治疗进展期SCLC的癌症免疫疗法。到目前为止,SCLC患者的治疗方法有限,所以我们很高兴能给患者带来一种新的治疗方法,与化疗相比,此疗法能提高患者生存率,并且该方法有望成为ES-SCLC的标准治疗。”
写在最后
阿替利珠单抗,相信NMPA的上市批准仅仅是开始,你的到来一定可以让更多SCLC患者重拾希望和信心,未来随着临床经验的不断丰富,将会为使更多患者获益。而与你并肩作战为SCLC成为慢性疾病而努力的样子,将会是世界上最浪漫的模样!
盼聚,祝春安。
你的卡铂•依托泊苷
2020年2月27日
参考文献
1. cell lung cancer. Genes Dev. 2015;29(14):1447–1462.
2. Jackman DM, Johnson BE. Small-cell lung cancer. Lancet Lond. Engl. 366(9494), 1385–1396 (2005).
3. Peifer M et al. Nat Gen. 2012;44(10):1104-1110.
4. Planchard D, Le Péchoux C. Eur J Cancer.2011;47(suppl 3):S272-S283.
5. Rudin CM et al. Nat Gen. 2012;44(10):1111-1116.
6. Hamada K et al. Genes Chromosomes Cancer. 1998;22(3):232-240.
7. Prudkin L et al. Clin Cancer Res. 2008;14(1):41-47.
8. George J et al. Nature. 2015;524(7563):47-53.
9. Diaz LA et al. Poster presentation at ASCO 2017. Abstract 3071.
10. KEYTRUDA [package insert]. Whitehouse Station, NJ: Merck & Co, Inc, 2017.
11. Kristjansen PE, Hansen HH. Management of small cell lung cancer: A summary of the Third International Association for the Study of Lung Cancer Workshop on Small Cell Lung Cancer. J Natl Cancer Inst. 1990;82(4):263–266.
12. Moss AC, Jacobson GM, Walker LE, et al. SCG3 transcript in peripheral blood is a prognostic biomarker for REST-deficient small cell lung cancer. Clin Cancer Res. 2009;15(1):274–283. doi: 10.1158/1078-0432.CCR-08-1163.
13. Pedersen N, Mortensen S, Sorensen SB, et al. Transcriptional gene expression profiling of small cell lung cancer cells. Cancer Res. 2003;63(8):1943–1953.
14. Liu SV, Horn L, et al. N Engl J Med. 2018 Dec 6;379(23):2220-2229.
15.https://www.gene.com/media/press-releases/14783/2019-03-18/fda-approves-genentechs-tecentriq-in-com
16. Makoto Nishio et al. Subgroup Analysis of Japanese Patients in a Phase III Study of Atezolizumab in Extensive-stage Small-cell Lung Cancer (IMpower133). Clin Lung Cancer , 20 (6), 469-476.e1
小调研
“小细胞肺癌免疫治疗学院”是医学界打造的肿瘤领域的学术专栏,每周通过线上传递一篇高质量的专业文章。为医生和患者提供SCLC及时、有效的免疫治疗资讯和临床最新进展。
