*仅供医学专业人士阅读参考

兼顾安全性与有效性,阿普米司特如何惠及中度及特殊部位银屑病患者?
银屑病是皮肤科常见的由多种免疫细胞参与的慢性、复发性、炎症性皮肤病,主要病理表现为表皮角质化过度及角化不全、棘层细胞肥厚、淋巴细胞浸润及血管扩张等 [1] 。银屑病患者不仅有皮肤和关节受损症状,还伴发糖尿病等代谢综合征、肥胖、心血管疾病等 [2] ,治疗过程漫长,且效果差,易反复,给患者的精神和身体造成极大痛苦,严重影响患者生活水平。
21世纪初期,生物疗法取得突破后,被率先引入用于治疗银屑病。从此,银屑病患者症状完全清除不再只是“纸上谈兵”。与此同时,小分子靶向药物的研发也非常活跃,其中一个被称为PDE4的靶点开始引起大众的关注。
2021年8月,国家药品监督管理局(NMPA)正式批准阿普米司特用于治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者。至此,中国首个也是目前唯一一个用于治疗斑块状银屑病的PDE4*制剂抑**诞生。那么,这款口服小分子药是如何对抗银屑病治疗这一难题,又是如何帮助患者走出“银”影,获益良多的呢?
现实与梦想的差距:银屑病治疗未被满足的临床需求
数据显示,全球有超过1.25亿银屑病患者。在我国,银屑病患者约650万,中重度患者约占50%以上 [3] ,加之银屑病病程慢性迁延,随着人口寿命的延长,患者数量必然会逐年增加。银屑病治疗虽已取得很大进展,但仍有许多问题亟待解决。
研究表明,银屑病高发于青壮年。《中国银屑病诊疗现状2020蓝皮书》指出,银屑病患者多见于19-44岁年龄段。对该年龄段患者工作状态进行分析,发现其失业占比10%左右 [4] 。《中国银屑病疾病负担和生存质量调研报告》同样表明,银屑病带来的社会负担不容小觑,有37%的患者因患银屑病失业,73%的患者因银屑病而降低工作效率,中重度银屑病患者中,失业率更是高达48% [5] 。与此同时,大众对银屑病的危害认知不足,易低估自身病情,后果则是延迟治疗,更是让病情进展“雪上加霜”。
此外,虽然临床上针对银屑病的治疗方案甚多,但绝大数患者对此满意度却不高。究其原因,主要为传统治疗药物靶点不够精准,且毒副作用较多,长期用药带来诸多挑战。而从临床治疗来看,生物制剂的出现虽有希望让患者持续拥有正常肌肤甚至实现“皮损全清”,但目前国内生物制剂的临床应用仍相当有限。根据《美国皮肤病学会杂志》发表的一项对银屑病和银屑病关节炎的跨国研究报告,有高达57%银屑病患者在使用传统口服治疗时因为药物安全性、耐受性或有效性问题而停止治疗;而使用注射的生物制剂的患者也有45%停止治疗,依从性不高 [6] 。以上种种均表明,银屑病的治疗道路曲折坎坷,如何解决这些患者的痛点问题,任重而道远。
南方医科大学皮肤病医院院长杨斌教授曾表示,“银屑病是一种慢性的、系统性的炎症性疾病,临床未满足需求高。2021年8月,创新口服PDE4选择性*制剂抑**‘阿普米司特’在中国获批,为国内银屑病患者提供了新的口服治疗选择。”
口服药“天花板”,打造中度、特殊部位银屑病患者治疗新选择
环磷酸腺苷(cAMP)在体内调节很多关键的生理过程,阿普米司特就是通过竞争性阻断PDE4对cAMP的降解作用,从而使细胞内cAMP水平增加,进而达到治疗和控制银屑病症状的目的 [7] 。该类小分子靶向口服药物的问世后,对银屑病治疗来说具有里程碑式的意义。以往传统口服药大多为广谱免疫*制剂抑**,在改善症状的同时,可能带来许多副作用。而阿普米司特作用机制明确,副作用更少,安全性更高;与需要注射给药的生物制剂相比,使用更为便捷,无需用药前筛查以及血常规、肝肾功能等实验室监测。目前,阿普米司特的临床疗效,在关键研究中也已经得到证实。
ADVANCE [8] 是一项多中心、随机、安慰剂对照、双盲3期研究,评估了阿普米司特治疗轻中度银屑病的疗效和安全性。该研究中,595例患者按1:1的比例随机分为2组,一组接受每日2次口服阿普米司特30mg(n=297)、另一组接受安慰剂(n=298),总共进行了为期16周的治疗。在完成16周治疗后,所有患者在开放标签扩展期接受阿普米司特治疗直至第32周。主要终点是第16周实现静态医生总体评估(sPGA)反应的患者百分比。
结果显示,该研究达到了主要终点:治疗第16周,与安慰剂组相比,阿普米司特组达到sPGA的患者比例显著更高(21.6% vs 4.1%,p<0.0001),并且疗效持续至到第32周。此外,在第16周,与安慰剂组相比,阿普米司特组在全部次要终点方面也有统计学意义的显著改善,包括:BSA-75应答率(33.0% vs 7.4%)、BSA≤3应答率(61.0% vs 22.9%)、WBI-NRS应答率(43.2% vs 18.6%)、头皮PGA(ScPGA)反应评分为皮损完全清除或几乎完全清除(ScPGA 0/1:44.0% vs 16.6%)。

图1 阿普米司特组与安慰组16周内达到SPGA反应的患者比例

图2 阿普米司特组与安慰组16周内BSA-75应答率、BSA≤3应答率、 WBI-NRS应答、ScPGA 0/1应答的患者比例
APRAISAL 研究 [9] 是一项多中心、观察性、为期 52 周的前瞻性研究,旨在探讨阿普米司特在改善银屑病患者皮肤病生活质量指数 (DLQI)、银屑病面积和严重程度指数 (PASI) 以及甲、头皮和掌跖受累的有效性。研究显示,在第6、16和24周,患者的的DLQI和PASI得分(P<0.001)均有所改善。在第24周,DLQI≤5,DLQI 0或1以及PASI-75的应答率分别为63.0%,25.0%和48.0%。甲银屑病患者PASI评分在6、16 和24周均呈进行性降低(P <0.001)。在第24周时,50.0%和51.7%的头皮(n=76)和掌跖(n=29)受累患者症状得到改善,即如果基线评分PGA≥3的患者,经治疗后PGA达到0或1;如果基线PGA评分为1或2的患者,经治疗后PGA达到0。这些中期结果均表明,阿普米司特在24周内显著改善了中度银屑病患者皮损程度、生活质量以及特殊部位受累情况。

图3 阿普米司特在第6、16 和24周实现PASI-50、PASI-75和 PASI-90的患者比例

图4 头皮银屑病患者在第6、16 和24周PGA评分情况
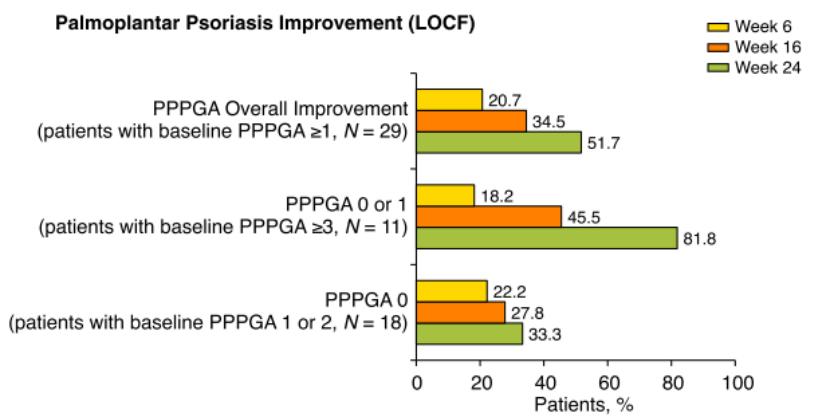
图5 掌跖银屑病患者在第6、16 和24周PGA评分情况
展望未来治疗模式,阿普米司特入局银屑病治疗“中坚力量”
杨斌教授表示,“阿普米司特起效迅速,疗效稳定持久,安全性好,且口服使用更加方便,是这个药的优势和特点。阿普米司特的作用特点决定了它的适用人群——中度斑块状银屑病成人患者。”
“这是因为,多数中度银屑病患者对传统口服药物的有效性和安全性存在顾虑,当综合了疗效、安全性、治疗负担和个人偏好等方面的因素进行药物选择时,疗效较好 、不良反应少且使用方便的阿普米司特将可能成为中度银屑病患者的全新选择。 ”
北京大学第三医院皮肤科主任张春雷教授则把视角转向了特殊部位银屑病患者:“特殊部位银屑病,尤其是皮损面积较小但伴有特殊部位的患者,临床治疗还存在诸多尚未满足的治疗需求,患者亟需有效、安全且便捷的新型治疗方法。”鉴于以前常用的治疗方式如外用药物治疗、光疗及系统治疗不尽人意,而阿普米司特因其特殊的靶向作用机制,为患者提供了一个全新的治疗方向。对此,张教授对于阿普米司特治疗特殊部位银屑病的临床疗效与安全性给予了充分肯定。
此外,包括《2020 AAD-NPF指南》 [10] ,《2019日本银屑病生物治疗指南》 [11] 及《2018德国S3指南》 [12] 等多个国际指南也都一致推荐阿普米司特用于成人中重度银屑病的治疗选择。
张春雷教授指出: “基于阿普米司特所 展现出的良好疗效与安全性及使用便捷性,在银屑病治疗中,阿普米司特将是一种不可替代的治疗选择。 未来,阿普米司特与大分子生物制剂序贯或联合用药、与传统系统治疗药物的联合用药将是值得我们去探索研究的领域。 ”
作为全新且迄今为止全球目前唯一获批的口服PDE4*制剂抑**银屑病治疗药物,阿普米司特承载了我们沉甸甸的期待。幸运的是,这款药物已经用坚实的循证医学证据证实其不负众望,在降低疾病活动度具有明确的优势,并被国内和国际权威指南认可和推荐。相信阿普米司特在中国的推广应用将会为改善银屑病患者治疗现状贡献“小分子“的力量。
专家简介

杨斌 教授
-
博导,国务院特贴专家,南方医科大学皮肤病医院院长
-
中华医学会理事
-
中国医师协会皮肤科医师分会副会长
-
中华医学会皮肤性病学分会委员、免疫学组成员
-
中国整形美容协会皮肤美容分会副主委
-
亚洲银屑病学会(ASP)理事
-
广东省医学会皮肤性病学分会主任委员
-
广东省医师协会皮肤科医师分会副主委
-
广东省整形美容协会副会长
-
近年来重点聚焦瘢痕疙瘩及皮肤淀粉样变的遗传易感性和分子机制研究。主持国家、省级课题及国际合作项目十余项,以第一作者或通讯作者发表论文110余篇,SCI收录30余篇。获“广东省医学领军人才”、“全国先进工作者”、“全国优秀中青年医师”、“广东医师奖”和“广东优秀院长”等荣誉称号。
专家简介

张春雷 教授
主要教育背景
- 北京医科大学(现北京大学医学部)医学博士 (1995)
- 瑞士苏黎世大学医院皮肤科博士后 (1998-1999)
- 美国得州大学MD安德森癌症中心皮肤科博士后(2000-2002) 主要工作任职
- 北京大学第三医院皮肤科主任、特聘教授和博士生导师(2012~)
- 国家皮肤与免疫疾病临床医学研究中心副主任(2019~)
- 北京大学医学部皮肤病与性病学系主任(2015-2018)
- 美国得州大学MD安德森癌症中心皮肤科助理教授(2008-2012) 主要学术任职
- 中华医学会激光医学分会副主任委员兼皮肤美容整形学组组长
- 中华医学会皮肤性病学分会银屑病学组副组长
- 中国医师协会皮肤科医师分会皮肤肿瘤学组副组长
- 北京医学会激光医学分会候任主任委员
- 北京医学会皮肤性病学分会副主任委员 主要研究领域
- 皮肤肿瘤尤其皮肤淋巴瘤、银屑病和皮肤美容
参考文献:
[1 ] 中华医学会皮肤性病学分会银 屑病专业委员会 . 中国银屑病诊疗指南(2018完整版)[J]. 中华皮肤科杂志, 2019, 52(10): 667-710.
[2] 宋树玲.银屑病流行病学、发病机制和治疗新进展[J].中国实用医药,2018,13(13):193-195. [3]丁晓岚,王婷琳,沈佚葳.中国六省市银屑病流行病学调查[J].中国皮肤性病学杂志,2010,24(07):598-601. [4]郑颖璠. 建标准化中心 “智导”银屑病规范管理[N]. 健康报,2021-04-28(006). [5]李慧贤,胡丽,郑焱,张键,刘文丽,高田原,牟宽厚,田琼.基于全球疾病负担(GBD)大数据的中国银屑病流行病学负担分析[J].中国皮肤性病学杂志,2021,35(04):386-392. [6]Lebwohl MG, Bachelez H, Barker J, et al. Patient perspectives in the management of psoriasis: results from the population-based Multinational Assessment of Psoriasis and Psoriatic Arthritis Survey. J Am Acad Dermatol. 2014;70(5):871-81.e830. [7]Schafer P. Apremilast mechanism of action and application to psoriasis and psoriatic arthritis. Biochem Pharmacol. 2012;83(12):1583-1590. [8]Stein Gold L, Papp K, Pariser D, et al. Efficacy and safety of apremilast in patients with mild-to-moderate plaque psoriasis: Results of a phase 3, multicenter, randomized, double-blind, placebo-controlled trial. J Am Acad Dermatol. 2022;86(1):77-85. [9]Ioannides D, Antonakopoulos N, Georgiou S, et al. Effectiveness and safety of apremilast in biologic-naïve patients with moderate psoriasis treated in routine clinical practice in Greece: the APRAISAL study. J Eur Acad Dermatol Venereol. 2021;35(9):1838-1848. [10]Chat VS, Uppal SK, Kearns DG, Han G, Wu JJ. Translating the 2020 AAD-NPF Guidelines of Care for the Management of Psoriasis With Systemic Nonbiologics to Clinical Practice. Cutis. 2021;107(2):99-103. [11] Saeki H, Terui T, Morita A, et al. Japanese guidance for use of biologics for psoriasis (the 2019 version). J Dermatol. 2020;47(3):201-222. [12]Nast A, Amelunxen L, Augustin M, et al. S3 Guideline for the treatment of psoriasis vulgaris, update–Short version part 1–Systemic treatment[J]. JDDG: Journal der Deutschen Dermatologischen Gesellschaft, 2018, 16(5): 645-669.
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场。
