文章来源:《中国医学前沿杂志(电子版)》2017年第9卷第5期
组织编写:中国抗癌协会胃癌专业委员会
免费全文*载下**链接:http://www.yixueqianyan.cn/CN/abstract/abstract2203.shtml
胃癌是严重威胁人类健康的一种恶性疾病,全球胃癌每年新增95万例,死亡72万例,其中 70%来自亚洲,而中国患者就占了将近一半[1,2]。腹膜转移复发是晚期胃癌患者死亡的首要原因之一;所谓腹膜转移,是指胃癌原发灶癌细胞经血行、淋巴或腹膜直接种植生长所致的癌症转移形式[3,4]。将近20%的胃癌患者在术前或术中诊断有腹膜转移,超过50%的T3、T4期患者在根治性切除术后发生腹膜转移,腹膜转移程度越高,生存期越短[5]。
目前,我国胃癌腹膜转移诊疗现状严峻,发病率高、早期诊断困难、患者预后差。为了规范胃癌腹膜转移的诊断和治疗,加强对高危患者的筛查,及早发现腹膜转移,制定合理有效的多学科综合治疗方案,从而延长胃癌腹膜转移患者生存时间并改善生活质量。中国抗癌协会胃癌专业委员会组织国内胃癌领域权威专家制定《胃癌腹膜转移防治中国专家共识》(以下简称为共识)。本共识适用于具有腹膜转移风险因素或确诊腹膜转移的胃癌患者。
注 1 :中国抗癌协会胃癌专业委员会组建共识制定专家组。首先由工作小组检索 Medline、Emb-ase、Cochrane 及万方中文期刊数据库,制订共识意见的草案,随后由专家组采用国际通用的德尔菲法(Delphi method)进行讨论和修订,直至达成共识 [6,7]。
注 2 :证据等级:
Ⅰ级:进一步研究几乎不可能改变对临床疗效评估结果的可信度,为高级别证据。
Ⅱ级:进一步研究有可能对疗效评估结果的可信度有重要影响,且有可能改变评估结果,为中级别证据。
Ⅲ级:进一步研究很有可能对疗效评估结果的可信度有重要影响,且极有可能改变评估结果,为低级别证据。
Ⅳ级:任何疗效评估结果都不确定,为极低级别证据。
注 3 :推荐级别:
Grade A :基于可得证据,非常确定获益大于风险和负担,则做出强推荐。
Grade B :基于可得的证据,认为获益、风险和负担相当平衡,或获益、风险的程度存在明显的不确定,则做出弱推荐。
1 胃癌腹膜转移的发生机制
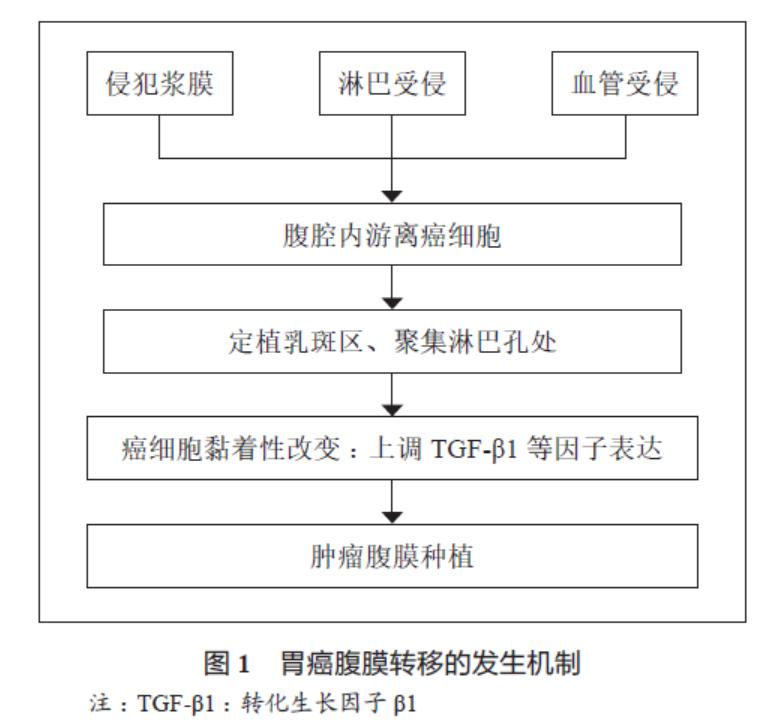
胃癌腹膜转移的发生机制尚不完全明确,"种子土壤"学说是目前认可度较高的发生机制理论 [8]。腹膜转移的发生取决于癌细胞(种子)和腹膜(土壤)的微环境 [9]。癌细胞分泌的转化生长因子 β1(transforming growth factor beta 1,TGF-β1)参与细胞外基质(extracellular matrix,ECM)的生成与成熟,而 ECM 可为 β1- 整联蛋白和 CD44H 提供配合基,最终促使游离癌细胞的浸润及黏附 [10,11] ;腹膜自身特异性结构(淋巴孔和乳斑区)也使得癌细胞易于"播种"。腹膜乳斑是一种特殊的免疫结构,由巨噬细胞围绕血管网构成,因为缺乏连续的间皮细胞层,容易造成游离癌细胞的定植[12,13]。此外,游离癌细胞聚集于连接乳斑区和腹膜下淋巴管的淋巴孔处,因淋巴孔特异性分布于横膈膜、肠系膜、网膜及盆腔腹膜的浆膜表面,故而这些部位在腹膜转移的早期就易受到累及 [5,12]。"种子土壤"学说发生机制的描述见图 1。
2 胃癌腹膜转移的诊断与分期
2.1 诊断
2.1.1 影像诊断 影像学诊断胃癌腹膜转移难度较大,通过典型征象确诊者多已属晚期,即使通过正电子发射型计算机断层显像(PET/CT)也难以在腹膜转移的早期阶段确诊,因而导致较高的假阴性率[14]。推荐 X 线计算机断层摄影(CT)作为胃癌腹膜转移的主要影像学检查手段[15-17]。CT诊断胃癌腹膜转移的敏感度为 33%~51%,特异度为95%~99%,优于超声(US)和 PET检查[16,18]。胃癌腹膜转移的典型CT征象包括:腹膜不均匀增厚、高强化或伴结节;网膜饼或大网膜多发索条、结节;肠系膜结节状增厚;腹盆腔大量积液 [18,19]。注意腹膜转移粘连侵犯导致的肾盂输尿管扩张、肝内外胆管扩张及肠梗阻等间接征象;注意少量腹水(尤其肝脾周围)对早期腹膜转移的提示意义。文献报道胃癌患者影像学检出腹水超过 50 ml,腹膜转移阳性率达75%~100%[17,20]。PACS工作站宽窗观察(脂肪间隙均质细颗粒状背景噪声清晰显示为准),避免遗漏小的转移灶;联合轴位、冠状位及矢状位三平面观察,提高对特殊部位转移灶的检出和定位能力;全面观察横结肠系膜、后腹膜、镰状韧带等胃周各韧带及系膜走行区域。MRI 可作为增强 CT 检查禁忌患者的备选手段,在低张和呼吸训练控制运动干扰的前提下可显示腹膜结构,并可应用扩散加权功能成像(DWI)辅助小转移灶的检出[21]。
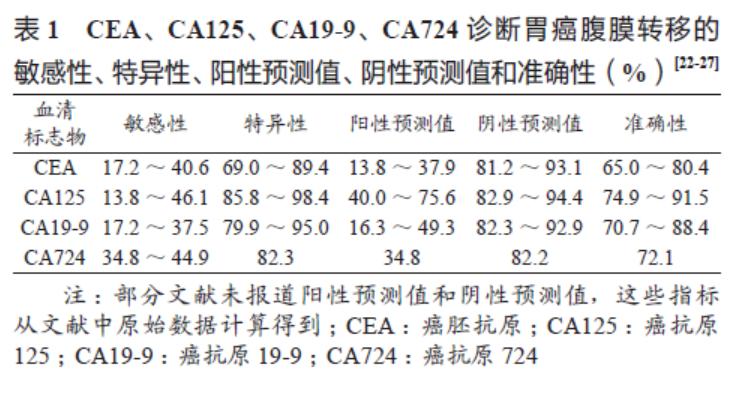
2.1.2 血清标志物检测 癌胚抗原(CEA)、癌抗原 125(CA125)、癌抗原 19-9(CA19-9)、癌抗原724(CA724)是胃癌常用的肿瘤标志物。尽管这些血清学指标的升高与腹膜转移呈正相关,但用于胃癌腹膜转移的诊断时,其敏感性和阳性预测值均较差。因腹膜间皮细胞在受到肿瘤侵犯时可以释放CA125入血,所以,理论上CA125是检测腹膜转移的潜在指标;尽管 CA125 的阳性预测值显著高于其他标志物,但其敏感性也无法满足临床需求。因此,血清标志物检测仅可作为辅助诊断,不作为腹膜转移诊断的依据。
2.1.3 诊断性腹腔镜检查 诊断性腹腔镜检查是有创检查,可以评估腹腔内的转移情况,了解腹膜转移的分布和大小,并获得明确的组织学及细胞学证据,用于指导制订临床治疗策略,进而评估治疗疗效及监测疾病进展 [28,29]。
目前,腹腔镜检查主要适用于进展期胃癌(cT2 ~ 4及任何 N 和 M)的治疗前诊断、术前治疗后的疗效评价 [29]。既往腹盆腔手术史明确、可疑严重腹腔粘连等无法接受腹腔镜手术、或心肺功能不能耐受麻醉及 CO2 气腹的患者,不能进行诊断性腹腔镜检查 [29]。
腹腔镜检查的手术操作规范如下 [29] :
(1)患者体位:平卧或平卧分腿位。
(2)建立气腹:气腹针穿刺或开放法,维持腹内压在 10 ~ 15 mmHg。
(3)放置套管:在脐下 1 cm 处作为观察孔,放置 10 或 12 mm 套管,右侧操作孔通常选择右侧腋前线与右肋弓交点下方 2 cm 处,放置 5 或 10 mm套管;左侧操作孔通常选择左侧腋前线与左肋弓交点下方 2 cm 处,放置 5 或 10 mm 套管;可酌情增加右侧第二操作孔,通常选择右侧腋前线平脐水平,放置 10 mm 套管。套管间应保持 5 cm 以上的距离。
(4)腹腔游离癌细胞检查:建立操作孔并充分止血后立即收集腹水或行腹腔灌洗,具体操作参见 2.1.4。
(5)腹腔探查:从右上腹开始,按顺时针方向进行,依次探查右侧膈肌和肝右叶、肝圆韧带、左侧膈肌和肝左叶、左侧壁腹膜及降结肠、盆腔和道格拉斯窝(女性注意探查双侧卵巢)、右侧壁腹膜及升结肠、大网膜、横结肠、结肠系膜、前腹壁、小肠及系膜,最后探查原发病灶及胃周淋巴结情况,记录肿瘤位置、大小、是否浸润浆膜、有无周围脏器浸润。对于胃体后壁肿瘤,需要切开胃结肠韧带,探查网膜囊,包括横结肠系膜和胰腺被膜。对腹腔内可疑病灶均应行快速冰冻病理检查,同时记录病灶位置、大小、是否融合及腹膜肿瘤指数(peritoneal cancer index,PCI)等;探查过程中可根据需要调整患者体位,推荐留取图片或录像作为记录。
(6)关闭切口:10 mm 以上切口需直视下缝合。
2.1.4 腹腔游离癌细胞检查 腹水或腹腔灌洗液细胞学检查是目前诊断腹腔内游离癌细胞的金标准,虽然其敏感性较低,但有助于发现肉眼无法识别的微转移。现有文献认为,腹腔内游离的癌细胞是形成腹膜转移的先决条件,是胃癌的独立预后不良因素 [30]。腹腔游离癌细胞阳性可作为Ⅳ期胃癌的独立诊断指标。诊断性腹腔镜检查应同时进行腹腔游离癌细胞检查。
腹腔游离癌细胞检查的操作规范如下 [29,31] :
(1)腹水的收集:如有足够量(≥ 200 ml)腹水则直接取腹水进行细胞学检查,如无腹水或腹水< 200 ml 者,则用> 250 ml 的温生理盐水依次冲洗双侧膈顶、肝下区、大网膜、双侧结肠旁沟及道格拉斯窝,避免直接冲洗原发病灶;于双侧膈下区、肝下区及道格拉斯窝收集> 100 ml 的灌洗液,行细胞学检查。
(2)标本的制作:腹水或腹腔冲洗液 2000 转离心 10 分钟;离心后小心吸出上清液,取细胞沉淀直接涂片 2 张,95% 乙醇固定至少 5 分钟,采用苏木精 - 伊红或巴氏染色法染色。
(3)结果的记录:腹腔细胞学检测结果阴性者记录为 CY0,阳性记录为 CY1。
综上,上述各项检查手段各有优劣,影像学和血清学检查欠缺敏感性,腹腔镜和病理学检查虽可确诊,但亦有一定的局限性,因此临床中需要综合患者的临床表现、病理分型、原发灶及转移淋巴结的分期、血清肿瘤标志物、影像学或功能影像等综合判定,必要时需要腹腔镜等有创检查手段进行明确。
2.2 分期
2.2.1 腹膜转移(P)(TNM 分期为 M1)[31] PX :有无腹膜转移不明者;P0 :无腹膜转移;P1 :有腹膜转移。
注 4 :结合我国目前临床现状,推荐采用日本胃癌学会制定的《胃癌分期规约》2010 年第 14 版中腹膜转移的分期标准,也可参考 2017 年第 15 版的分期标准。
PX :有无腹膜转移不明者
P0 :无腹膜转移
P1 :有腹膜转移
P1a:局限性转移(至仅局限在胃、大网膜、小网膜、横结肠膜前叶、胰腺膜、脾脏等附近
的腹膜)
P1b :转移至上腹部(横结肠至脏侧的腹膜)
P1c :转移至中下腹部
P1x :确定腹膜转移,但无法判断具体分布
注 5 :休格贝克腹膜癌指数(peritoneal carci-nomatosis index,PCI)是将腹膜瘤结节的分布和大小进行评分,而反映腹膜转移状况的一种分级方法。研究显示,PCI 与胃癌腹膜转移患者预后有一定的相关性 [32]。但考虑操作难度较大,且目前尚无基于此分级的治疗推荐,因此未在共识中引用。
2.2.2 腹腔游离癌细胞(CY)[31] CYX :未行腹腔灌洗液细胞学检查;CY0 :腹腔灌洗液细胞学检查无癌细胞;CY1 :腹腔灌洗液细胞学检查有癌细胞。
3 胃癌腹膜转移的预防
3.1 风险因素
(1)TNM 分 期 T3、T4 和 N+ :T3、T4 及 N+患者腹膜转移发生率为 25%,而 T1、T2 及 N0 患者仅为 4%[33] ;另外,N+ 患者发生腹膜转移风险较N0 患者高出 3.84 倍[34]。
(2)淋巴结外浸润:与没有淋巴结外浸润的患者相比,有淋巴结外浸润患者的腹膜转移风险上升近 18 倍 [35]。
(3)Borrmann 分型Ⅲ、Ⅳ:与 Borrmann Ⅰ、Ⅱ型患者相比,Borrmann Ⅲ、Ⅳ型患者的腹膜转移风险高出 2.06 倍,是独立风险因素 [36]。
(4)Lauren 分型弥漫型:弥漫型患者中腹膜转移发生率高达 80% 以上 [37]。
3.2 预防措施
3.2.1 外科预防 - 无瘤技术 可切除患者手术过程中应严格按照无瘤规范进行操作,尽量避免因手术操作而导致癌细胞脱落种植于腹腔内,防止医源性扩散。无瘤操作规范的建议如下 [38] :
(1)切口的保护:推荐常规使用切口保护套,特别注意切口上、下端的保护。
(2)手术时避免直接接触、挤压肿瘤,若肿瘤浸出浆膜层应以医用胶、纱布或手术薄膜覆盖。
(3)术中及时更换污染的手套及器械:探查、分离肿瘤时医生的手若触及破溃的肿瘤应及时更换手套,术中分离肿瘤的器械不可反复使用。
(4)拭血纱布要及时更换,不可反复使用。
(5)术毕用温热蒸馏水或生理盐水彻底冲洗术野及腹腔,冲洗液量应至少> 3000 ml。
(6)关腹前充分冲洗切口。
3.2.2 术后辅助化疗 术后通过系统性给药进行辅助化疗,可以杀灭手术无法清除的微小病灶,是降低术后复发和转移的有效手段。目前,临床常用口服氟尿嘧啶类药物 [ 替吉奥(S-1)、卡培他滨(CAP)] 单药或联合奥沙利铂(OXA)作为术后辅助化疗方案。为预防术后腹膜转移,辅助化疗方案的选择应考虑药物的特点。传统氟尿嘧啶类药物分子量小容易穿透血腹屏障,适合用于术后辅助化疗,但因其迅速被二氢嘧啶脱氢(DPD)分解代谢而失去抗肿瘤活性。新型口服氟尿嘧啶类药物 S-1 不仅可以穿透血腹屏障,而且含有吉美嘧啶(CDHP)能有效阻止 5- 氟尿嘧啶(5-FU)分解,所以可维持有效的药物浓度 [39]。
推荐方案:
S-1 80 ~ 120 mg/d,口服 4 周,停药 2 周,6周为一疗程;持续 1 年(Ⅱ级,Grade A);紫杉醇(PTX)序贯 S-1(Ⅲ级,Grade B);S-1/ 顺铂(CDDP)序贯 S-1,S-1/ 多西他赛(DOC)序贯 S-1,DOC/CAP/CDDP(Ⅳ级,Grade B)
循证证据:
(1)Sasako 等 [40] 在Ⅲ期随机对照研究 ACTS-GC 中纳入了 1059 例Ⅱ~Ⅲ期胃癌患者,比较单纯手术和 S-1 术后辅助化疗持续 1 年的疗效。结果显示,S-1 辅助化疗优于单纯手术 [5 年生存率分别为 61.1%和 71.7%,HR= 0.669,95%置信区间(CI):0.540 ~ 0.828],S-1 辅助化疗组较单纯手术组的术后腹膜转移风险显著降低了 31%。
(2)Kanda 等 [41] 回 顾 性 纳 入 了 70 对(140例)配对的Ⅱ~Ⅲ期胃癌患者使用倾向性匹配分析(prop ensity score matching analysis),发现 S-1 辅助化疗组较单纯手术预后更佳(3 年无复发率 71% ︰53%,P = 0.035),且腹膜转移率明显降低(5.7% ︰18.6%,P = 0.017)。
(3)Tsuburaya 等 [42] 在Ⅲ期随机对照研究SAMIT 中纳入了 1495 例 T4a 和 T4b 的胃癌患者,比较 PTX 序贯复方替加氟(UFT)或 S-1 和单药UFT 或 S-1 的疗效。PTX 序贯 S-1 组(355 例)较S-1 组(364 例)[ 第 1 ~ 14 天 S-1 80 mg/(m2•d),每 3 周一周期,持续 48 周 ] 有生存获益的趋势(但差异无显著性)及较小的腹膜转移风险(17% ︰22%,P 值不详)。因此,PTX 序贯 S-1 辅助化疗不劣于单药 S-1。
(4)Takahari 等 [43] 在一项Ⅱ期研究中,对纳入的 63 例Ⅲ期胃癌患者使用 S-1/CDDP 序贯 S-1辅助化疗(SP 方案)共 3 周期:第 1 ~ 21 天 S-180 mg/(m2•d),第 8 天 CDDP 60 mg/m2,每 5 周一周期;第 1 ~ 28 天序贯 S-1 80 mg/(m2•d),每6 周一周期,至术后 1 年 ]。3 年无复发生存率为74.1%(95%CI :60.8% ~ 83.5%),3 年生存率为84.5%(95%CI :72.3% ~ 91.6%),腹膜转移率为12.7%(8/63)。
(5)Fujitani 等 [44] 在一项Ⅱ期研究中,对纳入的 53 例Ⅲ期胃癌患者使用 S-1/DOC 序贯 S-1辅助化疗 [ 第 1 ~ 14 天 S-1 80 mg/(m2•d),第 1天 DOC 40 mg/m2,每 3 周一周期,共 4 周期;第1 ~ 28 天 S-1 80 mg/(m2•d),每 6 周一周期,至术后 1 年 ],3 年无复发生存率为 66.2%(95%CI :54.4% ~ 80.7%),3 年生存率为 78.4%(95%CI :67.9% ~ 90.6%),腹膜转移率为 7.5%(4/53)。
(6)Yoon 等 [45] 在一项Ⅱ期研究中,对纳入的 43 例Ⅲ b ~Ⅳ期(AJCC6,pT3N2,pT4N1 ~ 2M0,pTanyN3M0)胃癌患者使用 6 周期的 DOC/CAP/CDDP [ 第 1 天 DOC 60 mg/m2,第 1 ~ 14 天 CAP1875 mg/(m2•d), 第 1 天 CDDP 60 mg/m2, 每 3周一周期 ],平均随访 56.1 个月,3 年和 5 年无复发生存率分别为 48% 和 39%,3 年和 5 年发生存率分别为 59%和 41%,腹膜转移率为 27.9%(12/43)。
3.2.3 预防性腹腔热灌注化疗 腹腔内热灌注化疗(hyperthermic intraperitoneal chemotherapy,HIPEC)的优势是药物直接作用于癌细胞,影响腹膜微环境,抑制癌细胞种植;另一优点是不良反应小,对机体的免疫力影响小 [46]。但是,目前 HIPEC 作为预防性手段的临床证据不足,仍需进一步探索。本共识认为具有风险因素(参见 3.1)的患者,可以考虑术中预防性应用 HIPEC(Ⅲ级,Grade B)。
循证证据:
(1)一项荟萃分析显示,术中 HIPEC 单独(HR = 0.60 ;95%CI :0.43 ~ 0.83 ;P = 0.002)或合并早期术后腹腔化疗(HR = 0.45 ;95%CI :0.29 ~ 0.68 ;P = 0.0002)显著改善胃癌患者生存。术中腹腔常温灌注化疗有改善生存趋势(P =0.06),但是单独早期术后腹腔化疗或延迟术后腹腔化疗均无显著效果 [47]。
(2)Fujimoto 等 [48] 在一项术中 HIPEC 的随机对照研究中纳入了 141 例有浆膜浸润的胃癌手术患者,结果显示,HIPEC 组 [ 含丝裂霉素(MMC)10 μg/ml 的灌注液 3000 ~ 4000 ml 循环 120 分钟 ] 患者较对照组腹膜复发率显著降低(P = 0.000 084 7),其 2、4、8 年生存率分别为 88%、76%、62%,而对照组患者分别为 77%、58%、49%(P = 0.0362)。
(3)朱正纲等 [49] 的一项非随机对照研究显示,无腹膜转移的 T3、T4 患者术中给予 HIPEC(42 例,CDDP 50 mg/L 和 MMC 5 mg/L,总灌注药量为5000 ~ 6000 ml)优于单纯手术患者(54 例),术后 1、2、4 年 HIPEC 组患者生存率分别为 85.7%、81.0%、63.9%,单纯手术组患者分别为 77.3%、61.0%、50.8% ;HIPEC 组患者术后腹膜复发率(10.3%)低于单纯手术组(34.7%)。
4 胃癌腹膜转移的治疗
4.1 P1 CY0/1 胃癌患者的治疗
4.1.1 全身系统化疗 全身系统化疗是晚期胃癌的一种有效治疗方式,优于最佳支持治疗 [50]。目前,临床常用的氟尿嘧啶类联合铂类的两药方案疗效优于单药方案,毒性小于三药方案 [51]。腹膜转移是胃癌全身性疾病的局部表现,全身系统化疗是胃癌腹膜转移的标准治疗,也可根据患者一般状况、合并症、有无腹水、不良反应等结合腹腔化疗等局部治疗手段。
推荐方案:
S-1/CDDP(Ⅱ级,Grade A)、S-1/OXA(Ⅱ级,Grade A)、PTX(Ⅲ级,Grade A)、S-1单药(Ⅲ级,Grade A)、5-FU 持续静脉滴注(Ⅲ级,Grade A)
循证证据:
(1)Koizumiet 等 [52] 在Ⅲ期随机对照研究SPIRITS 中,共纳入 305 例晚期胃癌患者,比较SP 方案(S-1/CDDP)和 S-1 单药方案一线治疗晚期胃癌的疗效和安全性。结果显示:SP 组患者中位总生存时间(overall survival,OS)较单药组显著延长(13.0 个月︰ 11.0 个月,P = 0.04)。亚组分析显示:SP 方案对腹膜转移患者的疗效更佳(HR = 0.52,95%CI :0.33 ~ 0.82,P = 0.02)。
(2)Yamada 等 [53] 在Ⅲ期随机对照临床研究G-SOX 中,共纳入 685 例晚期胃癌患者,比较SOX 方案与 SP 方案一线治疗晚期胃癌的疗效和安全性。结果显示,SOX 组患者的中位无进展生存时间(progression free survival,PFS)非劣于 SP 组(5.5个月︰ 5.4 个月,HR = 1.004,95%CI:0.840 ~ 1.199,P = 0.0044),且 SOX 组毒性更低。亚组分析显示:SOX方案对腹膜转移患者的疗效更佳(HR=0.646,95%CI :0.433 ~ 0.946,P = 0.032)。
(3)Shirao 等 [54] 在Ⅲ期随机对照临床研究JCOG0106 中,共纳入 237 例胃癌腹膜转移患者,比较了 5-FU 单药静脉连续注射与 5-FU 联合甲氨蝶呤(MTX)的疗效和安全性。结果显示:联合方案并未延长患者生存期(中位 OS:10.6 个月︰ 9.4个月,P = 0.31),反而增加了血液学毒性。
(4)Boku 等 [55] 在Ⅲ期随机对照临床研究JCOG9912 中,共纳入 704 例晚期胃癌患者,比较5-FU 单药静脉连续注射、S-1 单药方案以及伊立替康(CPT-11)/CDDP 方案的疗效和安全性。结果显示:三组患者的中位 OS 分别为 10.8 个月、11.4个月。亚组分析显示:对于腹膜转移的胃癌患者,与 单 药 5-FU 相 比,S-1(P = 0.83) 或 CPT-11/CDDP(P = 0.07)并无明确的生存获益,且 CPT-11/CDDP 出现的 3/4 级血液学毒性更加明显。
(5)目前大型的Ⅲ期临床研究,涉及腹膜转移亚组分析的临床研究还包括 REGARD(二线雷莫卢单抗对比安慰剂)、RAINBOW(二线雷莫卢单抗 /PTX 对比雷莫卢单抗)、WJOG 4007(二线 PTX对比 CPT-11)和 GC0301/TOP-002(一线 S-1/CPT-11 对比 S-1),但上述研究并未发现某种治疗方案优于对照组 [56-59]。
(6)Nishina 等 [60] 在一项Ⅱ期多中心随机对照临床试验(JCOG0407)中,纳入 110 例经一线 5-FU方案(5-FU 持续静脉滴注或 5-FU 联合 MTX)治疗失败的腹膜转移患者,随机分至二线 PTX 组(第1、8、15 天 PTX 80 mg/m2,每 4 周一周期)或另一种 5-FU 方案组(即一线使用 5-FU 持续静脉滴注者二线使用 5-FU 联合 MTX,反之亦然)。PTX组和最佳 5-FU 的中位 OS 和中位 PFS 分别为 7.7个月︰ 7.7 个月和 3.7 个月︰ 2.4 个月(HR = 0.58,95%CI :0.38 ~ 0.88)。
(7)Moehler 等 [61] 在一项Ⅱ期多中心随机对照临床试验中,纳入了 114 例晚期胃癌患者,比较ILF 方案(CPT-11 /醛氢叶酸/ 5-FU)与 ELF 方案(足叶乙甙/醛氢叶酸/ 5-FU)一线治疗晚期胃癌的疗效和安全性。结果显示,ILF 组和 ELF 组患者的 PFS 和 OS 分别为 4.5 个月︰ 2.3 个月(HR =1.10,95%CI :0.75 ~ 1.62,P = 0.6116) 和 10.8个月︰ 8.3 个月(HR = 1.25,95%CI:0.83 ~ 1.86,P = 0.2818)。亚组分析显示:对于腹膜转移患者,ELF 组较 ILF 组的死亡风险更高(HR = 2.41,95%CI :0.99 ~ 5.82)。
综合已有研究证据,专家组推荐:对于一般情况良好的患者,予以 SP 或 SOX 方案(对于腹水较多的患者,因 CDDP 所需的水化可能导致腹水增多,故此类患者首选 SOX 方案);对于一般状况较差的患者,可考虑单药化疗(PTX、S-1、5-FU持续静脉滴注)。
4.1.2 腹腔灌注化疗 腹腔灌注化疗可以提高局部药物浓度,减轻全身不良反应。由于腹膜转移是全身系统性疾病的局部反应,因此全身系统化疗仍为核心治疗方案,腹腔灌注化疗为补充。目前,尚无大型临床研究确证腹腔灌注化疗的疗效,在 PHOENIX-GC 研究中观察到腹腔灌注 PTX 对中量腹水患者的临床疗效。因此应结合腹水分级考虑在系统化疗的基础上添加腹腔灌注化疗。国内有一些观察性研究和Ⅱ期研究显示,5-FU/CDDP/PTX/DOX 腹腔灌注化疗联合 CF/5-FU/OXA 对于晚期胃癌合并恶性腹水患者有一定疗效。
推荐方案:PTX(腹腔灌注化疗)联合 S-1/PTX(Ⅲ级,Grade B);5-FU/CDDP(腹腔灌注化疗)联合 5-FU/CAP/OXA(Ⅲ级,Grade B)
循证证据:
(1)Ishigami 等 [62] 在Ⅲ期随机对照临床研究PHOENIX-GC 中,将 183 例胃癌腹膜转移患者以2 ︰ 1 的比例随机分配至 IP 组 [PTX 腹腔灌注化疗联合 S-1/PTX 全身化疗方案:第 1、8 天 PTX 灌注 20 mg/m2,静脉滴注 50 mg/m2,第 1 ~ 14 天S-1 80 mg/(m2•d),每 3 周一周期 ] 或 SP 组 [ 第8 天静脉滴注 CDDP 60 mg/m2,第 1 ~ 21 天 S-180 mg/(m2•d),每 5 周一周期 ]。结果显示,IP 组和 SP 组患者的中位 OS 分别为 17.7 个月和 15.2 个月(HR = 0.72,95%CI:0.49 ~ 1.04,P = 0.08)。腹水量是影响预后的重要因素。将基线腹水因素进行校正后显示,IP 组患者的生存获益显著(17.7个月︰ 14.3 个月,HR = 0.64,95%CI:0.43 ~ 0.94,P = 0.023),特别是在中量腹水(腹水位于盆腔以上)的患者中,两组的差异明显(13.0 个月︰ 6.8个月,HR = 0.38)。
(2)李燕等 [63] 的一项观察性研究,纳入 81 例胃肠道恶性肿瘤并发腹腔积液患者,观察腹腔持续引流后直接腹腔化疗联合全身化疗治疗的疗效及不良反应。腹腔灌注药物氟尿嘧啶类药物和(或)CDDP,之后 1 周行以 5-FU 或 CAP 为基础联合表柔比星(EPI)、CDDP(或 OXA),进行 2 ~ 4 个周期的全身化疗。结果显示,81 例患者中腹腔积液完全缓解(CR)16 例(19.8%),部分缓解(PR)18 例(22.2%),稳定(SD)27 例(33.3%),进展(PD)20 例(24.7%),总有效(CR + PB)率为 42% ;总获益(CR + PR + SD)率为 75.3%,中位进展时间为 4 个月,中位生存期为 5.3 个月,1年生存率为 16.0%。
(3)黄万中等 [64] 在一项Ⅱ期临床研究中,纳入 43 例Ⅲ b ~Ⅳ期胃癌患者(其中 14 例合并腹膜转移),旨在评价多西紫杉醇腹腔灌注化疗联合CF/5-FU/OXA 的临床疗效和安全性。结果显示,多西紫杉醇腹腔灌注化疗联合全身化疗总有效(CR+ PR)率为 58.1%,1 年生存率为 67.4%,且患者对不良反应可以耐受。
(4)李翔 [65] 在一项观察性研究中,纳入23例晚期胃癌合并癌性腹水患者,给予 PTX 60 mg/m2 腹腔灌注,第 1、5、8 天;亚叶酸钙(LV)200 mg/m2静脉滴注 2 小时,第 1 ~ 4 天;5-FU 750 mg/m2 持续静脉滴注 24 小时,每天 1 次,第 1 ~ 4 天;OXA130 mg/m2 静脉滴注 2 小时,第 1 天。每 21 天为一周期,每 2 个周期评价疗效。结果显示,有效率为69.6%,疾病控制率为 86.9%,中位肿瘤进展时间为6.6 个月,1年生存率为 71.0%。
4.1.3 手术 对于确诊为腹膜转移的初治患者,现有证据显示手术联合化疗较单纯化疗没有显示生存优势,不推荐手术治疗。如果存在外科急症,如肠梗阻、出血、顽固性腹水等,多学科协作(multidisciplinary team, MDT)讨论后,可以考虑通过姑息性手术缓解相关症状。对于化疗后出现明确腹膜转移缓解(CY0P0)的患者,如一般状况较好,经过 MDT 讨论后,可以考虑手术治疗 [66]。但目前手术治疗胃癌腹膜转移仍缺乏前瞻性高级别证据,无论是减瘤手术还是姑息性手术,术后的获益人群仍然需要进一步明确 [67]。
5 胃癌腹膜转移相关并发症的处理
当胃癌腹膜转移患者出现癌性腹水和肠梗阻等并发症时,患者的生活质量和预后较差 [68]。针对并发症,目前分为对症治疗和抗肿瘤治疗两部分:对症治疗是以缓解症状为主的治疗,如腹水引流、利尿剂、低钠饮食、改善肠梗阻、维持营养状况等 [69] ;抗肿瘤治疗是根据患者并发症的程度,经MDT 讨论后,个体化地选择系统化疗、局部灌注治疗或最佳支持治疗。
5.1 对症治疗
5.1.1 癌性腹水的控制 约 10% 的胃癌患者存在腹水,而对于检出腹水> 50 ml 的胃癌患者,腹膜转移的发生率高达 75% 以上 [70]。腹水患者常伴腹痛、厌食、腹胀、恶心等症状,以及黄疸和肠梗阻等并发症,临床处理难度极大 [71]。针对癌性腹水,尚无基于循证证据的治疗指南。目前,腹水引流仍然是临床控制腹水的主要手段,每日引流量应根据患者症状、血电解质、白蛋白水平综合考虑。反复穿刺放腹水有引起有效循环血量下降、低钠血症、肾功能障碍、低白蛋白血症以及感染等并发症的危险 [72]。腹腔置管引流术适用于腹腔穿刺放液并发严重电解质紊乱或需反复腹腔穿刺放液的患者。该方法极少引起电解质紊乱,少有凝血机制障碍的危险,且引流管不易阻塞 [73,74]。
5.1.2 恶性肠梗阻的改善 恶性肠梗阻是胃癌腹膜转移发生后的主要临床表现之一,此类患者占恶性肠梗阻患者总数的 30% ~ 40%。目前因认识不足,缺乏有效的治疗手段,临床主要的处理原则是对症治疗 [75]。药物治疗需要联合应用抗分泌药物、止痛、止吐药物以及激素类药物来达到缓解恶性肠梗阻症状的目的 [76]。生长抑素类似物可达到良好的止吐效果 [77] ;皮质类固醇激素不仅可以发挥止吐作用,还可以减轻肿瘤周围及肠道的炎性病变和水肿,从而使肠梗阻得到缓解;抗胆碱类药物可减少消化道平滑肌运动 [78]。
此类患者通常不适宜手术治疗,或因术后的高死亡率及高并发症发生率而无法获益 [79]。但对于肿瘤引起的单一部位梗阻或非癌性因素导致的机械性梗阻,手术可作为治疗选择。
自扩张金属支架置入适用于胃幽门、十二指肠及结直肠梗阻的姑息治疗,被认为是腹腔转移癌所致结直肠梗阻的首选治疗方式 [80]。但对于多部位梗阻及腹腔广泛转移的患者,支架治疗属于禁忌。
全胃肠外营养(total parenteral nutrition,TPN)可改善患者的一般状况,纠正营养不良,TPN 适用于Karnofsky评分> 50分、预计生存时间> 2~ 3个月、瘤生长缓慢、可能接受进一步化疗、肿瘤尚未引起其他重要脏器功能损害的患者 [81]。
5.2 抗肿瘤治疗 腹水是影响患者生存预后的核心因素之一。临床实际中,不同腹水量患者的生存预后具有较大的差异。经 CT 检查评估腹水量将患者分级为:无腹水、少量腹水(腹水在盆腔以下)、中量腹水(腹水在盆腔以上)及大量腹水(腹水蔓延至整个腹腔并伴有症状),分别考虑予以不同的治疗策略 [62,82]。
5.2.1 无 / 少量腹水患者 全身系统化疗为核心治疗,参见 5.1.1。
5.2.2 中量腹水患者 在全身系统化疗的基础上,可以考虑联合腹腔灌注化疗,可以有效地控制腹水,改善生活质量,延缓恶液质,参见 4.1.2。
5.2.3 大量腹水患者 由于预期生存较差,大量腹水的患者往往被排除在临床研究之外。因反复引流以及多种临床症状,该类患者往往难以实施抗肿瘤治疗。为此,针对该类患者,引流缓解症状配合最佳支持治疗仍然是主要的治疗手段。对于腹水控制良好且体能较好的患者,可以经 MDT 讨论后给予抗肿瘤治疗。
6 结语
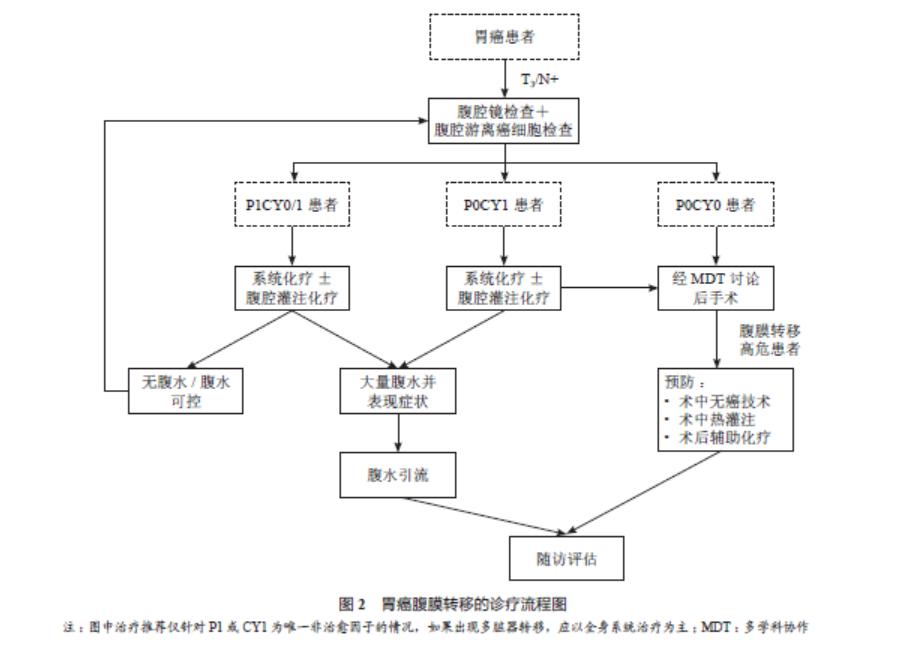
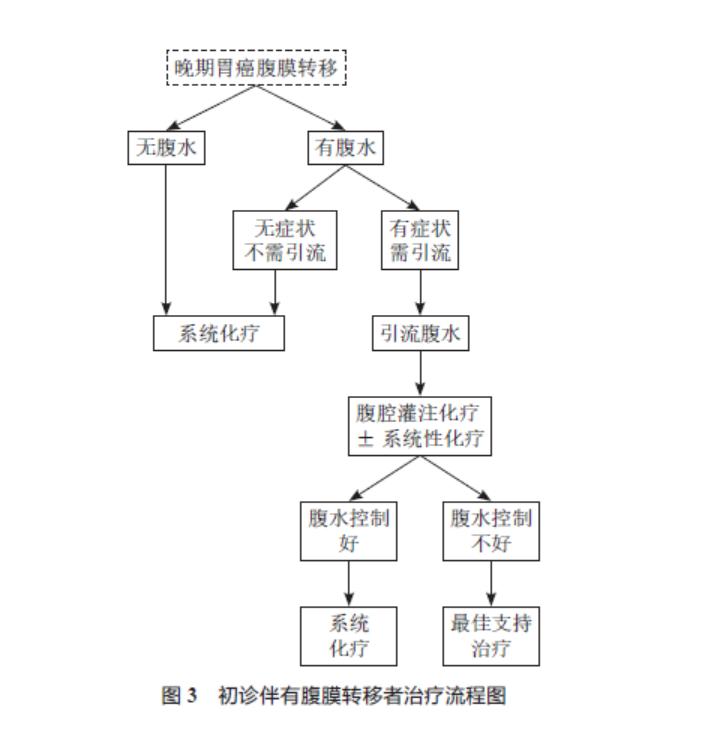
本共识以循证证据和临床现实为基础、以规范中国胃癌腹膜转移患者诊疗现状为出发点、以综合国内胃癌领域专家认知为原则而撰写。力求简单实用、科学严谨,具有普遍适用性。部分尚未在国内上市的药物(如卡妥索单抗),以及尚在研究阶段的治疗方案(如减瘤手术、术前新辅助腹腔灌注化疗、腹腔灌注贝伐珠单抗等),未列入其中。希望通过本共识的制定,能为广大临床医师提供工作参考。胃癌腹膜转移的诊疗流程见图 2。初诊伴有腹膜转移者治疗流程图见图 3。随着更多高级别临床研究的公布,专家委员会将及时对本共识内容进行更新和补充,以期不断提高我国胃癌的诊治水平。
致谢
中国抗癌协会胃癌专业委员会《胃癌腹膜转移防治中国专家共识》制定专家组(排名不分先后,以姓氏拼音顺序排列):
组 长:季加孚
副组长:沈 琳,徐惠绵,徐瑞华,朱正纲
执 笔:程向东,刘云鹏,李子禹 ,陕 飞,沈 琳,孙 宇,唐 磊,周 军,张小田

参考文献
[1] Globocan 2012: Estimated cancer incidence, mortality and prevalence worldwide in 2012 [Internet] WHO: International Agency for Research on Cancer[EB/OL]. [Accessed 8 April 2016] Available from: http://globocan.iarc.fr/Default.aspx.
[2] Shen L, Shan YS, Hu HM, et al. Management of gastric cancer in Asia: resource-stratified guidelines[J]. Lancet Oncol, 2013, 14(12):e535-547.
[3] Nashimoto A, Akazawa K, Isobe Y, et al. Gastric cancer treated in 2002 in Japan: 2009 annual report of the JGCA nationwide registry[J]. Gastric Cancer, 2013, 16(1):1-27.
[4] Fushida S, Oyama K, Kinoshita J, et al. Intraperitoneal Chemotherapy as a Multimodal Treatment for Gastric Cancer Patients with Peritoneal Metastasis[J]. J Cancer Ther, 2013, 4 (9A):6-15.
[5] Yonemura Y, Bandou E, Kawamura T, et al. Quantitative prognostic indicators of peritoneal dissemination of gastric cancer[J]. Eur J Surg Oncol, 2006, 32(6):602-606.
[6] Dalkey N, Helmer O. An Experimental Application of the Delphi Method to the Use of Experts[J]. Management Science, 1963, 9(3):458-467.
[7] Atkins D, Best D, Briss PA, et al. Grading quality of evide nce and strength of recommendations[J]. BMJ, 2004, 328(7454): 1490-1494.
[8] Paget S. Distribution of secondary growths in cancer of the breast[J]. Cancer Metastasis Rev, 1989, 8(2):98-101.
[9] Fidler IJ. The pathogenesis of cancer metastasis: the ’seed and soil’ hypothesis revisited[J]. Nat Rev Cancer, 2003, 3(6):453-458.
[10] Ahmed N, Riley C, Rice G, et al. Role of integrin receptors for fibronectin, collagen and laminin in the regulation of ova rian carcinoma functions in response to a matrix microenv iron-ment[J]. Clin Exp Met, 2005, 22(5):391-402.
[11] Miyazono K, Suzuki H, Imamura T. Regulation of TGF-β signaling and its roles in progression of tumors[J]. Cancer Sci, 2003, 94(3):230-234.
[12] Al-Shammaa HA, Li Y, Yonemura Y. Current status and future strategies of cytoreductive surgery plus intraperitoneal hyperthermic chemotherapy for peritoneal carcinomatosis[J]. World J Gastroenterol, 2008, 14(8):1159-1166.
[13] 徐惠绵,武建华.胃癌腹膜转移机理及其临床应用的研究进展 [J].中国肿瘤临床,2012,39(22):1687-1690.
[14] Lim JS, Kim MJ, Yun MJ, et al. Comparison of CT and 18F-FDG pet for detecting peritoneal metastasis on the preoper-ative evaluation for gastric carcinoma[J]. Korean J Radiol, 2006, 7(4):249-256.
[15] Kwee RM, Kwee TC. Modern imaging techniques for preope-rative detection of distant metastases in gastric cancer[J]. World J Gastroenterol, 2015, 21(37):10502-10509.
[16] Wang Z, Chen JQ. Imaging in assessing hepatic and peritoneal metastases of gastric cancer: a systematic review[J]. BMC Gastroenterol, 2011, 11:19.
[17] Yajima K, Kanda T, OhashiM, et al. Clinical and diagnostic significance of preoperative computed tomography findings of ascites in patients with advanced gastric cancer[J]. Am J Surg,2006, 192(2):185-190.
[18] Kim SJ, Kim HH, Kim YH, et al. Peritoneal Metastasis: Detection with 16- or 64-Detector Row CT in Patients Underg-oing Surgery for Gastric Cancer[J]. Radiology, 2009, 253(2): 407-415.
[19] 严超,朱正纲, 燕敏,等.多排 CT 对胃癌腹膜转移术前预测的单中心大宗病例研究 [J].中华胃肠外科杂志,2010,13(2):106-10.
[20] Chang DK, Kim JW, Kim BK, et al. Clinical significance of CT-defined minimal ascites in patients with gastric cancer[J]. World J Gastroenterol, 2005, 11(42):6587-6592.
[21] Fehniger J, Thomas S, Lengyel E et al. A prospective study evaluating diffusion weighted magnetic resonance imaging (DW-MRI) in the detection of peritoneal carcinomatosis in suspected gynecologic malignancies[J]. Gynecol Oncol, 2016, 142(1):169-175.
[22] 周鹏,曲辉,史惠文,等.血清糖类抗原 125 对胃癌腹膜转移及其预后的预测价值 [J].中华胃肠外科杂志,2014,17(10):1027-1030.
[23] Lai H, Jin Q, Lin Y, et al. Combined use of lysyl oxidase, carcino-embryonic antigen, and carbohydrate antigens improves the sensitivityof biomarkers in predicting lymph node metastasis and peritoneal metastasis in gastric cancer[J]. Tumour Biol, 2014, 35(10):10547-10554.
[24] Emoto S, Ishigami H, Yamashita H, et al. Clinical significance of CA125 and CA72-4 in gastric cancer with peritoneal dissem-ination[J]. Gastric Cancer, 2012, 15(2):154-161.
[25] Nakata B, Hirakawa-YS Chung K, Kato Y, et al. Serum CA 125 level as a predictor of peritoneal dissemination in patients with gastric carcinoma[J]. Cancer, 1998, 83(12):2488-2492.
[26] Hwang GI, Yoo CH, Sohn BH, et al. Predictive Value of Preoperative Serum CEA, CA19-9 and CA125 Levels for Perit-o neal Metastasis in Patients with Gastric Carcinoma[J]. Cancer Res Treat, 2004, 36(3):178-181.
[27] 张永乐, 薛英威,蓝秀文,等.肿瘤标记物 CA19-9、CEA 对胃癌转移和预后预测价值的分析 [J].哈尔滨医科大学学报,2010,44(2):181-188.
[28] National Comprehensive Cancer Network: NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Gastric Cancer Version 3[EB/OL]. (2015-03-23). https://www.nccn.org/professionals/physician_gls/f_guidelines.asp
[29] Li Z, Ji J. Application of laparoscopy in the diagnosis and treatment of gastric cancer[J]. Ann Transl Med, 2015, 3(9):126.
[30] Lee SD, Ryu KW, Eom BW, et al. Prognostic significance of peritoneal washing cytology in patients with gastric cancer[J]. Br J Surg, 2012, 99(3):397-403.
[31] Japanese Gastric Cancer Association. Japanese Classification of Gastric Carcinoma (The 14th Edition)[M]. Tokyo: 金原出版株式会社, 2010.
[32] Yonemura Y, Elnemr A, Endou Y, et al. Multidisciplinary therapy for treatment of patients with peritoneal carcinomatosis from gastric cancer[J]. World J Gastrointest Oncol, 2010, 2(2):85-97.
[33] De Andrade JP, Mezhir JJ. The critical role of peritoneal cytology in the staging of gastric cancer: an evidence-based review[J]. J Surg Oncol, 2014, 110:291-297.
[34] Yoo CH, Noh SH, Shin DW, et al. Recurrence following curative resection for gastric carcinoma[J]. Br J Surg, 2000, 87(2):236-242.
[35] Tanaka T, Kumagai K, Shimizu K, et al. Peritoneal metastasis in gastric cancer with particular reference to lymphatic advan-cement; Extranodal invasion is a significant risk factor for peritoneal metastasis[J]. J Surg Oncol, 2000, 75(3):165-171.
[36] Huang B, Sun Z, Wang Z, et al. Factors associated with peritoneal metastasis in non-serosa-invasive gastric cancer: a retrospective study of a prospectively-collected database[J]. BMC Cancer, 2013, 13:57.
[37] Esaki Y, Hirayama R, Hirokawa K. A comparison of patterns of metastasis in gastric cancer by histologic type and age[J]. Cancer, 1990, 65(9):2086-2090.
[38] 季加孚.胃肠道恶性肿瘤外科的无瘤技术和原则 [J].中国实用外科杂志,2005,25(4):254-256.
[39] Oshima T, Yamada R, Hatori S, et al. Pharmacokinetics of S-1 in patients with peritoneal dissemination of gastric cancer[J]. Oncol Rep, 2006, 16(2):361-366.
[40] Sasako M, Sakuramoto S, Katai H, et al. Five-Year Outcomes of a Randomized Phase Ⅲ Trial Comparing Adjuvant Chemo-therapy with S-1 Versus Surgery Alone in Stage Ⅱ or Ⅲ Gast-ric Cancer[J]. J Clin Oncol, 2011, 29(33):4387-4393.
[41] Kanda M, Murotani K, Kobayashi D, et al. Postoperative adjuvant chemotherapy with S-1 alters recurrence patterns and prognostic factors amongpatients with stage Ⅱ/Ⅲ gastric cancer: A propensity score matching analysis[J]. Surgery, 2015, 158(6):1573-1580.
[42] Tsuburaya A, Yoshida K, Kobayashi M, et al. Sequential paclitaxel followed by tegafur and uracil (UFT) or S-1 versus UFT or S-1monotherapy as adjuvant chemotherapy for T4a/b gastric cancer (SAMIT): a phase 3factorial randomised controlled trial[J]. Lancet Oncol, 2014, 15(8):886-893.
[43] Takahari D, Hamaguchi T, Yoshimura K, et al. Survival analysis of adjuvant chemotherapy with S-1 plus cisplatin for stage Ⅲ gastric cancer[J]. Gastric Cancer, 2014, 17(2):383-386.
[44] Fujitani K, Tamura S, Kimura Y, et al. Three-year outcomes of a phase Ⅱ study of adjuvant chemotherapy with S-1 plus docetaxel for stage Ⅲ gastriccancer after curative D2 gastrectomy[J]. Gastric Cancer, 2014, 17(2):348-353.
[45] Yoon S, Yoo C, Ryu MH, et al. Phase 2 study of adjuvant chemotherapy with docetaxel, capecitabine, and cisplatin in patients with curativelyresected stage Ⅲ B- Ⅳ gastric cancer[J]. Gastric Cancer, 2017, 20(1):182-189.
[46] 梁寒.胃癌腹膜转移的诊治策略 [J].中国肿瘤临床,2012,39(22):1696-1698.
[47] Yan TD, Black D, Sugarbaker PH, et al. A systematic review and meta-analysis of the randomized controlled trials on adjuvant intraperitoneal chemotherapy for resectable gastric cancer[J]. Ann Surg Oncol, 2007, 14(10):2702-2713.
[48] Fujimoto S, Takahashi M, Mutou T, et al. Successful intrape-ritoneal hyperthermic chemoperfusion for the prevention of postoperative peritoneal recurrence in patients with advanced gastric carcinoma[J]. Cancer, 1999, 85(3):529-534.
[49] 朱正纲,汤睿,燕敏,等.术中腹腔内温热化疗对进展期胃癌的临床疗效研究 [J].中华胃肠外科杂志,2006,9(1):26-30.
[50] Pyrhönen S, Kuitunen T, Nyandoto P, et al. Randomised comparison of fluorouracil, epidoxorubicin and methotrexate (FEMTX) plus supportive care with supportive care alone in patients with non-resectable gastric cancer[J]. Br J Cancer, 1995, 71(3):587-591.
[51] Van Cutsem E, Moiseyenko VM, Tjulandin S, et al. Phase Ⅲ study of docetaxel and cisplatin plus fluorouracil compared with cisplatin and fluorouracil as first-line therapy for advanced gastric cancer: a report of the V325 Study Group[J]. J Clin Oncol, 2006, 24(31):4991-4997.
[52] Koizumi W, Narahara H, Hara T, et al. S-1 plus cisplatin versus S-1 alone for first-line treatment of advanced gastric cancer (SPIRITS trial): a phase Ⅲ trial[J]. Lancet Oncol, 2008, 9(3):215-221.
[53] Yamada Y, Higuchi K, Nishikawa K, et al. Phase Ⅲ study comparing oxaliplatin plus S-1 with cisplatin plus S-1 in chemotherapy-naïve patients with advanced gastric cancer[J]. Ann Oncol, 2015, 26(1):141-148.
[54] Shirao K, Boku N, Yamada Y, et al. Randomized Phase Ⅲ study of 5-fluorouracil continuous infusion vs. sequential methotrexate and 5-fluorouracil therapy in far advanced gastric cancer with peritoneal metastasis (JCOG0106)[J]. Jpn J Clin Oncol, 2013, 43(10):972-980.
[55] Boku N, Yamamoto S, Fukuda H, et al. Fluorouracil versus combination of irinotecan plus cisplatin versus S-1 in metastatic gastric cancer: arandomised phase 3 study[J]. Lancet Oncol, 2009, 10(11):1063-1069.
[56] Fuchs CS, Tomasek J, Yong CJ, et al. Ramucirumab monot-herapy for previously treated advanced gastric or gastro-oesop-hageal junctionadenocarcinoma (REGARD): an interna tional, randomised, multicentre, placebo-controlled, phase 3 trial[J]. Lancet, 2014, 383(9911):31-39.
[57] Wilke H, Muro K, Van Cutsem E, et al. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previo-usly treated advancedgastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): a double-blind, randomised phase 3 trial[J]. Lancet Oncol, 2014, 15(11):1224-1235.
[58] Hironaka S, Ueda S, Yasui H, et al. Randomized, open-label, phase Ⅲ study comparing irinotecan with paclitaxel in patients with advanced gastriccancer without severe peritoneal metast-asis after failure of prior combination chemotherapy usingfl-uoropyrimidine plus platinum: WJOG 4007 trial[J]. J Clin Oncol, 2013, 31(35):4438-4444.
[59] Narahara H, Iishi H, Imamura H, et al. Randomized phase Ⅲ study comparing the efficacy and safety of irinotecan plus S-1 with S-1alone as first-line treatment for advanced gastric cancer (study GC0301/TOP-002)[J]. Gastric Cancer, 2011, 14(1):72-80.
[60] Nishina T, Boku N, Gotoh M, et al. Randomized phase Ⅱ study of second-line chemotherapy with the best available 5-fluorouracil regimen versusweekly administration of pacl-itaxel in far advanced gastric cancer with severe peritoneal meta stases refractory to 5-fluorouracil-containing regimens (JCOG0407)[J]. Gastric Cancer, 2016, 19(3):902-910.
[61] Moehler M, Eimermacher A, Siebler J, et al. Randomised phase Ⅱ evaluation of irinotecan plus high-dose 5-fluorouracil and leucovorin (ILF) vs 5-fluorouracil, leucovorin, and etoposide (ELF) in untreated metastatic gastric cancer[J]. Br J Cancer, 2005, 92(12):2122-2128.
[62] Ishigami H, Fujiwara Y, Fukushima R, et al. Phase Ⅲ study of intraperitoneal paclitaxel plus S-1/paclitaxel compared with S-1/cisplatin in gastric cancer patients with peritoneal metas-tasis: PHOENIX-GC trial. Poster presented at 2016 ASCO Annual Meeting; 4 June 2016; Chicago, Illinois, USA.
[63] 李燕,李洁,张晓东,等.腹腔联合全身化疗治疗胃肠道恶性肿瘤并发腹腔积液 81 例 [J].肿瘤研究与临床,2009,21(1):52-53.
[64] 黄万中,蒋华,刘燕文,等.多西紫杉醇腹腔灌注化疗治疗晚期胃癌Ⅱ期临床研究 [J]. 现代肿瘤医学,2011,19(5):960-963.
[65] 李翔.紫杉醇腹腔灌注化疗治疗胃癌恶性腹腔积液的临床研究 [J].江西医药,2015,50(5):390-393.
[66] Fujitani K, Yang HK, Mizusawa J, et al. Gastrectomy plus chemotherapy versus chemotherapy alone for advanced gastric cancer with a single non-curable factor (REGATTA): a phase 3, randomised controlled trial[J]. Lancet Oncol, 2016, 17(3):309-318.
[67] Feingold PL, Kwong MLM, Sabesan A, et al. Cytoreductive surgery and hyperthermic intraperitoneal chemotherapy for gastric cancer and other less common disease histologies: is it time?[J]. J Gastrointest Oncol, 2016, 7(1):87-98.
[68] Sangisetty SL, Miner TJ. Malignant ascites: A review of progn-ostic factors, pathophysiology and therapeutic measu res[J]. World J Gastrointest Surg, 2012, 4(4):87-95.
[69] Saif MW, Siddiqui IA, Sohail MA. Management of ascites due to gastrointestinal malignancy[J]. Ann Saudi Med, 2009, 29(5):369-377.
[70] Chang DK, Kim JW, Kim BK, et al. Clinical significance of CT-defined minimal ascites in patients with gastric cancer[J]. World J Gastroenterol, 2015, 11(42):6587-6592.
[71] Maeda H, Kobayashi M, Sakamoto J. Evaluation and treatment of malignant ascites secondary to gastric cancer[J]. World J Gastroenterol, 2015, 21(39):10936-10947.
[72] Smith EM, Jayson GC. The current and future management of malignant ascites[J]. Clin Oncol, 2003, 15(2):59-72.
[73] O’Neill MJ, Weissleder R, Gervais DA, et al. Tunneled peritoneal catheter placement under sonographic and fluorosc-opic guidance in the palliative treatment of malignant ascites[J]. Am J Roentgenol, 2001,177(3):615-618.
[74] Barnett TD, Rubins J. Placement of a permanent tunneled peritoneal drainage catheter for palliation of malignant ascites: a simplified percutaneous approach[J]. J Vasc Interv Radiol, 2002, 13(4):379-383.
[75] 张岂凡,郑宏群,孙凌宇,等.胃癌腹腔转移所致恶性肠梗阻的诊治及营养支持策略 [J].中国肿瘤临床,2014,41(12):749-752.
[76] O’Connor B, Creedon B. Pharmacological treatment of bowel obstruction in cancer patients[J]. Expert Opin Pharmacother, 2011, 12(14):2205-2214.
[77] Watari H, Hosaka M, Wakui Y, et al. A prospective study on the efficacy of octreotide in the management of malignant bowel obstruction in gynecologic cancer[J]. Int J Gynecol Cancer, 2012, 22(4):692-696.
[78] Prommer E. Anticholinergics in palliative medicine: an upd-ate[J]. Am J Hosp Palliat Care, 2013, 30(5):490-498.
[79] Olson TJP, Pinkerton C, Brasel KJ, et al. Palliative surgery for malignant bowel obstruction from carcinomatosis: a systematic review[J]. JAMA Surg, 2014, 149(4):383-392.
[80] Kim JH, Ku YS, Jeon TJ, et al. The efficacy of self-expanding metal stents for malignant colorectal obstruction by noncolonic malignancy with peritoneal carcinomatosis[J]. Dis Colon Rectum, 2013, 56(11):1228-1232.
[81] Tuca A, Guell E, Martinez-Losada E, et al. Malignant bowel obstruction in advanced cancer patients: epidemiology, management, and factors influencing spontaneous resolution[J]. Cancer Manag Res, 2012, 4:159-169.
[82] Iwasa S, Goto M, Yasui H, et al. Multicenter feasibility study of combination therapy with fluorouracil, leucovorin and pacli-taxel (FLTAX) for peritoneal disseminated gastric cancer with massive ascites or inadequate oral intake[J]. Jpn J Clin Oncol, 2012, 42(9):787-793.
