一、印度仿制药市场发展情况
印度是一个仿制药出口大国,有近3000家仿制药企业,印度仿制药销到200多个国家,仿制药出口量约占全球20%,美国有40%的仿制药从印度进口。印度政府数据(IEBF)显示,印度已经有超过500家经过美国FDA认证的制药工厂,从2012年至2016年,出口总额由101亿美元增长至169亿,2016年药品出口占印度全国出口总额4.9%。预计到2020年,印度仿制药出口额将达到400亿美元。
全球仿制药排名(截止2017年12月)前15的印度制药企业有:Sun Pharma(41亿美金)、Lupin(24亿美金)、Aurobindo(21亿美金)、Dr. Reddy(17亿美金)、Zydus Cadila(16亿美金)。
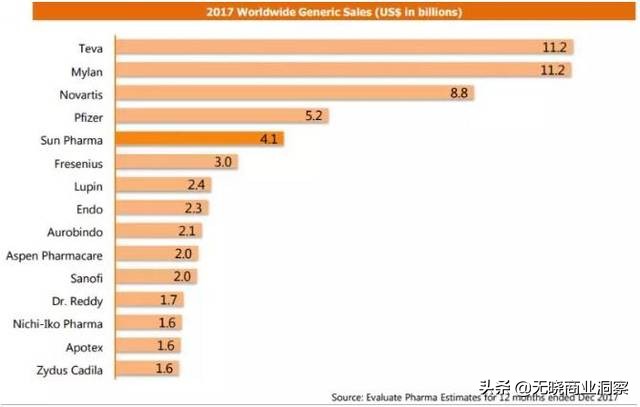
数据来源:IMS,火石整理
近年来,随着大批单抗品牌药面临专利到期,生物仿制药正呈现井喷式增长,根据Evaluate的统计,到2020年,过专利保护期的生物药将近874亿美金市场规模。近几年,印度生物仿制药规模提升较快,2014年印度仿制药商Cadila在印度推出全球首Humira(修美乐)生物仿制药Exemptia;2016年,印度制药公司Torrent推出了Humira(修美乐)第二个仿制药Adfrar。Rituxan(中文名美罗华,利妥昔单抗)的美国专利2015年到期,印度四家公司Torrent、Zenotech、Intas、Hetero的生物仿制药产品已经上市销售。
二、印度仿制药企业升级路径
仿制药行业的繁荣,给印度带来了"世界药房"的称号。从20世纪70年代至今,印度制药产业遵循了"大宗原料药—特色原料药—专利仿制药(不规范市场)—通用名药物(规范市场)—创新药物"这样的发展路径,在国内和国际市场中演绎了高速成长的"印度模式"。印度仿制药的这种发展模式有两个特点:
其一,国际化程度高。美国联邦食品药品管理局(FDA)的药物管理档案(drug master file,DMF)和欧盟的药典适用性认证(certificate of suitability,COS)注册是原料药进入美国和欧洲原料药市场有效而必需的支持性文件。获得DMF 和COS 文件的数量在一定程度上反映了制药产业的国际化程度,印度在这方面的申请量始终保持在较为稳定的高水平,文件总持有量呈不断攀升趋势,并稳居发展中国家前列。如2014年,印度获批的DMF 超过300个,涉及到的原料药占美国市场近三分之一的份额,而中国仅有印度的一半左右。
其二,"大宗原料药进口,特色原料药下游延申"道路。近年来,印度已取代日本成为中国原料药的最大买家之一。印度大量采购我国生产的青霉素G钾盐、7-ACA、硫氰酸红霉素等大宗产品,运回国内后再加工成制剂或其它产品出口获利。印度的12种关键药物非常依赖从中国进口药品,12种关键药物包括扑热息痛、二甲双胍、雷尼替丁、阿莫西林、环丙沙星、头孢克肟、乙酰水杨酸、抗坏血酸、氧氟沙星、布洛芬、甲硝哒唑、氨苄西林,其中8种药品被世卫组织列为基本药物。特色原料药是指为非专利企业及时提供专利刚刚过期药品的原料药,是集知识产权、国际市场与药政等多方要素于一身的产品,相比于大宗原料药来说,行业竞争程度低且利润率水平更高。在印度的专利政策和仿制药政策下,印度制药产业借助自身技术和成本上的比较优势,形成了成熟的原料药生产工艺技术,成功实现了由大宗原料药到特色原料药的产业升级,够配合非专利药物制剂生产企业的产品抢注。
在印度医药产业发展模式的引导下,印度仿制药企业蓬勃发展,在短短几十年间实现了由"低水平、完全仿制"向"高品质、仿创结合"的转变,产品能够在美欧日等发达医药市场占有一席之地。

三、印度仿制药的政策环境分析
印度仿制药的发展还得益于印度的专利强制许可制度,在专利强制许可制度下,印度药厂可以在未获得专利方许可的情况下,合法地生产和以较低价格销售仿制药。在专利药的专利被授予三年后,印度仿制药厂可向印度专利管理局提交强制许可申请。但是获批强仿需要满足三个条件。第一,专利方未向印度公众提供产品;第二,印度公众无法以合理价格获得产品;三是专利未在印度实施。
1970年以前,印度执行国际通行的化合物专利保护制度,外资药企药物专利受到严格保护,而本土药企研发能力薄弱,几乎无力无外资药企竞争。为改变这一现状,印度在1970年通过专利法,打破了外资药企的专利垄断。其具体方法是,将药物专利分为产品专利和方法专利,1970专利法只保护方法专利,意味着印度本土药企可以通过"逆工程"的方式对外资药企产品进行仿制。同时,1970专利法还大幅缩短了药物专利的保护时间。
1970年印度制定了《专利法》,但只保护整个生产工艺和过程。印度药企可以根据产品倒推工艺流程,将药品工艺进行改造,使得生产出的药品与己申请专利保护的药品不同。印度《专利法》还规定食品、药品、农业化学品和其他类有相似性的产品只能申请方法专利,使印度本土企业开始生产只在其他国家有产品专利的仿制药,这使得印度的药企快速完成了"产业升级",在世界仿制药行业占据了主导地位,被称为"世界药房"。然而印度制药企业生产出的仿制药会出口到其他国家,打破了西方发达国家对医药技术领域的专利垄断,欧美国家纷纷采取对策*制抵**印度药企,要求印度专利领域与((TRIPS协议》接轨。1994年印度与WTO达成协议。但印度对专利保护的进展依然很缓慢,直到2005年才通过《专利法》,专利保护才真正与国际社会接轨。印度《专利法》将药品专利强制许可的条件规定为"该发明专利无法满足公众合理的需求:公众无法以合理的价格获取该专利产品;该发明获得专利后未在印度境内投入实施"。并且规定药品专利强制许可"任何利益相关者"都可以申请。
2012年印度对由拜耳公司持有专利、治疗恶性肿瘤的药物索拉菲尼发布的强制许可令引起国际国内极大关注。该项强制许可令于2012年3月9日发布,之后拜耳公司提出复审,以及向印度知识产权上诉委员会(IPAB)提起上诉,均遭驳回,但IPAB将支付给拜耳公司的许可费从原来的销售额的6%提高至7%。从这份强制许可令可见,支持强制许可的主要理由包括专利药品的价格为公众无法合理负担,以及该专利未在本国充分实施(进口数量不能满足国内病人用药需求),因此,公共利益的合理需求未满足。强制许可令中还对拜耳公司提出的抗辩予以详细反驳和回应,如印度最终并未同意拜耳公司延迟一年实施强制许可的请求,而是决定了当时就发布这项强制许可令。
在举起专利大棒的同时,印度还通过了药品价格管制法案,其主要目的是为指定的大批量应用的原料药及主要制剂指定价格上限,保证消费者能够以较低的价格获得药品,限制药企在药物上获得较高利润。这一做法有效降低了药品的价格,同样使外资药企在印业务受阻。在1979年、1995年、2002年、2012年等年份,药品价格管制法案多次修改,药厂、流通、零售商的利润被进一步压缩。