前两期我们分享了宫内免疫的初步探索,宫内免疫:一种新的、友好的免疫方式,宫内免疫探索:子宫作为免疫诱导部位是否可行?今天我们继续分享使用精液递送宫内疫苗的考虑因素。
使用精液递送宫内疫苗的考虑因素
所有疫苗的目标都是产生足够高的群体免疫水平,降低流通病原的水平,通过群体免疫保护易感风险最大的个体(Fine,1993)。亚单位疫苗被认为是更为安全的疫苗,因为它没有完整的病原递送(因此没有毒力返强的危险)。然而它们通常免疫原性较低,需要佐剂来提升(Bastola等,2017)。佐剂辅助跨上皮屏障摄取抗原,募集APC,激活APC,诱导免疫反应(Th1、Th2、Th17型T细胞或CTL),建立储存库并保护抗原不被降解(Awate等,2013年;Pashine等,2005年;Srivastava等,2015年)。成功的粘膜疫苗应答可能需要这些作用机制中的一种或多种。因此有效的疫苗配方可能需要包含多种佐剂(Garg等,2017)。然而,由于宫内疫苗与活精共同使用,佐剂和抗原组合不可对精子功能或活力产生负面影响。我们最初开始研究混合疫苗与精液时,将几种商品化猪疫苗以非常低的剂量与精液混合,发现它们都具有杀精作用。因此我们要搜寻不杀精的佐剂。
我们使用可结合顶体活跃精子的花生凝集素进行计算机辅助精子分析和微观观察。通过剂量滴定测试商品化保存精液中的几种佐剂,我们发现宿主防御肽、poly IL:C(聚肌胞苷酸)和聚磷腈(TriAdj)、灭活的PPV和重组蛋白不会显著影响精子功能(Hamonic等,2020)。后续试验结果表明,配种时混用精液和PPV重组抗原或FliC抗原和/或灭活PPV加TriAdj进行宫内免疫不会影响精子功能或生殖力,胚胎发育健康,仔猪健康,断奶前日均增重与一般无异。这一结论还需要一些母猪数更大的试验来验证。虽然上述结果仅基于少数试验和数十只动物,但用TriAdj配制的宫内疫苗似乎不会对精子功能、胚胎活力、至少短期内的仔猪生长动力学产生负面影响(Choudhary等,2021;Hamonic等,2020)。
在猪等家畜使用宫内疫苗时,我们担心针对精子有可能产生的免疫反应,会导致今后的不孕不育或繁殖性能下降,人类、小鼠和兔使用精子特异性蛋白免疫后发生了这种情况(Clark&Schust,2013)。需仔细监测上百次宫内免疫和配种周期的影响,若导致繁殖性能降低,则不会被产业所接受。
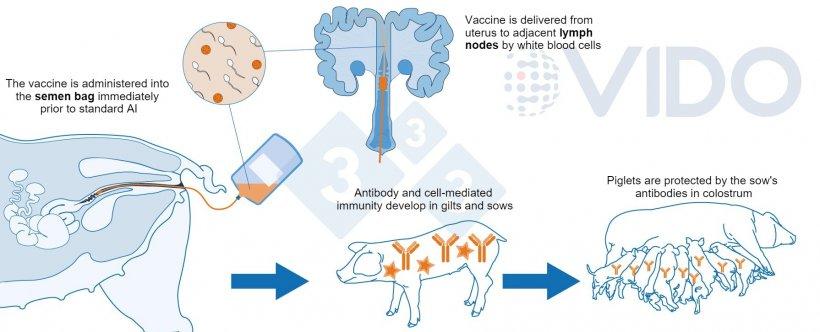
图 宫内疫苗的免疫机制:疫苗通过人工授精输送到子宫,以在母猪中产生抗体介导的细胞免疫反应。在初乳中产生抗体,并输送给哺乳的新生仔猪。
图源:pig333
动物的宫内免疫
已发现大鼠子宫单次接种疫苗可激发全身和局部的抗原特异性抗体介导的免疫反应(Wira&Sandoe,1989)。将绵羊红细胞两次直接接种于去卵巢大鼠的子宫腔中,在第二次免疫的2周后进行检测,发现子宫和阴道分泌物中具有明显的IgA和IgG抗体反应。使用雌二醇可降低阴道抗体水平(但不影响子宫抗体水平),表明这种反应依赖于激素。在两次免疫的动物唾液中也发现了IgG而非IgA抗体。不同于生殖道,雌二醇对唾液IgG水平没有影响。为在另一种动物模型中研究宫内免疫的效果,我们通过手术在兔的每个子宫角注入400微升,分别与TriAdj配制而成的卵清蛋白(OVA)、牛疱疹病毒的截短糖蛋白D(tGD)、猪细小病毒VP2和细菌硫氧还蛋白(rVP2-TrX)的融合蛋白(Pasternak等,2017)。对照组兔肌肉注射亚单位疫苗中的一种。
两个途径接种的疫苗都在全身、局部(子宫)和远端粘膜(肺和阴道)产生了抗原特异性体液反应。观察到的粘膜反应并不局限在上生殖道或在上生殖道内存在明显划分,反应程度似乎至少部分依赖于抗原。在后续研究中,以不同剂量分别将tgD或OVA疫苗(各以TriAdj配制)注入兔子宫腔,在32天后评估免疫反应(Pasternak等,2018)。宫内疫苗在血清中产生抗原特异性IgG和IgA,具有剂量依赖性。高、中剂量疫苗灌洗子宫和支气管肺泡可引起抗OVA和tgD的 IgG显著增加,但IgA抗体未显著增加。使用卵清蛋白(OVA)再次刺激高剂量疫苗组的脾细胞仅导致Th1细胞因子(IL2/IFNgamma)的基因表达略微显著增加,但无可观察到的增殖。我们必须指出,我们并未记录兔子的激素水平和/或任何表明它们处于发情期的迹象,因此很可能并非所有动物都处于发情周期的同一阶段。尽管如此,高剂量抗原在所有动物都能诱发免疫。
总而言之,研究结果证实了子宫免疫系统经刺激具有产生基本反应的能力,该反应在宫内免疫后可触发全身和粘膜免疫。
我们首先研究了猪子宫免疫系统是否能对加强免疫产生反应(Hamonic等,2020年)。每次配种前,给猪肌肉注射含灭活猪细小病毒的商品疫苗。妊娠、分娩和断奶后,下一次配种采取宫内免疫。我们将佐剂TriAdj配制的灭活PPV,在经产母猪配种前,立即加入精液袋,对照母猪根据制造商指示的肌肉途径接种商品化细小病毒疫苗。对照组和宫内免疫组血清中的抗PPV IgG、IgG1和IgG2抗体相当。我们随后在未肌肉注射过PPV 疫苗的初产母猪,进行单次宫内免疫(Hamonic等,2020年)。使用灭活PPV加TriAdj单次宫内免疫未能触发强大的全身性或粘膜抗体介导的免疫。我们推测精液对免疫反应存在负面影响,因为兔子宫单次免疫后显然可以诱导强大的免疫应答。另外两个原因可能是猪需要多次免疫来建立强大的粘膜免疫和/或TriAdj未能突破粘膜屏障并启动猪粘膜表面的APC募集。
为探究多次免疫是否能够诱导粘膜免疫反应,我们在初产母猪发情配种时使用TriAdj配制的重组PEDV棘突蛋白(PEDVS)进行3次宫内免疫(Choudhary等,2021)。宫内免疫的精子经反复冻融后,死亡但不破裂。由于母猪无法怀孕,预料之中,它们大约3周后发情。重复模拟配种,直至第3个配种周期,使用活精进行宫内免疫。通过这种方法人为缩短免疫间隔期,当然宫内免疫实际可在每次怀孕时根据需要进行。初产母猪正常发情,它们的活仔数与对照母猪相当,证实输精联合宫内免疫不会影响精子功能、生殖力,也不会产生明显的抗精子免疫反应。
经3次宫内免疫的猪,血清、子宫和初乳中的PEDVS抗体升高,且PEDV中和抗体滴度显著升高。初乳中含有较高的PEDVS中和抗体,可被动转移给哺乳仔猪。宫内免疫母猪的仔猪比对照母猪的仔猪约多存活1天,表明其对具有感染性的PEDV有部分抵抗力。我们怀疑初乳中的中和抗体量不足以保护仔猪免受疾病。
目前正在进行的研究为,以更强效的粘膜(无杀精作用)佐剂替代TriAdj,产生更强的免疫反应,以足以保护仔猪免受感染性PEDV或其它新生动物疾病的影响,或保护母猪免受繁殖性疾病(如PRRSV或PPV)的影响。其它研究包括,子宫如何作为免疫诱导位点。具体来说,我们探究疫苗是否能触发免疫细胞募集进入宫腔,这对诱导免疫至关重要,或者抗原是否穿过子宫壁,触发免疫。探究它如何穿过腔壁(细胞旁或细胞传递、树突状细胞延伸树突到肠腔内进行摄取等),以及抗原呈递给引流淋巴结还是淋巴聚集体。一旦明确了子宫作为免疫诱导位点的方式,我们就可利用这种作用机制来配制疫苗。
总之,我们倍感振奋,猪的宫内免疫似乎不影响精子功能、生殖力或仔猪生长动力学,并且它能够触发全身免疫和粘膜免疫。研究范围需要扩展更多可作为配方的佐剂,如配制成纳米颗粒,不会杀死精子。一旦完成,需要更大规模的试验来证明它可以产生强大的细胞和抗体介导的免疫,以保护母猪免受传染病和/或通过初乳中的中和抗体保护哺乳仔数。产业定能受益于一种可在母猪站定不乱动情况下给予的粘膜疫苗,且该免疫操作与现有的常规配种一举两得。
来源:IPVS 2022,原文可留言获取~