
栏目简介

彤心飞传是“心在线”与天津医科大学第二医院心脏科刘彤教授、郑州大学附属洛阳中心医院心内科谷云飞教授合作推出的一档深度资讯新专栏。将由刘彤教授从JACC、Circulation、EHJ、NEJM、JAMA、Lancet等国际权威杂志提供的海量信息中,每周精选出一篇最贴合国内临床现状、最能满足国内心脏科医生需求、最有指导意义、极富争议性等热点话题,由谷云飞教授整理文献资料,传达出最准确的关键点,再由刘彤教授给出精彩点评。在这里,你还可以听到谷云飞教授和刘彤教授的声音,绝对堪称美妙的享受哦。
心房颤动(房颤)是临床上常见的一种持续性心律失常,发病率逐年升高,并伴随血栓栓塞及其他不良临床事件[1]。对于房颤患者而言,抗凝治疗可以预防缺血性卒中及其他血栓栓塞事件,并改善患者远期预后[2]。在后华法林时代,非维生素K拮抗剂的新型口服抗凝药(NOAC)由于使用方便,在减少血栓事件及大出血方面不劣于甚至优于华法林,目前临床使用日益增多[3,4]。但是,房颤患者使用NOAC时仍然存在一定出血风险[5],特别合并多种疾病、合用多种药物时[6]。
在2006年至2009年期间进行了两次房颤患者的大型临床调查,约三分之二应用NOAC的患者(特别是老年人)同时服用了5种以上药物[7,8]。服用NOAC者合并应用多种药物可能增加血药浓度和出血风险[7]。目前关于NOAC药物-药物相互作用的结果主要来自动物实验、病例报告和有限的药代动力学分析[9,10],尤其与NOAC拥有共同代谢途径的药物(如CYP3A4和P-糖蛋白*制剂抑**)[11,12]备受关注。例如,酮康唑和克拉霉素可增加血浆中NOAC的活性水平和出血风险[10,13]。
然而,房颤患者常合并多种疾病,合并使用多种用药,这给NOAC相关出血风险的量化带来较大困难[6,14]。而且迄今在临床实践中,合并使用CYP3A4或P-糖蛋白*制剂抑**对NOAC使用者出血风险大小的影响,尚未有量化研究,故急需针对上述问题进行相关研究。本周三刚刚发表在《美国医学会杂志》(JAMA)上的一项研究[15],评估了服用NOAC者在合并使用12种临床常用且与NOAC具有共同代谢途径药物时的出血风险,对今后NOAC的临床使用具有重要指导意义。
该研究回顾分析了台湾2012年至2016年近28万(279734)例非瓣膜性房颤患者,其*共中**有91330例患者接受NOAC抗凝治疗。患者初次接受NOAC治疗时的临床特征见图1,合并用药情况见图2。患者基线平均CHA2DS2-VASC评分为3.9,平均HAS-BLED评分为3.3。随访期间,45347例(49.7%)患者使用达比加群,54006例(59.1%)使用利伐沙班,12886例(14.1%)使用阿哌沙班。由于台湾的医保结算分每季度进行,为了便于统计分析,应用人-季度进行评价。
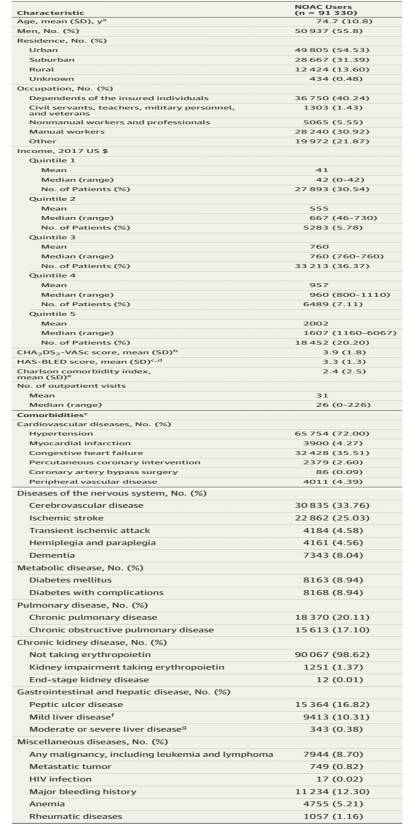
图1. 患者基线临床特征。
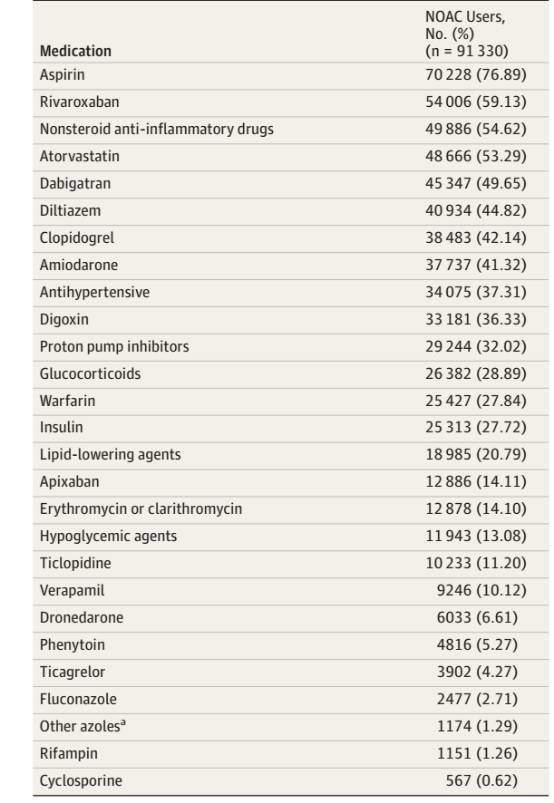
图2. NOAC患者合并用药情况。
研究的主要终点是大出血,定义为住院或急诊就诊出血,主要诊断为颅内出血、胃肠道出血、泌尿生殖系统或其他出血。创伤性出血患者被排除在外。每人-季度仅1次大出血事件纳入分析。次要终点包括不同部位的特异性出血。
在447037人-季度随访期间,共发生4770例大出血事件。其中包括1177次颅内出血和3341次消化道出血,182次其他部位出血。与NOAC合并最多的药物分别是阿托伐他汀(27.6%)、地尔硫卓(22.7%)和胺碘酮(21.1%)。NOAC合用胺碘酮、氟康唑、利福平和苯妥英钠可以增加大出血风险。
图3列出了NOAC合并12种用药的大出血发生率、校正发生率和校正发生率差异。与单用NOAC相比,合用不同药物导致的每1000人-年校正大出血发生率差异分别如下:胺碘酮为13.94(99%CI 9.76~18.13),氟康唑为138.46(99%CI 80.96~195.97),利福平为36.90(99%CI 1.59~72.22),苯妥英钠为52.31(99%CI 32.18~72.44)。其他合并用药并未增加大出血发生率。合用阿托伐他汀、地高辛、红霉素或克拉霉素的校正大出血发生率有所下降。
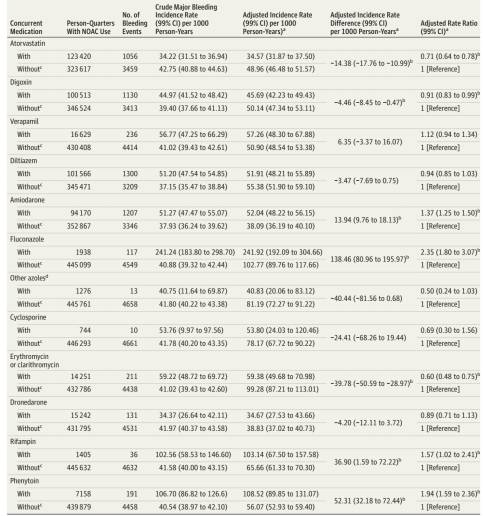
图3. 合并用药的NOAC患者大出血风险。
分别对达比加群、利伐沙班和阿哌沙班进行单独分析,合并用药导致出血风险增加的情况与上述主要结果相似。合用胺碘酮、氟康唑、利福平及苯妥因钠与更高的大出血风险相关。
大出血事件按出血部位划分为颅内出血、胃肠道出血或其他部位(包括泌尿生殖系统、胸腔、腹腔)出血。NOAC合用药物相关的不同部位大出血校正发生率差异结果与上述结果相似。
研究中除上述主要结果外还进行了如下三个补充分析。(1)评估氯沙坦合并使用12种药物的出血风险。研究结果提示,未见任何药物与氯沙坦合用与出血风险增加相关。(2)分析NOAC合用12种药物是否增加其他不良事件的发生,如骨折。结果提示,任何一种药物联用并未增加骨折发生风险。(3)将12种药物根据代谢途径分为P-糖蛋白*制剂抑**组(地高辛、维拉帕米、地尔硫卓、胺碘酮、环保霉素)、P-糖蛋白和CYP3A4*制剂抑**组(阿托伐他汀、氟康唑/酮康唑/伊曲康唑/伏立康唑/泊沙康唑、红霉素/克拉霉素、决奈达隆、利福平、苯妥因钠)。NOAC与两组药物合用均有较高的出血风险。
该研究结果提示:(1)应用NOAC者应尽量避免使用某些可能增加出血风险的药物,包括非瓣膜房颤患者临床常用的胺碘酮等;(2)合并使用胺碘酮、氟康唑、利福平、苯妥因钠与NOAC大出血风险增加相关,然而,目前指南不推荐与NOAC合并使用的一些药物,与大出血发生无明显相关。
刘彤教授点评
随着NOAC进入中国医保目录,且价格不断下降,其在房颤抗凝治疗中的临床应用更广泛,越来越多的非瓣膜性房颤患者开始接受NOAC治疗。但是,由于随机对照试验(RCTs)有严格的入选和排除标准,其研究结果可能无法完全外推至临床实践,这就迫切需要真实世界研究的结果。这些研究可以评估真实临床环境中干预实施的效果,特别是不同医疗环境、不同年龄、不同种族、有合并症及合并用药的真实情况。近年来JAMA等高影响因子杂志也相继发表了多篇有关NOAC的真实世界研究。
这项来自台湾的真实世界研究共入选91330例接受NOAC治疗的非瓣膜性房颤患者,评估合并应用12种CYP3A4*制剂抑**或P-糖蛋白*制剂抑**对NOAC治疗房颤患者大出血风险的影响。与NOAC合并使用最多的药物分别是阿托伐他汀(27.6%)、地尔硫卓(22.7%)和胺碘酮(21.1%),以上三种药物也是目前临床上的常用药物。
其结果显示,NOAC合用胺碘酮时增加患者大出血风险。此外,研究亚组显示,达比加群或利伐沙班合用胺碘酮时增加大出血风险,而阿哌沙班合用胺碘酮时不增加大出血风险(图3)。这与2014年发表的ARISTOTLE亚组分析结果一致,即阿哌沙班与胺碘酮合用较华法林与胺碘酮合用可显著降低房颤患者出血风险(J Am Coll Cardiol 2014;64:1541-50)。 因此,对于使用胺碘酮的房颤患者,目前相对安全的抗凝药物是阿哌沙班。
此外,NOAC合用氟康唑时显著增加大出血风险,是NOAC合用胺碘酮时出血风险的10倍,因此建议禁止此联合使用。令人意外的是,NOAC合用阿托伐他汀、地高辛时大出血发生率有所下降,特别是阿托伐他汀,此药同时还是CYP3A4*制剂抑**和P-糖蛋白*制剂抑**,其降低大出血风险的具体机制尚不清楚。
因此,虽然近期指南不推荐以上12种药物与NOAC合用,但是与其中一些药物如阿托伐他汀或地高辛合用,似乎是安全的。该研究给我们的另一个启示是,合并用药导致的NOAC血药浓度水平增高,似乎与出血风险增加无直接关系,可能与患者的自身情况及合用药物的代谢情况有关。
该研究的局限性如下:(1)数据库中缺乏患者肝肾功能的临床资料,这可能影响NOAC的代谢和出血风险;(2)缺乏依度沙班的相关数据;(3)没有评价NOAC不同剂量与其他药物合并使用对出血风险的影响。
❂ 专家简介

刘彤,天津医科大学第二医院心脏科主任医师,副教授,天津心脏病学研究所心房颤动诊疗中心副主任。美国Cedars-Sinai医学中心医学博士/博士后,天津医科大学博士生导师。主要从事心脏起搏与射频消融、心房颤动的基础和临床研究。现任中华医学会心脏起搏与电生理分会青年委员、中华医学会心脏起搏与电生理分会房颤工作组委员、中国心电学会委员、中国医师协会心力衰竭专业委员会青委会常务委员、中国心力衰竭学会常务委员兼秘书、中国心脏联盟晕厥学会委员。承担国家自然科学基金项目3项,获天津市科技进步奖2项,在JACC等SCI杂志发表第一作者及通讯作者论文60余篇,主编及主译英文专著各1部,副主编专著2部。

谷云飞,郑州大学附属洛阳中心医院心内科副主任,副主任医师,现任中国医师协会心脏重症委员会青年委员、中国老年保健医学研究会老年心血管分会青年常务委员、中国医促会心律与心电分会网络心电学组副主任委员、海医会心脏重症委员会河南分会秘书、河南省心电生理与起搏分会射频消融学组委员、河南省生物医学工程学会介入分会委员、河南省卒中学会心律失常房颤委员会委员,《实用心电学杂志》、《医师在线》杂志编委,洛阳心脏网、循环在线微信公众平台主编。2015年获河南省青年心电图大赛一等奖,发表各类论文20余篇,参译专著2部,参编专著1部。擅长心律失常的诊断治疗、疑难心电图分析,主攻心内科的临床电生理检查、射频消融及永久起搏器植入。
参考文献(滑动查看)
[1]Chugh SS, Havmoeller R, Narayanan K, et al. Worldwide epidemiology of atrial fibrillation:a Global Burden of Disease 2010 Study. Circulation.2014;129(8):837-847.
[2]Deedwania P, Acharya T. Anticoagulation in atrial fibrillation: is the paradigm really shifting? J Am Coll Cardiol. 2017;69(7):786-788.
[3]Ruff CT, Giugliano RP, Braunwald E, et al.Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials.Lancet. 2014;383(9921):955-962.
[4]Olesen JB, S?rensen R, Hansen ML, et al.Non-vitamin K antagonist oral anticoagulation agents in anticoagulant naive atrial fibrillation patients: Danish nationwide descriptive data 2011-2013. Europace. 2015;17(2):187-193.
[5]Ruff CT, Giugliano RP, Antman EM. Management of bleeding with non-vitamin k antagonist oral anticoagulants in the era of specific reversal agents.Circulation. 2016;134(3):248-261.
[6]Wang Y, Singh S, Bajorek B. Old age, high-risk medication, polypharmacy: a “trilogy” of risks in older patients with atrial fibrillation. Pharm Pract (Granada). 2016;14(2):706.
[7]Piccini JP, Hellkamp AS, Washam JB, et al. Polypharmacy and the efficacy and safety of rivaroxaban versus warfarin in the prevention of stroke in patients with non valvular atrial fibrillation.Circulation. 2016;133(4):352-360.
[8]Jaspers Focks J, Brouwer MA, Wojdyla DM, et al. Polypharmacy and effects of apixaban versus warfarin in patients with atrial fibrillation: post hoc analysis of the ARISTOTLE trial. BMJ. 2016;353:i2868.
[9]Wiggins BS, Northup A, Johnson D, et al.Reduced anticoagulant effect of dabigatran in a patient receiving concomitant phenytoin.Pharmacotherapy. 2016;36(2):e5-e7.
[10]Fralick M, Juurlink DN, Marras T. Bleeding associated with coadministration of rivaroxaban and clarithromycin. CMAJ. 188(9):669-672.
[11]Delavenne X, Ollier E, Basset T, et al.A semi-mechanistic absorption model to evaluate drug-drug interaction with dabigatran: application with clarithromycin. Br J Clin Pharmacol. 2013;76(1):107-113.
[12]Parasrampuria DA, Mendell J, Shi M,Matsushima N, et al. Edoxaban drug-drug interactions with ketoconazole,erythromycin, and cyclosporine. Br J Clin Pharmacol.2016;82(6):1591-1600.
[13]Green B, Mendes RA, Van der Valk R,et al. Novel anticoagulants—an update on the latest developments and management for clinicians treating patients on these drugs. J Oral Pathol Med. 2016;45(8):551-556.
[14]Heidbuchel H, Verhamme P, Alings M, et al.EHRA practical guide on the use of new oral anticoagulants in patients with non-valvular atrial fibrillation: executive summary. Eur Heart J. 2013;34(27):2094-2106.
[15]Chang SH, Chou IJ, Yeh YH,et al. Association Between Use of Non-Vitamin K Oral Anticoagulants With and Without ConcurrentMedications and Risk of Major Bleeding in Nonvalvular Atrial Fibrillation. JAMA. 2017 Oct 3;318(13):1250-1259. doi: 10.1001/jama.2017.13883.
往期回顾:
心在线 专业平台专家打造
编辑 王雪萍┆美编 柴明霞┆制版 潘欢
更多精彩,点击下方“阅读原文”查看。