作者: 杲杲
1月28日,推动药品集中带量采购工作常态化制度化开展的意见下发,意见中明确提到 “ 将带量采购常态化、制度化 ” , 未过评品种、中成药以及生物类似药将被纳入药品集采 。在国务院政策例行吹风会上,国家医保局副局长陈金甫指出了 集采的纳入标准 :“原研药加通过一致性评价的仿制药,只要达到三家就可以列入集采。” 选择的条件重点是医保目录内、临床必须、用药量大、金额高,形成了集采触发机制。这种做法既保证质量要求,也保证企业公平竞争的客观条件,也符合临床要求,更避免竞争规则的自由裁量权。
大批生物类似药即将上市
为生物类似药集采奠定基础
对于国家医保局在生物类似药纳入集采上的连续表态,生物制药作为集采“禁区”已被打破。前三批国采已经倒逼112个品种实现大降价,相关企业已经陆续战略调整,未来随着越来越多生物类似药的获批上市, 众多依靠高价生物药掘金中国市场的外资药企接受降价的挑战, 很快生物制药市场洗牌也会到来。
目前, 共有4个品种的生物药类似药(单抗类)获批并上市,涉及5家企业的9个产品 。其中, 阿达木单抗竞争最为激烈,加上原研共有5家企业竞争 。复宏汉霖和信达生物则是拥有最多生物类似药的企业,这两家仅成立十年左右的生物医药企业各获批了三个产品。
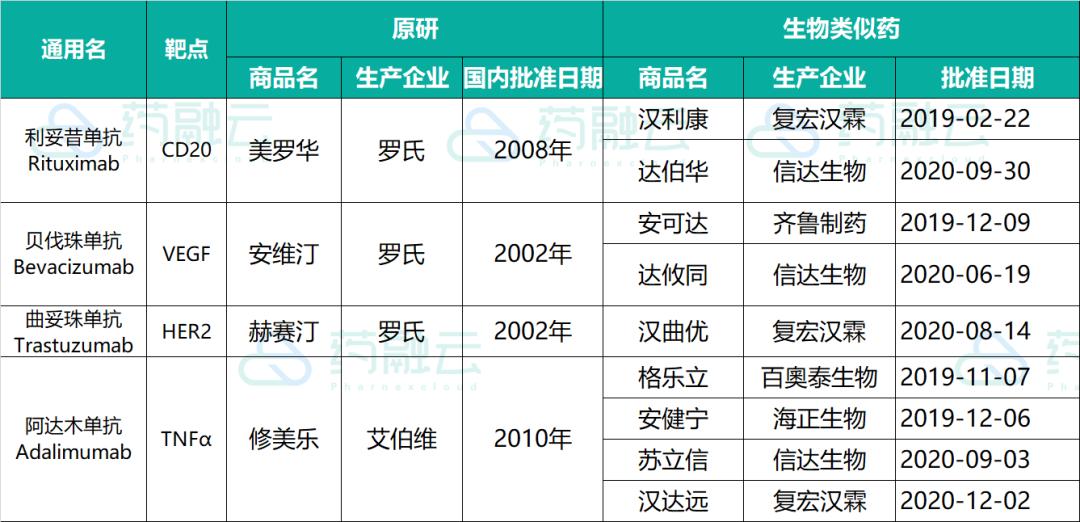
已上市生物类似药(单抗类)
此外,正大天晴、百奥泰、海正等多家生物类似药已提交上市申请, 这些产品将是今后首批集采纳入的对象 。到2022年国内的生物类似药预计将达到50多款。 截至2019年底,仅中国大陆地区的在研生物制药就接近400个,涉及100多家企业,覆盖众多生物药大品种。
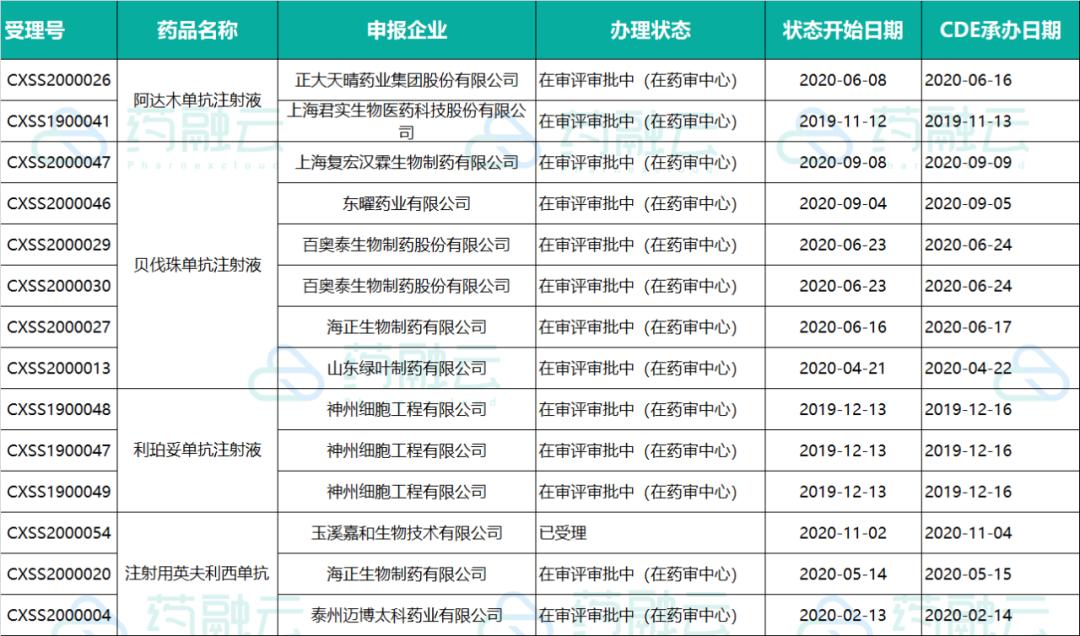
已提交申请生物类似药(单抗类)
阿达木单抗—国内已满 3 家(4+1)
阿达木单抗由美国艾伯维(AbbVie)公司开发,商品名[修美乐]。该产品是全球首个获批的抗炎性细胞因子肿瘤坏死因子(TNF)α的全人源重组人 IgG1 单克隆抗体,于 2003 年 1 月首次上市用于类风湿性关节炎。根据艾伯维最新财报显示,“药王”修美乐2012-2020年连续9年蝉联全球销售第一,2020年全球销售额临近200亿美元(增长3.46%)。修美乐于2010 年在我国获批上市,2019年价格由7586元/支下调至3160元/支,在 2019 医保谈判过程中,大降幅59% 成功进医保,达到1290元/支。 2019年阿达木单抗在全国销售额近亿元。
目前国内有四家企业的阿达木单抗类似药获批。2019年百奥泰和海正药业的生物类似药相继获批,信达生物和复宏汉霖也于2020年获批,其中信达生物速度最快,已经获批了6个适应症。另外,上海君实和正大天晴分别于2019年、2020年已提交上市申请,正在审评中。
根据药融云招投标数据显示,信达、百奥泰和海正三家类似药挂网价均为1150元/支, 2020年百奥泰半年报显示,格乐立第三季度国内销售额为 5770 万元,前三季度累计销售额 1 亿元。 在相同的定价下,各家企业已开始市场争夺战,去年10月信达公布苏立信的赠药政策:将拿出12000支苏立信用于该援助项目,低收入患者可以享受买4赠2的赠药援助;低保患者可以免费使用6支苏立信。 12月复宏汉霖也出台了赠药政策:1、低收入者自费购买3支汉达远,可申请免费捐赠1支;2. 低收入者自费购买6支汉达远,可申请免费捐赠3支。
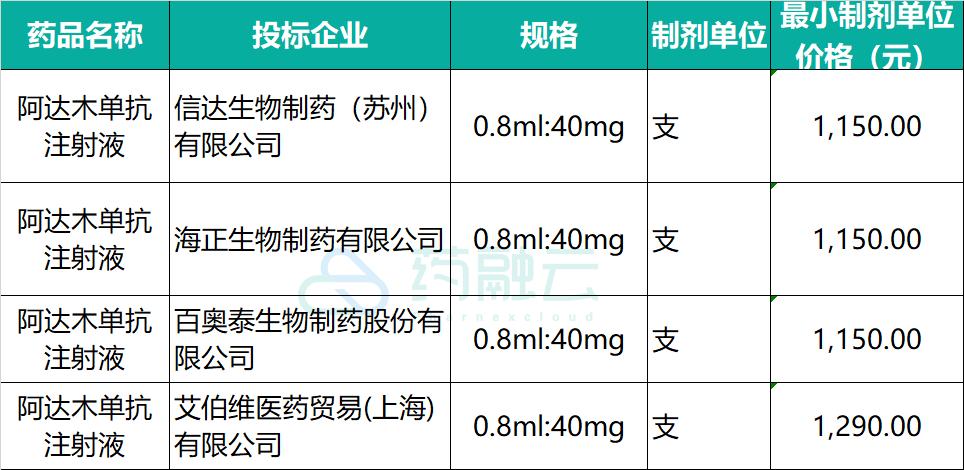
贝伐珠单抗—国内已满 3 家(2+1)
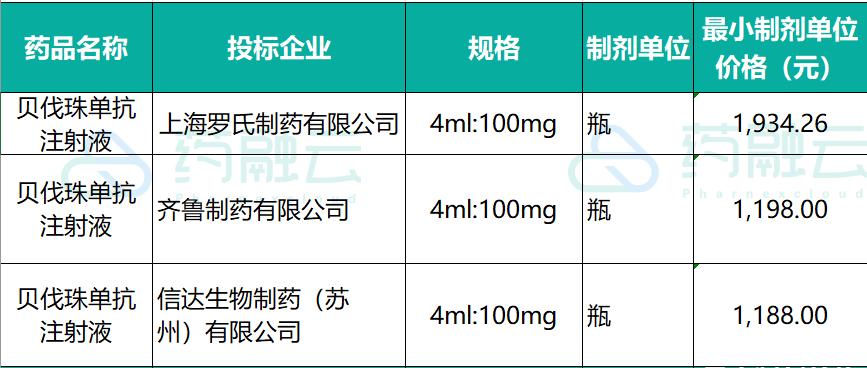
贝伐珠单抗由罗氏研制,是一种重组人源化抗血管内皮生长因子(VEGF)单抗,商品名为安维汀,同时也是全球第一款抗肿瘤血管生成药物。贝伐珠单抗于2004年2月获得FDA批准治疗转移性结直肠癌。根据罗氏最新财报显示, 2020年全球销售额为49.92亿瑞士法郎,降幅25%, 2019年国内销售达到15.6亿元左右,同比增长734.5%。
2010年,罗氏贝伐珠单抗在中国获批。2017年,贝伐珠单抗被纳入国家医保目录乙类范围。进入医保前,该药品中位中标价为5253元(100mg/瓶),经过此轮医保谈判后价格降至1998元(100mg/瓶),2018年又进一步降至1934元(100mg/瓶)。
贝伐珠单抗目前有两家企业生物类似药获批,分别是信达生物和齐鲁制药。2019年齐鲁制药获批贝伐珠单抗的首仿,并进入国家医保目录,定价则在一年内由从1266元/瓶降价至1198元/瓶。 齐鲁制药安可达2020年前三季度销售额为2.8亿元左右,共销售23.3万支。 2020年6月信达生物的达攸同获批,是第二个获批上市的国产贝伐珠单抗生物类似药,定价低于齐鲁制药,根据药融云数据显示为1188元/瓶。
同时,恒瑞医药、绿叶制药联合博安生物、贝达药业联合海正生物、百奥泰、三生制药2020年也先后提交了新药上市申请。此外还有东曜药业、华兰生物、复宏汉霖、神州细胞、康宁杰瑞、华海药业、特瑞思药业、正大天晴等多家企业在布局。百奥泰根据中国NMPA、美国FDA、欧盟EMA生物类似药相关指导原则开发的贝伐珠单抗注射液已分别向中国NMPA、美国FDA和欧洲EMA递交了上市申请;信达生物将贝伐珠单抗生物类似药在美国和加拿大的商业化权益授权给Coherus BioSciences,计划于2021年初向FDA递交生物制品许可证申请(BLA)。
利妥昔单抗—国内已满 3 家(2+1)
利妥昔单抗由美国罗氏公司开发,商品名为[美罗华],是一种靶向 CD20 的鼠/人嵌合的单克隆抗体,也是全球第一个被批准用于临床治疗非霍奇金淋巴瘤(NHL)的单克隆抗体。1997 年获得 FDA 的批准用于早期淋巴瘤的治疗,2000 年在我国进口上市。美罗华在2017年7月医保谈判成功进入国家医保目录,500mg/50ml/瓶的规格从16041元降至8298元,与此同时,小规格的价格也降到2418元,价格降幅高达58.45%。药融云招投标数据显示,美罗华再次降价,500mg/50ml降至7866/瓶,100mg/10ml降至2294/瓶 。2018年利妥昔单抗中国销售额约20.7亿元。
目前国内有两家企业的利妥昔单抗类似药获批 。2019年2月复宏汉霖的利妥昔单抗注射液汉利康获批上市,这是中国第一款生物类似药。 复宏汉霖最新的中标价格显示经过一年多的商业化后,其价格也有所下降,从1640元/瓶降至目前最低价格为1398元/瓶。 2019年,汉利康于中国境内(不包括港澳台地区)的销售额约为人民币 1.5 亿元。 2020年9月, 信达生物与礼来共同开发的的利妥昔单抗生物类似药获批。
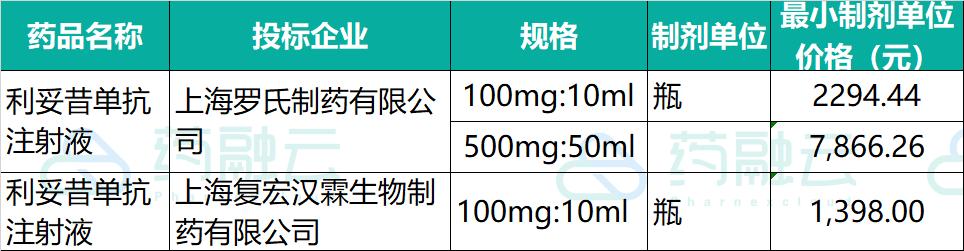
国内开发利妥昔单抗类似物并注册申报的企业已经超过10家,包括有三生国健、海正药业、正大天晴、华兰生物、丽珠单抗等知名企业。
曲妥珠单抗—国内2 家(1+1)
曲妥珠单抗是由罗氏公司旗下基因泰克公司研发,商品名[赫赛汀],是一款靶向人表皮生长因子2(Her2)的重组DNA衍生的人源化单克隆抗体,于 1998 年获得 FDA 批准,用于治疗 HER2 过度表达的转移性乳腺癌的药物。该品种为罗氏旗下王牌药品,长期占据了药物销售 TOP10 的名单。自上市以来,销量稳步增长,但是由于专利期的到来,2018 年之后销售呈下降趋势,2019 年全球销售额近 60 亿瑞士法郎,同比下降 13.5% ,2020年全球销售额近 37.32 亿瑞士法郎,同比下降 34%。
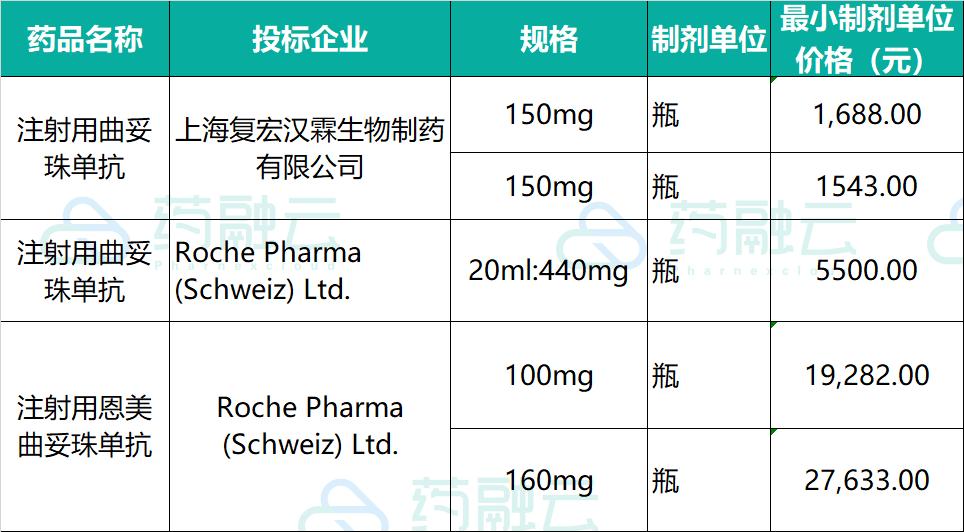
罗氏曲妥珠单抗于 2002 年在中国获批上市,2017年纳入医保,由21613元/瓶降至7600元/瓶 (440mg), 之后国内多家医院出现断货情况。 2019年经国家医保局再次谈判,原研再次降价完成医保续约,目前的单价约为5500元/瓶(440mg), 公开数据显示,2018年,赫赛汀在中国境内的销售额约27亿元; 2019年销售额达45.7亿人民币 。
国内目前仅有一家生物类似药获批。2020年8月复宏汉霖曲妥珠单抗生物类似药汉曲优获批上市,也是复宏汉霖第二个上市的生物药。复宏汉霖的生物类似药(汉曲优)目前定价为1688元/瓶(150mg),部分地区已经降到1543/瓶(150mg)。值得注意的是,汉曲优(欧盟商品名:Zercepac)已于7月获得欧盟委员会(EC)批准于欧盟上市, 成为首个登陆欧洲市场的“中国籍”单抗生物类似药 。
此外,7家本土药企的曲妥珠单抗已进入III期临床,分别是嘉和生物、海正药业、正大天晴、上海生物制品研究所、安科生物、华兰基因、艾迈医疗;华兰基因、万乐药业、齐鲁制药和迈博太科处于I期临床。
中成药集采—标准是难点
中成药谈判采购和集中采购,最大的难点在于标准, 中成药尚未制定出药品集采的统一标准, 中成药的标准只能用治疗位置或治疗领域来定义,比起化药来说更为复杂。或许借集采的机会,顺便建立质量标准,行业格局得以重塑,整个行业格局也得到重塑。
2020年下半年,青海省、浙江省金华市、河南省濮阳市等多地,陆续针对部分需求大、金额高的中成药品种进行了集采的试点,取得了显著降价成效。对此,国家医保局也公开表示,今后将继续指导地方开展中成药集采,根据临床用药需求,完善采购方式,合理确定集采范围。
首先集采的中成药应该是厂家众多的同名同方药,在2020年《中药注册分类及申报规则》,其实是划出了中成药带量采购的先后顺序,所以同名同方药会先集采,比如有众多厂家复方丹参片,然后再探索独家中药的“集采”。
【声明】本文为原创文章,首发于微信公众号:药融云。如需转载请联系授权!