本文来自微信公众号:X-MOLNews
副标题:简单链状酰胺参与的不对称Mannich反应
鉴于手性纯的β-氨基酸类衍生物普遍存在于天然产物和药物分子中,所以发展经济高效的方法学来实现该类化合物的不对称合成具有至关重要的科学意义和实用价值。其中不对称Mannich反应被认为是一种行之有效的合成方法,它采用亚胺和酰胺/酯为反应原料,同时符合原子经济性的概念。然而,简单的链状酰胺(如丙酰胺这类α位不含有任何活化基团的羰基化合物)却很少用于不对称Mannich反应中。其中一个反应难题便是这类酰胺的p K a较低,针对该问题, 日本东京大学 的 Shu̅ Kobayashi 教授课题组近年来一直致力于发展强Brønsted碱催化的反应体系,进而实现了弱酸性羰基化合物(如酯、酰胺、烷基腈、甲苯等)的加成反应。另一方面,不对称控制也是一大反应难题。传统的方法是采用手性Lewis碱(如手性冠醚)为多齿配体,让其与钾离子螯合,从而形成手性的金属物种(图1 (1))。
近日, Shu̅ Kobayashi 教授和同事 Yasuhiro Yamashita 教授等研究者发展了一种 新型的手性诱导模式 (图1 (2)) ,即手性钾盐K-Box能作为一种手性配体与KHDMS配位,原位生成一个全新的手性Brønsted碱催化剂 。该催化剂能够高活性、高选择性地 实现丙酰胺等简单酰胺和亚胺之间的不对称Mannich反应 ,从而高效地合成了一系列β-氨基取代的酰胺类化合物。相关结果发表在 J. Am. Chem. Soc. 上。
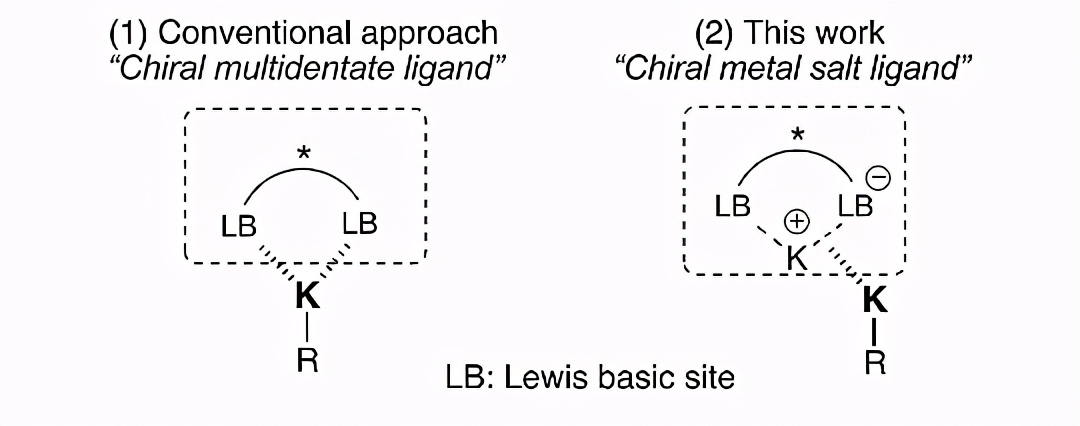
图1. 金属物种的手性修饰方法。图片来源: J. Am. Chem. Soc.
首先,作者选择2,4-二甲氧基苯基(DMP)保护的苯甲醛亚胺 1a 和 N,N -二甲基丙酰胺 2a 为模板底物,在KHMDS(10 mol %)的催化作用下于-78℃下筛选了不同的配体(图2),结果显示手性冠醚 L06 的对映选择性较差;噁唑啉类配体( L07 和 L1 )甚至都无法进行反应。幸运的是,作者发现KHMDS会和 L1 反应生成钾盐 K-L1 ,但是 K-L1 的碱性较弱,不足以攫取 2a 中的α-H,所以作者尝试调整KHMDS和 L1 的比例,最后发现当KHMDS的用量增大一倍时(即KHMDS 20 mol %、 L1 10 mol %),能以98%的收率、99:1的dr值以及91%的对映选择性得到目标产物 3aa (图2,entry 4)。

图2. 反应条件的摸索。图片来源: J. Am. Chem. Soc.
当体系中只加入KHMDS时,反应也会进行,但是收率非常低。此外,作者也尝试将KHMDS中的钾离子替换成其它阳离子(如钠离子、锂离子、铯离子),但是反应效果均不如KHMDS(图3)。他们也对底物 1a 中亚胺氮上的保护基、催化剂用量、底物 2a 的用量依次进行了考察,最后确定DMP是相对最好的亚胺保护基,1.1当量的 2 a、5 mol %的KHMDS和5 mol %的 K-L1 参与反应时,反应效果最佳。

图3. 碱金属效应。图片来源: J. Am. Chem. Soc.
在最优条件下,作者考察了该反应的底物范围(图4)。首先,他们对亚胺 1 中的芳环进行了考察,结果显示邻、间、对位甲基、甲氧基和溴原子取代的芳基亚胺都能够以高收率和高选择性转化为目标产物( 1b-1d、1g-1i 和 1l-1n )。另外,亚胺 1 中的芳环还能耐受多种*能官**团,例如乙基( 1e )、苯基( 1f )、氟原子( 1j )、氯原子( 1k )、三氟甲基( 1o )等。值得一提的是,2-萘基亚胺( 1p )、吡啶亚胺( 1q-1s )甚至烷基亚胺( 1t-1v )都能以良好至优异的收率和选择性实现这一转化,尽管2-吡啶亚胺的对映选择性较差。紧接着,作者研究了酰胺类化合物 2 中的取代基效应。他们发现当烷基酰胺上的碳链较长时( 2b-2e ),位阻较小的Box金属盐 K-L5 的催化活性更高。 N, N -二甲基乙酰胺( 2f )也能兼容该反应,以良好的收率(67%)和对映选择性(82% ee)得到目标产物。当丙酰胺上的氮原子被不同的基团取代时( 2h-2j ),反应均能取得良好至优异的收率和对映选择性。需要指出的是,丙酸叔丁酯( 2k )也能以良好的收率和对映选择性完成转化,不过非对映选择性较低。

图4. 底物拓展研究。图片来源: J. Am. Chem. Soc.
随后,作者对产物 3aa 进行了衍生化。如图5所示,氮原子上的DMP基团可以在CAN的条件下有效脱除,得到中间体 4aa ,后者经过苯甲酰基化,能以较高的收率转化为 5aa ,而且对映选择性没有任何损失(eq. 1)。此外,产物 3aa 还可以在酸性条件下以良好的收率转化成β-氨基酯 6aa (eq. 2)。值得一提的是,该反应还能以克级规模制备,并且反应的收率和选择性没有任何损失(eq. 3)。

图5. 产物衍生化和克级规模制备。图片来源: J. Am. Chem. Soc.
SCH-48462是一种胆固醇吸收*制剂抑**,它的结构特征是含有一个β-内酰胺单元。为此,作者采用KHMDS和 K-L5 为催化剂,以极好的收率和选择性完成了亚胺 1g 和酰胺 2g 之间的不对称Mannich反应。随后,将所得的产物 3gg 先后用三氟甲磺酸酐和氢氧化钠处理,以良好的收率得到β-内酰胺 7gg ,后者在CAN的条件下脱除DMP便得到 8gg 。在重结晶后, 8gg 的纯度能达到> 99% ee。最后,作者采用铜催化的C-N键偶联条件,便完成了光学纯的SCH-48462的合成(图6)。
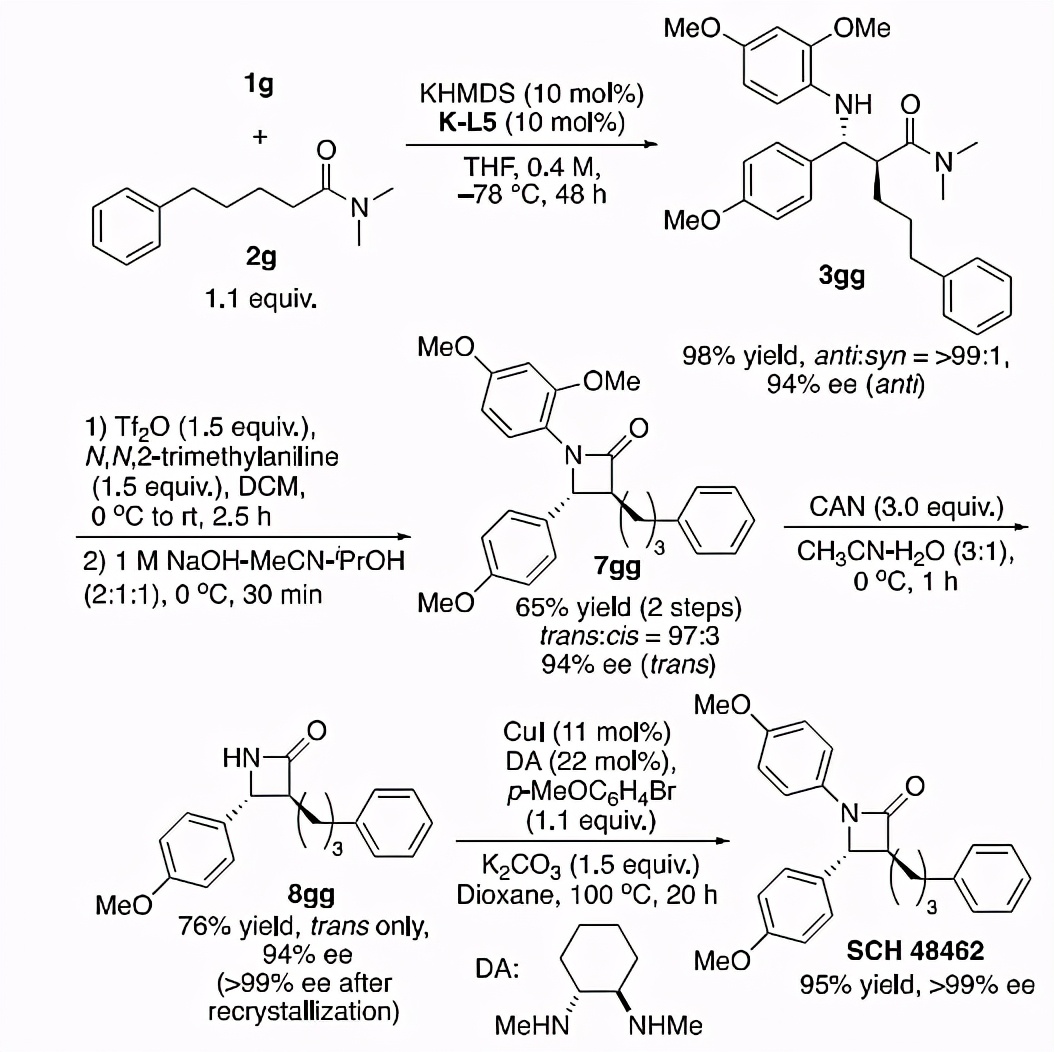
图6. 应用研究。图片来源: J. Am. Chem. Soc.
接下来,作者利用DFT计算对烯醇钾盐和 K-L1 的络合物进行了研究(图7)。结果显示两个钾离子对称分布在 L1 上的两个氮原子之间,而烯醇中间体又处于两个钾离子之间。核磁共振实验也证实了该结构具有对称性。因为烯醇钾盐和 K-L1 之间存在明显的静电作用,所以该络合物具有一定的稳定性。这暗示着烯醇钾盐中的钾原子和氧原子都被固定在一个手性环境中。

图7. 计算研究。图片来源: J. Am. Chem. Soc.
在此基础上,作者提出了可能的反应机理(图8)。首先,KHMDS和K-Box原位生成络合物 I ,后者作为碱攫取底物 2 中的α-H,生成了手性络合物 II (核磁共振实验证实了其存在)。因为络合物 II 的Lewis酸性更强而且二者聚集状态有所区别,所以络合物 II 的反应活性要高于游离的烯醇钾盐。随后,络合物 II 和亚胺 1 反应形成中间体 III ,并释放K-Box。此时,有两种可能的途径(Path A和B)再生络合物 II ,从而实现了催化循环。

图8. 反应催化循环。图片来源: J. Am. Chem. Soc.
总结
Shu̅ Kobayashi教授和Yasuhiro Yamashita教授等人利用手性KHMDS-Box钾盐( K-Box )催化体系实现了简单酰胺类化合物的不对称Mannich反应,以良好至优异的收率和非对映及对映选择性合成了一系列β-氨基取代的酰胺类化合物,同时还能用于生物活性分子SCH-48462的合成。该工作的一大亮点在于首次发现了一种新颖独特的手性配体K-Box钾盐,而且通过计算研究和核磁实验证实了该钾盐会与烯醇钾盐配位形成具有对称性的活性钾离子物种,从而促进不对称催化反应的完成。
Chiral Metal Salts as Ligands for Catalytic Asymmetric Mannich Reactions with Simple Amides
Yasuhiro Yamashita, Aika Noguchi, Seiya Fushimi, Miho Hatanaka, Shu̅ Kobayashi
J. Am. Chem. Soc ., 2021 , 143 , 5598-5604, DOI: 10.1021/jacs.0c13317
导师介绍
Yasuhiro Yamashita
https://www.x-mol.com/university/faculty/4277
Shu̅ Kobayashi
https://www.x-mol.com/university/faculty/4246