最常见的免疫相关性内分泌毒性反应是:垂体炎(导致垂体功能减退,包括中枢性甲状腺功能减退、中枢性肾上腺功能减退、中枢性性腺功能减退症)和甲状腺功能异常(主要是甲状腺功能减退和甲状腺炎)。其他免疫相关性内分泌疾病比较少见,比如原发性肾上腺功能减退、I型糖尿病、高钙血症和甲状旁腺功能减退等。
在开始免疫检查点*制剂抑**治疗前,推荐患者检测甲状腺功能(促甲状腺激素TSH和游离甲状腺激素FT4等)、血糖(空腹葡萄糖、糖化血红蛋白)、肾上腺功能(8am促肾上腺皮质激素ACTH和皮质醇,必要时加测4pm和12am的ACTH和皮质醇,了解激素节律变化)。
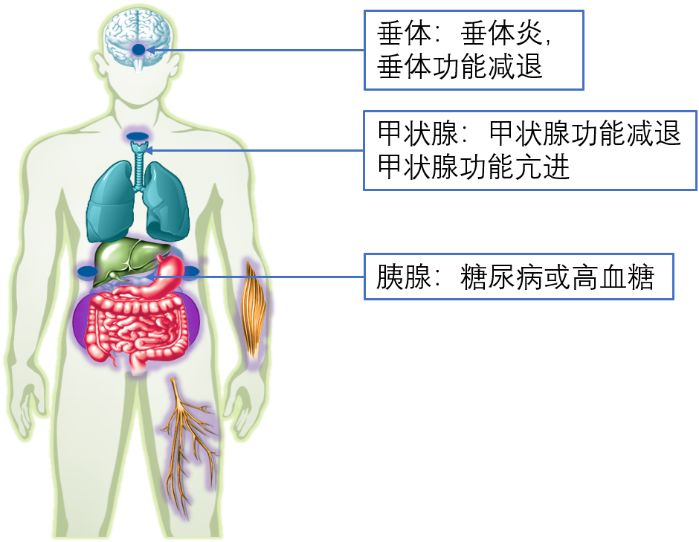
一、 垂体功能减退
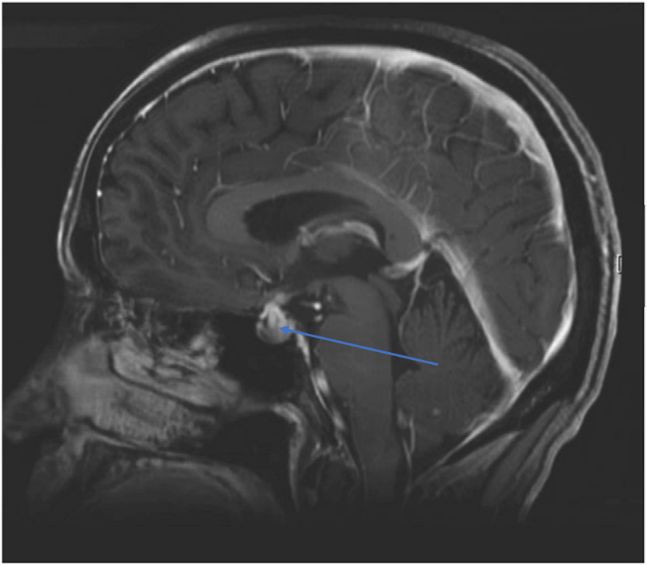
最常见于CTLA-4抗体(ipilimumab)治疗的患者,3mg/kg剂量组发生率≤10%,10mg/kg剂量组发生率17%;ipilimumab联合nivolumab发生率≤13%[1,2,3,4,5]。从开始使用ipilimumab到发生垂体功能减退的中位时间为8-9周[6,7]。症状包括头痛(约85%)和乏力(约66%)。如果甲状腺功能检查提示TSH和FT4均降低,则需高度怀疑垂体功能减退,最常见的是中枢性甲状腺功能减退(>90%),其次是中枢性肾上腺功能不全[8,9,10]。约75%患者会同时出现中枢性甲状腺功能减低和中枢性肾上腺功能减退;50%的患者会出现全垂体功能减退(包括肾上腺功能减退合并甲状腺功能减退和性腺功能减退)[10-12]。影像学检查垂体MRI可见垂体增大,垂体柄增厚、鞍区上凸、腺体信号不均匀强化等。
如果怀疑垂体功能减退的患者,需要进一步检测明确诊断。推荐的检查包括早晨8点甲状腺功能(TSH和FT4)、肾上腺功能(8am、4pm和12am的昼夜ACTH、皮质醇节律)、性腺功能(睾酮、雌激素、卵泡刺激素FSH、黄体生成素LH)、垂体鞍区MR。必要时请内分泌专科会诊。
如果患者确诊垂体功能减退,需要接受激素替代治疗(生理剂量的甲状腺激素)。入股同时存在肾上腺功能减低和甲状腺功能减低,应在使用甲状腺激素之前给予糖皮质激素,以避免出现肾上腺危象。如果患者出现严重头痛、视觉异常或肾上腺危象,应给予高剂量糖皮质激素。肾上腺功能减退和甲状腺功能减退是长期垂体功能减退的结果,多数情况下需要长期的激素替代治疗。
二、甲状腺功能异常
使用免疫检查点*制剂抑**的患者,发生甲状腺功能异常的概率大约为6-20%,包括甲状腺功能减退、甲状腺功能亢进和甲状腺炎。
如果患者出现无法解释的乏力、体重增加、毛发脱落、畏寒、便秘或者抑郁等症状,需要考虑甲状腺功能减退的可能。TSH升高、FT4降低是甲状腺功能减退的主要标志。确诊为甲状腺功能减退的患者建议左旋甲状腺素替代治疗,每4周复查甲状腺功能,以调整替代激素的剂量。

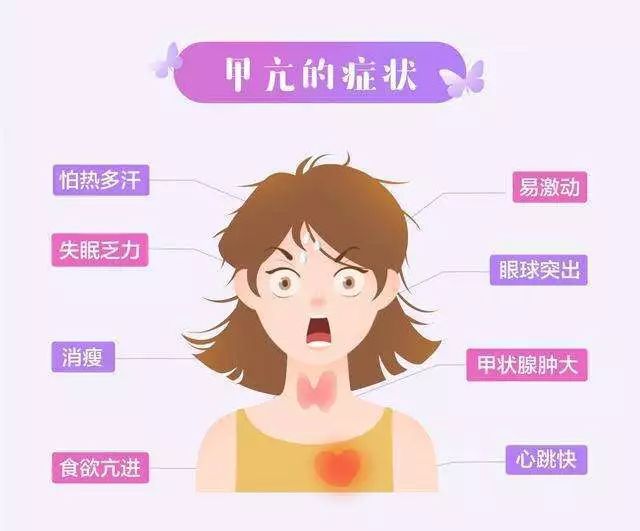
甲状腺功能亢进(FT4升高、TSH降低)主要是因甲状腺炎所引起,临床表现为体重下降、心慌、怕热、震颤、焦虑、腹泻等高代谢症状。多发生于使用免疫检查点*制剂抑**一个月后。如果怀疑甲状腺炎,需要排除其他因素,如Graves’病。推荐行促甲状腺受体抗体(TRAb)、甲状腺过氧化物酶(TPO)检测,必要时行影像学检查,如放射性碘摄取。通常甲状腺功能亢进呈自限性,甚至后期或转变为甲状腺功能减低。因此,甲状腺功能亢进的亚急性过程中可以保守治疗,观察为主,对于有症状的患者,可以给予β受体阻滞剂以控制高代谢症状;每2-3周复查甲状腺功能;一旦出现甲状腺功能减退,则建议使用甲状腺激素替代治疗[8,13]。
三、I型糖尿病或者高血糖
如果患者出现多尿、口渴、体重下降、恶心和或/呕吐,则需考虑I型糖尿病或者高血糖症,并且需要排除是否合并酮症酸中毒。可行糖化血红蛋白以及相关抗体检测:如谷氨酸脱羧酶GAD65,胰岛素抗体、抗胰岛细胞抗体等。C肽和胰岛素水平和释放曲线可以进一步明确。

四、免疫检查点*制剂抑**之内分泌不良反应管理
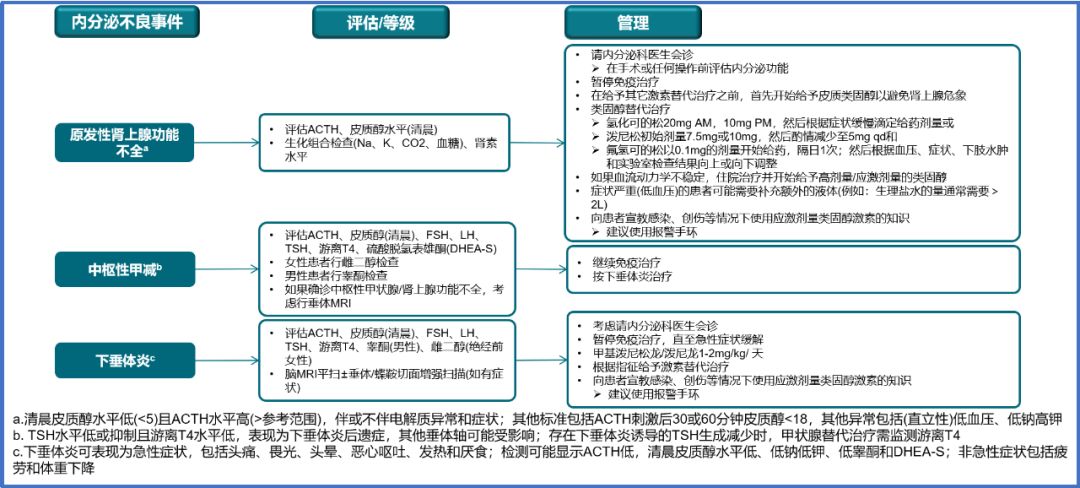
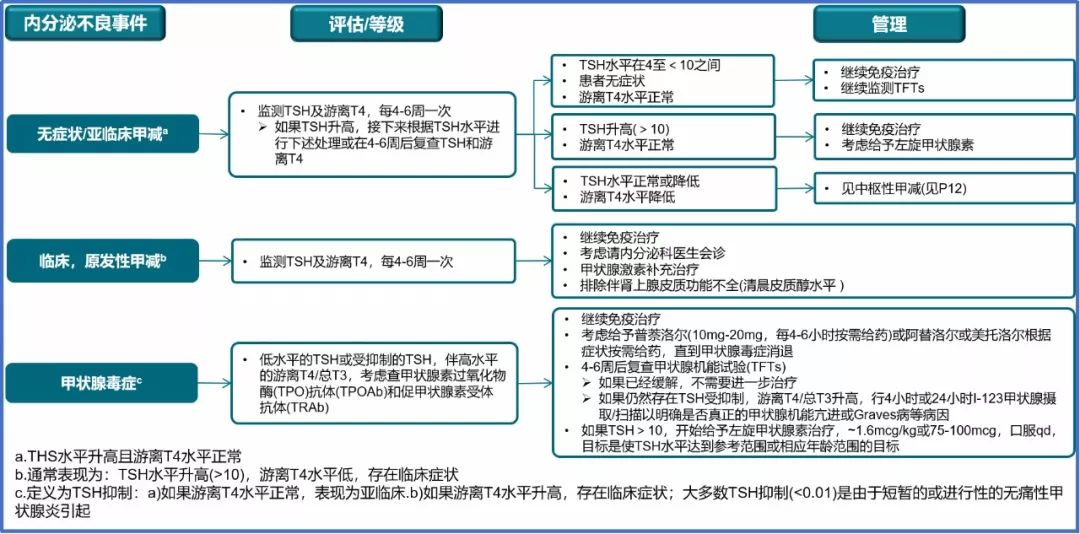
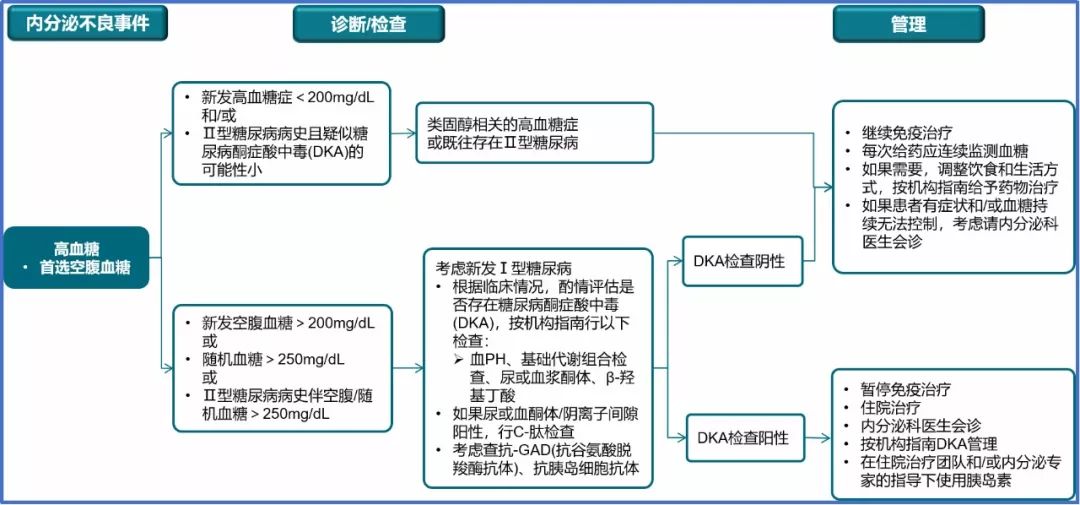

参考文献:
1. Eggermont AM, et al. Prolonged survival in stage III melanoma with Ipilimumab adjuvant therapy. N Engl J Med. 2016;375(19):1845–55.
2. Villadolid J, Amin A. Immune checkpoint inhibitors in clinical practice: update on management of immune-related toxicities. Transl Lung Cancer Res. 2015;4(5):560–75.
3.Ascierto PA, et al. Ipilimumab 10 mg/kg versus ipilimumab 3 mg/kg in patients with unresectable or metastatic melanoma: a randomised, double-blind, multicentre, phase 3 trial. Lancet Oncol. 2017;18(5):611–22.
4. Tarhini, A.A., et al., A phase III randomized study of adjuvant ipilimumab (3 or 10 mg/kg) versus high-dose interferon alfa-2b for resected high-risk melanoma (U.S. Intergroup E1609): Preliminary safety and efficacy of theipilimumab arms. Journal of Clinical Oncology, 2017. 35(15_suppl): p. 9500–9500.
5. Ryder M, et al. Endocrine-related adverse events following ipilimumab in patients with advanced melanoma: a comprehensive retrospective review from a single institution. Endocr Relat Cancer. 2014;21(2):371–81.
6. Kumar V, et al. Current diagnosis and Management of Immune Related Adverse Events (irAEs) induced by immune checkpoint inhibitor therapy. Front Pharmacol.2017;8:49.
7. Weber JS, et al. Toxicities of immunotherapy for the practitioner. J Clin Oncol. 2015;33(18):2092–9.
8. Dadu R, Zobniw C, Diab A. Managing adverse events with immune checkpoint agents. Cancer J. 2016;22(2):121–9.
9. Faje A. Immunotherapy and hypophysitis: clinical presentation, treatment, and biologic insights. Pituitary. 2016;19(1):82–92.
10. Marie Joelle Pitteloud RD, Cabanillas ME, Shah K, Mimi I-Nan H, Habra MA, Waguespack SG, et al. Hypophysitis in the Age of Cancer Immunotherapy: Experience in a Large Cancer Center, in Endocrine Society’s 97th Annual Meeting and Expo. San Diego: CA; 2015.
11. Corsello SM, et al. Endocrine side effects induced by immune checkpoint inhibitors. J Clin Endocrinol Metab. 2013;98(4):1361–75.
12. Blansfield JA, et al. Cytotoxic T-lymphocyte-associated antigen-4 blockage can induce autoimmune hypophysitis in patients with metastatic melanoma and renal cancer. J Immunother. 2005;28(6):593–8.
13. Byun DJ, et al. Cancer immunotherapy - immune checkpoint blockade and associated endocrinopathies. Nat Rev Endocrinol. 2017;13(4):195–207.