
一、引言
近年来,阿尔茨海默病药物得到广泛开发,并且主要集中在β淀粉样蛋白的开发中。在1998到2015年之间推出123种治疗阿尔兹海默症的药物[1],仅有三种药物和一种联合治疗方案获得FDA的上市批准,在这123种药物中没有一种能够治愈阿尔兹海默症,甚至也做不到连延缓疾病进程的目的。本文阐述阿尔茨海默病的三期临床失败药物,与大家分享和交流。
二、目前三期临床终止药物
总结目前三期失败药物的特征,分析药物失败的具体原因,通过总结前人的教训给予我们更深刻的启示。PS:更多相关药物具体信息可以到药渡网查询。
Suritozole
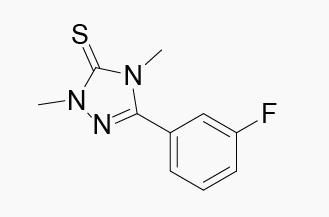
开发公司:赛诺菲
作用机制:GABAA受体反向激动剂
总结说明:曾处于临床三期,用于治疗阿尔茨海默病,但该研究已被终止。用于治疗重度抑郁症的研究曾处于临床二期,但该研究也已被终止。
失败原因:涉及到这个药物的报道截止到1997年,后续无相关文献报道。
Phenserinetartrate
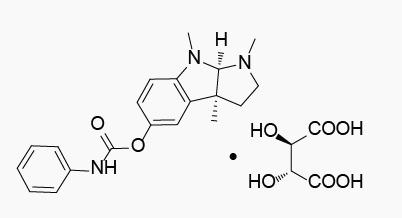
开发公司:该化合物最初由TorreyPines (2006年被Axonyx收购),于2008年授予QR Pharma全球独家开发权
作用机制:乙酰胆碱酯酶*制剂抑**
总结说明:曾处于临床三期,用于治疗阿尔茨海默症(AD),但该研究已被终止。
失败原因:2007年报道称,最近在欧洲的3期试验表明,本品的任何临床相关活性可能受其作用持续时间的限制[2]。
分析说明:Phenserine可能是适合的经皮给药的候选药物;实现足够量级的透皮通量,以支持认知功能在认知损伤的动物模型中产生的功效。 此外,透皮途径避免了对即时肝毒性和首过代谢的其它有害后果。在透皮(贴片)装置中从软膏载体中缓慢释放活性剂也可证明有利于维持Phenserine的作用持续时间,这已被认为是临床功效的限制因素。可以配制Phenserine经皮给药以提供临床益处,可有助于减少AD的胆碱能缺乏等[2]。
Zanapezil Fumarate
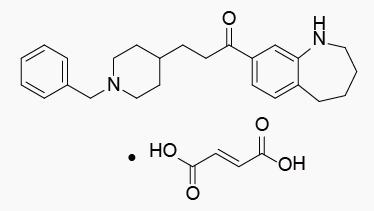
开发公司:武田
作用机制:乙酰胆碱酯酶*制剂抑**
总结说明:曾经处于临床三期,用于治疗阿尔茨海默症,但该项研究于2003年终止。
失败原因:2003年5月,由于在试验中缺乏剂量依赖效应,公司停止了该化合物的开发。
分析说明:由于缺乏剂量依赖性,导致其无法开发成药物。
Xanomeline
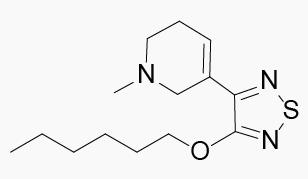
开发公司:最初由诺和诺德研发,后授权给礼来公司
作用机制:M1和M4型毒蕈碱型乙酰胆碱受体激动剂
总结说明:曾处于临床三期,用于治疗阿尔茨海默病,但该研究已被终止。
失败原因:结合最初研究表明毒蕈碱激动剂Xanomeline是亚型选择性毒蕈碱M1受体激动剂,并且是阿尔茨海默病的潜在的新治疗手段。然而,后来的体外和体内功能研究表明这种化合物可能更好地描述为亚型选择性M1/M4毒蕈碱受体激动剂[3]。
分析说明:Xanomeline的这种亚型在动物中存在典型的胆碱模拟物副作用,特别是胃肠道副作用。在健康志愿者和阿尔茨海默病患者中,已经报道了这些副作用的,并且在患者群体中,导致≥50%的停药率。显然,临床前研究尚不能预测这种不利特征,这表明或者是不如临床前研究预测的亚型选择性,或者对于毒蕈碱受体在人和动物之间存在差异。然而,在阿尔茨海默病患者剂量依赖性地改善行为障碍和社会行为方面,包括减少幻觉,激动,妄想,声音爆发和可疑。对认知的影响不如所测试的最高剂量时那么强烈。在阿尔茨海默病患者中的这些效应已经推动了毒蕈碱激动剂具有潜在的抗精神病效应的建议[3]。
Sabcomeline Hydrochloride

开发公司:最初由葛兰素史克研发,2001年授权Minster Pharmaceuticals (2010年被Proximagen收购),2010年BrainCells购买了该化合物。
作用机制:毒蕈碱M1受体拮抗剂
总结说明:曾经进行过用于治疗阿尔茨海默病的临床三期研究和用于治疗精神分裂症和重度抑郁症的临床二期研究。
失败原因:开展三期临床试验后,发现试验结果不良,终止了三期试验。
分析说明:三期临床试验过程中,并没有达到预期的目标。
Xaliproden Hydrochloride
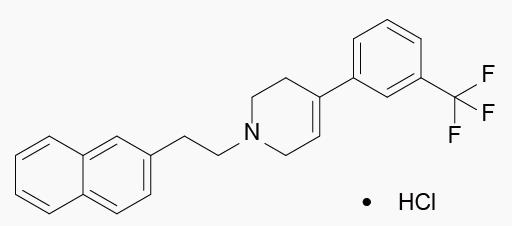
开发公司:赛诺菲
作用机制:5-羟色胺1A激动剂
总结说明:用于治疗阿尔茨海默症,肌萎缩性脊髓侧索硬化症及结直肠肿瘤。2001年,因治疗肌萎缩性脊髓侧索硬化症,Xaliproden获欧盟孤儿药资格。但是目前该研究已经终止。
失败原因:Sanofi-Aventis在2007年发布了新闻公告,声称该公司在III期临床试验中未能显示足够的疗效,因此停止了用于阿尔茨海默病的xaliproden的开发[4]。
分析说明:该公司进一步在其主页上指出,在阿尔茨海默病中用xaliproden进行的III期试验组中显示海马体萎缩显示的更慢;然而,该产品未显示对主要终点的统计学产生显著影响[4]。
Sabeluzole
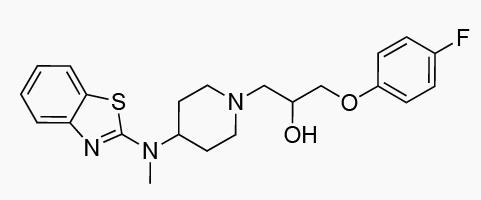
开发公司:最初由杨森公司开发,后授权给协和发酵麒麟
作用机制:钙离子通道拮抗剂
总结说明:曾处于三期临床,用于治疗阿尔兹海默病(AD)。但是,该临床研究已经终止。该药物也进行了用于治疗糖尿病性神经病变的研究,该研究曾处于哪个临床阶段未知,不过目前也已终止。
失败原因:最初开发用于治疗阿尔茨海默病,随后被研究用于其他应用。
分析说明:目前并没有实质性进展的报导,相继的临床研究也终止。
Ensaculin Hydrochloride
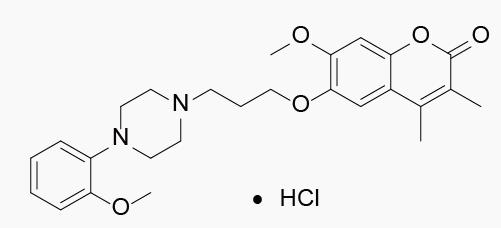
开发公司:由Dr.Willmar Schwabe研发
作用机制:N-甲基-D-天冬氨酸受体拮抗剂和5羟色胺1A受体激动剂
总结说明:曾进入临床三期,用于治疗阿尔茨海默病,该项研究已经终止。
失败原因:本品在人体试验中耐受性良好,但有效性方面未被证明。
分析说明:主要副作用是直立性低血压
Encenicline Hydrochloride
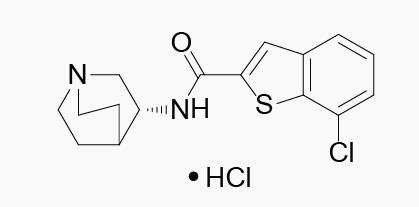
开发公司:最初由拜耳研发,后来授权给了EnVivo Pharmaceuticals(现在的FORUM Pharmaceuticals),随后FORUM制药于2009年将亚洲地区的开发权授权给田边三菱制药。
作用机制:*碱烟**α7激动剂
总结说明:曾处于临床三期,研究治疗阿尔兹海默症和精神分裂症相关的认知障碍。
失败原因:Encenicline的安全性和耐受性好,但在治疗精神病的疗效上未能达到试验一级终点(精神分裂病人认知功能的改善)。而Encenicline用于治疗阿尔茨海默病的研究试验因为胃肠副作用已被FDA叫停。2016年3月24号, FORUM Pharmaceuticals公司宣布Encenicline临床三期试验失败。
分析说明:尼古丁本身和很多其它受体结合,所以毒性太大,不能作为药物。另外尼古丁半衰期也太短。所以唯一可行的办法是寻找亚型选择性配体。Alpha 7受体和很多功能有关,这个受体可以作为一个和PD-1、TNF类似的技术平台,用于开发多种疾病的药物。但调节功能繁多的靶点更容易导致副作用。alpha受体激动剂和拮抗剂都被用于多个疾病的药物开发,但到目前为止临床试验胜少负多。Encenicline在阿尔茨海默病二期临床显著改善认知和生活功能并达到所有试验一级、二级终点,而且功能改善和血药浓度正相关。Encenicline在精神分裂症二期临床也改善认知功能。alpha 7也是在很多组织包括胃肠平滑肌高度表达的受体,所以出现中枢外副作用也不能算是完全意外。Alpha 7受体表达广泛,功能多样,其配体和其它很多中枢GPCR配体结构类似,所以开发十分复杂。
Semagacestat
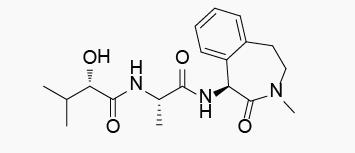
开发公司:礼来和Élan (现在为Perrigo)联合研发
作用机制:γ-分泌酶*制剂抑**
总结说明:曾经处于临床三期,用于治疗阿尔茨海默病(AD),该研究于2010年8月已经终止。
失败原因:本品并不能改善老年性痴呆患者的认知功能。它与日常生活活动、总体功能和生活质量等多个指标的临床恶化具有剂量相关性。在发现临床指标恶化后,出于安全性考虑,研究人员提前进行了无效分析,中止了该研究。礼来公司于2010年停止了该药的研发。
分析说明:积极治疗组临床恶化的一个可能原因是,抑制γ-分泌酶可能干扰Notch受体相关的核信号。Notch是一个跨膜蛋白,是γ-分泌酶底物,具有细胞表面受体功能,是参与胚胎发育和其他细胞与细胞间相互接触的蛋白质。与恶化相关的另一个因素可能与Semagacestat对靶标淀粉样前体蛋白代谢的影响有关。这项研究显示了淀粉样前体蛋白参与其中的生物标志物证据(例如,2个Semagacestat治疗组Aβ40和Aβ42水平均降低)。然而,3组脑脊液中上述Aβ蛋白的水平都没有显著变化,表明这个作用靶点是在外周而非在脑部有受累。“临床恶化代表的是中枢γ-分泌酶抑制、中枢Aβ减少的靶向效应,还是与其它抑制物质相关的未曾预料的效应,目前仍然没有答案。”
Solanezumab
开发公司:礼来
作用机制:β淀粉样蛋白的单克隆抗体
总结说明:2016年11月23日宣告该药第3次临床试验失败
失败原因:两项Solanezumab的临床测试包括研究药物对一种罕见的遗传性脑退化症疗效,以及新药对脑部发现类淀粉蛋白沉积、但未出现病征的人是否有效,开发者坚持新药对病征轻微的脑退化症患者似乎特别有效,能将脑部退化速度减慢三成。于是开发者安排了2100名轻度患者进行长达18个月的第3次实验,但最终仍失败。
分析说明:Solanezumab最终的治疗目标是延缓患有轻度阿尔茨海默症患者的疾病进展,有学者也提出医学界对于阿尔茨海默症的普遍治疗观点是越早治疗效果越好,最好能在淀粉样蛋白沉淀形成的初期。但事实上,在临床中精准发现这类病人暂时不具有可操作性,因为即使淀粉样蛋白沉淀会导致阿尔茨海默症这个假说仍然成立,也不可能对所有人的大脑进行扫描。其次,即使有淀粉样蛋白沉淀,部分患者并不会表现出阿尔茨海默症的症状,包括礼来的临床试验也是凭借患者的意识表现来判断哪类患者应该入组,所以对于阿尔茨海默症的诊断方法还有待继续进步,找到能够区分患者疾病严重程度以及预测出现何种生理病理变化的患者是疾病高危人群的生物标记物。在给药剂量上,Bernstein Research分析师Tim Anderson认为是Solanezumab的给药剂量偏低从而影响了试验的结果,而礼来之前也没有解释关于这个给药剂量是如何确定的。Solanezumab也许未来并不会完全从视线中消失,CreditSuisse分析师Vamil Divan认为现在否定淀粉样假说还为时太早,未来Solanezumab通过调整用药剂量或者与其他药物联用或许还有一线生机。
三、 个人体会
1、整理每个药物在三期失败的原因并进行原因分析
2、β淀粉样蛋白是近年来研发的主流方向
3、这里整合了前人经验,也有很多不足之处,欢迎各位老师批评指正
参考文献:
[1] Movement AsI. 2015.Researching Alzheimer’s Medicines:Setbacks andStepping Stones Summer 2015. PhMRA
[2] Utsuki T, Uchimura N,Irikura M et,Preclinical investigation of the topical administration ofphenserine: transdermal flux, cholinesterase inhibition, and cognitiveefficacy. J Pharmacol Exp Ther. 2007,321(1):353-61
[3] Naheed R. Mirza, DanPeters, and Robin G. Sparks.Xanomeline and the Antipsychotic Potential ofMuscarinic Receptor Subtype Selective Agonists. CNS Drug Reviews.2003,9(2):159–186
[4] Marc Porzner MD,Tobias Müller MD & Thomas Seufferlein MD.SR 57746A/xaliproden, anon-peptide neurotrophic compound: prospects and constraints for the treatmentof nervous system diseases. Expert Opin. Investig. Drugs (2009) 18(11):1765-1772
作者信息: heavybird
本人长期从事信息查询、立项调研和项目评估工作。擅长于数据资源的深入挖掘和有效利用,建立便捷有效的药物信息检索方法,通过将检索得到的药物信息进行收集和整合,系统地对药物进行立项调研和评估,为项目后续立项奠定基础。
转载声明:本文为投稿文章,如需转载,必须保留作者信息及本文来源。