不想错过界哥的推送?
戳上方蓝字“医学界肿瘤频道”关注我们
并点击右上角“···”菜单,选择“设为星标”
胃肠食管肿瘤资讯第6期。
本期提要
-
循环肿瘤DNA:不仅仅可以预测结直肠癌预后;
-
纳武利尤单抗三线治疗晚期胃/胃食管结合部癌有效、安全;
-
细胞减灭术联合腹腔热灌注化疗或为胃癌腹膜转移的重要选择
一
循环肿瘤DNA:不仅仅可以预测结直肠癌预后
近日,Wang等[1]和Reinert等[2]在《JAMA Oncology》发表的两项研究再次证实,循环肿瘤DNA(ctDNA)阳性对I~III期结直肠癌(CRC)患者预后有不良影响。同时,这两项研究还提示:ctDNA分析还可以作为分类检测,基于疾病复发风险对手术切除的CRC患者进行分层;ctDNA纵向数据分析或可改变CRC术后管理策略,包括对辅助化疗患者的选择、辅助化疗持续时间的优化以及更早发现临床复发。
■ ctDNA分析可作为常规监测策略的补充
对于手术切除的非转移性CRC患者,最佳监测方案仍不清楚。
Wang等的研究提示,ctDNA分析可作为常规监测策略(计算机断层扫描和血清癌胚抗原检测)的补充,作为分类检测基于疾病复发风险对手术切除的CRC患者进行分层。
该研究共纳入来自58例患者的319份血液样本。中位随访49个月,45例ctDNA阴性患者中,无1例复发。13例ctDNA阳性患者中有10例复发,复发率为77%。48例未复发的患者中,3例(6%)的ctDNA结果为阳性,但随后降至不可检测水平。此外,阳性ctDNA先于放射学和临床复发证据,中位提前时间为3个月。
■ ctDNA纵向数据分析或可改变术后管理策略
Reinert等的研究显示,来自ctDNA的纵向数据分析,通过使危险分层、辅助化疗监测和早期复发检测成为可能,可潜在改变CRC术后管理,包括对辅助化疗患者的选择、辅助化疗持续时间的优化以及更早发现临床复发。
在该项前瞻性、多中心队列研究中, 125例I~III期CRC患者和795份血浆样本被纳入分析。术前,94例患者中有84例(89.4%)可检测到ctDNA。确定性治疗后,纵向ctDNA分析发现,16例复发患者中有14例(87.5%)检测到ctDNA。
术后30天,ctDNA阳性患者复发的可能性是ctDNA阴性患者的7倍(HR 7.2;P<0.001)。辅助化疗后,ctDNA阳性患者复发的可能性也很大(HR 17.5;P<0.001)。然而,在确定治疗后的监测期间,ctDNA阳性患者复发的可能性是ctDNA阴性患者的40多倍(HR 43.5;P<0.001)。
多变量分析显示,调整已知的临床病理学危险因素后,ctDNA状态与复发独立相关。
二
纳武利尤单抗三线治疗晚期胃/胃食管结合部癌有效、安全
ATTRACTION-2试验的探索性亚组分析发现,无论先前使用曲妥珠单抗与否,纳武利尤单抗作为晚期胃/胃食管结合部癌患者的三线或之后治疗均是有效、安全的 [4]。研究结果近日发表于《Gastric Cancer》。
关于免疫检查点*制剂抑**在人表皮生长因子受体2阳性(HER2+)晚期胃/胃食管结合部癌患者中的疗效,目前尚缺乏数据。由于在ATTRACTION-2试验中没有捕获HER2状态,该项事后分析将先前使用曲妥珠单抗(Tmab+)状态作为HER2表达状态的替代,来评估纳武利尤单抗作为三线或之后治疗的疗效和安全性。
ATTRACTION-2是一项随机、双盲、安慰剂对照的3期多中心试验,患者按2:1比例随机分组,每2周接受纳武利尤单抗(3 mg/kg)或安慰剂,直至疾病进展或发生毒性需要停药。
该事后分析的主要疗效终点是总生存(OS),次要疗效终点包括无进展生存(PFS)、客观缓解率(ORR)、疾病控制率(DCR)、缓解持续时间(DOR)、至缓解时间(TTR)等。安全性终点为研究期间发生的不良事件(AE)和与治疗相关AE。
结果显示,纳入的493例患者中,81例有曲妥珠单抗使用史即Tmab+,包括接受纳武利尤单抗者59例,接受安慰剂者22例;412例没有使用过曲妥珠单抗(Tmab-),包括纳武利尤单抗者271例,安慰剂者141例。
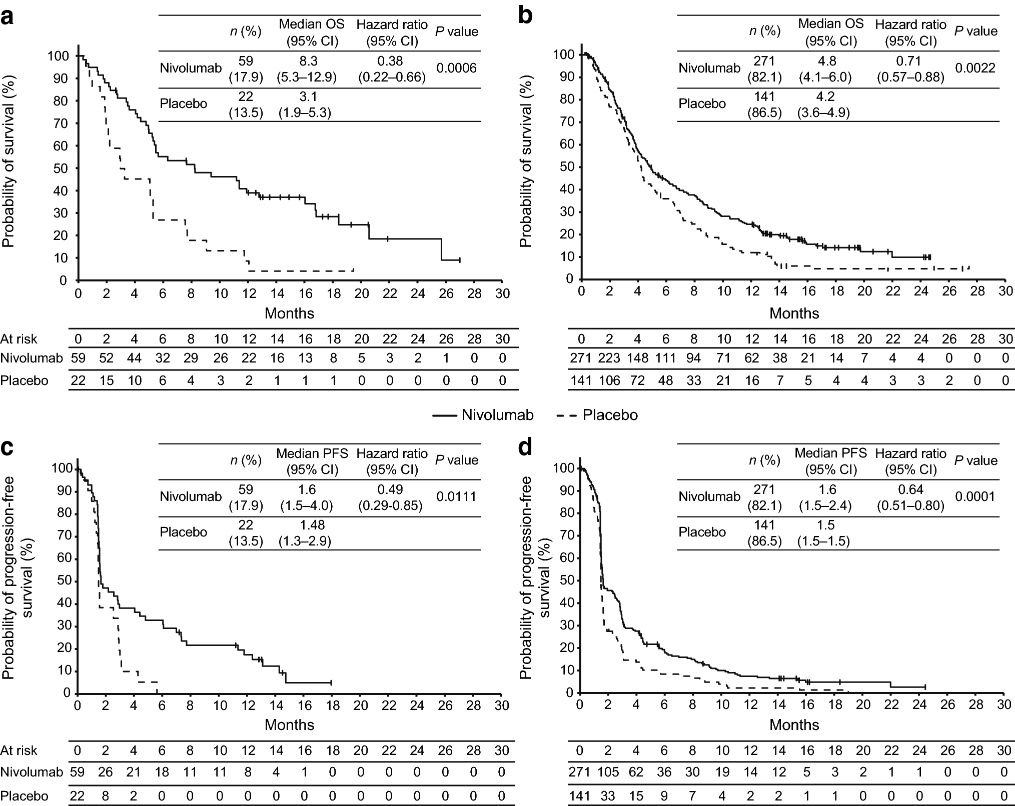
图1 患者的总生存和无进展生存情况
在Tmab+组和Tmab-组,接受纳武单抗者的OS显著长于安慰剂者(Tmab+:8.3个月 vs 3.1个月,HR 0.38,P=0.0006;Tmab-:4.8个月 vs 4.2个月,HR 0.71,P=0.0022)。两组中接受纳武单抗者PFS也明显长于安慰剂者(Tmab+:1.6个月 vs 1.5个月,HR 0.49,P=0.0111;Tmab-:1.6个月 vs 1.5个月,HR 0.64,P=0.0001)。
在Tmab+组和Tmab-组,接受纳武利尤单抗者的ORR分别为16.9%和7.7%,接受安慰剂者均未显示任何缓解。无论Tmab状态如何,纳武利尤单抗者的DCR均高于安慰剂者(Tmab+:42.4% vs 31.8%;Tmab-:30.6% vs 18.4%),肿瘤缩小(> 1%)患者比例也较高(Tmab+:38.8% vs 16.7%;Tmab-:36.4% vs 10.5%)。
此外,两组中纳武利尤单抗者的中位TTR分别为3.0个月和1.6个月,中位DOR分别为8.6个月和9.5个月。
总之,在Tmab +和Tmab-组,与安慰剂相比,纳武利尤单抗改善了OS、PFS、ORR、DCR和肿瘤负荷减少的患者比例,纳武利尤单抗治疗者具有持续和持久的治疗反应。
在安全性方面,Tmab+组和Tmab-组中纳武利尤单抗者的任何AE发生率相当;Tmab +组任何治疗相关AE发生率略高于Tmab组,而治疗相关严重AE的发生率相当。
三
细胞减灭术联合腹腔热灌注化疗或为胃癌腹膜转移的重要选择
目前,在大多数腹膜恶性肿瘤中,完全细胞减灭术(CRS)联合或不联合腹腔热灌注化疗(HIPEC)是唯一可延长患者生存期的治疗方法。但是,人们对于CRS-HIPEC治疗胃癌腹膜转移仍存争议。
CYTO-CHIP研究显示,与单纯CRS相比,CRS-HIPEC可明显改善胃癌腹膜转移患者的OS、无复发生存,且不增加并发症发生率或死亡率。对于在专业中心进行完全CRS的严格选择患者,CRS-HIPEC或是一种有价值的治疗选择[5]。结果近日发表于《Journal of Clinical Oncology》。
研究者从前瞻性数据库中确定了277例胃癌腹膜转移患者,这些患者接受了具有治愈意图的完全CRS(没有残留结节> 2.5 mm)治疗。其中180例接受了CRS-HIPEC和97例接受单纯CRS。使用腹膜癌指数评估肿瘤负荷。使用Cox比例风险回归模型并采用基于倾向得分的逆处理概率加权法(IPTW)来评估HIPEC的影响。
结果显示,IPTW调整后,CRS-HIPEC和单纯CRS组患者的中位OS分别为18.8个月和12.1个月,3年OS率分别为26.21%和10.82%,5年OS分别率为19.87%和6.43%,3年无复发生存率分别为20.40%和5.87%,5年无复发生存率分别为17.05%和3.76%,前者均显著优于后者。
两组患者的90天死亡率分别为7.4%和10.1%,主要并发症发生率分别为53.7%和55.3%,均无显著差异。
简言之,与单纯CRS相比,CRS-HIPEC可使严格挑选的患者获得更长的生存,且不增加术后并发症发生率和死亡率。
参考文献
[1]Wang Y, Li L, Cohen JD, et al. Prognostic Potential of Circulating Tumor DNA Measurement in Postoperative Surveillance of Nonmetastatic Colorectal Cancer[J]. JAMA Oncol. 2019 May 9. [Epub ahead of print]
[2]Reinert T, Henriksen TV, Christensen E, et al. Analysis of Plasma Cell-Free DNA by Ultradeep Sequencing in Patients With Stages I to III Colorectal Cancer[J]. JAMA Oncol. 2019 May 9. [Epub ahead of print]
[3]Morris V, Dasari A, Kopetz S. Can Circulating Tumor DNA in Early-Stage Colorectal Cancer Be More Than a Prognostic Biomarker?[J]. JAMA Oncol. 2019 May 9. [Epub ahead of print]
[4]Satoh T, Kang YK, Chao Y, et al. Exploratory subgroup analysis of patients with prior trastuzumab use in the ATTRACTION-2 trial: a randomized phase III clinical trial investigating the efficacy and safety of nivolumab in patients with advanced gastric/gastroesophageal junction cancer[J]. Gastric Cancer. 2019 May 13. [Epub ahead of print]
[5]Bonnot PE, Piessen G, Kepenekian V, et al. Cytoreductive Surgery With or Without Hyperthermic Intraperitoneal Chemotherapy for Gastric Cancer With Peritoneal Metastases (CYTO-CHIP study): A Propensity Score Analysis[J]. J Clin Oncol. 2019 May 14. [Epub ahead of print]
本文首发:医学界肿瘤频道
作者:辛迪
责任编辑:Sharon
征 稿
欢迎投稿到小编邮箱:zl@yxj.org.cn
请注明:【投稿】医院+科室+姓名
来稿以word文档形式,其他不予考虑
你在看我吗?
↓↓↓↓