昨日,CDE官网公示了拟纳入优先审评程序的抗肿瘤药物注册申请,公示期为5日。
根据总局《关于解决药品注册申请积压实行优先审评审批的意见》公告,CDE于2016年4月20日组织专家,按照《药品审评中心优先审评工作程序(试行)》,对申请优先审评的用于抗肿瘤适应症的药品注册申请进行了审核论证。
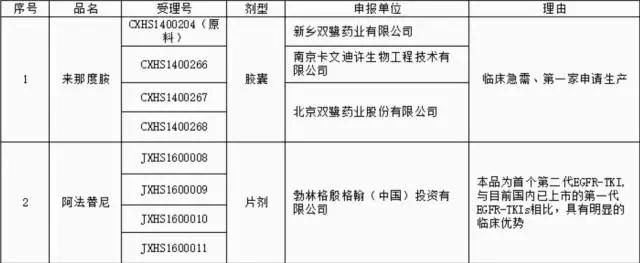
下述注册申请品种为临床急需或与我国现有治疗药品比较具有明显的临床优势,拟纳入优先审评程序:
来那度胺专利壁垒
来那度胺是美国Celgene公司开发的新一代抗肿瘤药,主要用于治疗骨髓增生异常综合症和多发性骨髓瘤。2005年12月27日,FDA通过快速审批程序批准该药上市。
2006年6月29日,FDA又批准该药联合地塞米松治疗预先接受过至少一种治疗的多发性骨髓瘤患者。
在2016年2月17日和2月20日,美国FDA和欧盟EMA相继扩展了来那度胺的治疗适应症——和地塞米松联合使用作为一线用药治疗多发性骨髓瘤。
事实上,美国Celgene公司的来那度胺上市后,其在中国申请了29件与来那度胺相关的专利。但由于印度专利体质不同,目前,印度Natco公司(Lenalid®)也在本国生产销售来那度胺胶囊。而我国尚无国产来那度胺制剂合法上市,主要依靠从美国Celgene公司进口。
尽管美国Celgene公司在我国申请的部分核心专利的有效期需到2024年才解禁,但因市场等因素的触动,多年来,中国相关药企无时不刻在关注。
而此次新乡双鹭药、南京卡文迪许生物、北京双鹭率先申请“优先审评”,无疑是在宣告其成功挑战了Celgene本品的专利壁垒及限制,实现了创新,未来或将改变疾病领域市场竞争格局。
阿法替尼将“全球化”
阿法替尼是一款治疗转移性非小细胞肺癌的靶向药物,其已在许多市场获得批准,包括欧盟、日本、台湾、加拿大(以上国家商品名为GIOTRIF)和美国(商品名为GILOTRIF),用于治疗特定类型的EGFR突变阳性NSCLC患者,至今国内尚未批准。
但对于阿法替尼,其实勃林格殷格翰2015年5月31日曾宣布,欧洲药品管理局人用药品委员会(CHMP)已经公布了肯定意见,建议批准阿法替尼用于在铂类药物化疗时或化疗后肿瘤有所进展的晚期肺鳞状细胞癌(SqCC)患者的治疗。其意味着勃林格殷格翰取得欧洲肺鳞状细胞癌市场控制权。
而勃林格殷格翰(中国)投资有限公司时隔一年在中国申请阿法替尼的“优先审评”,这或许更多的是出自“市场全球化”战略。
(田子夏)