2007年11月,索拉非尼作为抗血管生成的分子靶向药物开启了肝癌分子靶向治疗的大门,可以说是肝癌治疗史上的巨大进步。
尽管索拉非尼给肝外扩散和血管侵犯的患者提供了更多的选择,也在一定程度上实现了中晚期肝癌患者的长期生存,但由于其有效率低和副反应率高等原因,全球一直在试图开发新的能够替代甚至超越索拉非尼的靶向药物。
在随后的近十年内,针对肝细胞癌的靶向药物不断涌现,但纷纷败给了索拉非尼。直到2017年~2018年,瑞戈非尼、仑伐替尼、卡博替尼和雷莫芦单抗在临床试验中取得较好的研究成果而脱颖而出,并投入临床使用。但肝癌患者仍面临极大的治疗需求。
而这个冬天,TA来了
IMbrave 150是一项评估PD-L1免疫*制剂抑**atezolizumab(阿替利珠单抗)联合贝伐珠单抗用于治疗既往未接受过系统性治疗的不可切除的肝细胞癌(HCC)患者的研究。患者按照2:1的比例随机接受阿替利珠单抗和贝伐珠单抗联合治疗或索拉非尼治疗。
在近日举办的2019年欧洲肿瘤内科学会亚洲大会(ESMO-ASIA)的主席会议上公布该研究的结果。
结果显示,阿替利珠单抗联合贝伐珠单抗组的中位OS(总生存)尚未达到,索拉非尼组中位OS 为13.2个月。
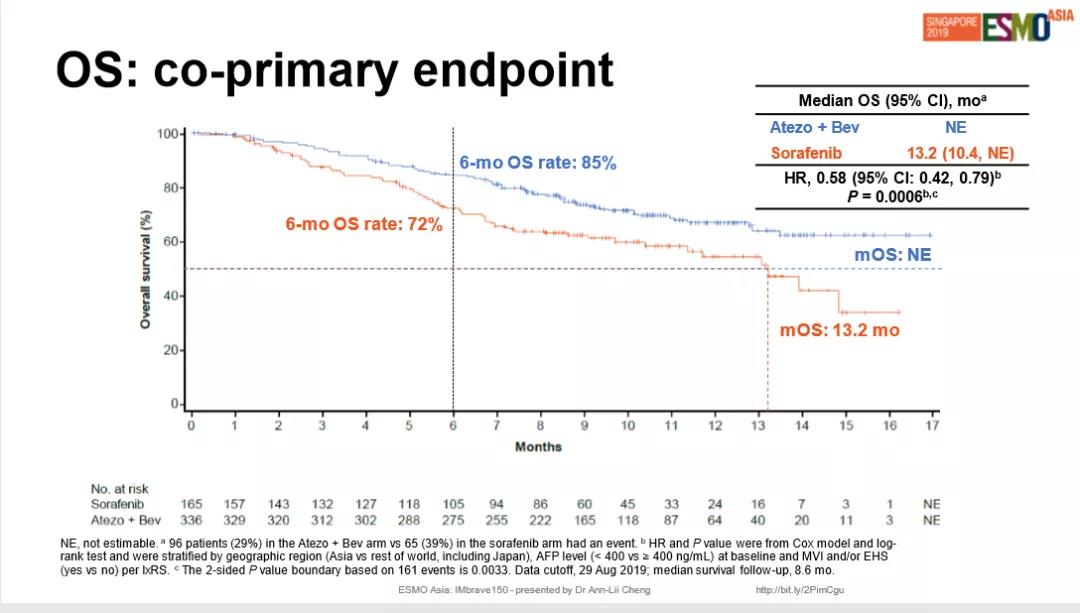
PFS(无进展生存期)方面,阿替利珠单抗联合贝伐珠单抗的中位PFS为6.8个月,索拉非尼组中位PFS为4.3个月。
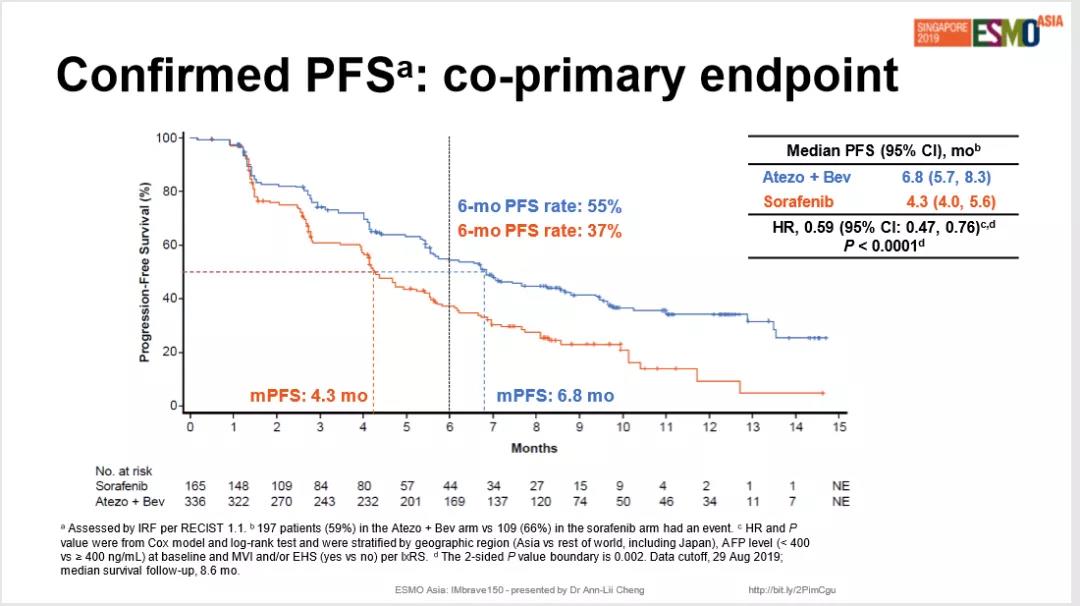
ORR(客观缓解率)方面,阿替利珠单抗联合贝伐珠单抗的ORR达27%,其中完全缓解达6%。
与索拉非尼相比,阿替利珠单抗联合贝伐珠单抗治疗降低42%的死亡风险,降低41%的疾病进展风险。此外,阿替利珠单抗联合贝伐珠单抗还能延缓患者报告生活质量发生恶化的时间(预先定义的描述性次要终点,至恶化发生的中位时间:11.2个月 vs 3.6个月)。
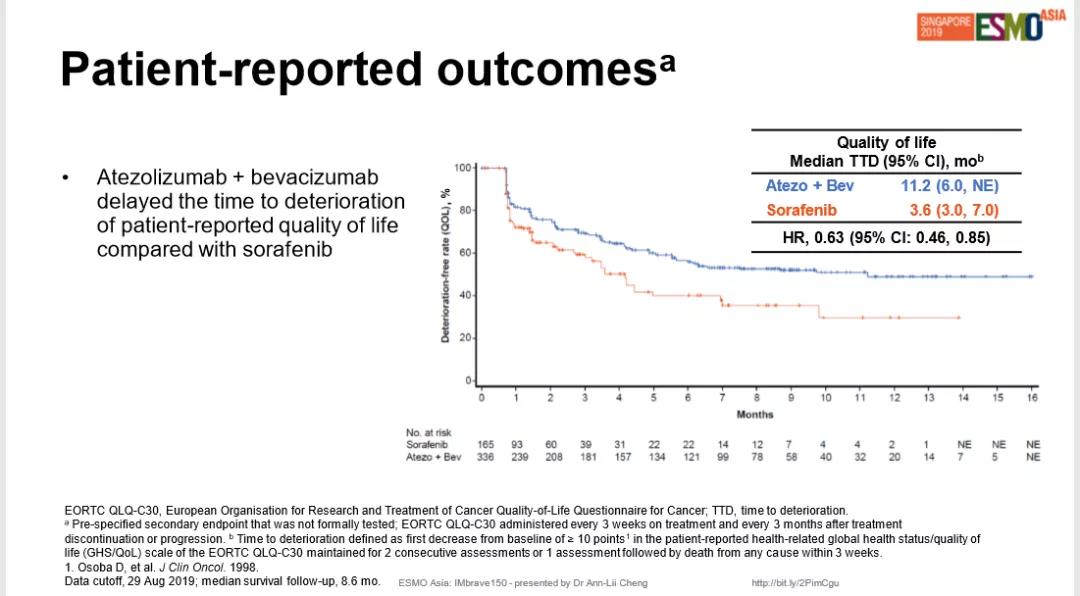
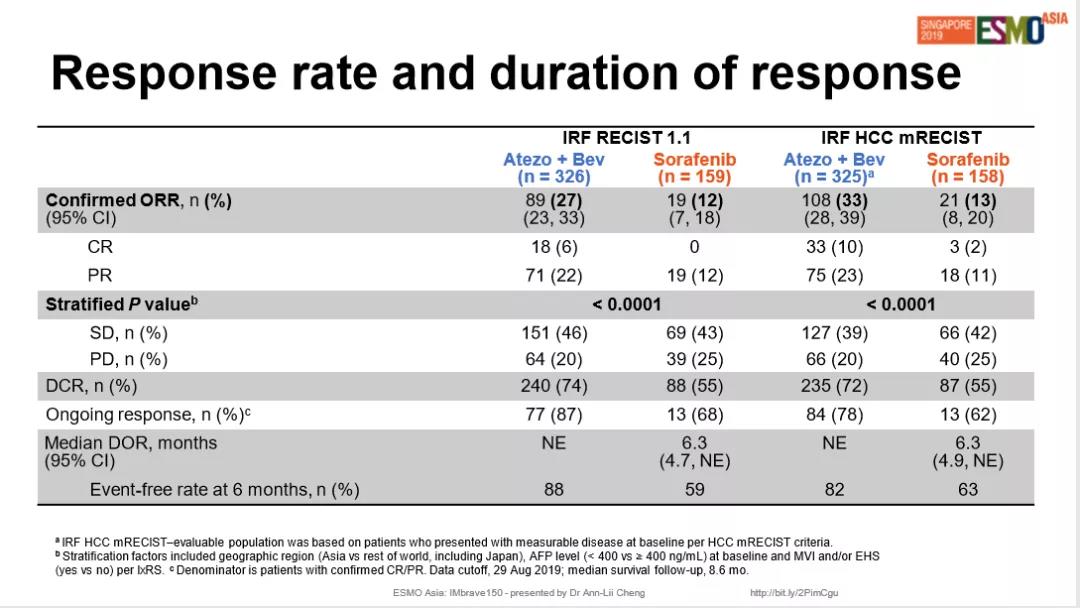
安全性方面,联合治疗组中57%的人发生了3~4级不良反应事件,其中36%与治疗相关;接受索拉非尼组中的有55%的人发生了3~4级不良反应事件,其中46%与治疗有关。总得来看,替利珠单抗与贝伐珠单抗联合治疗普遍耐受性良好且毒性可控,除了两种单药已知的安全性事件外,没有发现新的安全性问题。
IMbrave 150是全球首个获得成功的肝癌免疫联合治疗临床三期研究,成为近10年来首个一线能够提升肝癌生存数据OS,优于现有标准疗法索拉非尼的全新治疗方案,堪称历史里程碑事件。
据了解,该研究数据将提交给美国食品药品监督管理局、欧洲药品管理局和中国国家药品监督管理局用于阿替利珠单抗新适应症申请。期待该方案早日在国内获批!
当然除了等待新方案的获批,患者还有一个选择——参加临床试验。通过这种方式,患者可以先一步尝试这种新的治疗方案和药物,还能免去高昂的医疗费用。
这对于癌症患者来说,特别是那些目前无标准治疗或无力负担先进治疗的人,是个不错的选择。
目前正在开展一项信迪利单抗联合 IBI305 对比索拉非尼用于晚期肝细胞癌一线治疗有效性和安全性的随机、开放、多中心研究。
信迪利单抗是由信达生物自主研发的一种重组全人源化抗PD-1单克隆抗体注射液,临床前研究显示,信迪利单抗结构明确、稳定性好,具有良好的药物活性、动物药代动力学特性、药效学特征和安全性。
IBI305 是信达生物按生物类似药研发的重组抗 VEGF 人源化单克隆抗体注射液,是一种能特异性结合人 VEG-A 的单克隆抗体,根据药学、药效学、动物药代动力学的各项研究结果均显示,IBI305 与贝伐珠单抗具有较高的相似性。
如果你符合以下条件,那么将有机会加入本项目接受研究药物的免费治疗,并获得专业医生团队的随访指导。
- 经组织学/细胞学确诊为肝细胞癌;
- 未接受全身性治疗,比如化疗、靶向治疗等;
- 如既往接受过术后辅助化疗结束治疗时间至疾病复发时间>6个月;
点击“了解更多”