JP2022058019A
技术背景
对于风能和太阳能等可再生能源,由于环境的影响,发电量波动很大,因此需要一个大型的储能系统。最近,可再生能源发电成本已降至燃煤发电成本的一半以下,发电份额正在扩大。鉴于未来的广泛使用,需要改进电池生产。
蓄电池是节能、引入新能源、清洁汽车等不可或缺的设备,从各国经济增长的角度来看,蓄电池被定位为重要的关键设备。
目前,锂离子电池等蓄电池一直是电子设备行业和汽车行业的驱动力,但取决于电池的应用,温度特性和安全性不足正在推迟全面推广。因此,期望根据应用开发新的电池,同时实现电池的高性能和高安全性。对于产地分布不均的稀有金属和资源,考虑到市场价格的波动和难以获取的风险,风险管理非常重要。尽管从各个角度来看,稀有金属回收技术的发展正在取得进展,但仍需要开发由廉价、易得且生产区域分布不均匀的材料制成的电池。
目前,钠离子电池和全固态电池的开发正在作为能够解决这些问题的电池系统进行。
钠在海水中含量丰富,是地壳中的第六种元素。它价格低廉,易于获得,其来源不像锂那样分布不均。因此,预计资源采购风险将降低,电池成本将降低。
技术问题描述
尽管从最近的无稀有金属趋势来看,它是一种非常有吸引力的元素,但它的氧化还原电位比锂高约0.3V,其离子体积增加了一倍多,原子量增加了约3.3倍。简单地用钠离子代替传统锂离子电池的离子种类很难获得足够的电容量和循环特性。
此外,作为使用钠的电池系统,有钠硫电池和钠金属氯化物电池。钠硫电池由含有钠(如β-氧化铝和β〃-氧化铝)的氧化铝作为固体电解质、钠作为负极活性材料和硫作为正极活性材料组成。
在钠金属氯化物电池中,固体电解质和负极活性材料是相同的,使用诸如NaAlCl4、NiCl2、FeCl2、CoCl2和CrCl2的金属氯化物用作正极活性材料。
钠硫电池和钠金属氯化物电池不需要电解质溶剂,但与锂离子电池和钠离子电池不同,它们不在室温下工作。因此,通过来自外部的热源将电池的温度保持在250至350°C,并将负极活性材料和正极活性材料置于熔融状态,以提高固体电解质的离子电导率。
另一方面,全固态电池是使用固体电解质的电池系统。由于该固体电解质负责正极和负极之间的离子传导,因此可以在不使用钠离子电池(使用电解质溶液的钠蓄电池)所需的有机溶剂的情况下生产全固体电池。例如,钠离子电池仅使用六氟磷酸钠(NaPF6)盐作为电解液,但除了钠离子(Na+)之外,六氟磷酸离子(PF6-)也用于电池的充电和放电。因为它会移动,所以很难将钠离子出口率设置为1。
然而,无机固体电解质的浓度极化不发生,钠离子传输数几乎变为1。如果选择合适的电解窗电解质,全固态电池可以抑制副反应,例如活性材料的溶解反应、通过电解产生的气体以及电解质分解产物的沉淀。此外,全固态电池预计是具有优异安全性和可靠性的蓄电池,因为其不太可能引起气体或液体的点燃或液体的泄漏。
与常规蓄电池一样,全固态钠蓄电池由正极、负极和电解质组成,但电解质必须是固体并具有钠离子传导性。
正电极和负电极由能够通过充电和放电插入或合金化钠离子的活性材料和固体电解质组成。例如,用于正极的活性材料的实例包括TiS2(例如,参见非专利文献3)和NaMO2(下文中,M是Co、Ni、Mn或Fe)(例如,非专利文献4至6),Na2MnO3-NaMO2(例如,参见专利文献1)、NamP2O7(例如,参考专利文献2)等是已知的。用于负极的活性材料的实例包括硬碳(参见例如专利文献3)、软碳(参见,例如专利文献4)、诸如锡和锑的简单物质或化合物(例如,参见专利文献5和6),金属钠等是已知的。
通过迄今为止的大力研究和开发,已经发现了表现出高离子电导率的各种固体电解质(例如,参见专利文献7至10)。它们大多是由钠盐和无机衍生物组成的无定形或晶体。然而,由于这些是粉末状或片状材料,并且它们中的许多具有与水高度反应的性质,因此传统的电池生产方法不能原样应用。具体地,在全固态钠蓄电池中,与液体型钠离子电池不同,难以将电解质渗透到电极的活性材料层中以构建离子传导路径。因此,有必要在活性材料层中包括固体电解质,以增强固体电解质和活性材料的固体颗粒之间的离子导电性。
例如,在专利文献11、专利文献12和非专利文献7中,制备并烧制包含活性材料前体粉末和固体电解质粉末的电极混合物前体(活性材料层前体)。因此,已经提出了由活性材料和固体电解质组成的电极混合物(活性材料层)或使用该电极混合物的全固态钠蓄电池。例如,Na2FeP2O7结晶玻璃用作活性材料前体。玻璃和结晶玻璃通过烧制(热处理)结晶,在此过程中发生软化流动。因此,仅通过烧制而不加压,它就可以与固体电解质粉末结合。
此外,根据专利文献11、专利文献12和非专利文献7,将电极混合物前体施加到固体电解质层的一个表面,然后在400℃或更高温度下烧制以形成固体电解质层。在一个表面上形成电极混合物。
然而,由于固体电解质不具有电子传导性,因此难以确保电极的电子传导性和离子传导性。另一方面,虽然可以包括导电助剂,但是如果导电助剂的含量太大,则电极混合物的每单位质量的活性材料的量减少,并且充电/放电容量趋于降低。此外,烧结的抑制切断了离子传导路径,并且存在充放电容量和放电电压将降低的担忧。
解决路径
本发明人最初对通过在无机固体电解质的表面上直接形成电极混合物来改善全固态钠蓄电池的性能进行了勤奋的研究。当形成和集成时,电池电阻目前很高,并且增加单位面积的容量是有限制的。因此,本发明人没有在无机固体电解质的表面上直接形成电极混合物,而是进行了重复的研究,使得 电极混合物和无机固体电解质可以用作单独的构件以形成电池 。本发明已经完成。本发明可以解决现有技术的上述问题(问题)和本发明人新发现的问题。
本发明的第一方面涉及一种全固体钠蓄电池,其中在电极混合物和无机固体电解质之间插入有机固体电解质。
本发明的第二方面涉及根据权利要求1所述的全固态钠蓄电池,其中所述有机固体电解质包含聚乙二醇或环氧乙烷。
根据权利要求3,有机固体电解质还含有钠盐,当有机固体电解质的重量为1时,钠盐在0.1至1.5的范围内。根据1或2所述的全固态钠蓄电池。
本发明的第四方面涉及根据权利要求1至3中任一项所述的全固态钠蓄电池,其中所述有机固体电解质的厚度在0.1μm至500μm的范围内。
本发明的权利要求5是权利要求1至4中的任一项,其中所述无机固体电解质是硫化物基、氧化物基或氢化物基固体电解质,其厚度为1mm或更小,空隙率为20%或更小。关于上述全固态钠蓄电池。
本发明的第六方面涉及根据权利要求1至5中任一项所述的全固体钠蓄电池,其中所述无机固体电解质是含钠的氧化铝。
本发明的第七方面涉及根据权利要求1至6中任一项所述的全固体钠蓄电池,其中所述无机固体电解质的密度在2.7g/cc至3.5g/cc的范围内。
根据权利要求8,所述电极混合物包含多磷酸盐过渡金属氧化物,并且所述多磷酸盐过渡过渡金属氧化物是由通式NaaMbPcOd表示的晶体,其中M是Fe、Mn,并且它是Co、Ni和V中的至少一种,并且a、b和c为0.0<a≤3.5,b=1,1.0≤c≤3.0,3。根据权利要求1至7中任一项所述的全固态钠蓄电池,其中0≤d≤30。
本发明的权利要求9是权利要求1至8中的一项,其中所述电极混合物形成活性材料簇,其中连接了多个粒径在0.1μm至100μm范围内的颗粒。关于所描述的全固态钠蓄电池。
根据本发明的第十方面,除了活性材料之外,电极混合物还含有至少一种选自碳酸亚乙酯、碳酸聚乙烯酯、聚乙二醇和环氧乙烷的离子传导助剂。
根据权利要求10所述的全固体,其中所述电极混合物包含选自金属、碳材料、导电聚合物和导电玻璃的至少一种导电助剂。
根据权利要求11所述的全固态钠蓄电池,其中所述导电助剂是选自粉末状碳、纤维状碳和片状碳中的至少一种。
本发明的所有权利要求13,其中所述电极混合物是多孔的,当去除所述有机固体电解质时,空隙率在5%至50%的范围内。
本发明的第十四方面涉及根据权利要求1至13中任一项所述的全固体钠蓄电池,其中当去除有机固体电解质时,所述电极混合物是多孔的,孔径为0.1μm至100μm。
本发明的第十五方面涉及根据权利要求1至14中任一项所述的全固体钠蓄电池,其中,所述电极混合物包含粒度为0.1μm至100μm的无机固体电解质粉末。
16.本发明的第16方面涉及根据权利要求1至15中任一项所述的全固态钠蓄电池,其中所述电极混合物不包含树脂基粘合剂。
本发明的17涉及根据权利要求1至16中任一项所述的全固体钠蓄电池,其中,所述全固体钠电池使用钠金属、钠合金或钠离子存储材料作为对电极。
本发明的权利要求18是一种全固态钠蓄电池,其具有这样的结构,其中电极混合物与具有电子传导性的集电体电接触,并且集电体是具有通孔的金属。根据权利要求1至17中任一项所述的全固态钠蓄电池,其由非穿透性金属制成。
技术细节
1、为了实现上述目的,在根据本发明的全固态钠蓄电池1中,如图1所示,将有机固体电解质3放置在电极混合物2(活性材料层)和无机固体电解质4之间。其特征在于,它是通过插入电池配置的全固态钠蓄电池。根据该结构,通过施加电压,有机固体电解质3可以经由电极混合物2和无机固体电解质4移动钠离子。
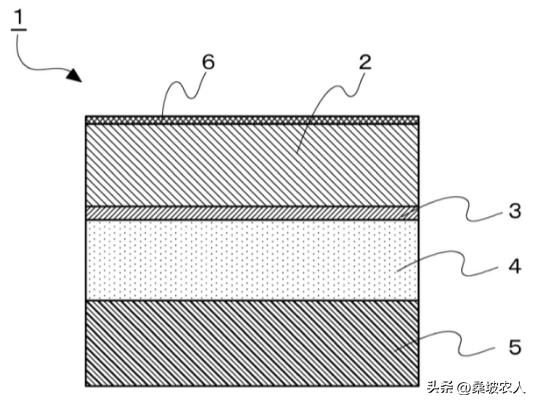
图1、单极性固态钠电池
2、根据本发明的全固体钠蓄电池被配置为使得有机固体电解质是通过聚合乙二醇或其衍生物而获得的聚醚,并且具体地包含聚乙二醇(PEG)或环氧乙烷(PEO)。更可取。PEG或PEO具有作为固体电解质的功能以及作为用于结合电极混合物和无机固体电解质的压敏粘合剂的功能。
PEG或PEO可以包含硫化合物*能官**团、氮化合物*能官**团、磷化合物*能官**团、丙烯酸酯*能官**团等。
上述PEG或上述PEO是与重均分子量(Mw)为1000以上且100万以下的乙二醇聚合的聚醚或其衍生物。最好有。虽然可以使用诸如碳酸亚乙酯(EC)的其他物质作为有机固体电解质,但优选PEG或PEO,因为其具有作为压敏粘合剂的优异功能。
特别是当电极混合物或作为被粘物的无机固体电解质在表面上具有不均匀形状或具有空隙时,由于电池的离子电阻降低,以改善与无机固体电解质之间的接触面积。
3、优选使有机固体电解质液化并将其施加到电极混合物或(/和)无机固体电解质上。此外,有机电解质可以是不可燃的离子液体。有机固体电解质可以通过将目标材料溶解在有机溶剂中而液化。有机溶剂没有特别限制,只要其能够溶解目标材料即可,其实例包括链烃溶剂和环状烃溶剂。链烃溶剂的实例包括碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、甲基碳酸乙酯(EMC)、过碳酸叔丁基异丙酯、二氯甲烷、腈基溶剂、醇基溶剂等,N-甲基-2-吡咯烷酮(NMP)、亚硫酸钠、碳酸乙烯酯(VEC)、碳酸丙烯酯(PC)、1,3-二恶烷-2-酮、苯、内酯等。
4、不可燃性离子液体只要具有离子导电性就没有特别限制,其实例包括不可燃性的离子液体,例如吡啶基、脂环族胺基和脂族胺基阳离子。通过选择与之结合的阴离子类型,可以合成各种不可燃的离子液体。阳离子例如咪唑鎓盐、吡啶鎓盐,基于鏻的离子和基于无机的离子的实例包括溴化物离子、三氟磷酸盐、四苯基硼酸盐和六氟磷酸盐。
不可燃的离子液体例如由阳离子如咪唑啉和阴离子如Br-、Cl-、BF4-、PF6-、(CF3SO2)2N-、CF3SO3-、FeCl4-的组合组成。它可以通过已知的合成方法获得。这种不可燃的离子液体可以用作电解质。
5、当组装电池时,即使在某种程度上混合了上述有机溶剂,也可以将其作为电池操作,但是由于可以抑制由于有机溶剂的挥发而导致的电池膨胀,因此可以通过减压或热处理将其充分去除。去除方法没有特别限制,例如,可以采用用于干燥锂离子电池中使用的电极浆料的方法。
当电极混合物或作为被粘物的无机固体电解质是多孔的时,有机固体电解质流过被粘物表面上的孔,使得由电池的离子传导产生的电阻(离子电阻)增加。
当电池被过度充电时,PEG或PEO在有机固体电解质中被氧化分解,从而抑制了电池的电压升高,并且失去了作为粘合剂的功能。
6、从强结合电极混合物和固体电解质的观点来看,PEG或PEO的分子量越高,越优选,但当重均分子量超过100万时,粘度变得太高并且难以处理。不仅如此,当含有稍后描述的钠盐时,离子电导率也变低。相反,当重均分子量小于1000时,粘附性差,并且当电池振动或震动时,电极混合物和无机固体电解质之间的界面被破坏,这往往是增加电池阻抗的因素。
在低分子量下,它是吸湿的,干燥过程需要时间。因此,重均分子量优选为1000以上,更优选为2500以上,上限为100万。这些可以是交联的或非交联的。
重均分子量可以通过例如使用液相色谱的凝胶渗透色谱(GPC)方法测量来确定。
7、从增加离子电导率的观点来看,有机固体电解质优选进一步包含钠盐。
当有机固体电解质的重量为1时,钠盐优选为0.1以上,更优选为0.3以上,进一步优选为0.4以上。然而,如果钠盐的含量太高,则有机固体电解质的粘度增加,并且电极混合物和固体电解质之间的粘附作用降低,因此该含量优选为1.5或更小,优选为1.2或更小。更优选0.7以下。对于具有低粘附作用的有机固体电解质,电池的充电/放电循环特性恶化。
钠盐是六氟磷酸钠(NaPF6)、高氯酸钠(NaClO4)、四氟硼酸钠(NaBF4)、三氟甲磺酸钠(NaCF3SO4)、双草酸硼酸钠(NaBC4O8)、二氟。可以使用选自磷酸钠(F2NaO2P)、双氟磺酰亚胺钠(F2Na NO4S2)、二氟硼酸钠(NaBF2O)等的至少一种。在上述钠盐中,NaPF6是优选的,因为它具有特别高的电负性并且容易电离。含有NaPF6的有机固体电解质在输入/输出特性和充电/放电循环特性方面优异。
8、从电池的优异离子导电性和高能量密度的观点来看,有机固体电解质的厚度优选在0.1μm至500μm范围内,优选在0.2μm至100μm范围。更优选的是,进一步优选0.5μm至50μm,并且期望1μm至20μm。可选地,有机固体电解质的质量优选在0.1mg/cm2至800mg/cm2的范围内,更优选在0.2mg/cm2至500mg/cm2范围内,并且0。更优选5mg/cm2至100mg/cm2,最优选1mg/cm2至20mg/cm2。
9、无机固体电解质包括硫化物型、氧化物型、氢化物型等,并且一种类型可以单独使用,或者两种或多种类型可以组合使用。从增加电池的能量密度和增加离子电导率的观点来看,这种无机固体电解质优选具有1mm或更小的厚度和20%或更小的孔隙率。
硫化物系统的实例包括A4SiS4、A4GeS4、A3PS4、A9.54Si1.74P1.44S11.7Cl0.3、A10GeP2S12、A3.25Ge0.25P0.75S4、A6PS5Cl、A2S-B2S3・ AI,A2S-P2S5-AB4。其实例包括A2S-SiS2/A4SiO4、A2S-P2S5、A7P3S11、A3.25P0.95S4(A表示Na或其他含Na的碱金属元素)。
氧化物体系的实例包括A1.3Al0.3Ti1.7(PO4)3、A0.34La0.51TiO2.94、A7LaZr2O12、A4SiO4/A2BO3、A3PO4-A4SiO4、A3BO3-A2SiO4、A2BO3-A2SO4、A2.9PO3。3N0.46、A1.07Al0.69Ti1.46(PO4)3、A3.3PO3.8N0.22、A2.9PO3.3N0.46(A表示Na或其他含Na的碱金属元素)、钠。其实例包括含有氧化铝的NASICON晶体(Na1+xZr2SixP3-xO12,0<x<3)等。
氢化物系统的实例包括ABH4、ABH4-AI、ABH4ABr、ABH4-AF、ABH4ACl等(A表示碱金属元素)。
无机固体电解质优选具有在0%至20%范围内的孔隙率。也就是说,无机固体电解质可以尽可能致密。通过将孔隙率设置为20%或更低,可以提高离子电导率。相反,当孔隙率超过20%时,离子导电性差,并且在充电期间可能发生微小的短路。
然而,除了使用单晶之外,制备孔隙率为0%的无机固体电解质是不现实的。因此,优选用有机固体电解质渗透无机固体电解质的空隙,以进一步提高离子电导率。这里,当无机固体电解质的密度超过3.5g/cc时,有机固体电解质难以渗透,因此密度优选为3.5g/cc或更低。
10、从与水接触时不可能产生有毒气体的观点来看,无机固体电解质优选为氧化物基电解质。其中,含有钠的氧化铝是优选的,因为它具有优异的电绝缘性和耐热性。
含有钠的氧化铝是由通式Na2O-xAl2O3(x=2至20)表示的晶体或陶瓷,并且具有钠离子分布在由氧化铝块形成的二维层之间的结构。β-氧化铝(Na2O-11Al2O3)和β”-氧化铝(β-双原氧化铝(Na_2O-5Al2O3))是已知的选项,但无论如何,氧化铝块形成的两个维度。由于钠离子在层之间移动,它起到固体电解质的作用。例如,含钠的氧化铝是α-氧化铝(Al2O3)和烧碱的混合物在1100°C至1500°C下烧制而成。
含有钠的氧化铝还含有至少一种选自Mg、Li、K、Rb、Zr、Pb、Y、Ag、Tl、Sr、Ca和Fe的金属或氧化物。更可取。对于含有钠的氧化铝,这些含量为5体积%或更少是优选的。结果,可以容易地获得含有致密钠的氧化铝,并且可以进一步提高离子电导率。
无机固体电解质可作为颗粒尺寸为0.1μm至100μm的粉末包含在电极混合物中。
11、电极混合物包括正电极混合物(正电极活性材料层)和负电极混合物(负电极活性物质层)。在本发明中,多磷酸盐过渡金属氧化物用于任何电极混合物中。最好将其包含在内。特别地,当电极混合物用作正极混合物时,多磷酸过渡金属氧化物用作活性材料。
多磷酸过渡金属氧化物优选为由通式NaaMbPcOd表示的晶体。
从多磷酸盐过渡金属氧化物的高离子电导率、充放电容量或输出特性的角度来看,0.0<a≤3.5,b=1,1.0≤c≤3.0,3.0。优选M是选自Fe、Mn、Co、Ni和V中的至少一种元素,且≤d≤30。
具体地说,Na2FeP2O7、Na3Fe2(PO4)3、NaFe3P3O12、Na2Fe3(PO4,3)、Na4Fe3(PO4)2(P2O7)、Na2MnP2O7、纳2CoP2O7、Na2NiP2O7、Na2Fe0.5Mn0.5P2O7、Na3V2PO7、Na2V2。它们的实例包括Na9V3(P2O4)3(PO4、2,并且它们可以单独使用或两种或多种组合使用。
在上述多磷酸盐过渡金属氧化物中,玻璃或结晶玻璃很容易合成为多磷酸盐过渡过渡金属氧化物前体,据说它在700°C或更低的烧制(热处理)过程中软化和流动并容易结晶。0.0<a≤3.0,b=1,1.1≤c≤2.9,3.5≤d≤12更为可取,0.7≤a≤2.4,因为其特性,B=1,1.2≤c≤2.8,4.0≤d≤11更好,1.7≤a≤2.3,B=1,1.4≤c≤2.7,最优选5.0≤d≤10。
12、当电极混合物用作正极混合物时,其可包含多磷酸过渡金属氧化物和另一正极活性材料。作为正极活性材料,使用包括过渡金属氧化物基材料、硫基材料、固溶体系等的已知材料。当电极混合物用作负电极混合物时,仅聚磷酸盐过渡金属氧化物不能获得实际的能量密度。因此,应含有多磷酸盐过渡金属氧化物和其他负极活性材料。包括基于过渡金属氧化物的材料、基于硫的材料、钠金属、与钠合金化的材料以及能够可逆地存储和释放钠离子的材料。
13、在根据本发明的全固态钠蓄电池中,除了活性材料之外,电极混合物选自碳酸亚乙酯(EC)、碳酸聚乙烯(PEC)、聚乙二醇(PEG)和环氧乙烷(PEO)。最好至少包含其中一种。
优选电极混合物含有选自EC、PEC、PEG和PEO中的至少一种作为导电剂,因为电极混合物的离子电阻可以降低。
尽管这取决于电极混合物的质量,但电极混合物中包含的EC、PEC、PEG和PEO的量优选在0.1mg/cm2至500mg/cm2和0.2mg/cm2的范围内。更优选约250mg/cm2的范围,并且更优选0.5mg/cm2至100mg/cm2。
根据该配置,包含在电极混合物中的选自EC、PEC、PEG和PEO的材料用作改善电极混合物中离子电导率的电解质。此外,介于电极混合物和无机固体电解质之间的有机固体电解质与电极混合物熔融并集成,以形成具有低阻抗的电池。结果,即使形成厚的电极混合物,也可以获得能够在室温环境中保持高放电容量的同时表现出优异的充放电循环特性的全固态钠蓄电池。
此外,当电池被过度充电时,电极混合物中包含的选自EC、PEC、PEG和PEO的材料被氧化分解,并且具有抑制电池电压升高的功能。
14、优选电极混合物含有导电助剂。导电助剂没有特别限制,只要其具有导电性即可,其实例包括金属、碳材料、导电聚合物、导电玻璃等,但据说其具有高的导电性和小的比重。从该观点来看,碳材料是优选的。具体实例包括乙炔黑(AB)、科琴黑(KB)、炉黑(FB)、热黑、灯黑、槽黑、辊黑、盘黑、炭黑(CB)和玻碳,可以使用其中一个或多个。
15、在上述电极混合物中,将至少含有多磷酸盐过渡金属氧化物的粉末填充在粉末模具中,并且在惰性气体或还原气体气氛中通过施加压力模塑的颗粒(片剂)。它可以在400°C至2000°C的温度下烧制而成。
然而, 由于需要超过100MPa的高压来造粒多磷酸过渡金属氧化物粉末,因此需要大型压力装置。因此,优选用树脂基粘合剂涂覆或支撑多磷酸过渡金属氧化物。通过在多磷酸过渡金属氧化物的表面上涂覆或支撑基于树脂的粘合剂,可以在100MPa或更低的压力下进行造粒。
通过使用这种粉末的压力模塑,树脂粘合剂在1MPa至100MPa的压力下彼此粘附,并且可以获得致密的颗粒。如果压力模塑中的压力小于1MPa,则树脂粘合剂难以彼此粘附。另一方面,如果压力超过100MPa,则该装置变大。
16、将 获得的颗粒进一步在惰性气体或还原气体的气氛中焙烧,以软化和流动多磷酸盐过渡金属氧化物。同时,树脂粘合剂被热分解。因此,电极混合物(焙烧后的颗粒)不含树脂,并且可以获得孔隙率在5%至50%范围内的多孔电极混合物。
只要温度可以在惰性气体或还原气体气氛下保持在400°C至2000°C的范围内5分钟或更长时间,烧制条件没有特别限制,但多磷酸盐过渡金属氧化物被软化并流动,并且使用树脂基粘合剂。从热分解的角度来看,温度优选在0.1°C/min至50°C/min的范围内升高,温度为400°C至2000°C,维护时间为5分钟或更长,10小时或更短。
17、为了在电极混合物中包括选自EC、PEC、PEG和PEO的材料,活性材料和这些材料可以混合并造粒,但使用多磷酸盐过渡金属氧化物的多晶玻璃。或者,在通过烧制玻璃来生产多磷酸盐过渡金属氧化物晶体的情况下,如果在预先包含EC、PEC、PEG和PEO的状态下烧制,则将其热分解,并将EC和PEC添加到混合物中,不能包含PEG、PEO。因此,在烧制多磷酸过渡金属氧化物的多晶玻璃或玻璃后,需要包含诸如EC、PEC、PEG和PEO的材料。
因此, EC、PEC、PEG、PEO等在煅烧后液化并应用于多磷酸盐过渡金属氧化物,通过浸渍酸过渡金属氧化物,电极混合物可以包含选自EC、PEC、PEG和PEO的材料。
18、对于EC、PEC、PEG、PEO等的液化,可以提高目标材料的温度,但优选添加有机溶剂以液化。有机溶剂没有特别限制,只要其能够溶解和液化目标材料即可。例如,可以提及链烃溶剂(DMC、DEC、EMC、二氯甲烷、醇型等)、环状烃溶剂(NMP、苯、内酯型等)等。优选通过减压或热处理去除有机溶剂。例如,可以采用用于干燥锂离子电池中使用的电极浆料的方法。
当电极混合物的厚度较大时,很难通过简单地施加液化的EC、PEC、PEG、PEO等来穿透 ,因此EC、PEC、PEG是烧制后的液化的多磷酸过渡金属氧化物。最好浸入PEO中。在这种状态下,通过进一步降低压力,可以在烧制后深入到多磷酸过渡金属氧化物中所含的孔隙中。减压环境的条件可以是低于大气压(负压)的压力。例如, 真空泵可用于创建表压为0 MPa至−0.1 MPa的负压环境。
19、本发明的全固态钠蓄电池优选具有电极混合物与具有导电性的集电体电接触的结构。集电体可以是具有通孔的金属或非穿透金属,但是通过使用非穿透金属来制造具有如图2所示的双极结构的全固态电池。双极电极可通过使由非穿透金属(例如金属箔或金属板)制成的集电体6与电极混合物2接触、 或在电极混合物上电镀或气相生长方法来制造 。它可以通过以下方法形成集电体6来获得:对于具有双极结构的全固态电池,可以用一个电池获得高电压。
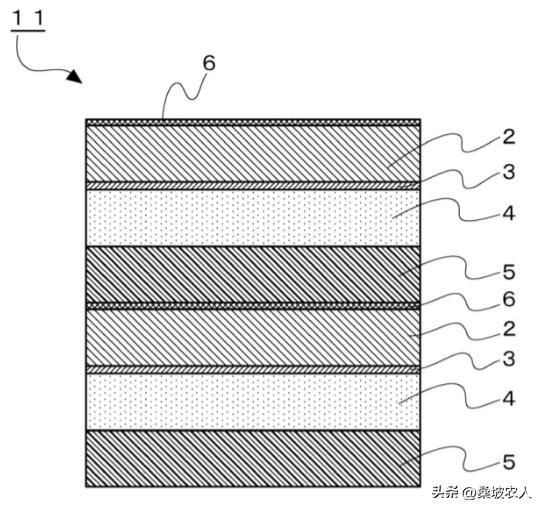
图2、双极性固态钠电池
20、另一方面, 当具有通孔的金属用作集电体时,集电体可以三维地填充电极混合物以从电极混合物收集电。结果,提高了电极混合物的电子传导性,并且可以获得具有优异输出特性的电池。此外,当通过烧制将包含活性材料前体的混合物制成电极混合物时,活性材料前体会导致大体积收缩,这会导致大的应力,但金属不会穿透电极混合物。通过填充,内聚应力被缓和,并且可以抑制电极混合物中裂纹的发生。 此外,当使用由于充电/放电而体积变化很大的活性材料时,电极混合物被抑制从集电体脱落,并且电池具有长的寿命。
这种集电体的材料没有特别限制,只要其具有电子导电性并且能够激励电极混合物中包含的活性材料即可。例如,可以提及金属、碳、导电陶瓷、导电玻璃等。具体地,可以使用诸如金、铝、碳、铜、钼、钛、铬、镍、钽、钨和铂的导电物质,以及包含这些导电物质中的两种或更多种的金属(例如,不锈钢、Al-Fe合金等)。其中,从获得材料廉价且输出特性优异的电池的观点出发, 优选铝或铝合金被碳涂覆的集电体 。更具体地,优选在金属表面上具有厚度为0.1μm至3μm的碳层的集电体。
实施例
<正极活性材料前体粉末的制备>通过熔融淬火方法制备正极活性材料前驱体。制备偏磷酸钠(NaPO3)、氧化铁(Fe2O3)和正磷酸(H3PO4)作为原料,使其组成为40Na2O-20Fe2O3-40P2O5(摩尔比),并在1350℃下在空气气氛中保持1小时。进行熔化。将获得的 熔融玻璃倒入一对冷却辊之间,并在淬火的同时模塑 。该玻璃体通过使用直径为20mm的ZrO2球石的球磨机粉碎10小时,并通过开口为120μm的树脂筛,获得平均粒径为7μm的粗玻璃粉末。此外,通过使用乙醇作为粉碎助剂并使用φ3mm ZrO2球磨机将该粗玻璃粉末粉碎80小时,以获得平均粒径为0.6μm的玻璃粉末(正极活性材料前体粉末)。得到作为粉末X射线衍射测量的结果,确认玻璃粉末是无定形的。
<正极活性材料粉末的制备>通过 在氮气气氛中在650°C下焙烧1小时使上述获得的玻璃体结晶,以获得晶体体 。该晶体通过使用直径为20mm的ZrO2球石的球磨机粉碎10小时,并通过开口为120μm的树脂筛,获得平均粒径为7μm的粗粉末。此外,通过使用乙醇作为粉碎助剂并使用直径为3mm的ZrO2球石的球磨机将该粗粉末粉碎12小时,以获得平均粒径为0.2μm的晶体粉末。该晶体粉末70重量%,作为碳源,以30重量%加入作为非离子表面活性剂的聚环氧乙烷壬基苯醚(质量平均分子量:660)。将其混合,然后在100℃下干燥1小时。然后,在氮气气氛中于620℃煅烧30分钟,以获得平均粒径为0.2μm的正极活性材料粉末。作为粉末X射线衍射测量的结果,确认正极活性材料粉末是源自Na2FeP2O7晶体的衍射线。
<电极混合物的制备(活性材料层)>通过将 涂有聚丙烯碳酸酯(PPC)的混合物粉末在氩气环境中成型到粉末模压模具 (NPA System Co.,Ltd.)中(Φ10 mm)来制备电极混合物(活性物质层),然后将通过施加30MPa的压力而成型的颗粒置于氮气(N2)/氢气(H2)混合气体(=96/4 vol.%)气氛中,温度为550°C,1h,3°C/min。在上述条件下烧制,然后 通过物理气相生长法(PVD)在颗粒的一侧形成300nm厚的金膜作为集电体 。通过烧制步骤,电极混合物中包含的所有PPC被热分解并变为二氧化碳气体,使得获得的电极混合物具有通过减去PPC获得的重量。
焙烧后的电极混合物的厚度为298μm,总重量为0.0307g,直径为9.242mm,电极混合物中所含活性材料的重量为0.02794g,确认了正极活性物质颗粒形成了其中多个正极活性物质粒子连接的簇,并且具有包括孔的多孔结构。该簇是通过使正极活性材料前体粉末软化和流动,并在烧制混合物粉末时将正极活性材料粉末彼此结合而形成的。确认正极活性材料前体粉末软化并流动并结晶,以沉淀Na2FeP2O7晶体。
<无机固体电解质的制备> 按原样使用组成式为Na1.6Li0.34Al0.66O17的Li2O稳定的β〃-氧化铝(由Ionotec制造)。无机固体电解质的厚度为1mm。
<有机固体电解质的制备>对于有机固体电解质,将重均分子量(Mw)为7000的聚乙二醇(PEG)和*腈乙**添加到NaPF6(1:0.3重量)中,并使用自旋转混合器(Sinky,Neritaro),2000rpm,1h)。
<制造全固态钠蓄电池> 在氩气环境中,在电极混合物和如上所述制备的无机固体电解质之间。通过以0.005g/cm2插入制备的有机固体电解质并使用金属钠作为对电极来制备。通过 用刷子将溶解在*腈乙**中的有机固体电解质涂覆到电极混合物中,然后真空干燥(60℃,1小时) ,插入有机固体电解质。
<电池过充电试验>在电池过充电测试中,在60°C、0.01C速率和4.5V充电截止电压的条件下进行恒流充电。比较实施例3和比较例2的充电曲线,如图所示。纵轴显示电池电压,横轴显示充电时间。充电超过100小时是过度充电区域。从图3可知,在实施例3的电池中,在4.2V附近确认了充电平台,未达到4.5V的充电截止电压。另一方面,在比较例2的电池中,没有确认4.2V附近的充电平台,并且电池被充电到充电截止电压。在实施例3的电池中,认为 介于电极混合物和无机固体电解质之间的有机固体电解质在约4.2V下被氧化分解。从该结果可知,通过在电池中具有有机固体电解质,可以抑制过充电 (参见表2)。
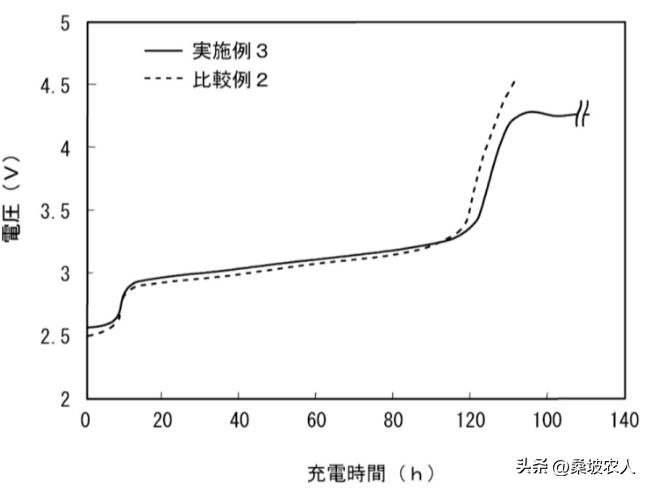
图3、充电曲线
此外,在60℃、0.01C速率、4.5V的充电截止电压和0.1C速率的条件下,用恒定电流恒定电压对实施例3的电池充电,直到SOC(充电状态)达到200%。当恒定电流放电直到电压达到2.0V时,未显示放电容量。很可能是由于有机固体电解质的氧化分解,电池电阻增加,电池关闭。
根据本发明的全固态钠蓄电池在室温环境中保持高放电容量的同时表现出优异的充电/放电循环特性,并且可以通过过度充电而关闭。因此,它有望应用于EV(电动汽车)和固定电源。