2019年全球上市新药荟萃
田田 Drugfocus药研视界 今天
2019年,全球共批准新分子实体(NME)和新生物药54个,其中NME有26个,生物药28个。按治疗领域分,抗肿瘤药依然是新药的重头戏,今年共批准13个新药,包括4个单抗类抗癌药和5个替尼类的靶向小分子药物,极大地丰富了肿瘤患者的临床选择。风湿免疫系统用药9个,包括用于治疗银屑病的新药3个,用于类风湿性关节炎的新药2个。血液系统用药各6个,神经系统用药、感染类和消化系统用药各4个。按上市国家来分,美国首次上市品种最多,有28个,日本次之,11个,中国第三,为5个。充分说明中国药企近年来明显加快了新药开发的进度,紧跟全球医药创新的脚步,并取得显著成效。
近年来,全球大多数国家通过授予在研或申报的新药特殊资格来加快新药上市时间,享有上市后市场独占权,以鼓励新药、孤儿药、儿科用药等的开发上市。2019年按特殊资格认定来分,突破性疗法品种有11个,大多同时给予优先审评/加速审批/快速通道资格,包括抗肿瘤药Entrectinib、Erdafitinib、polatuzumab vedotin、quizartinib dihydrochloride、tagraxofusp、zanubrutinib,风湿免疫用药upadacitinib,血液病用药emapalumab,产后抑郁用药brexanolone,神经系统用药onasemnogene abeparvovec,罕见病用药voxelotor。优先审评30个,快速通道13个,加速审批7个,孤儿药25个,儿科研究计划12个。
具体情况见下表。
2019年全球首次上市的新药
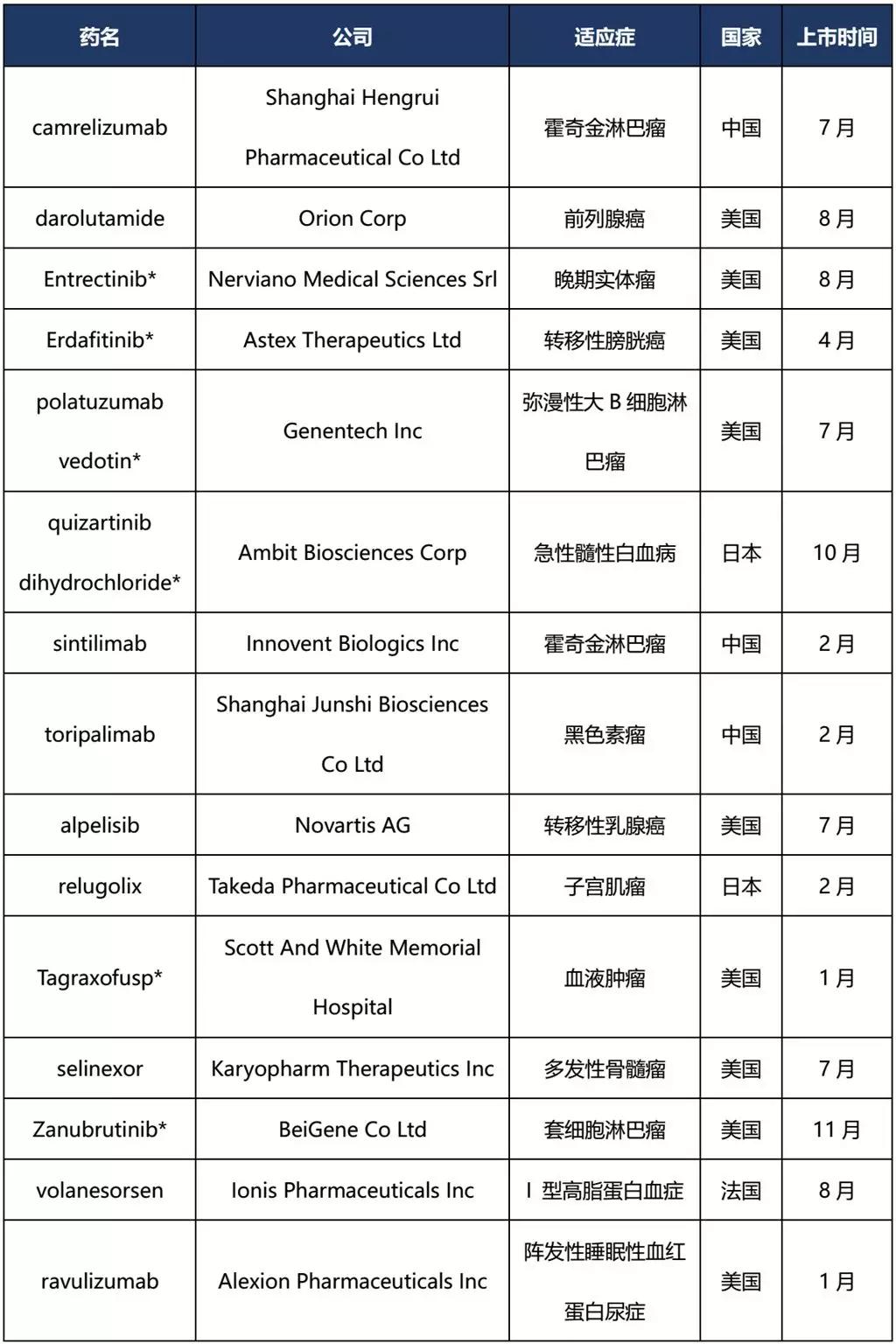
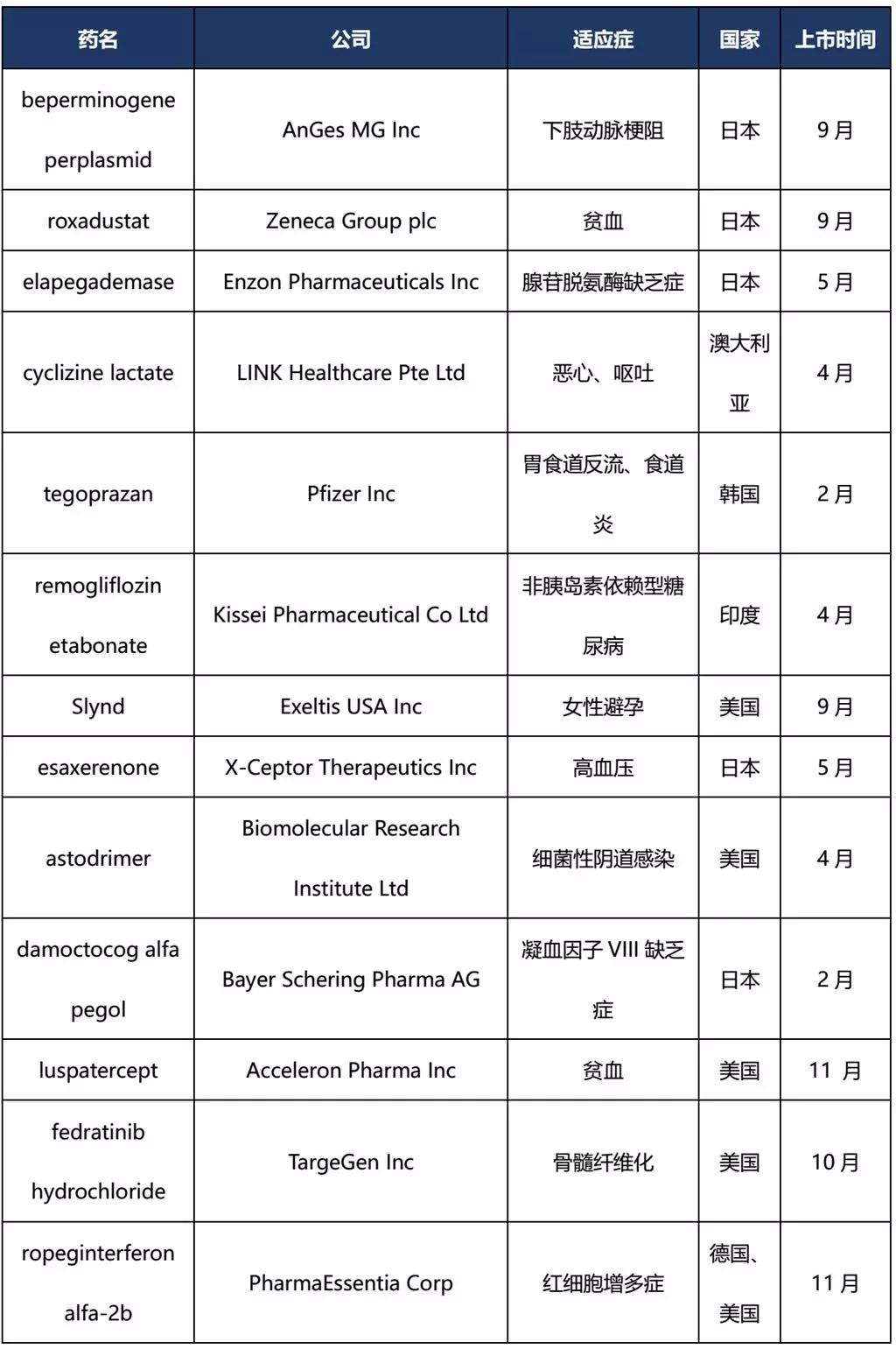
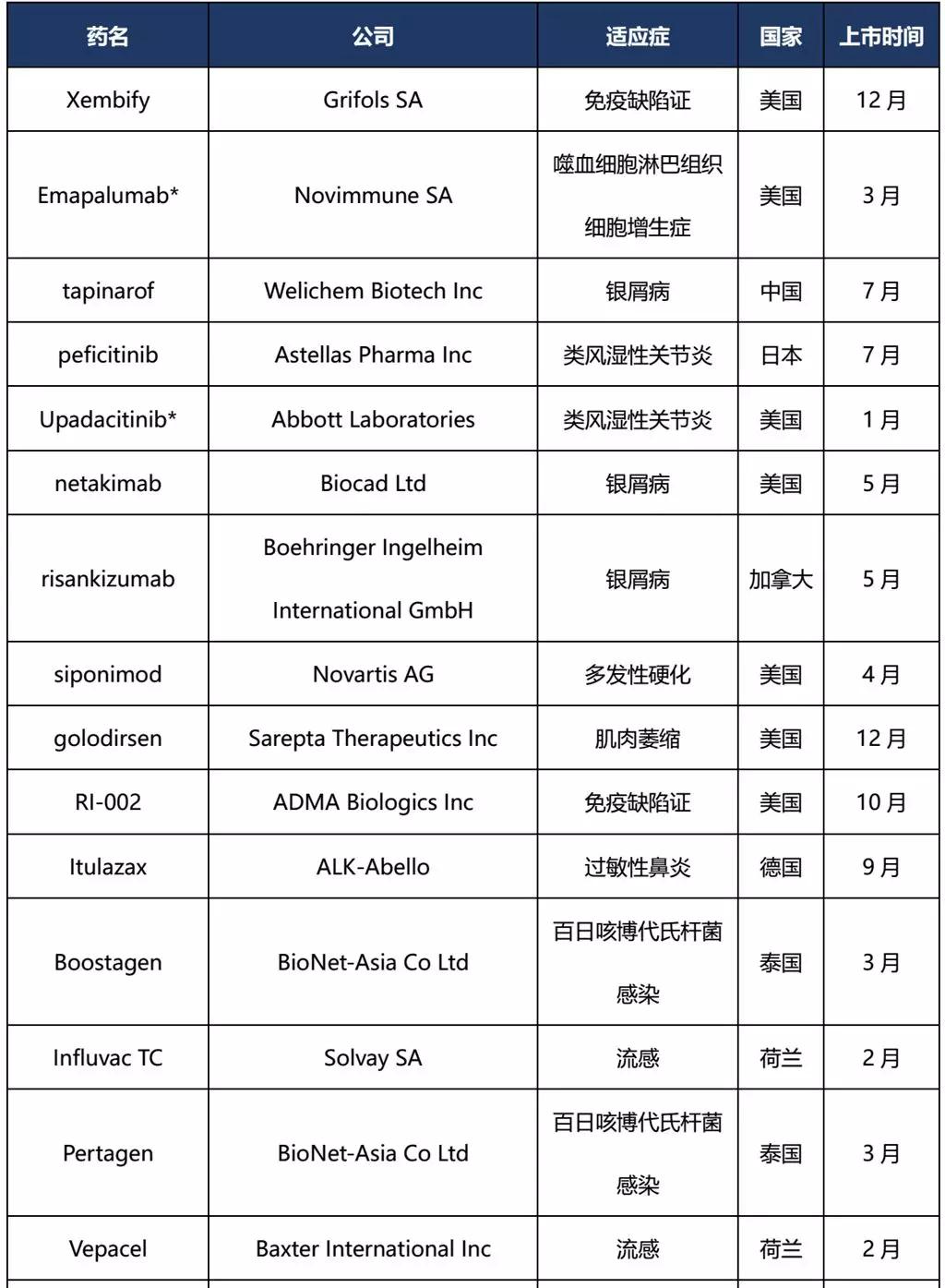
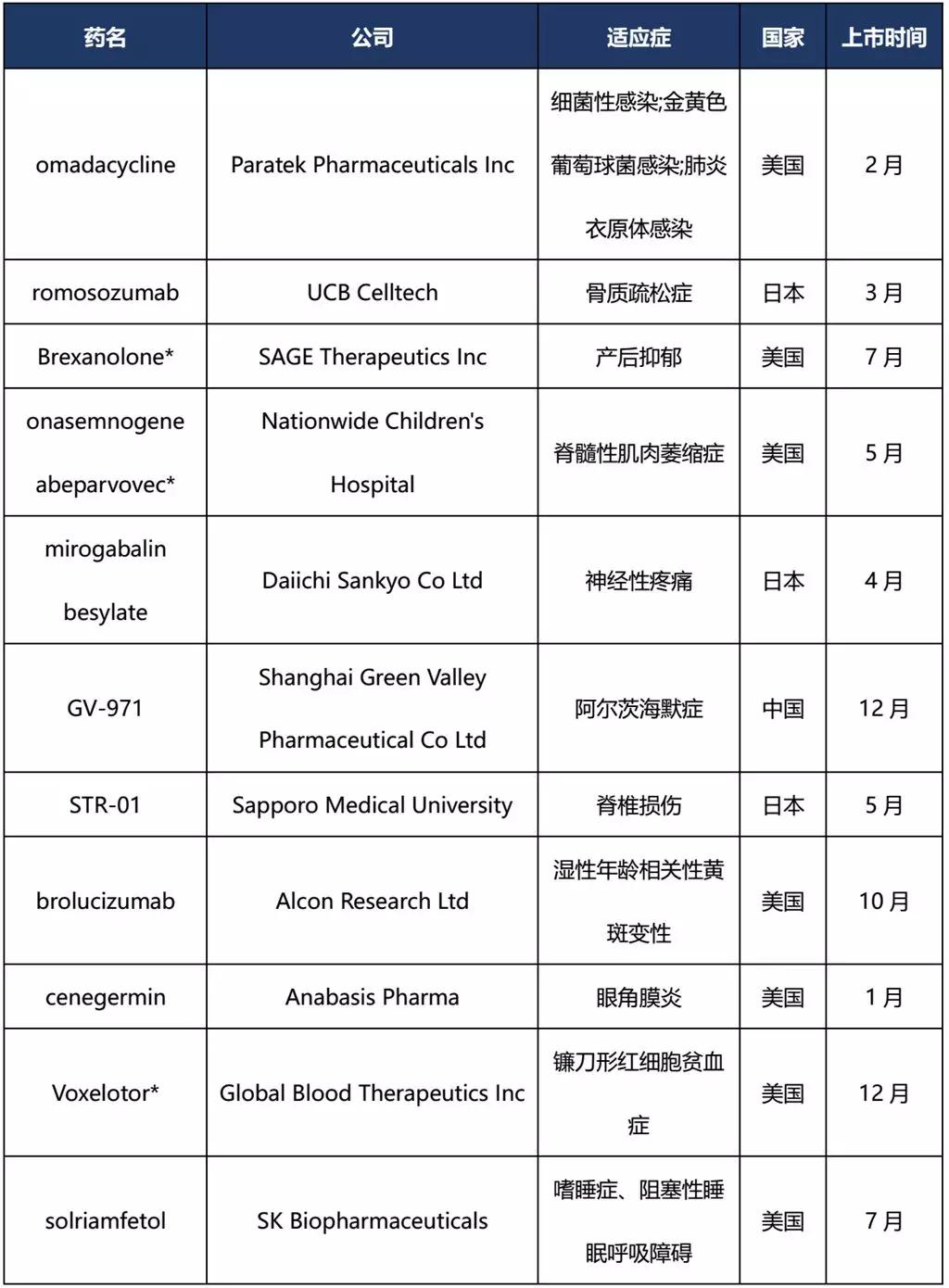
注:*品种为授予突破性疗法品种;数据来源:cortellis数据库
精彩纷呈
抗肿瘤药依然是领域老大,新药层出不断
广谱抗癌药Rozlytrek
8月15日,在美国获批上市。Rozlytrek(entrectinib)通过FDA的优先审查获得批准上市,用于治疗携带神经营养性酪氨酸受体激酶(NTRK)基因融合的成年和青少年癌症患者。这是FDA继Keytruda和Vitrakvi之后批准的第三款“不限癌种”的抗癌疗法,为不区分肿瘤来源广谱抗癌药物快速发展奠定了更坚实的基础。同时FDA批准Rozlytrek治疗携带ROS1基因突变的非小细胞肺癌患者(NSCLC)。据悉,Rozlytrek已于今年6月在日本首先获得批准上市,用于治疗神经营养性酪氨酸受体激酶融合阳性晚期复发性实体瘤成人及儿科患者。
Rozlytrek是一种新型“广谱”抗癌药,是日本批准靶向NTRK基因融合的首个肿瘤不可知论(tumor-agnostic,即与肿瘤类型无关)药物。NTRK基因融合已经在一系列难以治疗的实体瘤类型中得到了鉴定,包括胰腺癌、甲状腺癌、唾液腺癌、乳腺癌、结直肠癌和肺癌。
Rozlytrek已分别获美国、欧盟、日本授予突破*药性**物资格(BTD)、优先药物资格(PRIME)、SAKIGAKE资格(创新药物)和孤儿药资格。
首个获批治疗BPDCN的药物Elzonris
Tagraxofusp-erzs由Texas A&M University研发,之后Stemline Therapeutics公司获得了开发和商业化授权。于2018年12月21日获FDA批准上市,商品名为Elzonris®,用于治疗急性浆细胞样树突状细胞瘤(BPDCN)的成人及2岁以上的儿童患者。该药成为首个获批治疗BPDCN的药物,同时也是首个获批的CD123靶向药物。该药分别获得FDA(2011年)、EMA(2016年)用于治疗急性髓系白血病的孤儿药资格。
急性浆细胞样树突状细胞瘤(BPDCN)是一种侵袭性极强的罕见骨髓和血液系统恶性肿瘤,预后不良。它通常以皮肤病为首发症状,可同时涉及骨髓、淋巴结、其他软组织及中枢神经系统等。这一疾病在男性中更为常见,尤其在60岁以上人群中发病率更高。
Elzonris®是一种靶向CD123的细胞毒素,是由白介素-3和白喉毒素部分片段形成的重组融合蛋白,是静脉注射溶液。每次注射之前要预注射H1组胺拮抗剂(对乙酰氨基酚、皮质类固醇)和H2组胺拮抗剂。推荐用药为每天按体重12 μg/kg,15分钟内给药。连续注射5天,间隔视情况而定,21天为一个治疗周期。第一个治疗周期需要在住院期间进行,之后的用药周期可以在院内外进行。
全新靶点多发性骨髓瘤新药XPOVIO(selinexor)
7月3日,Xpovio获得美国FDA批准,联合地塞米松用于既往已接受至少4种疗法且其疾病对至少2种蛋白酶体*制剂抑**(PI)、至少2种免疫*制剂抑**(IMiD)、一种抗CD38单克隆抗体难治的复发难治性多发性骨髓瘤(RRMM)成人患者。Xpovio是一种核输出*制剂抑**,靶向核输出蛋白XPO1。值得一提的是,该药是首个也是唯一一个获FDA批准的核输出*制剂抑**,同时是首个也是唯一一个获FDA批准用于对蛋白酶体*制剂抑**、免疫调节剂和抗CD38单抗均难治的多发性骨髓瘤(MM)患者的处方药。此外,Xpovio也是自2015年以来首次针对骨髓瘤新靶点(XPO1)的批准药物。这款药物由德琪医药与合作伙伴Karyopharm Therapeutics合作开发,预计将于7月10日或之前在美国上市。
目前,该药也正在接受欧洲药品管理局(EMA)的加速审查。在美国和欧盟,Xpovio均被授予了孤儿药资格,在美国还被授予了快速通道资格。2019年1月28日Xpovio获得中国国家药品监督管理局临床批件,即将在今年8月启动临床试验。
前列腺癌(nmCRPC)新药Nubeqa(darolutamide)
7月30日,德国制药巨头拜耳(Bayer)抗癌新药Nubeqa(darolutamide)在美国获批上市,其用于治疗非转移性去势抵抗性前列腺癌(nmCRPC),该药将为临床医生在治疗nmCRPC患者时提供一种可显著延长无转移生存期的新治疗选择。Nubeqa是一种口服非甾体雄激素受体(AR)*制剂抑**,于7月底获FDA批准,用于肿瘤尚未扩散到身体其他部位且对降低睾酮水平的内科或外科治疗不再应答的前列腺癌患者。Nubeqa具有独特的化学结构,以高亲和力结合受体,表现出强烈的拮抗活性,从而抑制受体功能和前列腺癌细胞的生长。与其他现有的nmCRPC治疗方法不同,Nubeqa不跨越血脑屏障,因此潜在的药物相互作用以及中枢神经副作用(如癫痫、跌倒和认知障碍)更少。Nubeqa由拜耳与芬兰制药公司Orion合作开发。
风湿免疫类“重磅*弹炸**”药或将诞生
艾伯维JAK1*制剂抑**Rinvoq
8月16日,艾伯维备受业界关注的JAK1*制剂抑**类抗炎新药Rinvoq(upadacitinib)获得美国FDA批准,用于对甲氨蝶呤应答不足或不耐受(MTX-IR)的中度至重度活动性类风湿性关节炎(RA)成人患者的治疗。Rinvoq通过口服给药,推荐剂量为每日一次15mg,可作为单药疗法,也可与MTX或其他非生物类疾病修饰抗风湿药物(DMARD)联合用药,该药不适用于未接受过MTX治疗的患者。
日前,艾伯维公布了Rinvoq定价,年治疗费用为5.9万美元,与竞品修美乐(Humira)价格接近,后者需要定期注射,年治疗费用为6万美元。临床数据显示,Rinvoq在治疗中重度RA方面比Humira更有效。
III期临床项目SELECT是在RA领域开展的最大规模的注册III期项目之一,共有约4400例患者在5项研究中接受了治疗。项目评估了Rinvoq治疗各种类型RA患者的疗效、安全性和耐受性,包括生物类疾病修饰抗风湿药物(包括TNF*制剂抑**,如Humira)治疗失败或不耐受的患者、未接受过MTX治疗或对MTX治疗应答不足的患者。在5项研究中,Rinvoq均达到了主要终点和次要终点。
根据科睿唯安最近的一项分析,Rinvoq在2023年的销售额预计将超20亿美元。
银屑病新药netakimab(BCD-085,商品名 Efleira®)
该产品为重组人源抗白介素-17(IL-17)单克隆抗体。IL-17是一种炎症相关的细胞因子,当其功能异常时会导致自身免疫、炎症性疾病的发生。目前全球已有两个IL-17A抗体上市,分别为诺华的Cosentyx®(Secukinumab)(2018 年全球销售收入为28.37亿美元)和礼来的Taltz® (Ixekizumab)(2018年全球销售收入为 9.38亿美元)。BCD-085于2019年4月在俄罗斯上市,5月在美国上市,获批适应症为重度斑块性银屑病。第二个适应症强直性脊柱炎有望在2020年初获批。
罕见病用药持续发力
镰状细胞贫血症新药Oxbryta
11月25日,美国FDA加快批准Global Blood Therapeutics公司的Oxbryta(voxelotor)上市,用于治疗成人和12岁以上青少年患者的镰状细胞贫血症(SCD)。这也是首款美国FDA批准的靶向血红蛋白聚合过程的创新疗法,该疗法此前已获得美国FDA授予的突破性疗法认定、孤儿药资格、快速通道资格和罕见儿科疾病认定(rare pediatric disease designations)。
Voxelotor是一款每日口服一次的SCD创新疗法,通过增加血红蛋白对氧的亲和力达到疗效。由于氧合镰状血红蛋白不会聚合,voxelotor可防止红细胞发生镰状改变以及血红细胞的损毁。Voxelotor有着恢复正常血红蛋白功能和改善氧气输送的潜力。试验结果表明,接受剂量为1500 mg的voxelotor患者组中59.5%的患者血红蛋白水平提高超过1 g/dL,安慰剂组这一数值为9.2%。以往研究表明,血红蛋白水平降低与负面临床后果相关,而将血红蛋白水平提高1 g/dL可能显著降低SCD患者临床并发症和死亡率。
Oxbryta的常见副作用包括头痛、腹泻、腹痛、恶心、疲劳、皮疹和发热。
其它罕见病用药还有用于噬血细胞淋巴组织细胞增生症的emapalumab、弥漫性大B细胞淋巴瘤药polatuzumab vedotin、红细胞增多症用药ropeginterferon alfa-2b、阵发性睡眠性血红蛋白尿症用药ravulizumab、多发性骨髓瘤药selinexor、腺苷脱氨酶缺乏症新药elapegademase、肌肉萎缩新药golodirsen等。
中国创新药开发潜力巨大
2019年由中国药企开发上市的创新药共计5个,包括用于阿尔茨海默病的GV-971,两款用于治疗霍奇淋巴瘤新药分别为上海恒瑞的camrelizumab和信达与礼来联合开发的PD-1新药sintilimab,黑色素瘤新药toripalimab,用于治疗银屑病的新药tapinarof。由此可以看出,中国的新药创新能力越来越强,已经在全球热门的PD-1单抗方面有了长足的进步,在近几十年来全球都难以突破的阿尔茨海默病的治疗方面更是领先全球。
首个在中国上市的中国自主研发的PD-1单抗toripalimab
该药于2018年12月17日获得NMPA(原CFDA)有条件批准上市,用于治疗既往接受全身系统治疗失败后的不可切除或转移性黑色素瘤患者,商品名为拓益®。2019年2月正式上市销售。该药最初由上海君实生物医药科技股份有限公司和苏州众合生物医药科技有限公司(君实生物子公司)开发,是首个在中国上市的中国自主研发的PD-1单抗。toripalimab此次批准是基于已完成的中国晚期黑色素瘤II期研究的有效性数据和7项临床研究的安全性数据。针对晚期黑色素瘤在中国的临床II期研究(NCT03013101),截至2017年9月15日,共招募128名受试者(51名肢端、21名黏膜、18名慢性太阳损伤(CSD)和38名非CSD或来源不明)。截至2018年1月4日,审查委员会对121名可评估的受试者进行了临床试验,观察1例CR、24例PR和48例SD的结果得出ORR为20.7%、DCR为60.3%。这与慢性太阳损伤CSD(35.3%)和非CSD(33.3%)相比,口腔(14.3%)和黏膜(0%)亚型的ORR较低。在肢端(53.1%)和黏膜(42.1%)的黑素瘤受试者中获得显著的DCR。由于大多数响应(23/25)仍在进行中,中位响应时间尚未获得。该研究中没有因治疗引起的死亡。与治疗相关的AEs为1/2级,在18%的受试者中与治疗相关的AEs为3/4级。toripalimab的临床试验结果显示:治疗既往接受全身系统治疗失败的不可切除或转移性黑色素瘤患者的客观缓解率达17.3%,疾病控制率达57.5%,1年生存率达69.3%。
第二个获批上市的国产PD-1抗体Sintilimab(信迪利单抗,IBI308)
该药是一种全人源IgG4单抗,靶向结合PD-1,该药是由信达生物和礼来联合在中国开发,2019年2月在中国上市销售。2018年4月,NMPA受理sintilimab治疗复发性或难治性经典霍奇金淋巴瘤(R/R cHL)NDA,并授予优先审查。II期注册研究ORIENT-1(NCT03114683)对96例患者最小随访24周,总缓解率79.2%、疾病控制率97.9%。目前,sintilimab正在III期研究ORIENT-11(NCT03607539)评估一线治疗非鳞状非小细胞肺癌(nsq-NSCLC)、III期研究ORIENT-12(NCT03629925)评估一线治疗鳞状非小细胞肺癌(sq-NSCLC)。2018年12月27日sintilimab获NMPA批准,成为第二个获批上市的国产PD-1抗体。
治疗阿尔茨海默病新药九期一®(甘露特钠,代号:GV-971)
11月2日,国家药品监督管理局批准了上海绿谷制药有限公司治疗阿尔茨海默病新药——九期一®(甘露特钠,代号:GV-971)的上市申请,用于治疗轻度至中度阿尔茨海默病,改善患者认知功能。九期一®通过优先审评审批程序在中国大陆的上市为全球首次上市,填补了这一领域17年无新药上市的空白。这款中国原创、国际首个靶向脑-肠轴的阿尔茨海默病治疗新药,将为广大阿尔茨海默病患者提供新的治疗方案。
自发现阿尔茨海默病100多年来,全球用于临床治疗的药物只有5款。全球各大制药公司在过去的20多年里,相继投入数千亿美元研发新的阿尔茨海默病治疗药物,320余个进入临床研究的药物已宣告失败。
九期一®是由中国科学院上海药物研究所耿美玉研究员领导研究团队,坚持22年,在中国海洋大学、中国科学院上海药物研究所与上海绿谷制药有限公司接续努力研发成功的原创新药。临床前作用机制表明,九期一®通过重塑肠道菌群平衡,抑制肠道菌群特定代谢产物的异常增多,减少外周及中枢炎症,降低β淀粉样蛋白沉积和Tau蛋白过度磷酸化,从而改善认知功能障碍。靶向脑-肠轴的这一独特作用机制,为深度理解九期一®临床疗效提供了重要科学依据。
九期一®的研发得到了国家“863计划”、国家自然科学基金、国家“973计划”、“重大新药创制”国家科技重大专项、中国科学院战略性先导科技专项(A类)、上海市科技计划等项目的资助。
编辑:绰绰
