
01
要点概括
1.神经元体外活细胞成像已成为了解大脑发育和功能的关键方法。神经元发育的动态过程,如神经突起和生长锥的形成,以及细胞内细胞器的运输,在创建信息传输所需的复杂3D神经网络方面起着至关重要的作用。
2.大多数研究使用基于荧光的成像,这会产生大量的光毒性,限制成像频率或实验持续时间,并且会对神经突等脆弱结构造成实质性损害,从而在实验中引入伪影,导致数据不准确。
3. Nanolive实现了神经元活细胞无标记成像,由于在极低功率下使用相干光干涉,因此不会产生光毒性,从而可以在不干扰细胞活动、形态或行为的情况下研究活体神经元中的复杂动态过程。
02
Nanolive在神经元研究方面的应用
Nanolive活细胞成像在神经生物学方面的潜力巨大,下面列举三个案例。
案例1研究显示了未分化初级皮质神经元暴露于神经轴突刺激介质后发生的形态学变化的时间线。高精度分割法用于计算感兴趣的细胞指标(例如体积、形状和干重)。这些计算与在单个神经元中观察到的行为直接相关。
案例2和案例3研究集中于干细胞在神经分化过程中经历的亚细胞形态变化。这在单细胞(案例2)和群体水平(案例3)上都得到了检验。我们希望本应用描述将有助于激励研究人员利用纳米活细胞成像技术彻底改变他们的研究。
案例一:原代皮层神经元轴突生长动力学的定量研究
背景:
在发育过程中,神经元建立细胞间通讯所需的过程(神经突)需要经历复杂的形态变化,包括生长锥的形成、轴突的规格变化和分支。神经元形态的细微异常与几种神经退行性疾病的发生有关;将异常神经元的从充满异质*行为性**的正常的神经元中区分开来需要对轴突生长动力学有详细的了解。在这个案例研究中,我们展示了Nanolive活细胞成像为监测神经元发育提供了一个完美的解决方案。
试验方法:
Step1:未受刺激的*皮人**质神经元细胞(hCN2,ATCC,USA)在DMEM培养基+10% FBS中单层生长,青霉素(20单位/毫升)和链霉素(20毫克/毫升)。温度(37°C)和气体(5%CO2)为保持不变。对未受刺激的细胞进行成像。
Step2: 添加神经轴突刺激培养基(25 ng/mlβ神经生长因子、0.5 mM dbcAMP和0.5 mM IBMX),并在添加培养基后20 h、3 d、9 d和20 d对细胞进行再次成像。使用Nanolive的3D Cell Explorer,以6s/张频率采集图像。
Step3: 使用内部开发的工具对生成的图像进行最大强度z投影、分割(细胞体显示为绿色,神经突显示为橙色,分开)和量化。
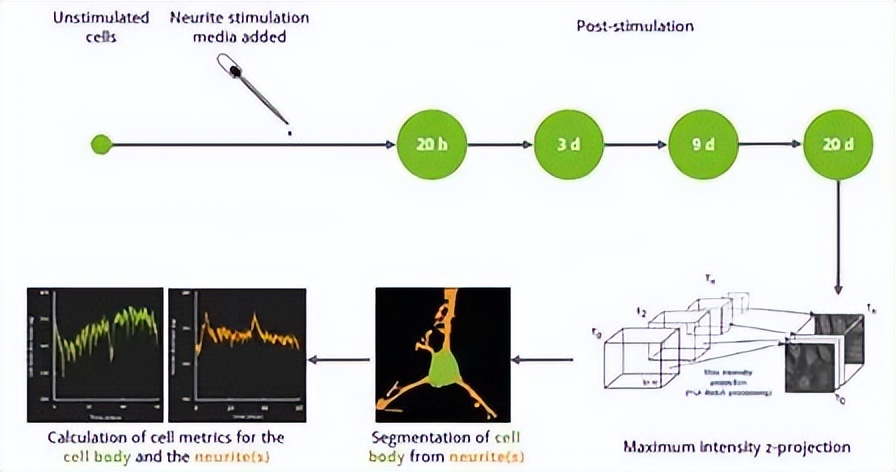
试验结果:
1.未受刺激的初级皮质神经元暴露于神经轴突刺激介质后的形态学变化的时间表
在下图中,显示了每个实验时间点的一帧(顶行),以及它的相应的分割图像(底行),其中细胞体显示为绿色,神经突起显示为橙色。
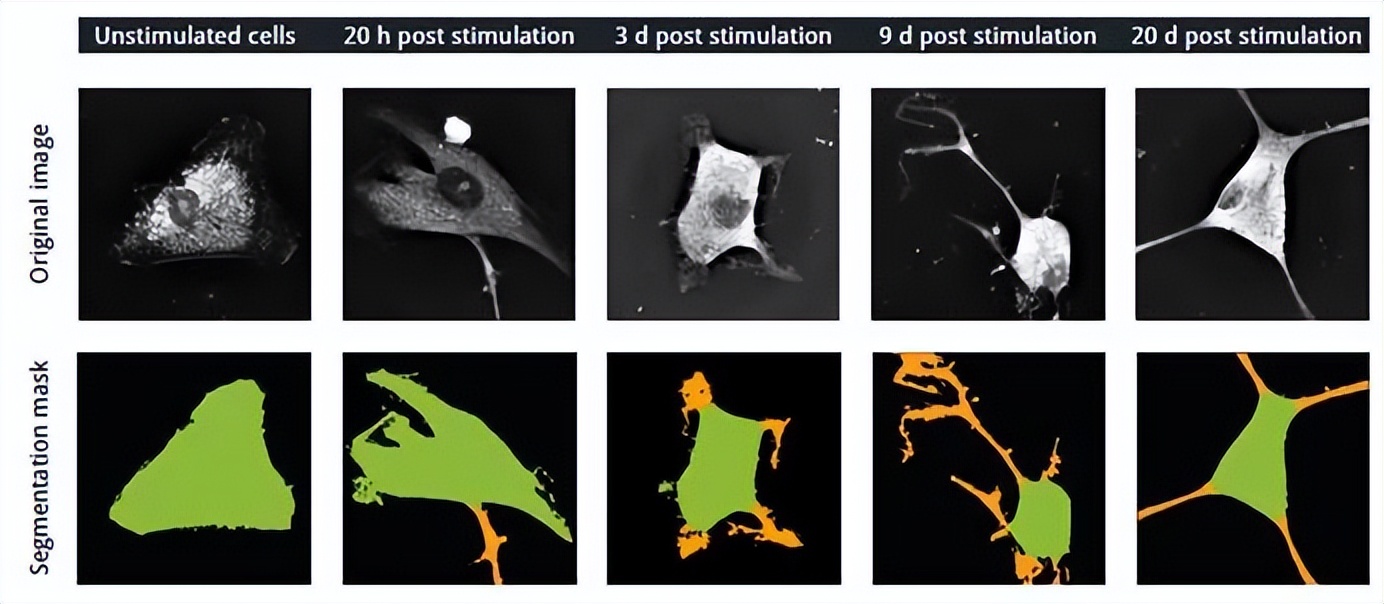
a.未受刺激的细胞具有典型的未分化形态;平的,三角形的,并且很好地分布在培养皿的表面。明亮的圆形小泡充满细胞质,含有神经元物质。
b.刺激后20h,细胞仍然散布在培养皿表面,但已形成第一个神经轴突(分割图像中为橙色)。
c.刺激后3d,细胞已形成高级生长锥,具有复杂的分枝形态。
d.刺激后9d,细胞开始呈现典型的神经元形态;细胞体已经收缩,五个神经突起已经形成。
e.在刺激后20d,细胞出现了多极生理学,有四个清晰、细长的神经突起。
*分割模型的高精度;没有遗漏任何细节。精细的突起、棘突和静脉曲张都被高精度捕获,证实了Nanolive活体成像可以用来监测神经元的精细形态变化。
2.以高精度可视化和量化动态行为的精细尺度
在本例中,我们量化了添加刺激介质20h后生长的初级神经轴突的动态行为
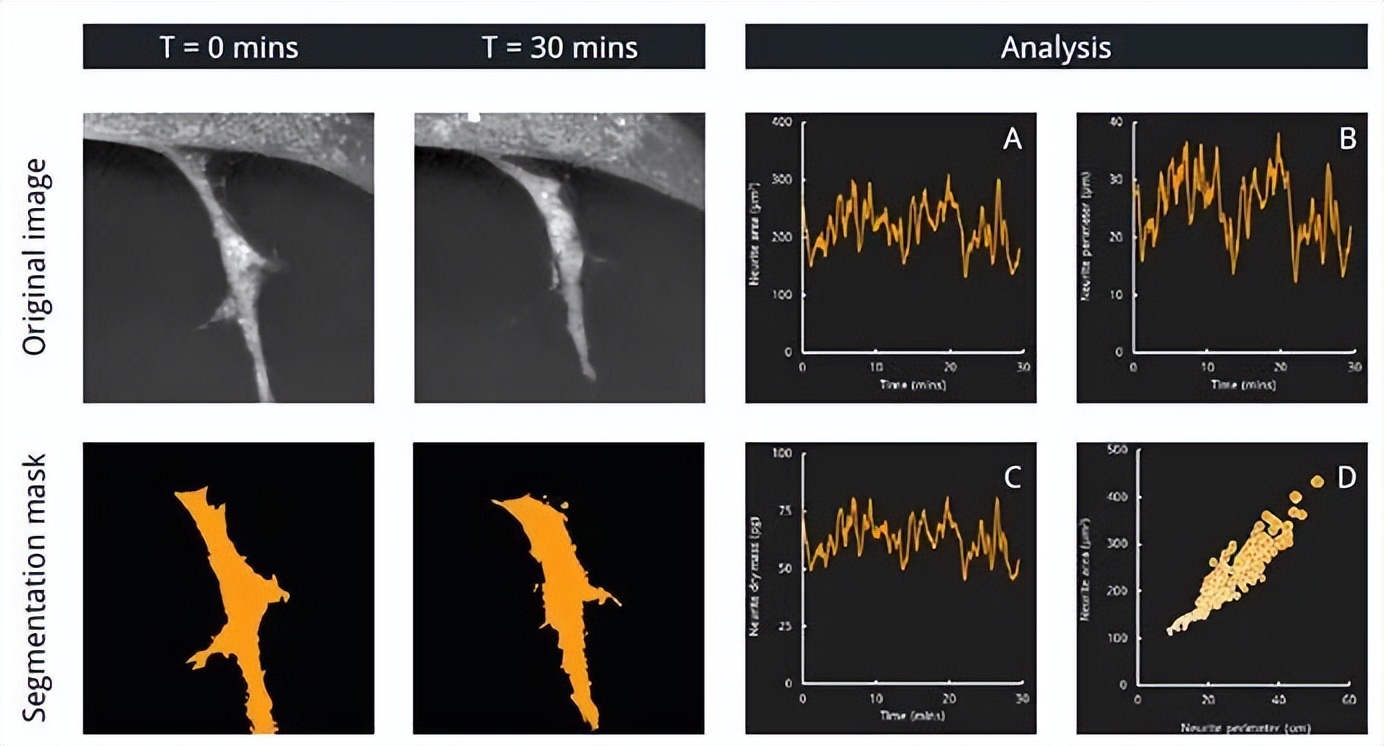
a.Nanolive活体成像的高分辨率和高精度检测神经轴突体积和形状的变化。神经轴突面积(A)、周长(B)和干质量(C)的大幅波动反映了这些变化的速度和动态性。
b.气泡图(例如,气泡大小代表干质量的D)可用于调查三个变量A、B和C之间的关系。
3.调查新行为观察的潜在原因
两个细胞在加入神经轴突刺激培养基后3d成像。高时间分辨率Nanolive活体成像技术的发展使我们能够捕捉到一种新的细胞脉冲行为。这里,我们检查一个脉冲单元中的单元度量。
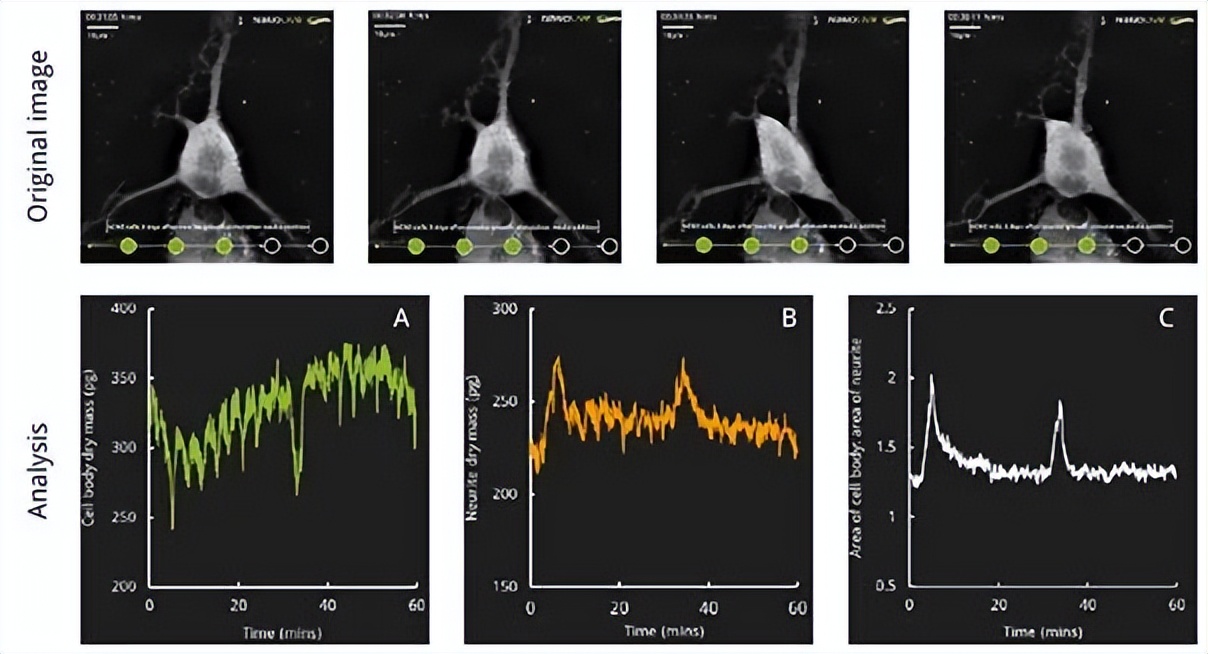
a.据我们所知,这是首次在初级皮质神经元中观察到脉冲。这一现象在视频中更为清晰,但即使在上面的静止图像中,随着细胞收缩,细胞体的形状也发生了明显的变化。
b.细胞指标准确反映视频中捕获的行为。例如,细胞体在膨胀时积累干物质,然后在收缩时干物质急剧减少,然后趋于稳定(A),而在神经突起的干物质中观察到相反模式(B)。
c.细胞体与神经突面积之比的峰值(C)表明,这可能是细胞注射物质(从而生长)其神经突的方式,尽管这一假设需要通过额外的实验加以证实。
d.未来可能在更长的时间内监测神经元,以确定这些脉冲事件是否是周期性的,并计算收缩之间经过的时间。
4.检查神经突的形态可塑性,确定细胞物质在神经突之间的分布
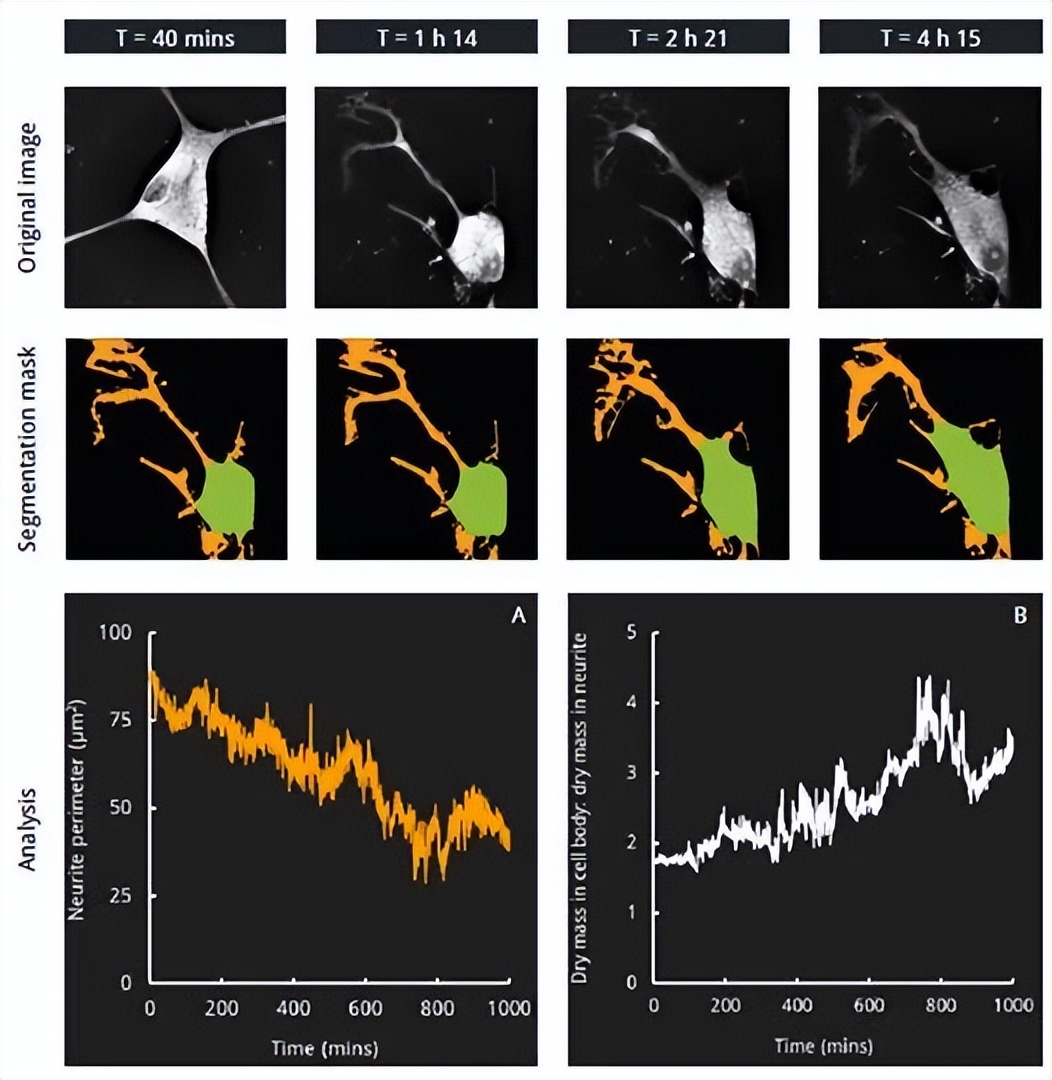
a.我们像以前一样对生长锥进行了分割,但这次我们进一步进行了分析,为每个神经突添加了一个唯一的对象标识符,并跟踪干质量随时间的变化。
b.右侧的图表显示,某些神经轴突的干质量波动比其他神经轴突大,波动的幅度不一定与神经轴突的大小有关。
c.这种类型的分析可用于研究神经轴突随时间变化的形态可塑性,并确定a)细胞材料在神经轴突之间的分布情况以及b)哪些神经轴突正在生长/收缩。
5.量化形状随时间的复杂变化
在视频中,在添加神经轴突刺激9d后成像的细胞在形状上经历了复杂的变化。这里展示了准确量化这些变化的可能性。
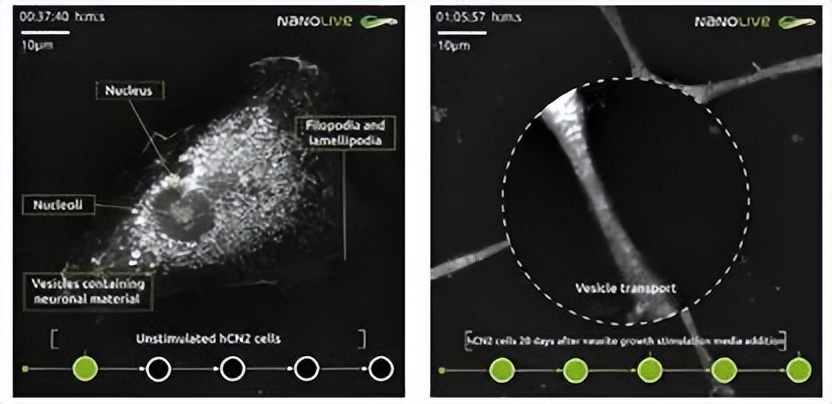
a.从未受刺激的细胞(左)到神经突刺激后20d(右),细胞细胞质中存在小泡(含有神经元物质)。
b.未来会量化神经元内或神经元之间细胞内转运的内容或动力学。
结论
1.本案例研究中所做的许多观察都是新的,Nanolive提供了一种非侵入性、无标签的选择,用于脆弱的细胞如神经元的研究。
2.这些观察结果为研究开辟了新方向,本案例的研究展示了大量有待开发的定量信息。
案例二:单细胞水平上的干细胞向神经定向分化
背景
Nanolive的显微镜为科学家提供了实时监测干细胞分化过程中发生的亚细胞形态变化的机会。该案例分析了间充质干细胞(MSC)在神经源性分化培养基中发生的形态学变化。
试验方法
Step1:人脐带基质间充质干细胞在完全神经源性分化培养基中培养13d后分化。
Step2:使用3D Cell Explorer对细胞成像20h,采集频率为30s/张。
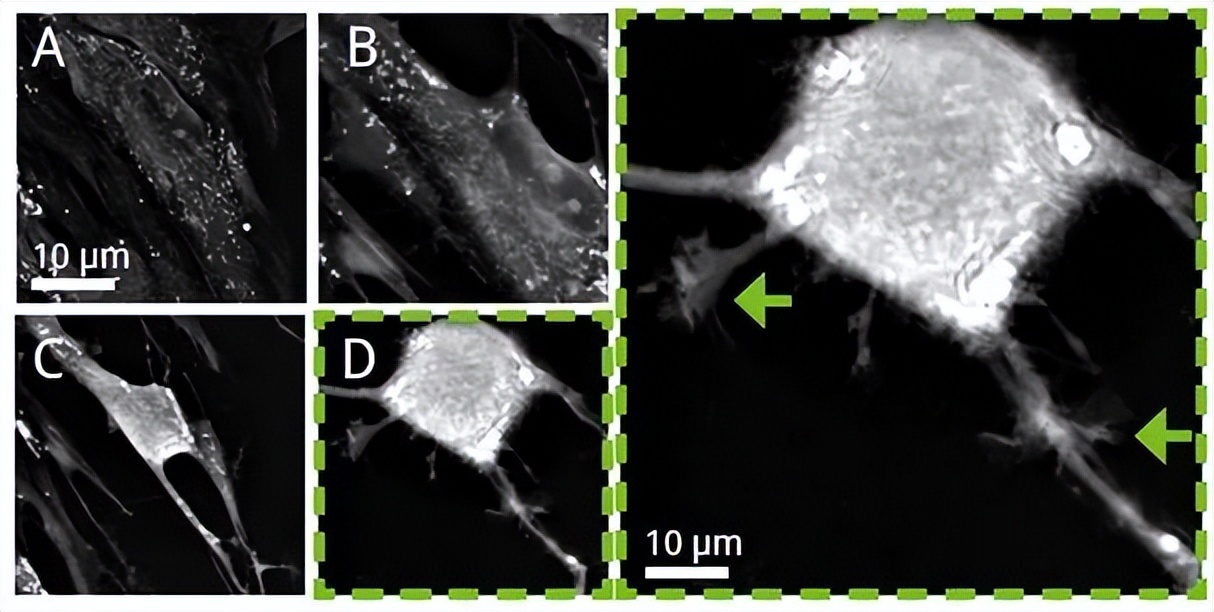
观察内容
1.这是第一次实时拍摄活干细胞分化过程中的画面。
2.Nanolive提供了细胞发生形态变化的高分辨率亚细胞图像:
A.细胞具有正常、健康MSC的形态;细胞质延长,细胞核可见
B.肌动蛋白细胞质开始收缩(折射率的增加使细胞看起来更亮)
C.细胞浓缩成长方体。然而,它仍然通过四个端口与相邻单元相连形成细长突起
D细胞发育出分支的原生质延伸,类似树突,以快速、随机的方式延伸和收缩。可以观察到小泡在拉长的突起内移动(正在运输)。
3.这样的观察可以彻底改变我们对干细胞分化过程中细胞形态、代谢活性和反应性变化的理解。
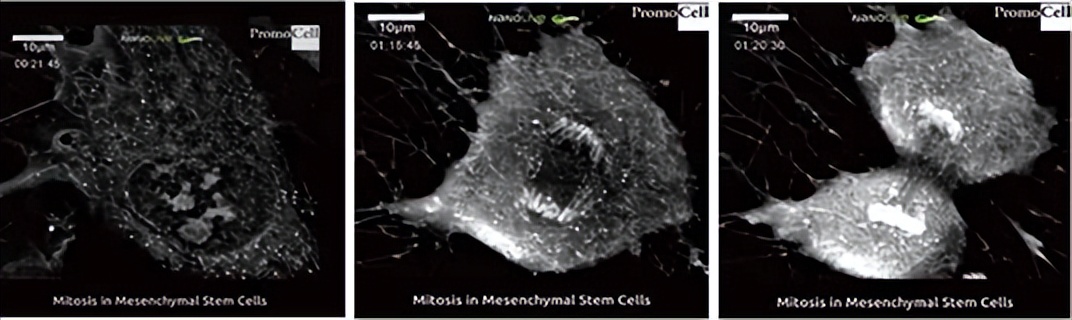
案例三:群体水平上的干细胞神经分化
背景
在本案例研究中,使用Nanolive下一代自动化显微镜CX-A对干细胞分化的观察从单细胞水平扩展到人群水平。CX-A的大视场(高达1 mm2)、多种成像模式和简单而高效的离体技术为罕见和不可预测的细胞事件(如分化)成像提供了一个强大的解决方案,具有高空间分辨率,并且不影响3D Cell Explorer的细胞器级分辨率。
试验方法
脐带基质人MSC在涂有纤维连接蛋白的CX-A兼容的35 mm玻璃底培养皿中培养4d。然后将培养基切换到神经源性分化培养基(PromoCell,德国)2d,然后开始成像。采用5×5网格扫描模式,以每4.5min/张的频率自动采集图像,持续22h。生成的图像沿Z轴进行最大投影,然后缝合在一起生成视频。
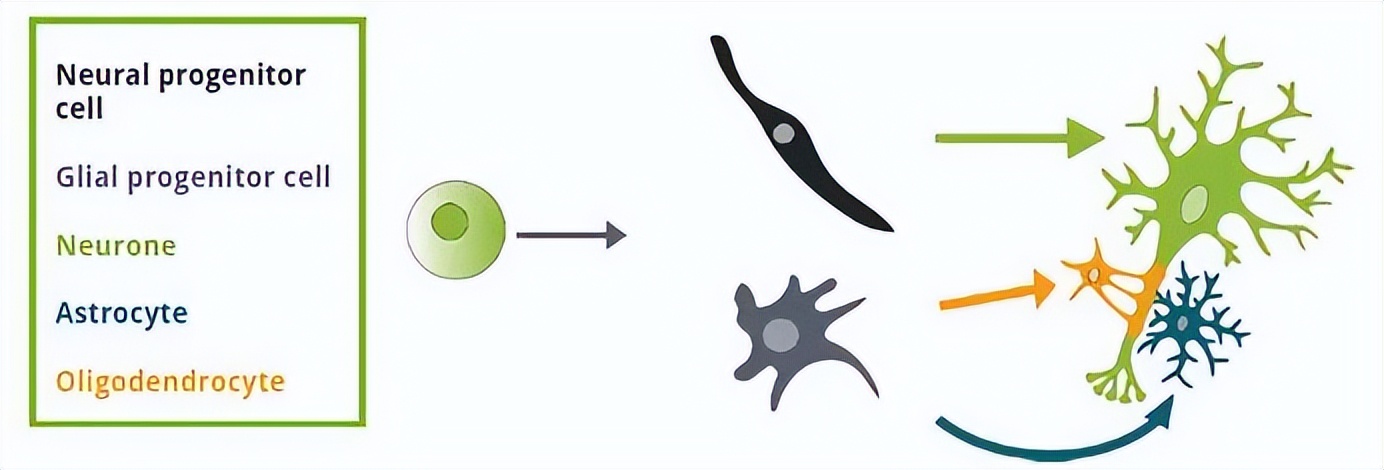
上面的示意图显示了两种可能的干细胞谱系在暴露于神经源性分化线索后可以发生的变化。神经细胞只能由神经祖细胞生成,而星形胶质细胞和少突胶质细胞则由胶质祖细胞生成。

观察内容
1.无标签和光毒性技术的非侵入性意味着非常敏感的细胞事件,如干细胞分化,可以长期成像,无需处理干扰。
2.CX-A的广阔视野允许在群体水平上评估细胞表型和形态的多样性。监测多个细胞的反应会给实验带来更大的统计意义,并最大限度地增加观察罕见事件的机会。
3.高分辨率使我们能够观察到极其精细、脆弱的结构,如细胞之间的接触点。
4.利用该技术,可以根据细胞形态特征识别神经分化过程各个阶段的细胞。
观察步骤
Step1:肌动蛋白细胞骨架收缩

当细胞开始发育出神经元形态时,它会收缩并失去与邻近细胞的联系。这个过程发生得有多快?细胞的大小/体积/质量的平均变化是多少?分化细胞与多少细胞保持连接?什么时候切断联络点?Nanolive高空间分辨率为解决时间线的精细细节提供了可能性。
Step2:液泡形成
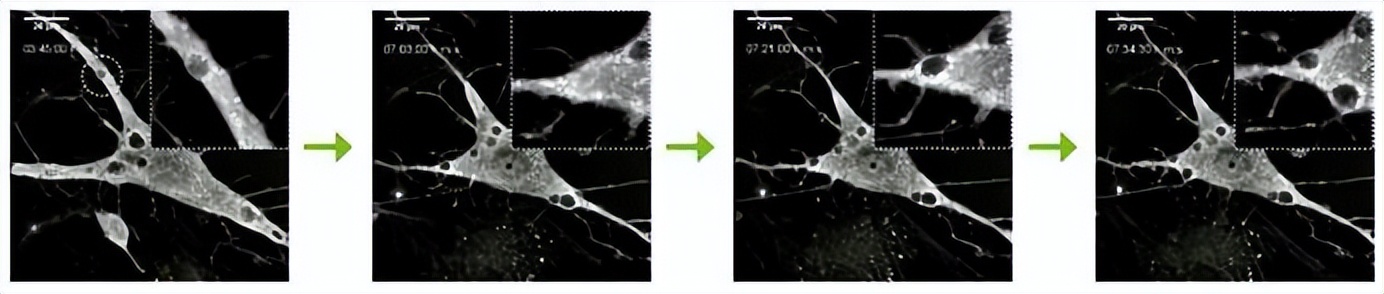
Nanolive高空间分辨率第一次能够捕捉到分化过程中液泡的形成。这个过程在分化中的意义是什么?细胞是否可以回收旧的成分以适应新的细胞功能?量化简单与细胞大小/体积/质量相关的空泡数量等指标可以揭示这种现象的重要性。
第二点涉及液泡形成的空间分布;图像显示,液泡在细胞的外围形成,然后向细胞的中心移动。绘制液泡的空间分布图并追踪它们的运动可能是有意义的。
Step3: 轴突延长
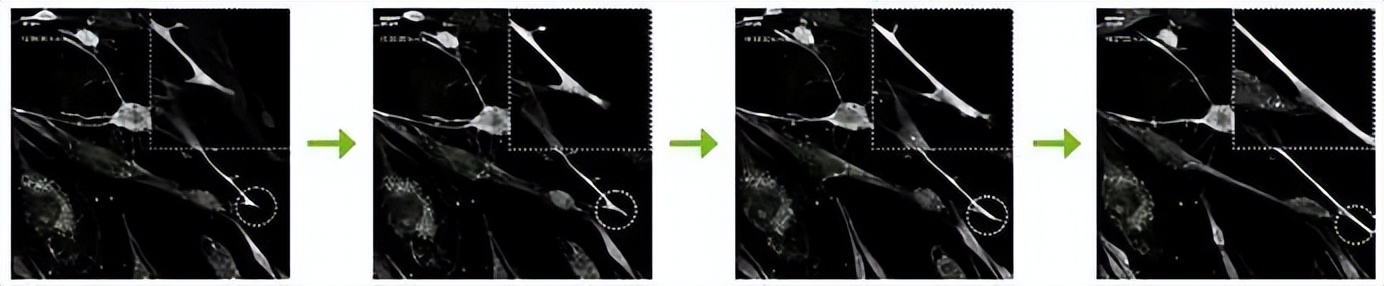
轴突的伸长方向与发育中的细胞体相反。这种增长有多快?轴突的直径在生长过程中会发生变化吗?在发育中的轴突末端,我们观察到一个小的手指状突起,似乎探测到它前面的表面。这个结构可能是突触末端吗?在发育过程中,我们观察到树突的丢失和小泡沿着轴突流向生长区;这可能是被运输到生长区的用于再生树突状的材料吗?
结论
1.本案例研究中的所有数据都是从CX-a上拍摄的单个视频中获得的,突出了数据的丰富性。
2.Nanolive为研究细胞提供了无创、无标签的选择,不受外界干扰。
3.这些观察结果为研究开辟了几个有趣的新方向并展示了大量有待开发的定量信息
03
参考文献
1.Knowles, R. B. et al. Plaque-induced neuriteabnormalities: implications for disruption of neural networks in Alzheimer’sdisease. Proc. Natl.Acad. Sci. 96(9), 5274-5279. (1999).
2.Nagy, J. et al. Altered neurite morphology andcholinergic function of induced pluripotent stem cell-derived neurons from apatient with Kleefstra syndrome and autism. Transl. Psychiatry. 7(7),e1179-e1179. (2017).
3.Wissner-Gross, Z. D. et al. Large-scale analysisof neurite growth dynamics on micropatterned substrates. Integr. Biol.3(1), 65-74 (2011).



NanoLive 3D Explorer是由瑞士 Nanolive 公司于2014年在中国推出的一款实时无标记活细胞断层扫描3D显微镜,NanoLive 3D Explorer(简称3D显微成像系统)整合全息技术及旋转扫描技术为一体,无需任何标记即可对细胞在200nm 尺度上进行3D结构探索,并能进行一系列量化实验,如细胞迁移、胞内囊泡追踪、亚细胞器定位、细胞或微生物体积测定、细胞骨架、微丝等无标记分析。



不同于传统的细胞成像需要固定并染色,使用实时无标记活细胞断层扫描3D显微镜几乎不需要样品制备,采用非入侵式、无标记成像,利用任何细胞组分不同折射率的透光信息,对细胞组分进行数字化“染色”,可轻松区分细胞核、细胞质和细胞器。



由于无需任何标记物,不用担心荧光标记对细胞二次影响,通过连续观测可提供在生理条件下活细胞更多的变化信息,从而为生命本质活动研究提供探索工具。



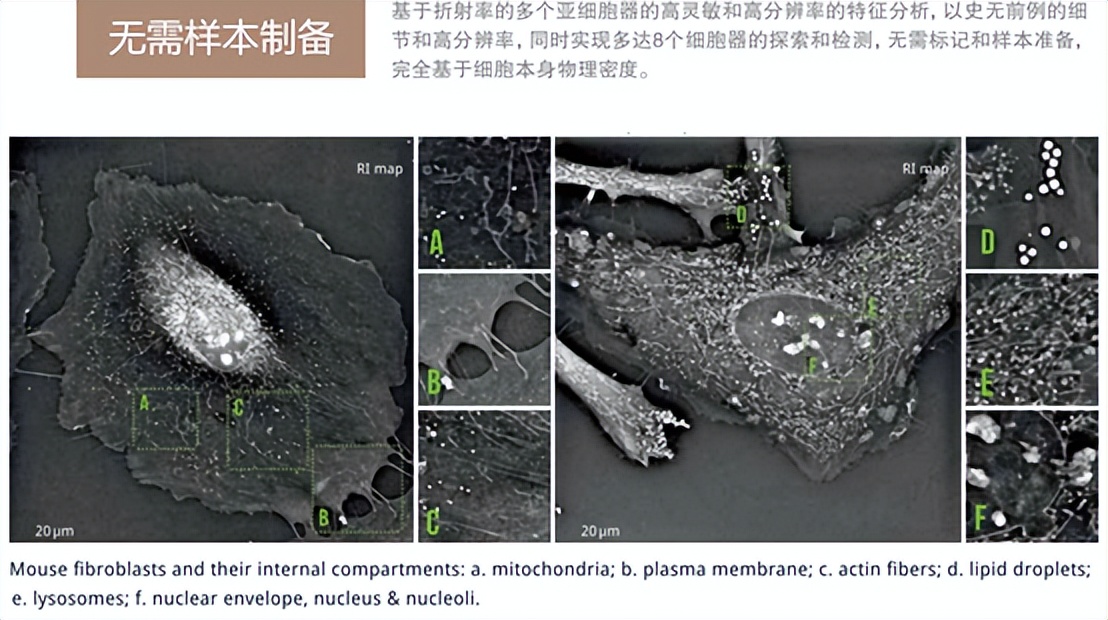



可搭载载台式孵育系统,在不干扰细胞自然生理机能的条件下研究细胞生长、分化、死亡的生命周期,可连续观察细胞几秒到数周,以每秒的速度实时追踪细胞各个结构和它们的机动性与动态性。






3D Explorer整合了完整的活细胞3D成像技术,首次亮相2014年ASCB会议时就一举获得众多业内人士好评,从技术上引领了当前生命科学研究的前沿热点。

主要获奖情况:




昆明纳瑞科技有限公司
昆明市北京路1088号领域时代大厦A座14层04室
想省事,找我们!
END