虽然老师们总吐槽课本太简单,同学们总吐槽课本上废话太多,知识点不肯明明白白列出来,但课本的重要性大家都心知肚明。
包sir 找到一份资料,帮助大家划出了高中化学课本每一页的重难点,无论是课前预习,还是考前回归课本,希望这份资料能帮你提高效率。

必修一
1.P4
常见危险化学品的标志,主要知道常见物质的性质与标志相对应。如酒精为易燃液体、高锰酸钾为氧化剂、浓硫酸为腐蚀品、KCN为剧*品毒**。如P10习题第二题选B。
2. P6-7
熟记过滤、蒸发、蒸馏装置图,分别需要哪些仪器?蒸馏烧瓶中温度计水银球的位置,冷凝管水流方向(若冷凝管竖直冷凝水流方向)。蒸馏烧瓶和普通*瓶的烧**区别。
3. P7
除去粗盐中的Ca、Mg、SO等杂质,先加入过量的BaCl,至沉淀不再产生后,再加入过量的NaCO、NaOH,充分反应后将沉淀一并滤去,经检测发现滤液中仍含有一定量的SO,其原因是BaSO和BaCO的Ksp差不大,当溶液中存在大量的CO时,BaSO就会部分转化为BaCO。其中NaCO的作用是:除Ca和过量的Ba。所以试剂加入顺序NaCO在之BaCl后。
4. P9
萃取和分液:分液装置图,分液漏斗的结构(两活塞、两小孔)。溴水呈橙色、溴的(苯)CCl橙红色。碘水呈黄色,碘的(苯)CCl呈紫红色。萃取后分液,上下层液体分别从上下口倒出。注意实验1-4的第(2)步、(4)步操作的注意事项及规范的文字表述。P9关于CCl的注解①
5. P10
第6-7题 氯离子、CO和SO的检验方法。
6. P16
配制一定物质的量浓度的溶液()。重点注意步骤、图示、注解、注意事项(包括P18习题6)、学与问等。称量固体时托盘天平只保留一位,量筒量取液体时也只保留一位。容量瓶使用的第一步操作:检查是否漏水(简称“查漏”)。
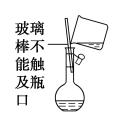
“查漏”的方法:向容量瓶中加入适量水,盖好瓶塞,左手食指顶住瓶塞,右手托住瓶底,将容量瓶倒转过来看瓶口处是否有水渗出,若没有,将容量瓶正立,将瓶塞旋转180度,重复上述操作,如果瓶口处仍无水渗出,则此容量瓶不漏水。若漏水,可以在瓶塞处涂凡士林。常见容量瓶的规格有50 mL、100 mL、250 mL、500 mL、1000 mL 几种。如配制溶液时明确知道所需容量瓶规格,则需将容量瓶规格一并答上。如图所示:用玻璃棒引流时,玻璃棒末端应插入到刻度线以下,且玻璃棒靠近容量瓶口处且不能接触瓶口。定容时,胶头滴管不能伸入容量瓶。配制一定物质的量浓度的溶液所需要的实验仪器:托盘天平、量筒、玻璃棒、容量瓶(容量一定要指明)、胶头滴管、烧杯、药匙。重要的实验步骤:计算→称量(量取)→溶解(稀释)→转移(轻摇)→定容→摇匀→倒出装瓶。定容时视线与凹液面最低处相平,直到液面与刻度线相切。
7. P26-27
认真阅读科学探求、科学史话、胶体的定义、胶体的性质、Fe(OH)胶体制备、区别胶体和溶液的方法等知识:FeCl溶液呈棕黄色,制备Fe(OH)胶体的操作方法是:在沸水中滴加饱和FeCl溶液,继续煮沸至红褐色,停止加热。将0.1mol FeCl制成胶体,所得的胶粒数小于0.1N,Fe(OH)胶体不带电,Fe(OH)胶粒带正电。 FeCl溶液和Fe(OH)胶体最本质的区别是胶体粒子大小在1nm-100nm之间,区别这两种分散系最简单的方法是丁达尔效应。胶体粒子不能透过半透膜,能透过滤纸。氯化铁溶液与氢氧化铁胶体具有的共同性质是:加热蒸干、灼烧后都有氧化铁生成。常见的胶体有:Fe(OH)胶体、Al(OH)胶体、硅酸胶体、淀粉溶液、蛋白质溶液、血液。工厂中常用的静电除尘装置就是根据胶粒带电的性质设计的。
8. P24-25
分类的方法及物质的分类及实践活动:特别注意:NO、CO为不成盐氧化物,NO溶于水生成HNO,但HNO的酸酐为NO。酸酐不一定都是氧化物,如*酸酐醋**。酸性氧化物、碱性氧化物不一定都与水反应生成对应的酸和碱。SiO能和强碱反应,也能和HF反应,但不是两性氧化物。1mol HPO最多和3molNaOH,说明HPO为三元酸;1mol HPO最多和2molNaOH反应,说明HPO为二元酸,NaHPO为正盐;1mol HPO最多和1molNaOH反应,说明HPO为一元酸,NaHPO为正盐。
9. P30
电解质和非电解质:纯净的酸、碱、盐、金属氧化物、水是电解质;其它纯净的化合物一般是非电解质;淀粉、盐酸、*水氨**、单质铜既不是电解质,也不是非电解质(前三者为混和物、后者不是化合物)。BaSO的水溶液不易导电,但BaSO是强电解质。一水合氨是弱电解质。NaHSO在熔化状态下的电离方程式为NaHSO=Na+ HSO。证明某化合物为离子化合物最简单的方法是:在熔化状态下是否导电,若导电则为离子化合物
10. 物理变化和化学变化:化学变化过程中有旧化学键的断裂,同时又有新化学键的形成,但有化学键断裂的变化未必就是化学变化,如NaCl晶体熔化、SiO晶体的熔化,分别破坏了离子键、共价键,但属于物理变化。一种原子变为另一种原子涉及原子核的变化,不属于化学变化。CuSO等电解质溶液的导电属于化学变化。煤的气化、液化、煤的干馏、裂化、裂解为化学变化。石油的分馏为物理变化。
11. P37 氧化还原反应的实质是有电子转移(得失或偏移);学与问;常见的氧化剂和还原剂;P38生产和生活中的氧化还原反应;P42复习题中的2、3题关注维生素C及黑*药火**。
12. 钠及其化合物
P46
图3-2观察金属化学性质的一些实验。注意镁还可以在氮气、CO中燃烧。
P47
图3-3观察钠的真面目是银白色,用小刀切割后很快变暗,是因为氧化成了NaO,如果点燃金属属钠,产物为NaO,实验3-2中,加热金属钠用坩埚,不用蒸发皿,坩埚放在泥三角上。NaO呈淡黄色。钠保存在石蜡油或煤油中,钠着火不能用水灭火,只能用干燥的沙土来灭火。
P48
镁、铝是比较活泼的金属单质,但在空气中能稳定存在,其原因是:镁铝表面生成了一层致密的氧化物保护膜,图3-6中观察到的现象是铝箔熔化,但不滴落。这说明氧化铝的熔点高于铝。铝是银白色金属,比镁要硬,熔点比镁铝价电子数多且离子半径小,金属键强,铁、铝分别遇冷的浓硫酸、浓硝酸发生钝化现象。钝化属于化学变化。
P50
钠与水反应时钠在水面上,钠与乙醇反应是,钠在乙醇下面,二都相比较与水反应快,这说明水中的氢比醇羟基中的氢活泼。P50铁粉与水蒸气反应的实验中,湿棉花的作用是提供反应所需要的水蒸气。检验有氢气生成的实验现操作是:点燃肥皂泡,有尖锐的爆鸣声。特别注意反应方程式的书写P51。
P51
图3-10说明金在自然界中可以以游离态形式存在。单质的化学性质极不活泼。下面的注解中四羟基合铝酸纳,属于配位化合物。铝和NaOH溶液的反应也可以写成:
2Al+2NaOH+6HO==2Na[Al(OH)]+3H↑
P53 关注科学视野:未来金属钛
P55 向NaO与水反应后的溶液中滴入酚酞,现象是:先变红,后褪色。与水反应先生成HO,再分解成HO和O。过氧化钠用作呼吸面具或潜水艇中的氧气来源的原因。NaO与HO和CO反应,转移电子数与NaO的物质的量相等。
P56
图3-12的颜色深说明CO的第一步水解程度大于其第二步水解。碳酸钠和碳酸氢钠溶解后,用手摸试管底部,溶解碳酸钠的试管温度明显升高。水解虽然是吸热的,形成水合离子的过程是放热的。
P56
仔细观察图3-13,试管底略高于试管底,酒精灯火焰的位置。该实验证明NaCO和NaHCO稳定性差的是NaHCO。所以除去NaCO固体中有少量NaHCO常用加热法,NaCO和酸反应可以看成先生成NaHCO,再继续反应生成CO。
NaCO和NaHCO溶解性相对较小的是NaHCO,向饱和的NaCO溶液中通足量的CO现象是有晶体析出,化学方程式为NaCO (饱和)+ HO + CO == 2 NaHCO↓。所以除去NaHCO溶液中有少量NaCO方法通入过量的CO。
分别取NaCO溶液和NaHCO溶液两种试液分别滴加少量的澄清石灰水,均有白色沉淀,发生的离子反应方程式分别为Ca+CO=CaCO↓、2HCO+Ca+2OH= CaCO↓+2HO+CO。
侯氏制碱法中的碱是指NaCO。向氨化的饱和食盐水中通CO有晶体析出(一定先通NH再通CO)。过滤,将所得的晶体加热得NaCO。有关反应为:NH+CO+NaCl=NHCl+NaHCO↓, 2 NaHCO NaCO + HO + CO↑。
P57
焰色反应:焰色反应不属于化学变化。焰色反应是金属或其化合物,如钠的焰色为黄色,是指钠的单质或化合物在火焰上灼烧焰色都是黄色。观察K的焰色要用蓝色钴玻璃,其作用是滤去黄色的光。每次焰色反应前铂丝都要用盐酸洗净,在外焰上灼烧到没有颜色时,再蘸取待检测物质。节日燃放的烟花,就是碱金属的焰色反应。
13. 镁 及其化合物
镁可以分别在N、CO中燃烧,化学方程式分别为3Mg + N
 MgN、
MgN、
2Mg+2CO
 2MgO+2C。将镁和N燃烧产物溶于水,有沉淀和气体生成:
2MgO+2C。将镁和N燃烧产物溶于水,有沉淀和气体生成:
MgN+8 HO=3Mg(OH)↓+2NH↑。
从海水中来提取MgCl时的流程:加氢氧化钙,过虑洗涤得氢氧化镁沉淀,用盐酸溶解沉淀,通过蒸发浓缩、冷却结晶得到MgCl·6HO晶体,再在HCl气体环境中加热MgCl·6HO晶体得到无水MgCl,HCl气流主要是为了抑制Mg水解;电解熔融的MgCl,不用MgO电解来制备Mg是因为MgO熔点很高,需要能量高。
14.铝及其化合物
铝是地壳中含量最多的金属元素,工业上不用电解AlCl来制备铝的原因是AlCl是分子晶体在熔融的状态下不导电(必修二P93第6题从铝土矿中提取铝的有关反应)。
P58
氧化铝的性质用途:氧化铝为两性氧化物,是电解质。
P58
实验3-7、实验3-8
氢氧化铝是两性氢氧化物,为弱电解质。实验室制备Al(OH)的离子方程式为:Al + 3NH·HO == Al(OH)↓+ 3NH,不用NaOH等强碱原因是Al(OH) + OH == AlO+ 2HO,以下几种方法也可以得到氢氧化铝。
取0.25ag铝(铝的质量为a g)溶于适量的盐酸中,再取0.75a g铝溶于适量的强碱溶液中,将两溶液混合即得白色沉淀,3AlO + Al + 6HO == 4Al(OH)↓;
偏铝酸钠溶液中通CO。CO少量与过量时也可以得到氢氧化铝。(CO少量)CO + 3HO + 2NaAlO == 2Al(OH)↓+ NaCO、(CO过量)CO + 2HO + NaAlO == Al(OH)↓+ NaHCO。
Al和AlO的转化:Al + 4OH == AlO + 2HO、AlO + 4H == Al + 2HO
AlO和HCO不能共存。不是双水解,是得质子的能力不同引起的:
AlO+HCO+HO= Al(OH)↓+ CO
明矾的净水:明矾、FeCl·6HO被称作净水剂,原因是Al、Fe水解形成胶体(Al + 3HOAl(OH) (胶体)+ 3H),吸附水中的悬浮物,使之沉降已达净水目的,只有净水作用,无杀菌、消毒作用。
向明矾溶液是加入Ba(OH)溶液,沉淀的质量最大和沉淀的物质的量最大的离子方程式分别为:Al+2SO+2Ba+4OH=AlO+2BaSO↓+2HO 、2Al+3SO+3Ba+6OH= 2Al(OH)↓+3BaSO↓
泡沫灭火器Al(SO)溶液不能装在铁桶中是因为Al水解显酸性,NaHCO溶液不能装在玻璃桶中是因为HCO水解呈碱性。泡沫灭火器反应原理:Al +3 HCO == Al(OH)↓+CO↑。
15.铁及其化合物
P59
铁中含有碳等杂质,使铁的熔点降低,在常温下浓硫酸和浓硝酸使铁钝化。铁的氧化物中,赤铁矿(FeO)红棕色粉末,俗称铁红,常用着红色油漆和涂料。也是炼铁的原料。磁铁矿(FeO)具有磁性,俗称磁性氧化铁,是黑色晶体。FeO是一种黑色粉末,在空气里加热就迅速氧化成FeO.铁在Cl中燃烧无论Fe或Cl过量均生成FeCl,但可以用化合反应生成FeCl,相关反应为:2Fe + 3Cl 2FeCl,Fe +2 FeCl == 3FeCl。铁的氧化物与非氧化性酸,强氧化性酸,还原性酸反应的特殊性。FeO+8H= 2Fe+Fe+4HO,FeO+6H+2I=2Fe+I+3HO,3FeO+10H+NO=3Fe+NO↑+5HO。Fe被氧化,Fe被I还原。
P60
铁的氢氧化物:在制备Fe(OH)时可以加热到沸腾除水中的氧,冷却后再配溶液,也可以加比水轻,不溶于水的有机溶剂(苯)封住液面,加NaOH溶液时胶头滴管要伸入到溶液中接近试管底,防止Fe被氧化,可以加入铁粉,Fe(OH)氧化成Fe(OH)的现象为白色絮状沉淀迅速变成灰绿色,最后红褐色,化学方程式4Fe(OH) + O + 2HO == 4Fe(OH)。加热FeCl溶液,最终得到的是FeO。氧氧化铁、氢氧化亚铁分别与强氧化性酸,还原性酸反应的:(OH)+6H+2I=2Fe+I+6HO,
3Fe(OH)+10H+NO=3Fe+NO↑+8HO。
Fe、Fe的性质及其检验。检验Fe通常有以下几种方法:
①加KSCN溶液,无明显变化,再加氯水,溶液变血红色。Fe+3SCN≒Fe(SCN)。
②加氢氧化钠溶液,出现白色絮状沉淀迅速变成灰绿色,最后红褐色。4Fe(OH) + O + 2HO == 4Fe(OH)。
③加溶KFe(CN)溶液,生成蓝色沉淀。3Fe+2[ Fe(CN)]=Fe[ Fe(CN)]↓
检验Fe通常有以下几种方法:
接观察溶液是棕黄色。滴加氢氧化钠溶液,出现红褐色沉淀;滴加KSCN溶液,有血红色溶液出现;加入苯酚溶液,呈紫色。
P62
图3-21铜绿的主要成分为Cu(OH)CO。
P62
第10题,FeCl溶液作为刻制印刷电路时的“腐蚀液”,其离子方程式为:
Cu +2 Fe== 2Fe+Cu.
P64
倒数第二段:合金的硬度大于它的纯金属成分,合金的熔点低于它的成分金属。青铜是我国使用最早的合金。
P65
钢是用量最大、用途最广的合金。根据其化学成分,可以分为碳素钢和合金钢。
P70 第6题。选C。
16.硅及其化合物
P74
碳是构成有机物的主要元素,而硅是构成岩石与许多矿物的基本元素。硅是一种亲氧元素,在自然界中它总是与氧相互化合的,在自然界中主要以熔点很高的氧化物SiO及硅酸盐的形式存在。结晶的SiO是石英,其中无色透明的是水晶,具有彩色环带或层状的称为玛瑙。沙子中含有小粒的石英晶体。纯净的SiO是现代光学及光纤制品的基本原料。可以用HF刻蚀玻璃,是因为SiO可与HF酸反应(SiO+4HF=SiF↑+2HO),但SiO不是两性氧化物。SiO为酸性氧化物,但不溶于水生成硅酸。盛碱溶液的试剂瓶一般用橡胶塞(P76图4-6)因为SiO易与强碱溶液反应,生成硅酸钠使试剂瓶受腐蚀。SiO为原子晶体,不存在单个的SiO分子,1mol的SiO中含有4mol的Si-O键。
P76
HSiO是一种酸性比HCO还弱的弱酸。“硅胶”吸附能力强,常用作实验室和袋装食品、瓶装药品的干燥剂。HSiO可以由可溶性的硅酸盐与相对较强的酸用作生成HSiO。在NaSiO溶液中分别加入盐酸和通入CO,其化学方程式分别为NaSiO+2HCl=2NaCl+HSiO↓、NaSiO+HO+CO=NaCO+
HSiO↓。若CO过量,则反应为:NaSiO+2HO+2CO=2NaHCO+HSiO↓
P77
硅酸钠(NaSiO) 的水溶液俗称水玻璃,不能燃烧,不易被腐蚀,热稳定性强,是制备硅胶和木材防火剂的原料。NaSiO写成氧物的形式可以表示为NaO·SiO。
P77
资料卡片硅酸盐组成写成的方法。
P78
通玻璃是以纯碱、石灰石和石英为原料,在玻璃窑中熔化制得的。水泥是以黏土和石灰石为主要原料,在水泥回转窑中煅烧,再加入适量的石膏研成细粉。普通玻璃和水泥的共同原料是石灰石。
P78
碳化硅(俗称金刚砂),属于原子晶体。碳化硅、硅刚、硅橡胶、人工制造的分子筛等的性质和用途。
P79
科学视野:新型陶瓷
P79
晶体硅属于原子晶体,金刚石,晶体硅,碳化硅熔点由低到高的顺序为晶体硅<碳化硅<金刚石。导电性介于导体和绝缘体之间,是良好的半导体材料。在常温下可与氟气、氢氟酸(Si+4HF=SiF↑+2H↑)和强碱发生反应(Si+2OH+HO=SiO+2H↑)。
P80
硅的应用:图4-12、图4-13、硅是人类将太阳能转化为电能的常用材料。
P81
习题5:仪器坩埚的种类及使用注意事项
P81
第9题硅的制备及提纯:粗硅的制取生成的CO,由硅的氧化物制取硅主要的三个化学反应。理解“从沙滩到用户”。
17.氯及其化合物
P82
氯元素是重要的“成盐元素”。主要以NaCl的形式存在于海水和陆地的盐矿中,海水不能直接饮用。
P82
科学视野-氯气的发现和确认及思考与交流。
P83
Cl是一种黄绿色有强烈剌激性气味的有毒气体。闻Cl的正确操作方法(图4-15)。铁在氯气中燃烧产生棕色的烟(2Fe+3Cl
 2FeCl),氢气在氯气中燃烧(H+Cl
2FeCl),氢气在氯气中燃烧(H+Cl
 2HCl)产生苍白色火焰(图4-16)。说明燃烧不一定要有氧气参加。
2HCl)产生苍白色火焰(图4-16)。说明燃烧不一定要有氧气参加。
P84
很多自来水厂用氯气杀菌、消毒。是由于氯气溶于水生成的HClO有强氧化性。HClO是一元弱酸,其酸性比HCO弱,HClO不稳定,在光照条件下分解为盐酸和O、氯水保存在棕色试剂瓶中。干燥的氯气无漂白作用。氯气溶于水的化学方程式为HO+Cl≒HCl+HClO,标况下,2.24L氯气溶于水,转移电子数小于0.1N,酸性条件下,Cl和ClO不能共存,将Cl通入紫色石蕊溶液现象是先变红,后褪色。氯水有关还原剂反应的方程式,除漂白作用,化学方程式都以Cl作为反应物。如淀粉-KI试纸遇氯水变蓝(2I+Cl=2Cl+I),氯水滴加到NaS溶液中有淡黄色沉淀(S+Cl=2Cl+S↓)。Cl溶于水有漂白作用,SO也有漂白作用,将Cl和SO等体积混合溶于水,漂白作用消失,原因是:Cl+SO+2HO=4H+2Cl+ SO
P85
工业上制漂*粉白**的反应为:2Cl+2Ca(OH)=CaCl+Ca(ClO)+2HO,漂*粉白**有主要成份是CaCl和Ca(ClO),有效成份是Ca(ClO),漂*粉白**空气中失效相关的化学方程式为Ca(ClO)+CO+HO=CaCO+2HClO,2HClO=2HCl+O↑。漂白液是以NaClO为有效成分的溶液,又叫“8.4”消毒液,因水解而略呈碱性,它不能和洁厕精共用,原因是NaClO+2HCl=NaCl+Cl↑+HO。漂白液、漂*粉白**和漂粉精可用漂白棉、麻、纸张的漂白剂,又可以用作游泳池及环境的消毒剂。
P85-86 Cl的检验
P88
第14题:主要涉及Cl的实验室制法。如右图:
烧瓶中发生的化学反应方程式为:
MnO+4HCl(浓)
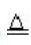 MnCl+Cl↑+2HO
MnCl+Cl↑+2HO
若用KMnO代替MnO,发生的化学反应方程式2KMnO+16HCl(浓)=2MnCl+2KCl+5Cl↑+8HO,C中盛装的是饱和食盐水,其作用是除去氯气中HCl,原因是饱和食盐水可以溶解HCl同时可降低氯气在水中的溶解度。D中盛装的是浓硫酸,其作用是除去氯气中的水蒸气,若D为干燥管,可以盛装PO或CaO。F中盛装的是NaOH溶液、其作用是除去多余的氯气。E的收集方法为向上排空气法。
18.硫和硫的化合物
P89
空气质量日报的各项指标中,有二氧化硫和二氧化氮的指数。P107如第4题,选C。游离态的硫存在于火山喷口附近或地壳的岩层里。硫俗称硫黄,是一种黄色晶体,不溶于水,微溶于酒精,易溶于CS。试管内壁的硫可以用热碱洗涤
(3S+6NaOH2
 NaS+NaSO+3HO)。
NaS+NaSO+3HO)。
P89
硫铁矿(FeS,其中硫为-1价)、黄铜矿(CuFeS、其中硫为-2价、Fe为+2价)、石膏(CaSO·2HO)、芒硝(NaSO·10HO)
P90
实验4-7,SO能使品红褪色,加热又恢复原来的颜色,这是由于它能与某些(遇紫色石蕊溶液只变红)有些物质化合生成不稳定的无色物质,该不稳定的无色物质会慢慢分解,受热则很快分解恢复原来的颜色。SO的漂白是化合作用,属于暂时性漂白,NaO、HClO的漂白为强氧化性,为永久性漂白,不能恢复原来的颜色。SO还能杀菌消毒,SO和某些含硫化合物的漂白作用也被一些不法厂商非法用来加工食品,以使食物增白,食用这类食品对人体的肝、肾等有严重的损害,并有致癌作用。空气中SO的主要来源是大量燃烧煤、石油等化石燃料,其次是来自火山爆发和金属冶炼厂、硫酸厂等的工业废气。
P95
第1题,往煤中加石灰石CaCO,煅烧得到CaO,煤燃烧产生的SO和生石灰产生反应生成,CaSO再被氧化成CaSO,从而减少了SO排放量。
实验室制取二氧化硫的化学方程式为:NaSOHSO(较浓)=NaSO+SO↑+HO。
SO有还原性,与NaO化合生成NaSO(NaO+SO=NaSO),使酸性KMnO溶液褪色(2KMnO+5SO+2HO=KSO+2MnSO+2HSO),SO气体通入澄清石灰水先浑浊后澄清(SO+Ca(OH)=CaSO↓+HO、2SO+Ca(OH)=Ca(HSO))
P91
资料卡片。HS是一种无色,有臭鸡蛋气味有剧毒的气体。CuSO溶液中通HS气体,有黑色沉淀生成(CuSO+HS=CuS↓+HSO),电石气乙炔中混有的HS、PH气体可用硫酸铜溶液除杂,该反应也是弱酸制强酸的典型例子。
19.氮的氧化物
P91
在放电或高温的条件下,N和O可以直接化合[ N+O=2NO(放电)],NO常温下易与O化合生成红棕色的NO,所以不能用排空气法收集NO。NO溶于水生成HNO(3NO+HO==2HNO+NO)。工业上制取HNO的原理。以3NO+HO=2HNO+NO 和2NO+O==2NO两个反应为基础作变形处理。
当V(NO): V(O)=4:1时,NO可完全转化为硝酸: 4NO+O+2HO=4HNO
当V(NO): V(O)=4:3时,NO可完全转化为硝酸: 4NO+3O+2HO=4HNO
P93
光化学烟雾主要是由氮氧化物引起的,它来源于汽车尾气。而酸雨由SO和NO引起的。正常雨水的PH值在5.6左右,由于溶解了CO的缘故,当空气中大量N和S的氧化物随雨水降落下来就会使得雨水的PH值小于5.6而形成酸雨。
P95
第2题涉及汽车尾气的产生和处理。答案为:(1)高温下促使N和O化合,另一原因可能是汽车汽缸内用于点燃汽油蒸气的电火花促使N、O放电反应。N+O=2NO(高温或放电)(2)2CO+2NO=2CO+N(催化剂)(3)①②

































本文转载自包学习网站。
关于知识点总结,大家认为还有哪个科目需要了解呢~
欢迎留言分享!
包sir 为大家准备呀,哈哈哈哈哈哈!
