前言
2023年第一季度已经结束,前几天有朋友问怎么看有哪些品种属于不批准的?我说可以有个免费的送达信息下的药品通知件可以查询。最近正好在做这些品种的整理,就拿出来跟圈友们分享一下。
一第一部分:怎么查询不批准的品种目录?

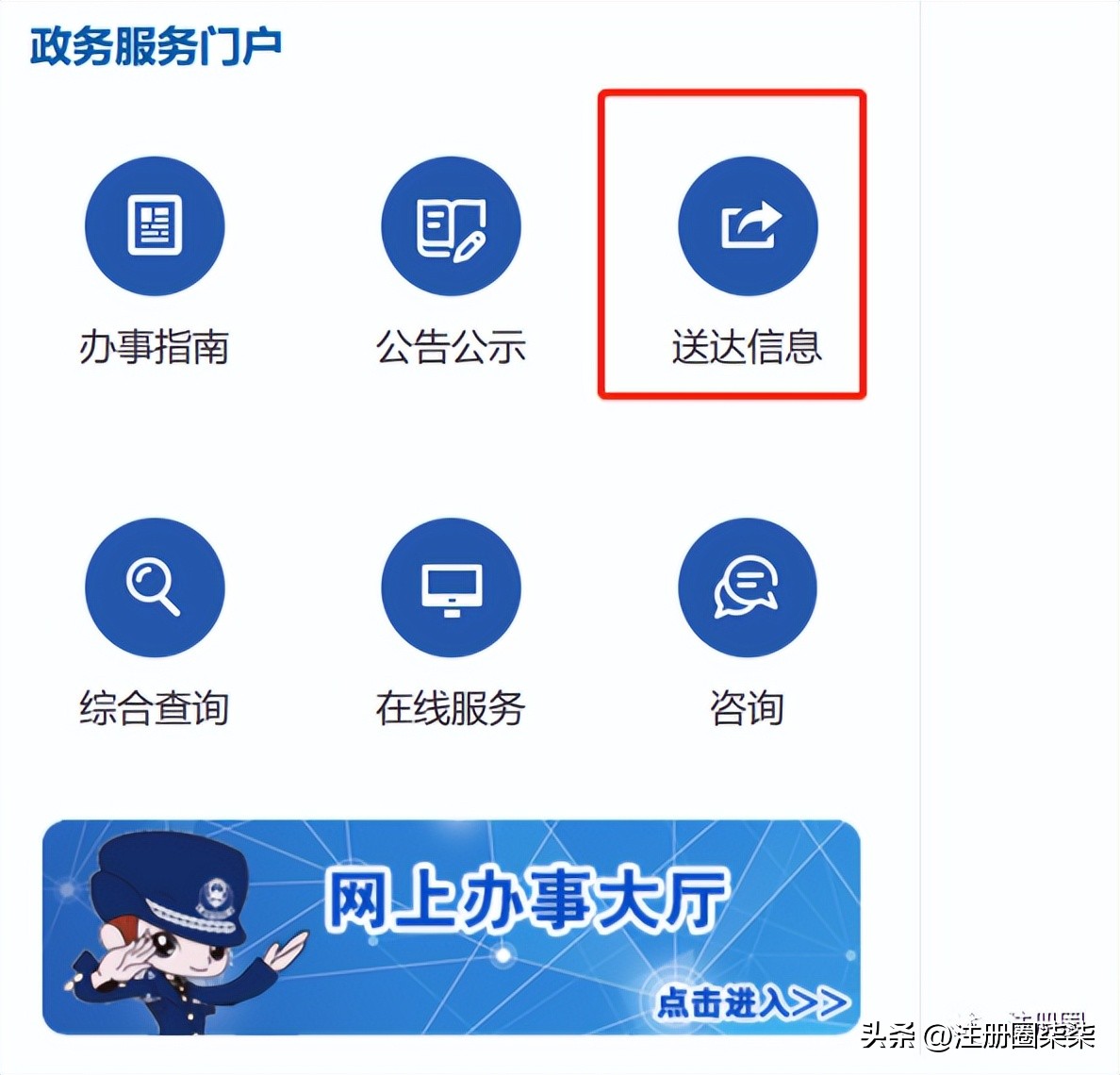
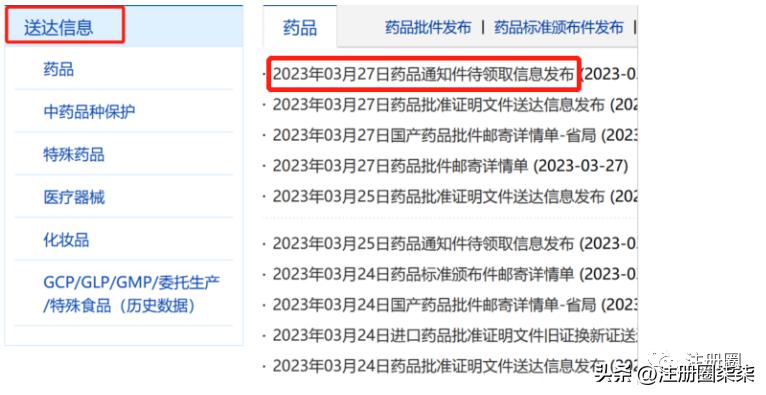
二第二部分:对第一季度的不批准品种进行汇总
2023年至今共发布药品通知件28批次,共234个受理号,其中一致性评价的18个,化药仿制药申请的67个;笔者对仿制药申请的67个进行了研究。
▲ 表1-2023年一致性评价未通过的品种一览表
|
序号 |
受理号 |
承办日期 |
品种名称 |
企业名称 |
签发日期 |
|
1 |
CYHB1850101国 |
2018/7/2 |
注射用奥沙利铂 |
江苏恒瑞医药股份有限公司 |
2023年3月24日 |
|
2 |
CYHB2250008 |
2022/1/11 |
醋酸地塞米松片 |
上海世康特制药有限公司 |
2023年3月23日 |
|
3 |
CYHB1950608国 |
2019/9/13 |
抗凝血用枸橼酸钠溶液 |
成都青山利康药业有限公司 |
2023年3月15日 |
|
4 |
CYHB2250667国 |
2022/10/26 |
硫酸阿托品注射液 |
遂成药业股份有限公司 |
2023年3月13日 |
|
5 |
CYHB2250273国 |
2022/5/11 |
胞磷胆碱注射液 |
吉林百年汉克制药有限公司 |
2023年3月3日 |
|
6 |
CYHB2250564国 |
2022/9/7 |
叶酸片 |
甘肃兰药药业有限公司 |
2023年3月2日 |
|
7 |
CYHB2050764国 |
2020/12/9 |
碘解磷定注射液 |
上海旭东海普药业有限公司 |
2023年2月23日 |
|
8 |
CYHB2150819国 |
2021/8/26 |
注射用哌拉西林钠他唑巴坦钠 |
苏州二叶制药有限公司 |
2023年2月23日 |
|
9 |
CYHB2151121国 |
2021/12/30 |
氨茶碱片 |
天津力生制药股份有限公司 |
2023年2月23日 |
|
10 |
CYHB2350043 |
2023/1/12 |
注射用氨苄西林钠舒巴坦钠 |
苏州二叶制药有限公司 |
2023年2月15日 |
|
11 |
CYHB2350044 |
2023/1/12 |
注射用氨苄西林钠舒巴坦钠 |
苏州二叶制药有限公司 |
2023年2月15日 |
|
12 |
CYHB2350045 |
2023/1/12 |
注射用氨苄西林钠舒巴坦钠 |
苏州二叶制药有限公司 |
2023年2月15日 |
|
13 |
CYHB2040038国 |
2020/9/30 |
苯磺酸左氨氯地平片 |
苏州东瑞制药有限公司 |
2023年2月3日 |
|
14 |
CYHB2150680国 |
2021/6/21 |
雷贝拉唑钠肠溶片 |
上海上药信谊药厂有限公司 |
2023年1月10日 |
|
15 |
CYHB2250348国 |
2022/6/14 |
黄体酮注射液 |
浙江仙琚制药股份有限公司 |
2023年1月11日 |
|
16 |
CYHB2250349国 |
2022/6/14 |
黄体酮注射液 |
浙江仙琚制药股份有限公司 |
2023年1月11日 |
|
17 |
CYHB2250429国 |
2022/7/11 |
头孢羟氨苄咀嚼片 |
金鸿药业股份有限公司 |
2023年1月12日 |
|
18 |
CYHB2250430国 |
2022/7/11 |
头孢羟氨苄咀嚼片 |
金鸿药业股份有限公司 |
2023年1月12日 |
▲ 2023年 仿制药未获批的品种清单
|
序号 |
受理号 |
受理时间 |
品种名称 |
企业名称 |
签发日期 |
|
1 |
CYHS1100644 |
2011/11/16 |
注射用头孢地嗪钠 |
悦康药业集团股份有限公司 |
2023年3月24日 |
|
2 |
CYHS1100645 |
2011/11/16 |
注射用头孢地嗪钠 |
悦康药业集团股份有限公司 |
2023年3月24日 |
|
3 |
CYHS1200405 |
2012/8/20 |
复方氨基酸(15)双肽(2)注射液 |
西安力邦制药有限公司 |
2023年3月24日 |
|
4 |
CYHS2101583国 |
2021/8/16 |
注射用高纯度尿促性素 |
上海天伟生物制药有限公司 |
2023年3月24日 |
|
5 |
CYHS2200457国 |
2022/3/17 |
硫酸氨基葡萄糖胶囊 |
华润三九医药股份有限公司 |
2023年3月24日 |
|
6 |
JYHS2100049国 |
2021/3/26 |
盐酸厄洛替尼片 |
Dr.Reddy's Laboratories Limited (注册代理机构:瑞迪博士(北京)药业有限公司) |
2023年3月24日 |
|
7 |
JYHS2100050国 |
2021/3/26 |
盐酸厄洛替尼片 |
Dr.Reddy's Laboratories Limited (注册代理机构:瑞迪博士(北京)药业有限公司) |
2023年3月24日 |
|
8 |
CYHS2100141国 |
2021/2/2 |
吸入用复方异丙托溴铵溶液 |
天津梅花生物医药科技有限公司 |
2023年3月21日 |
|
9 |
CYHS2101415国 |
2021/7/8 |
注射用头孢曲松钠 |
湖南恒生制药股份有限公司 |
2023年3月21日 |
|
10 |
CYHS2200463国 |
2022/3/21 |
二硫化硒洗剂 |
杭州和泽坤元药业有限公司 |
2023年3月21日 |
|
11 |
CYHS2201463国 |
2022/9/7 |
注射用头孢他啶阿维巴坦钠 |
南京恩泰医药科技有限公司 |
2023年3月21日 |
|
12 |
CYHS2300310 |
2023/2/2 |
吸入用乙酰半胱氨酸溶液 |
济南康桥医药科技有限公司 |
2023年3月21日 |
|
13 |
JYHS2000042国 |
2020/11/4 |
奥卡西平片 |
Sun Pharmaceutical Industries Limited(注册代理机构:深圳市康哲生物科技有限公司) |
2023年3月21日 |
|
14 |
JYHS2000043国 |
2020/11/4 |
奥卡西平片 |
Sun Pharmaceutical Industries Limited(注册代理机构:深圳市康哲生物科技有限公司) |
2023年3月21日 |
|
15 |
CYHS2101973国 |
2021/11/5 |
玻璃酸钠滴眼液 |
苏州欧康维视生物科技有限公司 |
2023年3月13日 |
|
16 |
CYHS1100780 |
2012/3/5 |
注射用磷酸氟达拉滨 |
连云港杰瑞药业有限公司 |
2023年3月7日 |
|
17 |
CYHS1300034 |
2013/7/11 |
盐酸莫西沙星氯化钠注射液 |
浙江莎普爱思药业股份有限公司 |
2023年3月7日 |
|
18 |
CYHS2101361国 |
2021/7/2 |
他达拉非片 |
苏州弘森药业股份有限公司 |
2023年3月7日 |
|
19 |
CYHS2101362国 |
2021/7/2 |
他达拉非片 |
苏州弘森药业股份有限公司 |
2023年3月7日 |
|
20 |
CYHS2101549国 |
2021/8/10 |
盐酸伐地那非片 |
广西强寿药业集团有限公司 |
2023年3月7日 |
|
21 |
CYHS2200309国 |
2022/2/14 |
利奈唑胺干混悬剂 |
浙江普利药业有限公司 |
2023年3月7日 |
|
22 |
CYHS2200555国 |
2022/4/19 |
他达拉非片 |
昆明源瑞制药有限公司 |
2023年3月7日 |
|
23 |
JYHS2200049国 |
2022/5/24 |
左甲状腺素钠片 |
Cipla Ltd.(注册代理机构:西普拉(中国)医药有限公司) |
2023年3月7日 |
|
24 |
JYHS2200050国 |
2022/5/24 |
左甲状腺素钠片 |
Cipla Ltd.(注册代理机构:西普拉(中国)医药有限公司) |
2023年3月7日 |
|
25 |
CYHS1200593 |
2012/8/27 |
马来酸桂哌齐特注射液 |
成都华宇制药有限公司 |
2023年3月1日 |
|
26 |
CYHS2201693国 |
2022/11/18 |
利丙双卡因乳膏 |
河北新张药股份有限公司 |
2023年3月1日 |
|
27 |
CYHS2000458国 |
2020/7/4 |
舒更葡糖钠注射液 |
江苏悦兴药业有限公司 |
2023年2月20日 |
|
28 |
CYHS2101962国 |
2021/11/3 |
*粟罂**乙碘油注射液 |
烟台鲁银药业有限公司 |
2023年2月20日 |
|
29 |
CYHS2200514国 |
2022/3/31 |
达格列净片 |
北京伟林恒昌医药科技有限公司 |
2023年2月20日 |
|
30 |
CYHS2200515国 |
2022/3/31 |
达格列净片 |
北京伟林恒昌医药科技有限公司 |
2023年2月20日 |
|
31 |
CYHS2200530国 |
2022/4/7 |
吸入用盐酸氨溴索溶液 |
湖北兴华制药有限公司 |
2023年2月20日 |
|
32 |
CYHS2200631国 |
2022/4/22 |
磷酸奥司他韦干糖浆 |
迪康倍(苏州)生物医药科技有限公司 |
2023年2月21日 |
|
33 |
CYHS2200830国 |
2022/6/3 |
西甲硅油乳剂 |
舒泰神(北京)生物制药股份有限公司 |
2023年2月20日 |
|
34 |
CYHS2300003国 |
2023/1/4 |
盐酸溴己新口服溶液 |
合肥国药诺和药业有限公司 |
2023年2月20日 |
|
35 |
CYHS2300004国 |
2023/1/4 |
盐酸溴己新口服溶液 |
合肥国药诺和药业有限公司 |
2023年2月20日 |
|
36 |
CYHS2101111国 |
2021/4/28 |
甲磺酸仑伐替尼胶囊 |
南京方生和医药科技有限公司 |
2023年2月17日 |
|
37 |
CYHS2201861国 |
2022/11/1 |
布洛芬注射液 |
山东罗欣药业集团股份有限公司 |
2023年2月17日 |
|
38 |
CYHS2201926国 |
2022/11/9 |
氟比洛芬凝胶贴膏 |
武汉法玛星制药有限公司 |
2023年2月17日 |
|
39 |
CYHS2000859国 |
2020/12/8 |
阿哌沙班片 |
福安药业集团宁波天衡制药有限公司 |
2023年2月13日 |
|
40 |
CYHS2101963国 |
2021/11/11 |
*粟罂**乙碘油注射液 |
上海葆隆生物科技有限公司 |
2023年2月13日 |
|
41 |
JYHS2101057国 |
2021/11/26 |
替莫唑胺胶囊 |
Lotus Support Services S.R.L.(注册代理机构:艾特士(上海)健康管理咨询有限公司) |
2023年2月13日 |
|
42 |
JYHS2101058国 |
2021/11/26 |
替莫唑胺胶囊 |
Lotus Support Services S.R.L.(注册代理机构:艾特士(上海)健康管理咨询有限公司) |
2023年2月13日 |
|
43 |
JYHS2200029国 |
2022/4/11 |
他克莫司胶囊 |
Biocon Pharma Limited;(注册代理机构:深圳市康哲生物科技有限公司) |
2023年2月13日 |
|
44 |
JYHS2200030国 |
2022/4/11 |
他克莫司胶囊 |
Biocon Pharma Limited;(注册代理机构:深圳市康哲生物科技有限公司) |
2023年2月13日 |
|
45 |
JYHS2200031国 |
2022/4/11 |
他克莫司胶囊 |
Biocon Pharma Limited;(注册代理机构:深圳市康哲生物科技有限公司) |
2023年2月13日 |
|
46 |
CYHS1501084 |
2015/9/2 |
注射用头孢美唑钠 |
湖南天圣药业有限公司 |
2023年2月6日 |
|
47 |
CYHS2101440国 |
2021/7/16 |
注射用阿奇霉素 |
南京海纳医药科技股份有限公司 |
2023年2月6日 |
|
48 |
CYHS2102141国 |
2021/12/6 |
注射用利福平 |
重庆华邦胜凯制药有限公司 |
2023年2月6日 |
|
49 |
CYHS2200048国 |
2022/1/12 |
艾曲泊帕乙醇胺片 |
常州制药厂有限公司 |
2023年2月6日 |
|
50 |
CYHS2200113国 |
2022/1/18 |
恩格列净片 |
天地恒一制药股份有限公司 |
2023年2月6日 |
|
51 |
CYHS2200603国 |
2022/4/18 |
利伐沙班片 |
宜昌人福药业有限责任公司 |
2023年2月6日 |
|
52 |
CYHS2200604国 |
2022/4/18 |
利伐沙班片 |
宜昌人福药业有限责任公司 |
2023年2月6日 |
|
53 |
JYHS2000045国 |
2020/11/25 |
盐酸鲁拉西酮片 |
MSN Laboratories Private Limited;(注册代理机构:南通万嘉医药科技有限公司) |
2023年2月6日 |
|
54 |
CYHS1401906 |
2016-04-08 |
低钙腹膜透析液(乳酸盐-G1.5%) |
上海长征富民金山制药有限公司 |
2023年1月31日 |
|
55 |
CYHS1401907 |
2016-04-08 |
低钙腹膜透析液(乳酸盐-G2.5%) |
上海长征富民金山制药有限公司 |
2023年1月31日 |
|
56 |
CYHS1401908 |
2016-04-08 |
低钙腹膜透析液(乳酸盐-G4.25%) |
上海长征富民金山制药有限公司 |
2023年1月31日 |
|
57 |
CYHS1800079国 |
2018/5/4 |
替米沙坦片 |
浙江华海药业股份有限公司 |
2023年1月31日 |
|
58 |
CYHS1800080国 |
2018/5/4 |
替米沙坦片 |
浙江华海药业股份有限公司 |
2023年1月31日 |
|
59 |
CYHS1800081国 |
2018/5/4 |
替米沙坦片 |
浙江华海药业股份有限公司 |
2023年1月31日 |
|
60 |
CYHS2000840国 |
2020/12/3 |
塞来昔布胶囊 |
常州制药厂有限公司 |
2023年1月31日 |
|
61 |
CYHS1800370国 |
2018/10/26 |
替米沙坦氢氯噻嗪片 |
浙江华海药业股份有限公司 |
2023年1月19日 |
|
62 |
CYHS1800371国 |
2018/10/26 |
替米沙坦氢氯噻嗪片 |
浙江华海药业股份有限公司 |
2023年1月19日 |
|
63 |
CYHS2101448国 |
2021/7/21 |
艾地骨化醇软胶囊 |
四川国为制药有限公司 |
2023年1月19日 |
|
64 |
CYHS2200238国 |
2022/1/29 |
盐酸阿比多尔片 |
武汉人福利康药业有限公司 |
2023年1月19日 |
|
65 |
JYHS1900001国 |
2019/1/17 |
阿立哌唑片 |
Aurobindo Pharma Limited(注册代理机构:阿乐滨度(上海)贸易有限公司) |
2022年12月30日 |
|
66 |
CYHS2102272国 |
2021/12/24 |
托拉塞米注射液 |
南京正科医药股份有限公司 |
2023年3月28日 |
|
67 |
CYHS2202027国 |
2022/11/22 |
西格列汀二甲双胍缓释片 |
越洋医药开发(广州)有限公司 |
2023年3月27日 |
三第三部分:抛转引玉,浅析不批准原因
3.1 短时间内给出不批准品种
在分析之前,我想跟大家分享一下, 2022年11月22日到2022年12月29日疫情影响,这期间不计算工作日。这个大家了解一下,具体可以见温馨提示。
《药品注册管理办法》中指出,药品审评需要200个工作日,而前60个工作日,CDE各部门会对品种进行立卷审查,存在严重不符合审评要求的,会直接给予不批准。笔者曾遇到因为不符合豁免临床理由,直接申请上市的情况。属于上述情况的有6个品种,具体见表3:
▲ 表3-较短时间给予不批准的品种清单
|
受理号 |
受理日期 |
药品名称 |
企业名称 |
签发日期 |
注册分类 |
备注 |
|
CYHS2201861国 |
2022/11/1 |
布洛芬注射液 |
山东罗欣药业集团股份有限公司 |
2023年2月17日 |
化3 |
CYHS2201969(2022年11月12日重新申报) |
|
CYHS2201926国 |
2022/11/9 |
氟比洛芬凝胶贴膏 |
武汉法玛星制药有限公司 |
2023年2月17日 |
化4 |
/ |
|
CYHS2201693国 |
2022/11/18 |
利丙双卡因乳膏 |
河北新张药股份有限公司 |
2023年3月1日 |
化4 |
CYHS2300553(2023年2月18日重新申报) |
|
CYHS2300003国 |
2023/1/4 |
盐酸溴己新口服溶液 |
合肥国药诺和药业有限公司 |
2023年2月20日 |
化3 |
CYHS2300640于2023.2.25日重新申报 |
|
CYHS2300004国 |
2023/1/4 |
盐酸溴己新口服溶液 |
合肥国药诺和药业有限公司 |
2023年2月20日 |
化3 |
CYHS2300641于2023.2.25日重新申报 |
|
CYHS2300310 |
2023/2/2 |
吸入用乙酰半胱氨酸溶液 |
济南康桥医药科技有限公司 |
2023年3月21日 |
化4 |
/ |
对于上述6个品种,根据《药品注册申请审评期间变更工作程序(试行)》:发生可能影响药品安全性、有效性和质量可控性的重大变更,申请人应当撤回原注册申请,补充研究后重新申报。发生除重大变更以外的其他涉及技术的变更,申请人应当在原注册申请的专业审评状态提出补充申请,该补充申请与原注册申请关联审评。如提交的补充申请,经审评确认属于重大变更的,补充申请不予批准,同时申请人应当撤回原注册申请,补充研究后重新申报。笔者猜测,这里很可能是发生了影响药品安全性、有效性和质量可控性的重大变更或者本身还需要提交补充技术资料等。
此外,两个品种可能存在较大的缺陷,笔者在这里大胆猜测一下如非临床研究不充分,质量与参比制剂Q1、Q2不完全一致等缺陷而导致不批准。
3.2 僵尸品种的清理
CDE也在对一些僵尸品种进行清理,涉及10个受理号,7个品种。这些品种大部分是15年之前申报的,其技术要求已经无法符合现在的审评要求,所以CDE及时做出审评,有些品种企业一直在进行研究,也需要CDE给予结论后,企业按照最新的技术要求进行审批。
|
受理号 |
受理日期 |
品名 |
生产企业 |
签发日期 |
注册分类 |
备注 |
|
CYHS1100644 |
2011/11/16 |
注射用头孢地嗪钠 |
悦康药业集团股份有限公司 |
2023年3月24日 |
原化6 |
/ |
|
CYHS1100645 |
2011/11/16 |
注射用头孢地嗪钠 |
悦康药业集团股份有限公司 |
2023年3月24日 |
原化6 |
/ |
|
CYHS1100780 |
2012/3/5 |
注射用磷酸氟达拉滨 |
连云港杰瑞药业有限公司 |
2023年3月7日 |
原化6 |
/ |
|
CYHS1200405 |
2012/8/20 |
复方氨基酸(15)双肽(2)注射液 |
西安力邦制药有限公司 |
2023年3月24日 |
原化6 |
/ |
|
CYHS1200593 |
2012/8/27 |
马来酸桂哌齐特注射液 |
成都华宇制药有限公司 |
2023年3月1日 |
原化6 |
/ |
|
CYHS1300034 |
2013/7/11 |
盐酸莫西沙星氯化钠注射液 |
浙江莎普爱思药业股份有限公司 |
2023年3月7日 |
原化6 |
/ |
|
CYHS1501084 |
2015/9/2 |
注射用头孢美唑钠 |
湖南天圣药业有限公司 |
2023年2月6日 |
原化6 |
/ |
|
CYHS1401906 |
2016/04/08 |
低钙腹膜透析液(乳酸盐-G1.5%) |
上海长征富民金山制药有限公司 |
2023年1月31日 |
原化6 |
CYHS2300883重新按化4申报,申报时间2023年3月24日 |
|
CYHS1401907 |
2016/04/08 |
低钙腹膜透析液(乳酸盐-G2.5%) |
上海长征富民金山制药有限公司 |
2023年1月31日 |
原化6 |
|
|
CYHS1401908 |
2016/04/08 |
低钙腹膜透析液(乳酸盐-G4.25%) |
上海长征富民金山制药有限公司 |
2023年1月31日 |
原化6 |
3.3 多个规格申报其中一个不批准
笔者在调研中发现10个品种,涉及多个规格,其中一个规格不批准,其他规格已经批准,或者仍在审评。具体如下:
|
受理号 |
受理时间 |
品种名称 |
企业名称 |
签发日期 |
注册分类 |
正在审评 |
已有结论 |
|
JYHS1900001国 |
2019/1/17 |
阿立哌唑片 |
Aurobindo Pharma Limited(注册代理机构:阿乐滨度(上海)贸易有限公司) |
2022年12月30日 |
化5.2 |
批准:JYHS1900002\JYHS1900004 不批准:JYHS1900003 |
|
|
CYHS2101415国 |
2021/7/8 |
注射用头孢曲松钠 |
湖南恒生制药股份有限公司 |
2023年3月21日 |
化3 |
CYHS2101414\CYHS2101413 |
|
|
CYHS2101448国 |
2021/7/21 |
艾地骨化醇软胶囊 |
四川国为制药有限公司 |
2023年1月19日 |
化4 |
批准:CYHS2101447 |
|
|
CYHS2101549国 |
2021/8/10 |
盐酸伐地那非片 |
广西强寿药业集团有限公司 |
2023年3月7日 |
化4 |
CYHS2101548 |
|
|
CYHS2101973国 |
2021年11月5日 |
玻璃酸钠滴眼液 |
苏州欧康维视生物科技有限公司 |
2023年3月13日 |
化4 |
批准CYHS2101972;CYHS2101898;CYHS2101897、CYHS210123 不批准:CYHS2101238 |
|
|
CYHS2200113国 |
2022/1/18 |
恩格列净片 |
天地恒一制药股份有限公司 |
2023年2月6日 |
化4 |
CYHS2200114 |
|
|
CYHS2200309国 |
2022/2/14 |
利奈唑胺干混悬剂 |
浙江普利药业有限公司 |
2023年3月7日 |
化3 |
CYHS2200308 |
|
|
CYHS2200603国 |
2022/4/18 |
利伐沙班片 |
宜昌人福药业有限责任公司 |
2023年2月6日 |
化4 |
CYHS2200602 |
|
|
CYHS2200555国 |
2022/4/19 |
他达拉非片 |
昆明源瑞制药有限公司 |
2023年3月7日 |
化4 |
CYHS2200556 |
|
|
CYHS2200631国 |
2022/4/22 |
磷酸奥司他韦干糖浆 |
迪康倍(苏州)生物医药科技有限公司 |
2023年2月21日 |
化3 |
CYHS2200630国 |
|
|
CYHS2102272国 |
2021/12/24 |
托拉塞米注射液 |
南京正科医药股份有限公司 |
2023年3月28日 |
化3 |
CYHS2102273 |
对于不同规格的品种,在选题立项时需要慎重考虑。不批准的原因,笔者无法查到品种申报的具体规格,推测原因有①比如利奈唑胺干混悬剂参比制剂公示平台中仅一个规格,而申请人申请了两个;②比如有一些规格是否满足临床的最小使用量;③比如规格工艺不一致,无法豁免BE等等。
3.4 公平性原则:
*粟罂**乙碘油注射液是一个比较有意思的品种,其申报时间见下图,恒瑞在2021年9月份获得批准文件,查询国家备案平台上的数据,该品种进行了240例的临床试验。而烟台鲁银药业有限公司并未进行临床申请,直接按4类进行申报,故笔者推测,出于公平性原则,国家给予不批准。

*粟罂**乙碘油注射液申报情况截图
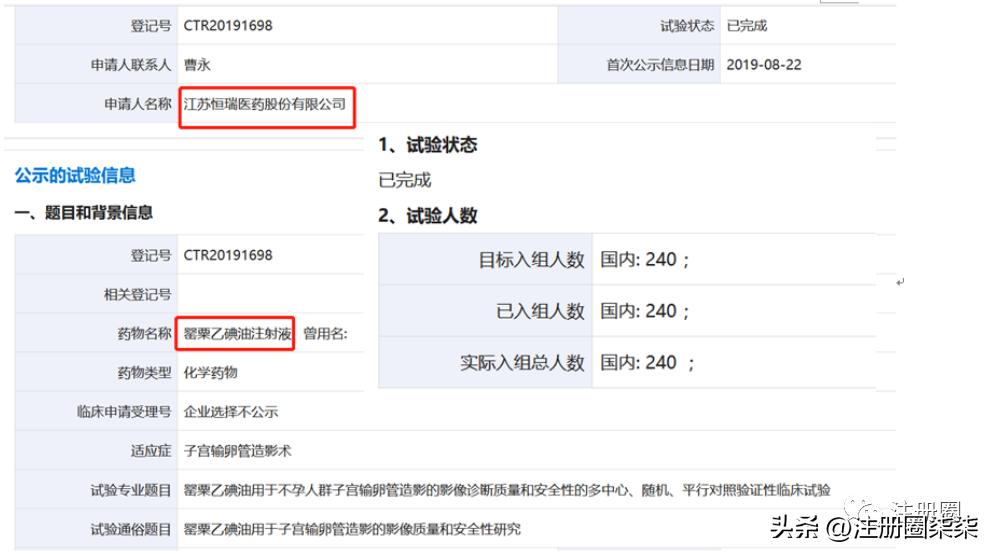
对于仿制药67个受理号,18个一致性评价来说,笔者分析是浅显的,也是不深刻的。但是笔者希望不批准品种是一次失败的教训,不批准的企业站在这个失败之母的肩上,我们能走得更远。期待大家继续深入挖掘。
声明:本文转载来源于公众号【注册圈】,文章版权归原作者所有,如若了解更多信息可自行前往查看。
原文链接:https://mp.weixin.qq.com/s/t1v8ZVsvUWsvwJZfXmy4FA