与急性冠脉综合征(acute coronary syndrome, ACS)相似,也存在急性主动脉综合征(acute aortic syndrome, AAS)的概念。与ACS相比,AAS比较少见,临床表现特异性差,可能导致诊断延迟甚至误诊,同时预后也更差。
作者:费金韬 郑博
机构:北京大学第一医院
本文为作者授权医脉通发布,未经授权请勿转载。
不断变化的主动脉
这是近期JACC: Case Reports上的一个案例。64岁男性,因首次发作压榨性胸痛前往急诊科就诊。简单体格检查后确定血流动力学稳定,体温正常,心血管查体没有明显异常。既往长期高血压(控制不佳),长期吸烟,家族史无异常。
为患者进行了心电图、经胸超声心动与冠脉造影检查,初步排除了ACS的可能性。随后为患者进行了主动脉CTA检查,显示主动脉弓远端与降主动脉存在壁内血肿,好在还未出现连通、溃疡与夹层(图A1/A2)。
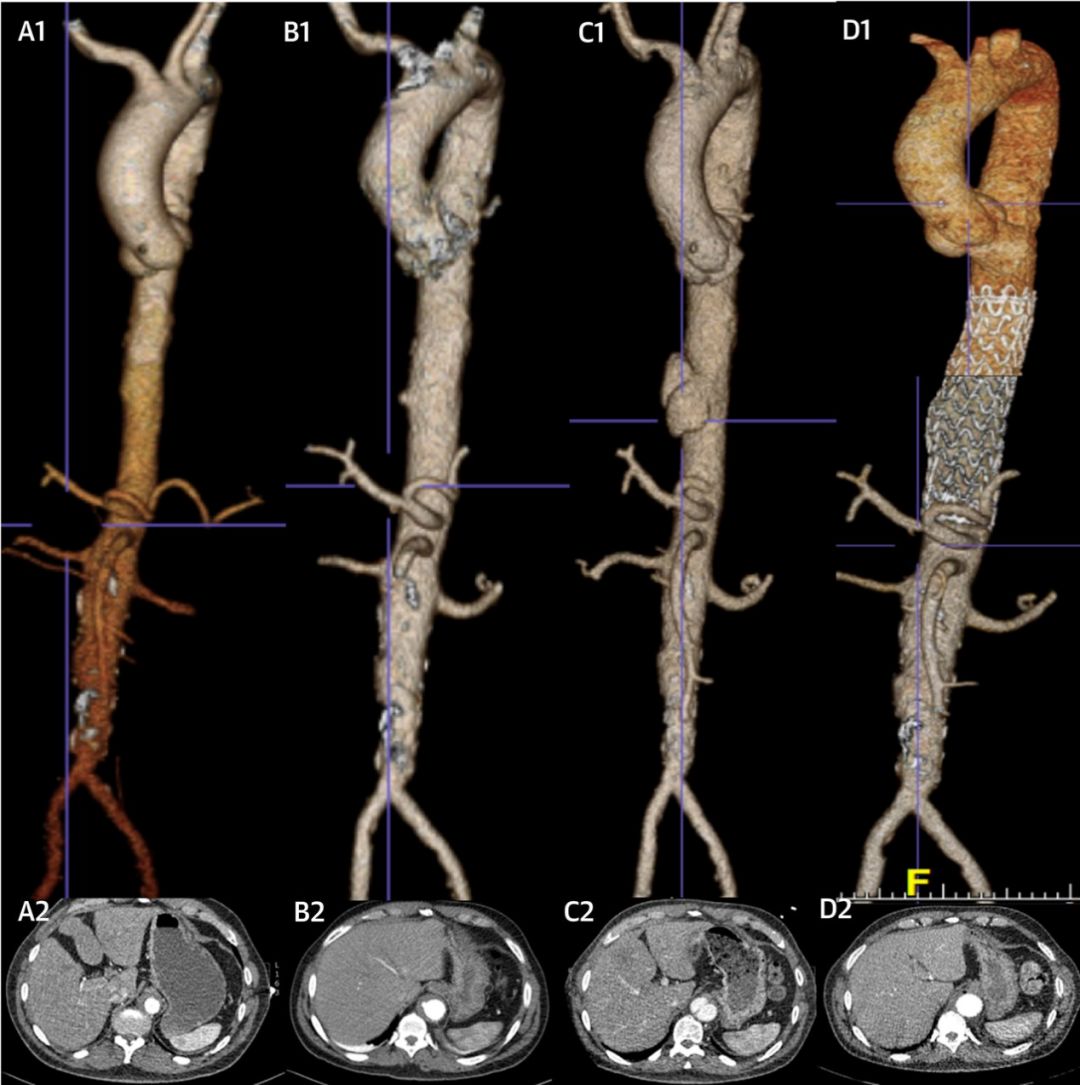
图1 入院(A)、7天(B)、30天(C)、术后(D)的主动脉CTA
入院后将血压控制于SBP 100-110mmHg左右,但患者在第7天时复查主动脉CTA仍发现降主动脉的壁内血肿进展为穿透性主动脉溃疡,并且怀疑已经出现主动脉夹层(图B1/B2)。在30天时再复查主动脉CTA,降主动脉处的穿透性溃疡进展为Stanford B型主动脉夹层与假性动脉瘤,但主动脉弓远端的壁内血肿自行吸收(图C1/C2)。在整个进展过程中患者一直没有症状。
考虑到保守治疗下降主动脉病变不断进展,于是在全麻下使用TEE与X线透视指导对患者进行了胸主动脉腔内修复术(thoracic endovascular aortic repair, TEVAR)。3个月后复查主动脉CTA显示主动脉夹层假腔内已经形成血栓,主动脉形态稳定(图D1/D2)。
AAS的分类
AAS是一组主动脉内膜、中膜完整性遭破坏的疾病,主要分为急性主动脉夹层(acute aortic dissection, AAD)、主动脉壁内血肿(intramural haematoma, IMH)与穿透性主动脉溃疡(penetrating aortic ulcer, PAU)。
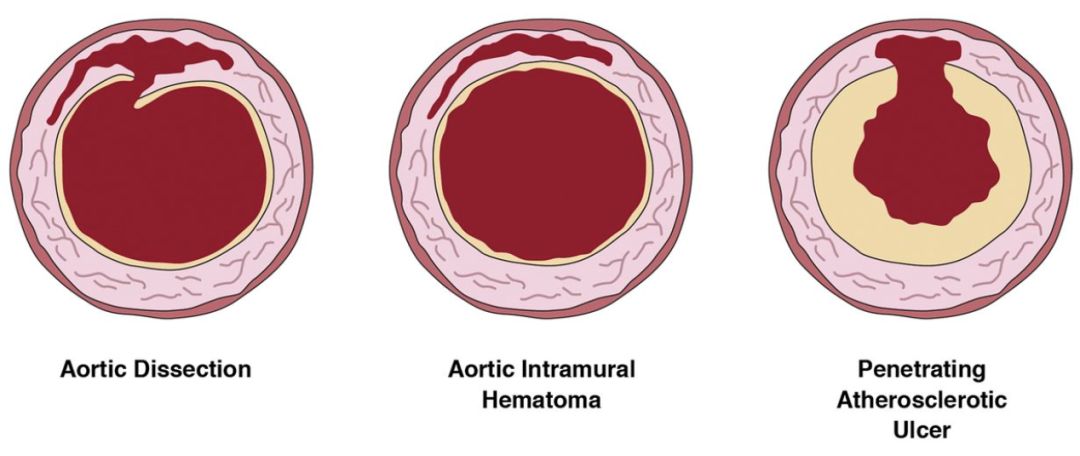
图2 AAD、IMH与PAU示意图
致命性胸痛病因中常提到的AAD大约可以占到AAS的80%,为内膜撕裂后血液进入血管壁形成“真腔”及“假腔”;其次IMH占约15%,是主动脉中膜形成血肿,但尚未出现内膜破裂;最少见的PAU占约5%,指主动脉粥样硬化斑块的溃疡从内膜延伸至中膜。正如上面的案例,几种AAS起病后并非一成不变,IMH与PAU可以逐渐进展为AAD。
哪些因素容易导致AAS?
导致AAS的原因可以分为2类:动脉壁压力增加或者动脉壁本身异常。
动脉壁压力增加最常见的原因是高血压,尤其是未控制的高血压,绝大多数患者存在高血压病史。药物、嗜铬细胞瘤导致的瞬时血压升高也会增加风险,另外还有主动脉缩窄、外伤、举重等增加主动脉压力的情况。
动脉壁异常可以来自马凡综合征、二叶主动脉瓣畸形等遗传原因,也可以来自动脉粥样硬化、动脉炎、动脉壁感染、心脏手术等非遗传原因。相比于老年患者更易受高血压影响,<40岁患者最重要的病因是马凡综合征及其它结缔组织疾病。导管介入操作也存在主动脉壁损伤的风险,好在风险比较低。
如何发现AAS?
借鉴AAD的概念,所有AAS根据累及部位不同可以分为A型(累及升主动脉)与B型(不累及升主动脉)。
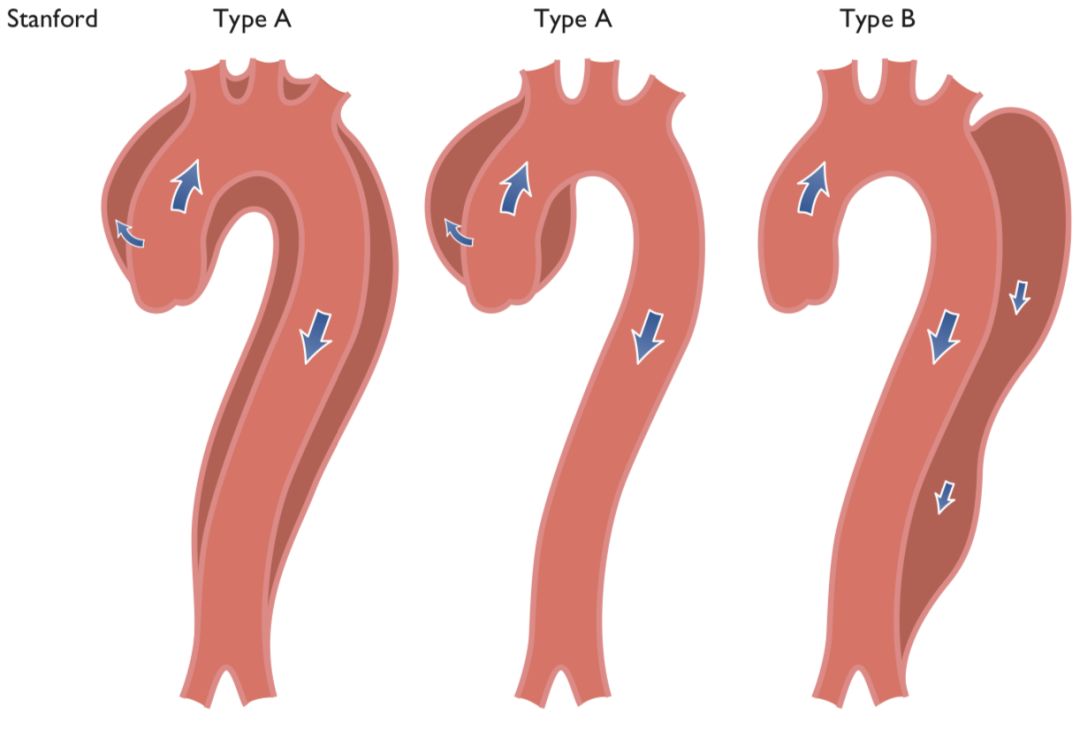
图3 Stanford分型
绝大多数AAS患者会突然出现剧烈撕裂样锐痛,A型患者常见胸痛,可以放射至颈部、下颌;B型患者常见背痛、腹痛。随着病变范围进展,疼痛顺着血管走行区域扩散,但这种游走性疼痛并不常见(<20%)。
约三分之一的患者可以出现上肢、下肢或颈动脉的脉搏弱,不过真正的肢体缺血很少见。平常较为关注的双侧血压不对称没有具体发生比例,但理论上不会很常见。与病变部位相关,心脏、脑部、小肠、肾脏都可能出现缺血,尤其值得注意的是10%-15%的AAD患者可以出现心肌缺血表现,A型AAD的患者甚至有25%会出现肌钙蛋白升高,很容易误诊为ACS而接受抗栓治疗。
累及主动脉根部时可以导致主动脉瓣反流,大约三分之一的患者可以听到主动脉瓣反流杂音,心脏听诊十分重要。主动脉瓣严重反流会导致急性左心衰与心源性休克,是除了主动脉破裂以外患者最常见的死亡原因。
实验室检查中D-二聚体地位很高,AAD患者D-二聚体迅速升至非常高的水平,发病1小时内就可以辅助诊断,敏感性很强但特异性不强。尽管敏感性接近100%,但在排除诊断时仍然存在缺陷,比如AAD假腔内很快形成血栓或者IMH、PAU患者D-二聚体就可以不升高。有一些新型生物标志物可以用于AAS的诊断,但目前尚未进入实际应用。
可靠的影像学检查包括UCG(TTE与TEE,尤其是TEE)、CTA与MRI。在国际主动脉夹层注册表中,62%的患者选择了CTA,32%的患者选择了TEE,只有1%的患者选择MRI。由于MRI检查时间长、在急诊不普及,对于AAS这种急症来说的确实用性不强,我们更关注什么情况下选择CTA、什么情况下选择UCG。
UCG的优点在于机器便携,可以进行床旁检查,更适合用于病情不稳定的患者。TTE可以观察主动脉根部及近端升主动脉,也可以评估主动脉瓣受累、心包压塞等并发症情况,但成像效果较差,同时无法看到更远处的主动脉病变。TEE可以更近距离观察胸主动脉,对于寻找夹层破口效果较好,且可以观察整个胸主动脉,另外能用于介入术中指导器械植入,但TEE检查时需要镇静。无论是TTE还是TEE都主要针对AAS中的AAD,观察IMH及PAU效果差。
对于病情仍较稳定的患者,CTA是首选。相比UCG,CTA对主动脉观察更完全,不受操作者水平影响(适合随访),可以发现主动脉分支受累情况,AAD、IMH及PAU均能观察。缺点为使用造影剂及X线辐射,但大多可以忽略。
AAS如何处理?
首先需要降低主动脉壁张力、阻止损伤进展,因此需要阿片类药物镇痛并严格控制血压、心率。AAS患者往往就诊时血压高、心率快,无论2017年ACC/AHA还是2018年ESC的高血压指南均认为应尽快将收缩压降至120mmHg以下、心率降至60bpm以下。最理想的降压药物为静脉β受体阻滞剂,为了尽快降压有时也会合用硝普钠或硝酸甘油。要避免单纯使用扩血管药物,因为会使交感激活。
对于A型AAS,无论是AAD、IMH还是PAU,均应紧急外科手术修复。在患者外科手术风险极高且病变解剖合适的情况下,必要时可以尝试介入治疗,但治疗效果不确定。
对于B型AAS,由于预后好于A型,最佳治疗策略尚不确定。如果患者主动脉病变没有明显进展且没有主动脉分支缺血表现,可以单纯进行药物治疗,也可以考虑尝试TEVAR或外科手术。如果患者病变持续进展,就像我们前文的病例,TEVAR或者外科手术的必要性很高,相对微创的TEVAR可以作为首选。
参考文献:
[1] Yuan X, Chan J S K, Mitsis A, et al. The Dynamic Evolution of Aortic Intramural Hematoma[J]. JACC: Case Reports. 2019; 1(4): 560-563.
[2] Authors/Task Force members, Erbel R, Aboyans V, et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC)[J]. European heart journal. 2014; 35(41): 2873-2926.
[3] Bossone E, LaBounty T M, Eagle K A. Acute aortic syndromes: diagnosis and management, an update[J]. European heart journal. 2017; 39(9): 739-749d.
[4] Baliga R R, Nienaber C A, Bossone E, et al. The role of imaging in aortic dissection and related syndromes[J]. JACC: Cardiovascular Imaging. 2014; 7(4): 406-424.
[5] Carroll B J, Schermerhorn M L, Manning W J. Imaging for acute aortic syndromes[J]. Heart. 2019.
[6] Clough R E, Nienaber C A. Management of acute aortic syndrome[J]. Nature Reviews Cardiology. 2015; 12(2): 103.