
阅读文章前辛苦您点下“关注”,方便讨论和分享,为了回馈您的支持,我将每日更新优质内容。

所研制的简易电化学H2O2传感器具有良好的可重复性。对于同一个传感器,当加入相同浓度的H2O2所对应的响应信号基本保持一致,且4次测试的RSD仅为1.58%,说明该传感器可重复性好,能够进行连续性检测,这对于现场检测具有非常重要的意义。再现性是另一个重要的传感器性能参数。
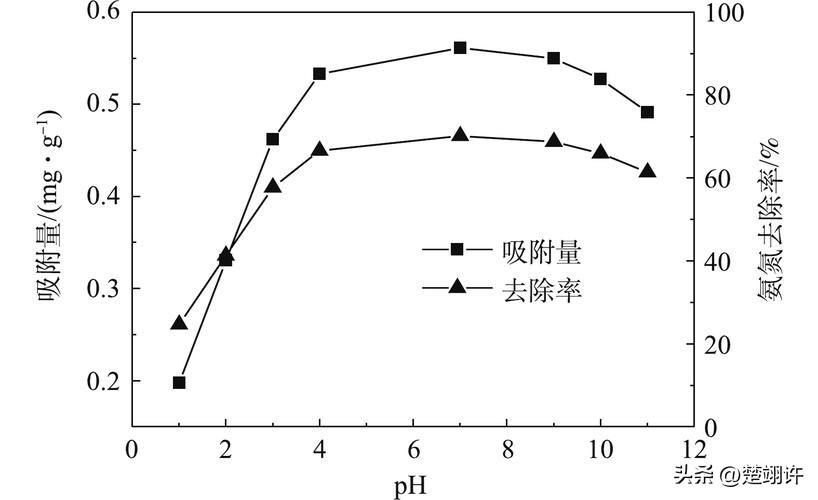
用相同的方法制作了三支电极用来检测相同浓度的H2O2,得到的测试结果的RSD为3.83%。因此,我们所研制的简易电化学H2O2传感器的再现性也是可以接受的。
所研制的简易电化学H2O2传感器在实际样品中的应用为了评估该传感器在实际应用中的可行性,将所研制的简易电化学H2O2传感器分别用来检测纯净水、自来水以及汾河水等实际样品。
在给定的实际水样中加入标准浓度为500M的H2O2,并对每个水样进行回收率研究。从表中我们观察到,该传感器在三种实际样品中的回收率较为理想,介于92.77%到101.02%之间。此外,研究结果进一步证明了该传感器对实际样品中的H2O2检测具有很好的特异性,可以将其应用于实际检测中。
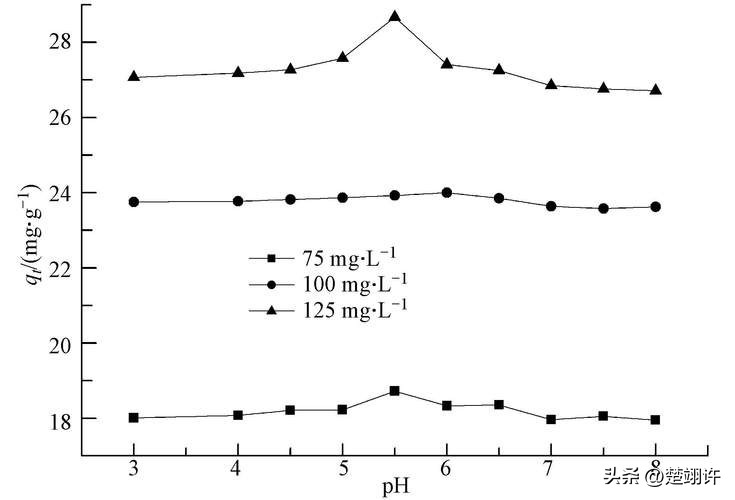
将自行设计合成的AgNPs@PA修饰到GCE上构建了一种简易的电化学H2O2传感器。(2)利用LSV法对比了GCE与AgNPs@PA/GCE的电化学响应,验证了AgNPs@PA/GCE对H2O2具备高电催化还原活性。
考察了AgNPs@PA负载量对修饰电极的电化学传感响应的影响;结果显示,当负载量为15L时,修饰电极对H2O2的电催化还原活性最大。
所研制的简易电化学H2O2传感器检测H2O2时,响应时间(~0.3s)极短,对H2O2的检测呈现良好的线性关系(R2为0.99832、0.99606),且线性范围(1−4M、4−6000M)较宽,灵敏度(~14934.9A/mM/cm2、~570.6A/mM/cm2)较高,检测限(1.5M)较低,呈现出良好的综合检测性能。
根据Randles-Sevcik方程计算出了AgNPs@PA/GCE的有效电极表面积,并进一步计算出参与电催化还原H2O2反应的电子数为2,从理论计算的角度验证了我们关于“H2O2的双电子还原”的假设。
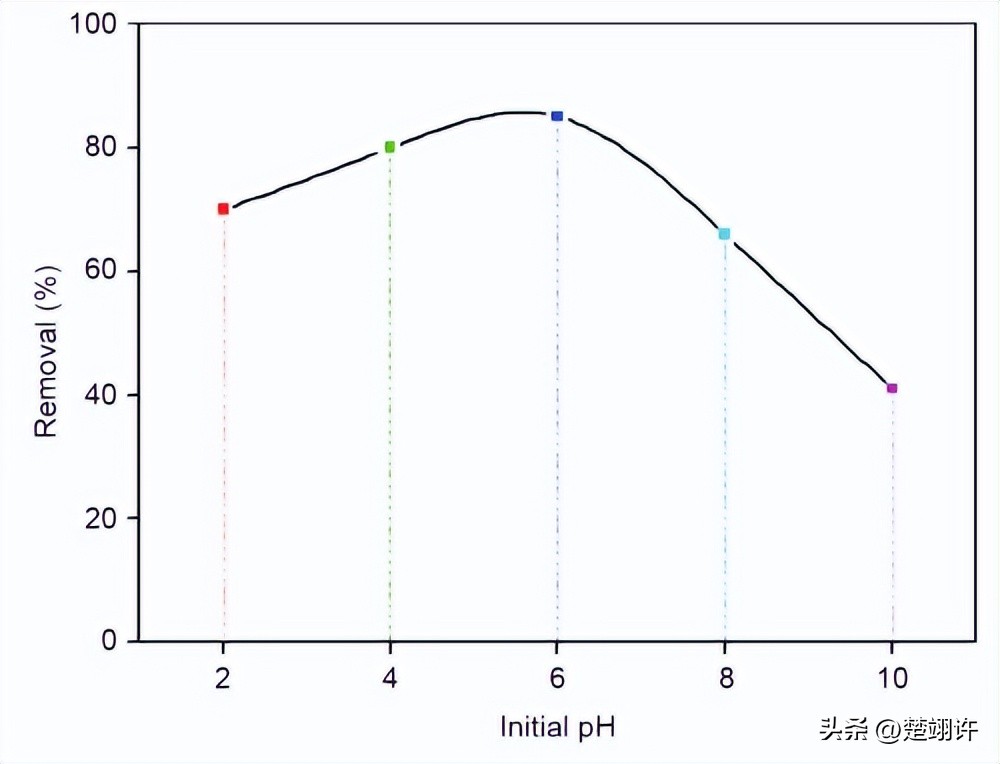
对AgNPs@PA/GCE电催化还原H2O2过程进行了全面的动力学分析,结果表明H2O2的还原反应处于准可逆状态;并在此基础上量化了H2O2还原的动力学参数。
测试表明,该传感器具备良好的选择性、抗干扰性、可重复性与再现性以及实际应用的可行性。第四章HCl/PA−CPAniH的制备及其在AgNPs@PA/GCE中的应用在上一章中,我们基于AgNPs@PA构建了一种由纳米材料直接修饰的简易电化学H2O2传感器。
这种传感器具有较低的检测限、较高的灵敏度且线性范围集中在较低浓度;但在线性关系、噪音以及检测范围方面有待进一步改善。然而,在电催化活性物质和无机电极材料之间选择一种合适的界面材料是提高传感器性能的关键,有望改善AgNPs@PA/GCE的部分性能。
近年来,聚丙烯腈/聚苯胺复合薄膜、壳聚糖/卡拉胶聚电解质复合材料等许多材料都被用于界面材料的研究, 其中导电聚苯胺水凝胶综合了有机导体和水凝胶的双重优异性能,从而引起了不少研究者的关注。
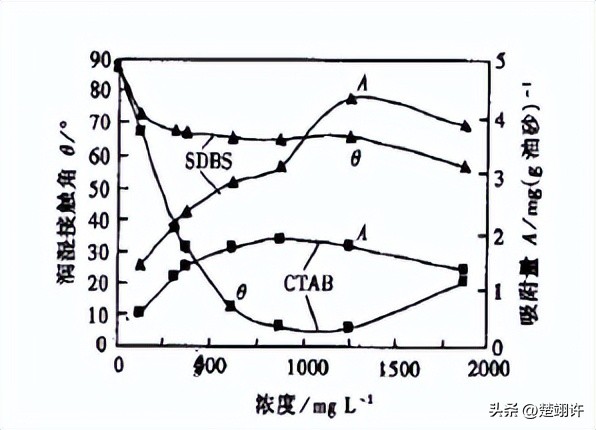
对于导电聚苯胺而言,利用质子酸掺杂半氧化半还原态的聚苯胺使其表现出良好的导电性成为将聚苯胺由绝缘态变为导电态的常用方法。目前,已有大量工作针对聚苯胺酸掺杂展开了研究。
特别是,PA因其对聚苯胺具备掺杂和交联的双重功能而受到众多研究人员的青睐。然而,这些有关聚苯胺酸掺杂的研究主要以单掺杂形式;有关共掺杂聚苯胺的研究工作,尤其是以HCl和PA为掺杂剂对聚苯胺进行共掺杂的研究更为少有。
在此,我们引入拥有掺杂和交联双重功能的PA以及具备强电离能力的HCl作为掺杂剂对聚苯胺进行共掺杂,而导电聚苯胺因为PA和HCl而引入大量亲水基团且形成相互交联的微观网络,呈现出水凝胶的特性。
本章以苯胺(Ani)为单体,以HCl和PA为掺杂剂,同时利用PA作为交联剂,在APS的引发下制备了CPAniH。在实验中,探究了HCl/PA共掺杂比例对CPAniH的影响,并对HCl/PA−CPAniH的合成过程及合成机理进行了分析、解释。
此外,本章还对HCl/PA−CPAniH的导电性能与导电机理、水凝胶方面特性进行了表征、研究。最后,我们利用HCl/PA−CPAniH作为基体,并负载AgNPs@PA从而构建了一种新的电化学H2O2传感器,并初步考察了该传感器对H2O2的检测性能。
实验药品及仪器实验所用原料及试剂如表HCl/PA−CPAniH的制备根据文献并作出适当改进来进行HCl/PA−CPAniH的合成。
具体步骤为:向10mL离心管中加入一定量(0、0.25、0.5、0.75mL)(0、0.25、0.5、0.75mmol)盐酸溶液(1M)和去离子水并保持总体积为2mL;混合均匀后,继续加入0.460mL(5mmol)经减压蒸馏提纯后的苯胺单体溶液;待溶液再次混匀后,加入0.921mL(1mmol)植酸溶液,并搅拌至混合溶液澄清透明,记为A液。
另外,向1.5mL离心管中加入1mL去离子水和0.286g(1.25mmol)过硫酸铵,并超声至完全溶解,记为B液。将A液、B液储存于4°C冰箱中至温度冷却后,迅速将A液、B液混合均匀并放置在4°C冰箱中反应10min。
最后,将形成的水凝胶在去离子水中透析3天,用以纯化所得水凝胶。4.2.3AgNPs@PA/(HCl/PA−CPAniH)/GCE的制备先按照与相同的步骤对GCE进行前处理。然后,将配制好的并储存于4°C冰箱中至温度冷却的A液、B液取出,并迅速将A液、B液混合均匀;在溶液颜色变为深绿色之前,取10L混合溶液滴涂于GCE表面。
随后,将该电极放置在4°C冰箱中反应10min,使其充分凝胶。接着将电极浸泡在35°C去离子水中30min,以除去低聚物和其他多余离子,得到(HCl/PA−CPAniH)/GCE。
修饰电极经过干燥后,取一定体积(10、15、20、25L)AgNPs@PA溶胶(浓度为212.1mg/L,根据ICP-OES测试)滴涂于修饰电极表面,并在室温、黑暗环境下干燥制得AgNPs@PA/(HCl/PA−CPAniH)/GCE。随后,将修饰电极在去离子水中浸泡一夜,以除去物理吸附。
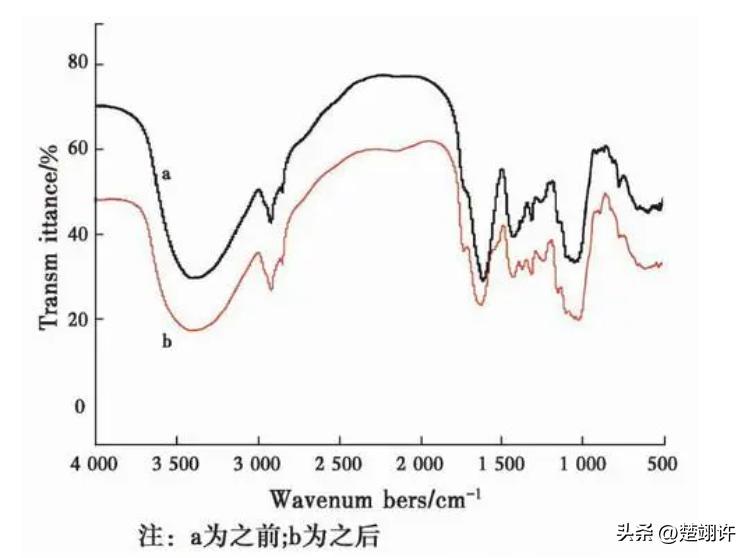
最后,在室温、黑暗环境下干燥,且在不用时存放在4°C冰箱中。测试与表征4.2.4.1傅里叶变换红外光谱仪(FT-IR)利用傅里叶变换红外光谱仪(TENSOR27)测试不同HCl/PA共掺杂比例下产物、所用Ani单体以及去掺杂后聚苯胺的*能官**团,波数范围为4000−400cm-1。
循环伏安法(CV)测试不同HCl/PA共掺杂比例下CPAniH在含和0.1MKCl的0.1MpH=7.4PBS溶液中进行CV测试;其中,电压扫描范围为-0.2−0.6V,扫速为50mV/s。
另外,(HCl/PA−CPAniH)/GCE在同样的电解液中以不同扫速进行CV测试;其中电压扫描范围为-0.2−0.6V,扫速依次为10、20、40、60、80、100、200mV/s。此外,AgNPs@PA/(HCl/PA−CPAniH)/GCE在同样的电解液中进行CV测试。
其中,电压扫描范围为-0.2−0.3V,扫速为50mV/s。接触角测试水接触角数值及其图片通过JC2000D型接触角测量仪测试。 每个样品重复测量四次并取其平均值。
扫描电子显微镜(SEM)及能谱仪(EDS)将冻干后的HCl/PA−CPAniH以及AgNPs@PA/(HCl/PA−CPAniH)样品粘贴在导电胶带上,并用扫描电子显微镜(S4800)观察其形貌结构及元素分布。
开路电位测定聚合时间以GCE为工作电极,铂丝电极为对电极,SCE为参比电极,将A液、B液充分混匀后用作电解液,利用开路电位测试聚合过程,并观察开路电位变化。
紫外可见分光光度计(UV-Vis)使用紫外可见分光光度计(UV-1800)测试HCl/PA−CPAniH合成过程中不同反应物、产物的吸收峰。
其中扫描范围为200−1000nm,扫描速度为中速,扫描步长为0.5nm。4.2.4.7电化学阻抗谱(EIS)测试裸GCE和(HCl/PA−CPAniH)/GCE在含和0.1MKCl的0.1MpH=7.4PBS溶液中进行EIS测试。
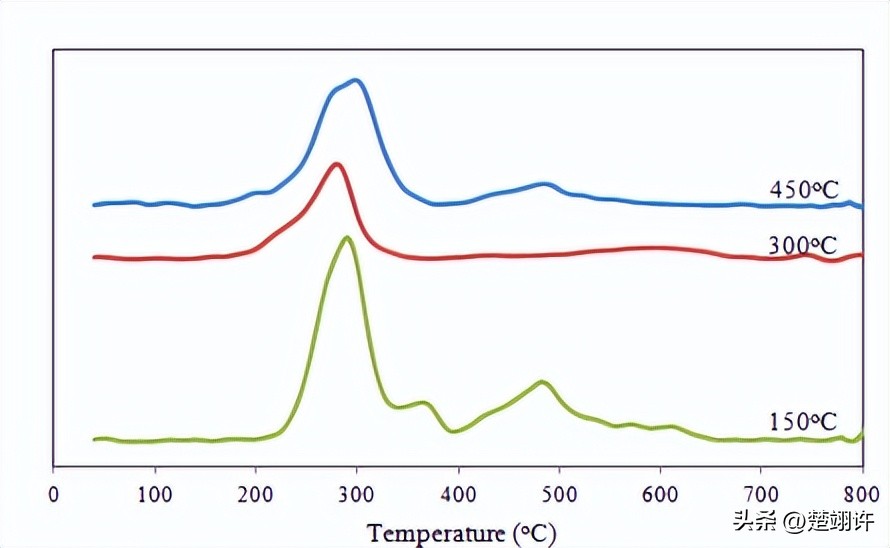
其中,频率范围为0.01Hz−100kHz,幅值为5mV,直流电位为0.199V。热重分析仪(TG)采用热重分析仪(STA449F3)对HCl/PA−CPAniH进行含水率测试。
其中测试温度范围为25−600°C,升温速率为10°C/min且在100°C下维持30minX射线衍射仪(XRD)利用X射线衍射仪(DX2700B)对干燥前后HCl/PA−CPAniH以及干燥后AgNPs@PA/(HCl/PA−CPAniH)进行了测试。
其中扫描范围为10−90°,扫描速度为4°/min。4.2.4.10N2吸附-脱附分析采用ASAP2460型N2物理吸附仪测试冻干后HCl/PA−CPAniH的BET比表面积。
样品在70°C真空环境中脱气12小时,并在-196°C下进行测试。电化学检测H2O2电化学测量在CS电化学工作站上采用三电极体系进行。
其中,以修饰后的GCE为工作电极,铂丝电极为对电极,SCE为参比电极。测试前,电解液需要用高纯N2鼓泡15min以除去其中的溶解氧。实验中给出的所有电压都是相对于SCE而言。
AgNPs@PA/(HCl/PA−CPAniH)/GCE对的电催化还原性能中的LSV测试修饰电极在含4mMH2O2的0.1MpH=7.4PBS溶液中进行LSV测试。测试时,电压扫描范围为-1−0V,扫描方向为负扫,扫速为100mV/s。
AgNPs@PA负载量对修饰电极的电化学传感响应的影响中的LSV测试不同体积(10、15、20、25L)的AgNPs@PA溶胶(浓度为212.1mg/L,根据ICPOES测试)所制得修饰电极在含4mMH2O2的0.1MpH=7.4PBS溶液中进行LSV测试。
测试时,电压扫描范围为-1−0V,扫描方向为负扫,扫速为100mV/s。 对H2O2的时间-电流测试在持续搅拌下施加-0.5VvsSCE的工作电位,向0.1MpH=7.4PBS溶液中每间隔100s逐次滴加H2O2来获得j-t曲线。
其中,搅速为250rpm,初始电位为-0.5VvsSCE,高电位为-0.5VvsSCE,低电位为-1VvsSCE,脉冲宽度为2000s,阶跃次数为1。HCl/PA共掺杂比例对CPAniH的影响实验中,我们探索了HCl与PA的4种物质的量比例(0:1、0.25:1、0.5:1、0.75:1)对CPAniH的影响,以寻求最佳比值。
参考文献:
[1]乔德亮,胡冰,曾晓雄.酶固定化及其在食品工业中应用新进展[J].食品工业科技,2008,1:304-308.
[2]渠文霞,岳宣峰.细胞固定化技术及其研究进展[J].陕西农业科学,2007,6:121-123