第五章 化工生产中的重要非金属元素
第一节 硫及其化合物
第1课时 硫和二氧化硫
一、硫
1.硫元素的位置、结构与性质
(1)硫元素位于元素周期表的第三周期、第ⅥA族,硫原子的最外电子层有6个电子,在化学反应中容易得到2个电子,形成-2价硫的化合物。
(2)与氧元素相比,得电子能力相对较弱,非金属性比氧的弱。故在富含O2的地表附近的含硫化合物中,硫常显+4价或+6价,而氧显-2价。
2.硫单质的物理性质
硫(俗称硫黄)是一种黄色晶体,质脆,易研成粉末。硫难溶于水,微溶于酒精,易溶于二硫化碳。
3.硫单质的化学性质
(1)氧化性表现为与金属、H2反应:
与Fe、Cu、H2反应的化学方程式分别为S+FeFeS、S+2CuCu2S、S+H2H2S,在这些反应,S均作氧化剂。
(2)还原性表现为与O2反应,其化学方程式为S+O2SO2,反应中S作还原剂。
点拨:(1)硫的氧化性较弱,与变价金属反应,生成低价态的金属硫化物。
(2)硫与氧气反应,无论氧气是否过量,只生成SO2。
二、二氧化硫
1.物理性质
二氧化硫是一种无色、有刺激性气味的有毒气体,密度比空气的大,易溶于水。在通常情况下,1体积的水可以溶解约40体积的SO2。
2.化学性质
(1)具有酸性氧化物的性质
①与H2O反应的化学方程式为SO2+H2O

H2SO3。
②与碱(如NaOH)反应的化学方程式为SO2+2NaOH===Na2SO3+H2O。
(2)还原性
SO2在一定条件下与O2反应的化学方程式为
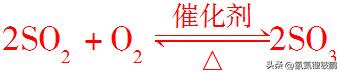
,生成的SO3也是酸性氧化物,与H2O反应的化学方程式为SO3+H2O===H2SO4。
(3)氧化性
SO2与H2S反应的化学方程式为SO2+2H2S===3S+2H2O。
(4)漂白性
①SO2通入品红溶液中,品红溶液褪色,加热时,溶液又变红色。
②SO2的漂白原理:SO2与某些有色物质生成不稳定的无色物质。这些无色物质容易分解又使有色物质恢复原来的颜色。
③应用:SO2在工业上应用于漂白纸浆、毛、丝等;此外SO2可用于杀菌消毒,还是一种食品添加剂。
3.可逆反应
(1)正反应:向生成物方向进行的反应。
(2)逆反应:向反应物方向进行的反应。
(3)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
点拨:可逆反应要注意“两同”:同一条件、同时进行。

SO2的漂白性

|
实验操作 |
实验现象 |
实验结论 |
|
用试管取2 mL SO2的水溶液,向其中滴入1~2滴品红溶液,振荡,观察溶液的颜色变化 |
溶液褪色 |
SO2或亚硫酸溶液能使品红溶液褪色 |
|
加热试管,注意通风,再观察溶液的颜色变化 |
溶液恢复原来的颜色 |
SO2与品红溶液结合生成的无色物质不稳定,加热易分解而使溶液恢复原来的颜色 |
1.若将Cl2通入品红溶液中,现象是什么?若再加热,又有什么现象?
提示:品红溶液褪色;再加热时,不能恢复原来的颜色。
2.若将等物质的量的SO2和Cl2同时通入品红溶液中,溶液的漂白性是“强强联合”吗?为什么?
提示:不是。若将等物质的量的SO2和Cl2相混合后,在溶液中发生反应:SO2+Cl2+2H2O===H2SO4+2HCl,从而失去漂白能力。

1.物质具有漂白性是指物质能使有机色素褪色,如新制氯水使有色花瓣褪色,SO2使品红溶液褪色等。SO2的漂白原理与新制氯水的不同,其原理是SO2能与某些有色物质结合生成不稳定的无色物质,这些无色物质容易分解而使有色物质恢复原来的颜色。
2.虽然SO2具有漂白性,但SO2使某些溶液褪色并不都是由于其漂白性。SO2使有机色素褪色属于漂白,SO2使无机物褪色不属于漂白。
SO2
3.SO2虽具有漂白性,但不能漂白指示剂。因此将SO2通入紫色石蕊溶液中,溶液只会变红,不会褪色。

SO2、CO2的性质比较与检验

1.分别将SO2、CO2通入澄清石灰水中,有什么现象?石灰水能鉴别SO2和CO2气体吗?
提示:澄清石灰水均变浑浊;若继续通入,浑浊均变澄清,不能用石灰水鉴别SO2和CO2气体。
2.举例说明可以用于检验SO2的试剂有哪些?
提示:品红溶液、溴水、酸性KMnO4等。
3.若要证明某气体是CO2和SO2的混合气体,需用哪些试剂?顺序如何确定?
提示:可用品红溶液、酸性KMnO4溶液和澄清石灰水。混合气体→品红溶液→酸性KMnO4溶液→品红溶液→澄清石灰水。

1.CO2与SO2的主要化学性质比较
|
物质 |
SO2 |
CO2 |
|
与碱反应 |
通入澄清石灰水中先生成沉淀,当气体过量时沉淀又溶解: Ca(OH)2+SO2===CaSO3↓+H2O CaSO3+SO2+H2O===Ca(HSO3)2 |
通入澄清石灰水中,先生成沉淀,当气体过量时沉淀又溶解: Ca(OH)2+CO2===CaCO3↓+H2O CaCO3+CO2+H2O===Ca(HCO3)2 |
|
氧化性 |
SO2+2H2S===3S+2H2O |
CO2+C2CO |
|
还原性 |
能被酸性高锰酸钾溶液、HNO3、NO2、氧气、氯水、溴水、碘水、Na2O2、H2O2、Ca(ClO)2等氧化剂氧化 |
无 |
|
漂白性 |
能与某些有色物质生成不稳定的无色物质而使有色物质褪色 |
无 |
2.鉴别SO2和CO2的常用方法
(1)用品红溶液鉴别:褪色的是SO2,不褪色的是CO2。
(2)用酸性KMnO4溶液鉴别:褪色的是SO2,不褪色的是CO2,原理:SO2被氧化。
(3)用溴水(或氯水)鉴别:褪色的是SO2,不褪色的是CO2,原理:Br2+SO2+2H2O===H2SO4+2HBr(或Cl2+SO2+2H2O===H2SO4+2HCl)。
(4)用H2S溶液鉴别:出现淡黄色浑浊的是SO2,无明显现象的是CO2,原理:2H2S+SO2===3S+2H2O。
3.SO2和CO2混合气体的检验和除杂方法
(1)除去CO2中混有的SO2,常将混合气体通过盛有饱和NaHCO3溶液的洗气瓶洗气。
(2)检验SO2和CO2混合气体中CO2的方法
―→―→―→―→
除去SO2 检验CO2
第2课时 硫酸 硫酸根离子的检验
一、硫酸
1.工业制硫酸的原理示意图
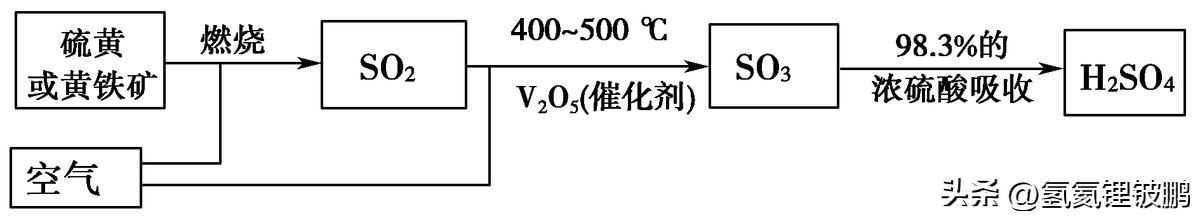
上述流程涉及的化学方程式为S+O2SO2或4FeS2+11O22Fe2O3+8SO2,2SO2+O2

2SO3,SO3+H2O===H2SO4。
2.硫酸的酸性
(1)电离方程式:H2SO4===2H++SO。
(2)写出稀硫酸与Zn、CuO、NaOH溶液、NaHCO3溶液反应的离子方程式分别为Zn+2H+===Zn2++H2↑、CuO+2H+===Cu2++H2O、H++OH-===H2O、HCO+H+===CO2↑+H2O。
3.浓硫酸的特性
(1)吸水性:浓硫酸能吸收存在于周围环境中的水分,可用于作干燥剂。
(2)脱水性:浓硫酸能将蔗糖、纸张、棉布和木材等有机物中的氢元素和氧元素按水的组成比脱去。
(3)强氧化性
①与金属Cu反应的化学方程式为2H2SO4(浓)+CuCuSO4+SO2↑+2H2O。反应中氧化剂是浓硫酸,还原剂是Cu,还原产物为SO2。
②与非金属的反应
浓硫酸与木炭反应的化学方程式为C+2H2SO4(浓)CO2↑+2SO2↑+2H2O。反应中氧化剂为浓硫酸,还原剂为C,还原产物为SO2。

实验制H2时,往往用稀硫酸而不用浓硫酸的原因是什么?
提示:浓硫酸具有强氧化性与金属反应时不产生H2而是产生SO2。
二、常见的硫酸盐
1.石膏(化学式为CaSO4·2H2O),加热失水变为熟石膏(化学式为2CaSO4·H2O),应用于制作各种模型和医疗用的石膏绷带,工业上还用于调节水泥的硬化速率。
2.硫酸钡又称“重晶石”或“钡餐”,用于生产其他钡盐的原料或消化系统X射线检查的内服药剂。
3.硫酸铜为白色粉末,CuSO4结合水后变为蓝色晶体胆矾(化学式为CuSO4·5H2O),又称蓝矾。无水CuSO4可用于检验H2O的存在。胆矾和石灰乳混合制成一种常用的农药——波尔多液。
三、硫酸根离子的检验
1.SO的检验
(1)实验探究:①稀硫酸或Na2SO4溶液现象为有白色沉淀生成,加盐酸后白色沉淀不溶解
②Na2CO3溶液现象为有白色沉淀生成,加盐酸后白色沉淀溶解且放出气体
(2)SO的检验一般思路:待测液无沉淀无气体生成白色沉淀生成
2.粗盐中可溶性杂质的除去
|
杂质 |
加入的试剂 |
化学方程式 |
|
Na2SO4 |
BaCl2溶液 |
Na2SO4+BaCl2===BaSO4↓+2NaCl |
|
MgCl2 |
NaOH溶液 |
MgCl2+2NaOH===Mg(OH)2↓+2NaCl |
|
CaCl2 |
Na2CO3溶液 |
CaCl2+Na2CO3===CaCO3↓+2NaCl |

浓硫酸的三大特性

探究1:蔗糖的脱水实验
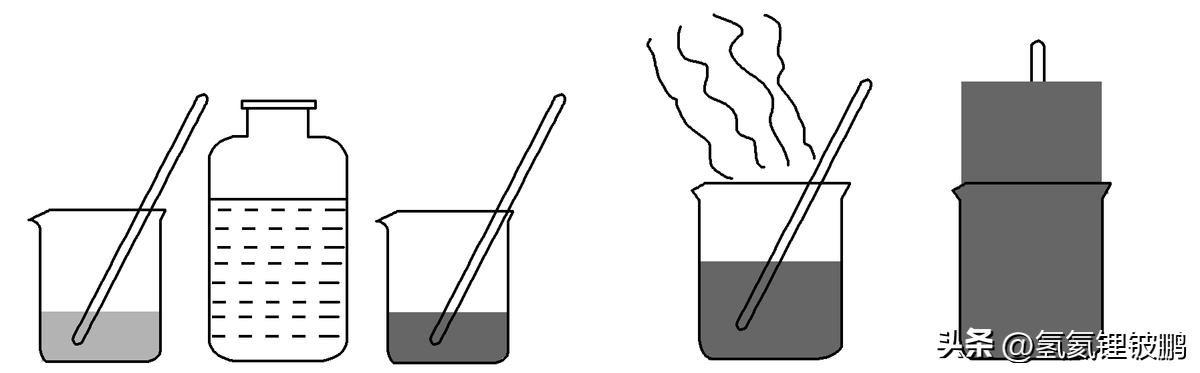
现象1:蔗糖逐渐变黑。原因是浓硫酸具有脱水性:
C12H22O1112C+11H2O。
现象2:蔗糖体积膨胀,形成黑色疏松多孔的海绵状的炭,并放出有刺激性气味的气体。原因是浓硫酸具有强氧化性,把C氧化成CO2,并有SO2气体放出。
探究2:浓硫酸与Cu的反应
[实验装置]
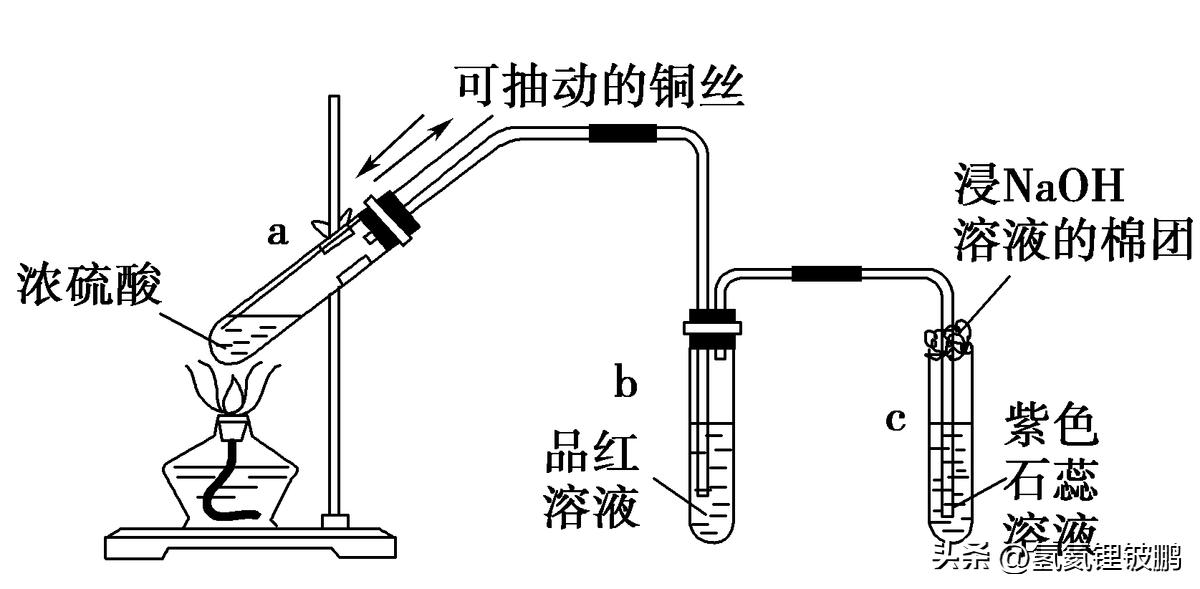
[问题思考]
1.a、b、c试管中的现象分别是什么?
提示:a中铜丝变黑,有气体逸出;b中品红溶液逐渐变为无色;c中溶液变为红色。
2.浸NaOH溶液棉团的作用是什么?写出反应的离子方程式。
提示:吸收尾气SO2,防止污染空气。
SO2+2OH-===SO+H2O。
3.b中现象说明了什么?
提示:浓硫酸与Cu共热生成SO2,同时说明SO2具有漂白性。
4.Cu与浓硫酸的反应中,浓H2SO4表现了什么性质?
提示:强氧化性和酸性。

浓硫酸的三大特性
|
吸水性 |
可吸收周围环境中的水分或结晶水 |
作吸水剂,可以用来干燥O2、N2、CO2、Cl2等气体,不能干燥碱性气体(NH3)和还原性气体(H2S、HI等) |
|
|
脱水性 |
将有机物中的氢、氧元素按水的组成比例脱去 |
如向蔗糖中加入浓硫酸:C12H22O1112C+11H2O |
|
|
强氧化性 |
与金属反应 |
常温 |
与Fe、Al接触,金属表面会生成一层致密的氧化膜而钝化 |
|
加热 |
大多数金属(Au、Pt除外)可被浓硫酸氧化,如Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O |
||
|
与非金属反应 |
可以和C、S、P等非金属反应,如:C+2H2SO4(浓)CO2↑+2SO2↑+2H2O |
||
|
与某些还原性物质(H2S、HI等)反应 |
H2S+H2SO4(浓)===S↓+SO2↑+2H2O |
||
点拨:(1)常温下与活泼金属反应(铁、铝除外)表现强氧化性和酸性,生成硫酸盐和SO2,硫酸变稀后,生成的气体为H2。
(2)加热与不活泼金属(如Cu)反应时,即使金属过量也不能使H2SO4完全反应,也不会产生H2。
(3)浓硫酸与金属反应时,既表现酸性又表现强氧化性,而与非金属反应时,只表现强氧化性。

SO的检验和粗盐的提纯

1.分析下列说法是否正确?不正确的说明原因。
(1)溶液中加入BaCl2溶液,若有白色沉淀生成,说明溶液中含有SO。
(2)溶液中加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,说明溶液中含有SO。
(3)溶液中先加入盐酸,无沉淀生成,再加BaCl2溶液有白色沉淀生成,说明溶液中含SO。
(4)溶液中加入硝酸酸化的Ba(NO3)2溶液,有白色沉淀生成,说明溶液含SO。
提示:(1)错误,Ag+、CO、SO等离子干扰。
(2)错误,Ag+干扰。
(3)正确。
(4)错误,SO干扰。
2.如何除去NaCl溶液中的Ca2+?
提示:溶液中加入过量的Na2CO3溶液,过滤,再向滤液中加入适量稀盐酸,调节溶液pH为中性。

1.SO的检验
(1)一般思路
待检验溶液无明显现象(若有沉淀,则静置后取上层清液)观察有无白色沉淀产生(若有白色沉淀产生,则说明待检验溶液中含有SO;若无白色沉淀产生,则说明待检验溶液中不含SO)。
(2)排除干扰
①Ag+干扰:用盐酸酸化可排除Ag+的干扰。
②CO、SO、PO干扰:BaCO3、BaSO3、Ba3(PO4)2都是白色沉淀,与BaSO4白色沉淀不同的是,这些沉淀可溶于强酸中,因此检验SO时,必须先用盐酸酸化。不能用硝酸酸化,因在酸性条件下,SO、HSO等会被溶液中的NO氧化为SO,从而干扰检验结果。
2.除去粗盐中可溶性杂质的步骤
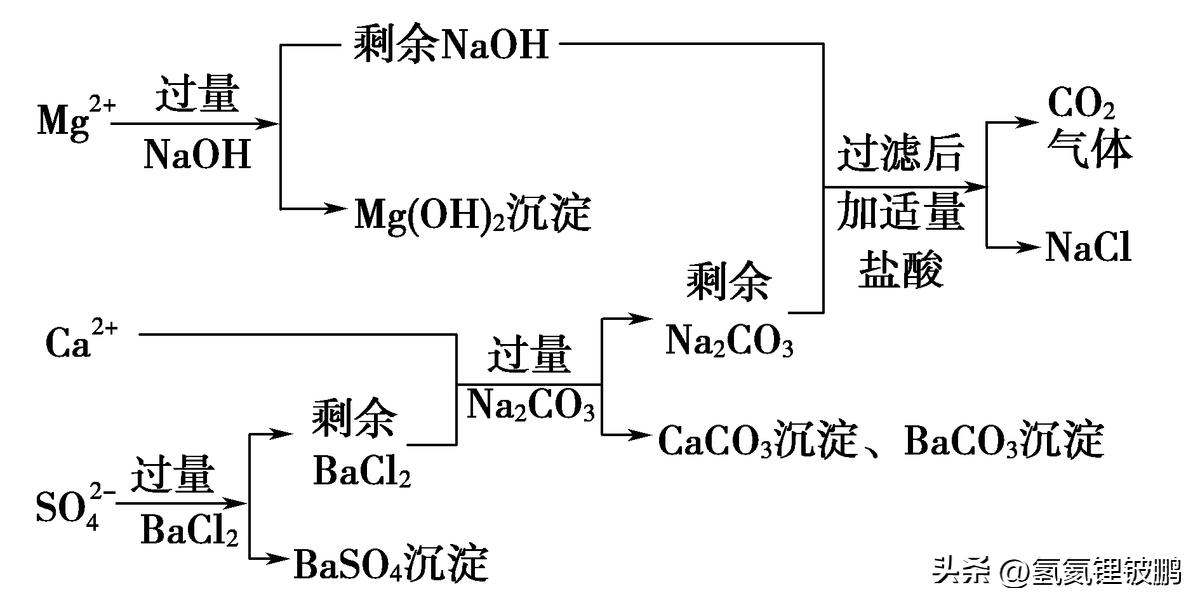
点拨:粗盐提纯时为使杂质离子完全除去,要加入过量的试剂,后续试剂要能够将前面所加的过量试剂除去,由此可知碳酸钠溶液要在氯化钡溶液之后加入,碳酸钠既要除去杂质钙离子还要除去过量的钡离子。
物质的分离和提纯的“三个必须”和“四个原则”
(1)三个必须

①除杂试剂必须稍过量。
②过量试剂必须除尽,且容易除去。
③除杂途径选最佳,有多种杂质时除杂顺序必须合理。
(2)四个原则
第3课时 不同价态含硫物质的转化
一、自然界中硫的存在和转化
1.硫的存在
(1)在自然界中硫元素主要以化合态形式存在,如组成生命体的蛋白质中含有硫。在岩层深处和海底的无氧环境下,通常以硫化物的形式存在,如黄铁矿(FeS2)、黄铜矿(CuFeS2)。在地表附近,硫化物转化为硫酸盐,如石膏(CaSO4·2H2O)、芒硝(Na2SO4·10H2O)等。
(2)游离态的硫存在于火山口附近或地壳的岩层中。
2.硫的转化
火山口附近的硫单质会被大气中的氧气氧化成二氧化硫,二氧化硫可被进一步氧化成三氧化硫。
二、常见硫的价态及转化
1.硫元素常见的化合价有-2、0、+4和+6,可以通过氧化还原反应实现不同价态含硫物质的相互转化。利用氧化剂,可将硫元素从低价态转化到高价态;利用还原剂,可将硫元素从高价态转化到低价态。
2.硫的不同价态所对应的常见化合物
(1)含有-2价硫的物质有酸:H2S,盐:Na2S、NaHS等。
(2)含有+4价硫的物质有氧化物:SO2 ,酸:H2SO3,盐:Na2SO3、NaHSO3等。
(3)含有+6价硫的物质有氧化物:SO3,酸:H2SO4,盐:Na2SO4、NaHSO4等。

含硫物质之间的转化

1.下图是人们总结的不同价态硫元素的转化关系,请分析各种元素在氧化还原反应中表现氧化性还是还原性,并举例说明。
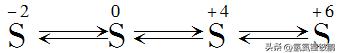
提示:只表现还原性,只表现氧化性,、既表现氧化性又表现还原性。举例略。
2.以硫元素为基础原料,合成硫酸,请设计合成路线。
提示:SSO2SO3H2SO4或
SSO2H2SO3H2SO4。

1.不同价态硫元素之间的相互转化
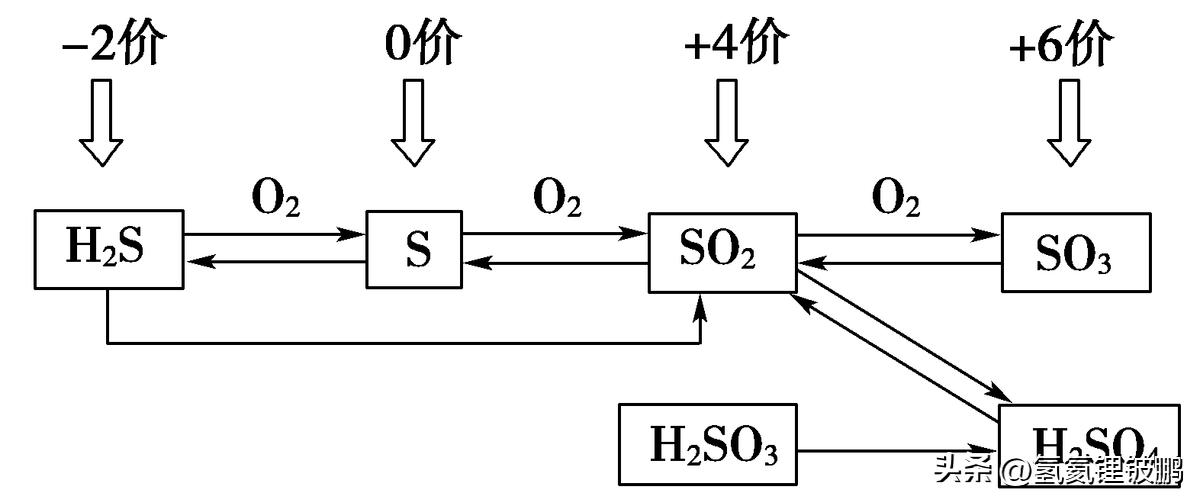
不同价态硫元素之间的相互转化主要通过氧化还原反应实现。上述转化中,从左到右,硫元素化合价升高,需加入氧化剂。从右到左,硫元素化合价降低,需加入还原剂。
2.相同价态硫元素之间的转化
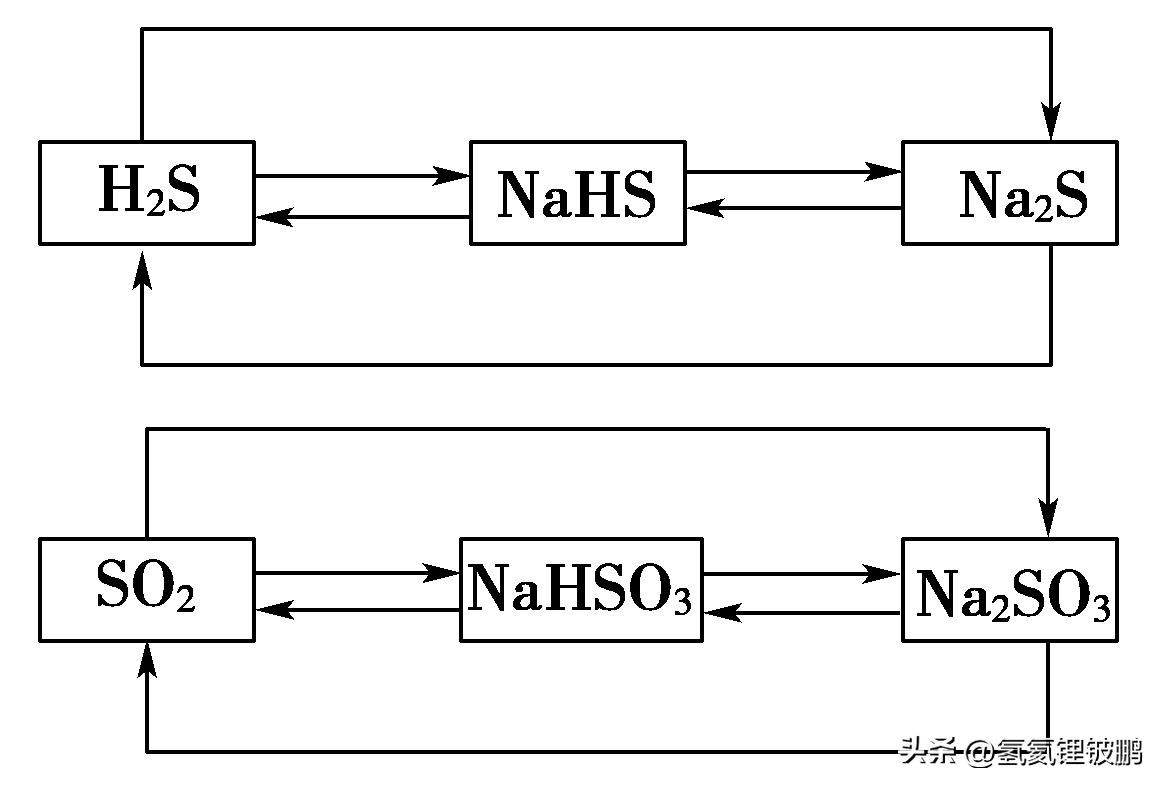
以上两种转化关系均属于相同价态硫元素之间的转化,从左到右的转化,加入碱可以实现;从右到左的转化,加入酸可以实现。
微专题1 常见漂白剂的归类分析
三类漂白剂的比较
|
类型 |
原理 |
举例 |
特点 |
备注 |
|
氧化型 |
将有机色质内部“生色团”破坏掉 |
HClO、NaClO、Ca(ClO)2、Na2O2、H2O2、O3等 |
不可逆、持久 |
无选择性 |
|
加合型 |
与有机色质内部“生色团”化合成无色物质 |
SO2 |
可逆、不持久 |
有选择性 |
|
吸附型 |
将有色物质吸附而褪色 |
活性炭 |
物理变化 |
吸附色素 |
点拨:当Cl2与SO2(体积比为1∶1)混合后通入品红溶液时,品红溶液不褪色,因为SO2+Cl2+2H2O===H2SO4+2HCl。