|
课前延伸学案 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
课题 |
第3章第1节 碳的多样性(第1课时) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
课型 |
新授课 |
备课人 |
XXX |
单位 |
XXXXXX |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
预习 目标 |
1、了解碳元素在自然界的存在形态。 2、了解同素异形体的含义。 3、初步了解金刚石、C60 、石墨的结构。 4、掌握Na2CO3和NaHCO3的主要性质。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
回 顾 预 习 回 顾 预 习 |
【复习巩固】 1、向澄清石灰水中通入少量二氧化碳气体有何现象?你能写出该反应的化学方程式吗? 2、你还记得碳酸钙的主要化学性质有哪些吗?你能写出这些反应的化学方程式吗?(提示:与盐酸反应、高温分解) 【自主预习】 阅读教材内容,试试能不能解决下列问题: 1.什么是同素异形体?到现在为止,你能列举出哪些同素异形体呢? 2.你能完成下表的空白吗?
填完表格后思考:表中的三种物质是什么关系呢?你是依据什么得出该结论的呢? 阅读教材内容,试试能不能解决下列问题: 1、你能在下列空白处写出该物质或者其主要成分的化学式吗? 一氧化碳(______)、二氧化碳(______)、碳酸(______)、碳酸钠(______)、碳酸氢钠(______)、大理石(______)、方解石、白云石、菱锌矿(______)、菱铁矿(______)、菱镁矿(______ )。 2、什么是碳酸盐?什么是碳酸氢盐?请你写出你所知道的碳酸盐、碳酸氢盐的名称。 3. 你能通过完成下表空白,掌握碳酸钠和碳酸氢钠的主要性质吗? (有关反应用化学方程式表示)
4.你能列举出生活中常见的有机化合物吗? 完成上述问题后认真体会“碳元素形成的单质及其化合物的多样性”。 课下阅读化学前沿栏目《C60与碳纳米管》了解C60与碳纳米管在生产生活中的广阔的发展前景。 【自我评估】 1、向下列物质分别滴加盐酸时,会产生相同气体的是( ) ①大理石 ②钟乳石 ③ 锅垢 ④贝壳 ⑤蛋壳 A.①② B.④⑤ C.①②③ D.①②③④⑤ 2、下列物质的化学名称、化学式和俗名一致的是( ) A、碳酸钙 CaCO3 石灰石 B、氢氧化钠 NaOH 纯碱 C、碳酸钠 Na2CO3 苏打 D、碳酸氢钠 NaHCO3 苏打 3、在“勇气”号、“机遇”号火星探测器的表面覆盖有石墨瓦,这是主要利用了石墨( ) A、具有导电性、防辐射 B、密度小、减轻机身重量 C、熔点高、化学性质稳定 D、硬度小、有润滑作用 4、请你写出下列反应的离子方程式 ⑴Na2CO3与盐酸_____________ ⑵NaHCO3与盐酸_____________ ⑶NaHCO3与NaOH溶液_____________ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
我 的 困 惑 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
答案:1、D 2、C 3、D4、 (1)CO32—+2H+=H2O+CO2↑ (2)HCO3—+H+=H2O+CO2↑(3)HCO3—+OH—= CO32—+ H2O

|
课堂探究 |
|||||||||||||||
|
课题 |
第3章第1节 碳的多样性(第1课时) |
||||||||||||||
|
课型 |
新授课 |
备课人 |
XXX实验中学 XXX |
||||||||||||
|
教学 目标 |
1、了解碳元素在自然界的存在形态。 2、理解同素异形体的含义。 3、初步了解金刚石、C60 、石墨的结构。 4、掌握Na2CO3和NaHCO3的主要性质。 |
||||||||||||||
|
合作探究 |
|||||||||||||||
|
一、多种多样的碳单质 [ 问题探究 ] 1、金刚石和石墨同是碳元素组成的单质,它们的物理性质相同吗?为什么?化学性质呢? 2、你有方法证明金刚石、石墨均是由碳元素组成的吗?它们彼此之间是什么关系呢? 1797年英国化学家钱南为了测出金刚石的成分,做了一个非常昂贵的实验。他将金刚石放在密闭的、充满氧气的箱子里进行燃烧(箱子是纯金制的),结果却令人非常意外—箱子里的气体成分竟然是二氧化碳。 3、你觉得理解“同素异形体”这一概念的关键点在哪里呢? 【随堂诊断1】 下列叙述中,正确的是 ( ) A、C60是新发现的一种化合物 B、氧气和臭氧互为同素异形体 C、石墨转变为金刚石的反应属于氧化还原反应 D、由碳元素组成的物质一定是纯净物 二、广泛存在的含碳化合物(回顾碳酸钙的性质) [ 活动探究 ]预测碳酸钠和碳酸氢钠有哪些化学性质并设计实验探究 提供的试剂:碳酸钠、碳酸氢钠、盐酸、澄清石灰水、CaCl2溶液、NaOH 溶液 提供的仪器:试管、胶头滴管、酒精灯、铁架台等 比较碳酸钠和碳酸氢钠与盐酸反应快慢 实验记录: 实验结论: [小结] 碳酸钠和碳酸氢钠的主要化学性质有: 【随堂诊断2】 判断下列反应能否发生,能反应的写出相关离子方程式,不能反应的说明理由。
[ 问题探究1 ]如何实现Na2CO3和NaHCO3之间的相互转化呢? [ 问题探究2 ]如何鉴别一瓶无色溶液是Na2CO3溶液还是NaHCO3溶液呢? |
|||||||||||||||
|
【本节小结】 |
|||||||||||||||
|
【当堂检测】 |
|||||||||||||||
|
1、金刚石、石墨和C60的性质有所不同,原因是( ) A、构成原子不同B、各自的原子排列方式不同C、具有不同的几何外形D、硬度不同 2、以下物质的主要成分属于碳酸盐的是( ) ①纯碱②蛋白质③大理石④方解石⑤胡萝卜素⑥菱铁矿⑦淀粉 A、只有①②④⑥B、只有①②③④⑥⑦C、只有①③④⑤D、只有②③④⑤ 3、为了除去混在Na2CO3粉末中的少量NaHCO3,最合理的方法是( ) A、加热B、加NaOH溶液C、加盐酸D、通入足量CO2 4、除去NaHCO3溶液中少量Na2CO3的方法是( ) A、加热B、加NaOH溶液C、加盐酸D、通入足量CO2 5、下列反应的离子方程式正确的是( ) A、Na2CO3溶液与Ba(OH)2溶液反应:CO32-+Ba2+=BaCO3↓ B、NaOH溶液与Ca(HCO3)2溶液反应:HCO3-+OH-=CO32-+H2O C、NaHCO3溶液与盐酸反应:CO32-+2H+=CO2↑+H2O D、NaHCO3溶液与CaCl2溶液反应:CO32-+Ca2+=CaCO3↓ 答案:1B 2C 3A 4D 5A |
|||||||||||||||
|
课后延伸 |
|||||||||||||||
|
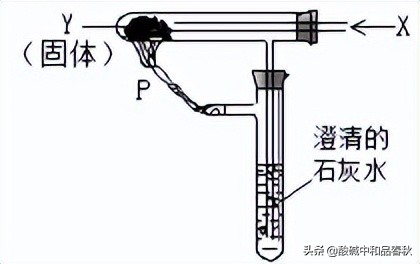
1. 下列说法不正确的是( ) A.金刚石和石墨都是由碳元素组成的纯净物 B.石墨能导电,金刚石不能导电 C.造成金刚石和石墨物理性质差异的主要原因是组成两种物质的元素不同 D. C60是一种新型化合物 2.跟Na、Na2O、 Na2O2、 NaOH 、Na2CO3 、NaHCO3六种物质都能反应的是( ) A. 水 B.二氧化碳 C.硫酸 D氢氧化钙溶液 3.某二价金属的碳酸盐和碳酸氢盐的混合物与足量盐酸反应,消耗H+和产生二氧化碳的物质的量之比为5:4。该混合物中碳酸盐和碳酸氢盐的物质的量之比为( ) A.1:3 B.2:3 C.3:4 D.4:5 4. 关于Na2CO3和NaHCO3的下列说法中正确的是 ( ) A.Na2CO3不如NaHCO3易溶于水 B.NaHCO3比Na2CO3稳定 C.石灰水能和NaHCO3反应,不于Na2CO3反应 D.Na2CO3和NaHCO3与等物质的量浓度的盐酸反应,NaHCO3产生的气泡快 5.按如图装置持续通人气体x,并在管口P处点燃,结果使澄清石灰水变浑浊,则X、Y可能是( )
A.H2和NaHCO3 B.CO和Na2CO3 C.CO和CuO D.H2和Fe2O3 6.现有25mL 2mol/L的Na2CO3 溶液和75mL 1mol/L的稀盐酸,①将Na2CO3溶液缓缓滴加到盐酸中 ②将稀盐酸缓缓滴加到Na2CO3溶液中,在标准状况下产生的气体是( ) A. 均为0.84L B. 均为0.56L C. ①>② D. ①<② 7.碳酸氢钠受热容易分解为碳酸钠。现加热5.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31g,则原混合物中碳酸钠的质量为 ( ) A.3.38g B.4.58g C.4.16g D.4.41g 8.为除去碳酸钠溶液中的碳酸氢钠,可采用的方法为_____________ ,该反应的离子方程式为_____________ ;为除去碳酸氢钠溶液中的碳酸钠可采用的方法为_____________ ,该反应的离子方程式为_________________。 |
|||||||||||||||
友情提示:
需要本头条号资料的友友,私信,无偿提供相关word版、课件、视频[握手]