 备战
2022
年高考化学-工艺流程专项复习系列
备战
2022
年高考化学-工艺流程专项复习系列
专项 4 -温度条件的控制
一.升高温度
1.促进某些离子的水解,如高价金属阳离子,易水解的阴离子
【练习 1 】目前世界上新建的金矿中约有 80% 都采用氧化法提金。某工厂利用锌冶炼渣回收金、银等贵金属的流程如下图所示 :
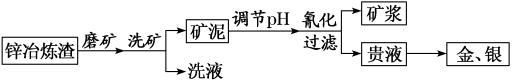
已知 HCN 有剧毒,其 Ka(HCN)=5×10 -10 , Au + +2CN - =[Au(CN) 2 ] - 平衡常数 KB=1×10 38
“氰化 ” 环节中,金的溶解速率在 80℃ 时达到最大值,但生产中控制反应液的温度在 10-20℃ ,原因是 :___________________________( 答一点即可 ) 。
【答案】温度的升高,促进了氰化物的水解,增加了 HCN 的挥发速度;温度的升高, Ca(OH) 2 的溶解度减小,部分碱从溶液中析出。
【练习 2 】某化工厂 “ 用含 NiO 的废料 ( 杂质为 Fe 2 O 3 、 CaO 、 CuO 等 ) 制备羟基氧化镍 (2NiOOH·H 2 O)的工艺流程如图:
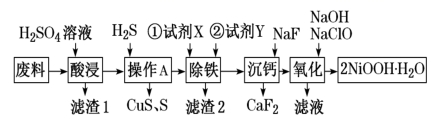
如图是酸浸时镍的浸出率与温度的关系,则酸浸时合适的浸出温度是 ____________℃ ,若酸浸时将温度控制在 80℃ 左右,则滤渣 1 中会含有一定量的 Ni(OH) 2 ,其原因可能是 _________________________ 。
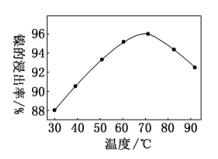
【答案】 70 随着温度的升高, Ni 2+ 水解程度增大,从而形成一定量的 Ni(OH) 2 沉淀
【解析】由图可知当温度在 70° 左右时镍的浸出率较高,故酸浸时适宜的温度为 70°C ; Ni 2+ 能水解,生成 Ni(OH) 2 ,升温能促进水解,所以 80℃ 左右滤渣 1 中会含有一定量的 Ni(OH) 2 。
【练习 3 】氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于 H 2 SO 4 、 HNO 3 和醇,微溶于水,可溶于浓盐酸和*水氨**,在潮湿空气中易水解氧化成绿色的碱式氯化铜 [Cu 2 ( OH ) 3 Cl]。以海绵铜(主要成分是 Cu 和少量 CuO )为原料,采用硝酸铵氧化分解技术生产 CuCl 的工艺过程如下:
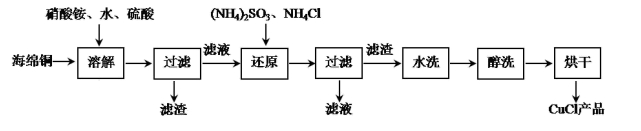
( 1 )析出的 CuCl 晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于 70℃ 干燥 2h ,冷却密封包装。 70℃ 真空干燥、密封包装的原因是 ____________________________________________________________ 。
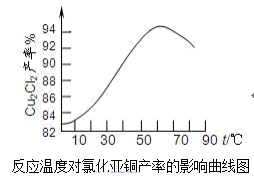
( 2 )如图是各反应物在最佳配比条件下,反应温度对 CuCl 产率影响.由图可知,溶液温度控制在 60℃ 时, CuCl 产率能达到 94% ,当温度高于 65℃ 时, CuCl 产率会下降,其原因可能是 ______________________________________________________________________________________________ 。
【答案】( 1 )真空干燥可以加快乙醇和水的挥发,密封包装可以防止 CuCl 在潮湿空气中水解、氧化;
( 2 )因在 60℃ 时 CuCl 产率最大,根据信息可知,随温度升高,促进了 CuCl 的水解, CuCl 被氧化的速度加快。
【练习 4 】 TiO 2 ·xH 2 O沉淀与双氧水、*水氨**反应 40min 所得实验结果如下表所示:
温度 /℃
30
35
40
45
50
TiO 2 ·xH 2 O转化率
92
95
97
93
88
分析 40℃ 时 TiO 2 ·xH 2 O转化率最高的原因 _____________________ 。
【答案】 40℃ 时 TiO 2 •xH 2 O转化率最高,因低于 40℃ , TiO 2 •xH 2 O转化反应速率随温度升高而增加,超过 40℃ ,双氧水分解与氨气逸出导致 TiO 2 •xH 2 O转化反应速率下降
【解析】 40℃ 时 TiO 2 •xH 2 O转化率最高,因低于 40℃ , TiO 2 •xH 2 O转化反应速率随温度升高而增加,超过 40℃ ,双氧水分解与氨气逸出导致 TiO 2 •xH 2 O转化反应速率下降。
2.促进平衡向吸热方向移动
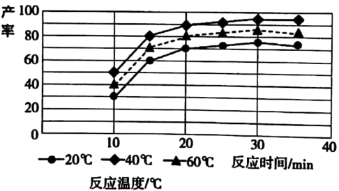
【练习 1 】二硫化钼是重要的固体润滑剂,被誉为 “ 高级固体润滑油之王 ” 。利用低品相的辉钼矿 ( 含 MoS 2 、 SiO 2 以及 CuFeS 2 等杂质 ) 制备高纯二硫化钼的一种生产工艺如图:
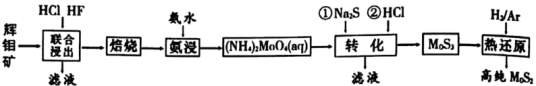
( 4 )由图分析可知产生 MoS 3 沉淀的流程中选择的最优温度和时间是 ___________ ,利用化学平衡原理分析低于或高于最优温度时, MoS 3 的产率均下降的原因 _______________________________________ 。
( 5 )利用低品相的原料制备高纯产品是工业生产中的普遍原则。如图所示,反应 [Ni(s)+4CO(g)
 Ni(CO)
4
(g)] ΔH<0在充满
CO
的石英管中进行,先在温度为
T
2
的一端放入未提纯的粗镍粉末,一段时间后,在温度为
T
1
的一端得到了纯净的镍粉,请结合平衡移动原理,判断温度
T
l
_________T
2
(填
“
>
”
、
“
<
”
或
“=”)
。
Ni(CO)
4
(g)] ΔH<0在充满
CO
的石英管中进行,先在温度为
T
2
的一端放入未提纯的粗镍粉末,一段时间后,在温度为
T
1
的一端得到了纯净的镍粉,请结合平衡移动原理,判断温度
T
l
_________T
2
(填
“
>
”
、
“
<
”
或
“=”)
。

【答案】( 4 ) 40℃ 、 30min 温度太低,反应 MoS 4 2- +2H +
 MoS
3
↓+H
2
S↑产生的
H
2
S气体不易逸出,不利于平衡正向移动生成
MoS
3
;温度太高,反应物盐酸挥发,导致溶液中
c(H
+
)下降,上述平衡逆向移动,也不利于生成
MoS
3
(
5
)
>
MoS
3
↓+H
2
S↑产生的
H
2
S气体不易逸出,不利于平衡正向移动生成
MoS
3
;温度太高,反应物盐酸挥发,导致溶液中
c(H
+
)下降,上述平衡逆向移动,也不利于生成
MoS
3
(
5
)
>
【解析】( 4 )根据图象可知, 40℃ 、 30min MoS 3 沉淀率达到最大,所以最优温度和时间是 40℃ 、 30min ;温度太低,反应 MoS 4 2- +2H +
 MoS
3
↓+H
2
S↑产生的
H
2
S气体不易逸出,不利于平衡正向移动生成
MoS
3
;温度太高,反应物盐酸挥发,导致溶液中
c(H
+
)下降,上述平衡逆向移动,也不利于生成
MoS
3
,所以低于或高于最优温度时,
MoS
3
的产率均下降;
MoS
3
↓+H
2
S↑产生的
H
2
S气体不易逸出,不利于平衡正向移动生成
MoS
3
;温度太高,反应物盐酸挥发,导致溶液中
c(H
+
)下降,上述平衡逆向移动,也不利于生成
MoS
3
,所以低于或高于最优温度时,
MoS
3
的产率均下降;
( 5 ) [Ni(s)+4CO(g)
 Ni(CO)
4
(g)] ΔH<0,正反应放热,升高温度平衡逆向移动,生成
Ni
单质,在温度为
T
1
的一端得到了纯净的镍粉,所以
T
l
>T
2
。
Ni(CO)
4
(g)] ΔH<0,正反应放热,升高温度平衡逆向移动,生成
Ni
单质,在温度为
T
1
的一端得到了纯净的镍粉,所以
T
l
>T
2
。
3.加快反应速率或溶解速率
【 2020新课标 Ⅰ 】钒具有广泛用途。黏土钒矿中,钒以 +3 、 +4 、 +5 价的化合物存在,还包括钾、镁的铝硅酸盐,以及 SiO 2 、 Fe 3 O 4 。采用以下工艺流程可由黏土钒矿制备 NH 4 VO 3 。
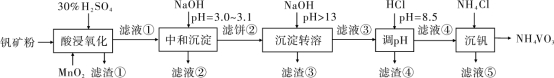
“酸浸氧化 ” 需要加热,其原因是 _________________________________________ 。
【答案】加快酸浸和氧化反应速率(促进氧化完全)
【解析】 “ 酸浸氧化 ” 需要加热,其原因是:升高温度,加快酸浸和氧化反应速率(促进氧化完全),故答案为:加快酸浸和氧化反应速率(促进氧化完全);
 【练习
2
】炼油厂烷基化反应产生的废液中含硫酸
91%
、难挥发有机物
7%
。实验室以软锰矿
(
主要含
MnO
2
,还含少量
Fe
、
Al
等元素
)
处理废液并制取
MnSO
4
·H
2
O晶体,其实验流程如图:
【练习
2
】炼油厂烷基化反应产生的废液中含硫酸
91%
、难挥发有机物
7%
。实验室以软锰矿
(
主要含
MnO
2
,还含少量
Fe
、
Al
等元素
)
处理废液并制取
MnSO
4
·H
2
O晶体,其实验流程如图:
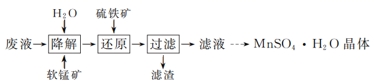
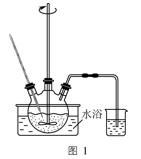
( 1 )研究温度对 “ 降解 ” 过程中有机物去除率的影响,实验在如图 1 所示的装置中进行。
① 在不同温度下反应相同时间,发现温度从 60℃ 升高到 95℃ 时,有机物去除率从 29% 增大到 58% ,其可能的原因是: MnO 2 的氧化能力随温度升高而增强; ______________________________________ 。
【答案】温度升高,反应速率加快
【解析】 ① 升高温度,反应速率加快,在相同时间内有机物反应的更多,去除率增加。
【练习 3 】 “ 浸取 ” 步骤中,能加快浸取速率的方法有 ___________( 任写两种 ) 。
【答案】将橄榄石尾矿粉碎、适当增大盐酸的浓度、适当提高反应的温度等
【解析】 “ 浸取 ” 步骤中,能加快浸取速率的方法有将橄榄石尾矿粉碎、适当增大盐酸的浓度、适当提高反应的温度等。
4.使沸点相对低的原料气化,或者降低在溶液中的气体溶解度
【练习 1 】实验室用如图所示的装置模拟燃煤烟气脱硫实验:
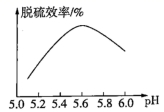
研究发现石灰石浆液的脱硫效率受 pH 和温度的影响。燃煤烟气流速一定时,脱硫效率与石灰石浆液 pH 的关系如图所示,在 pH 为 5.6 时脱硫效果最佳,石灰石浆液
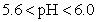 时,脱硫效率降低的原因可能是
___________________________
,燃煤烟气通入石灰石浆液时的温度不宜过高的原因是
___________________________
。
时,脱硫效率降低的原因可能是
___________________________
,燃煤烟气通入石灰石浆液时的温度不宜过高的原因是
___________________________
。
【答案】石灰石的溶解度减小,与
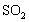 的反应变慢 温度升高,
的反应变慢 温度升高,
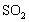 的溶解度减小
的溶解度减小
【解析】由脱硫效率与石灰石浆液 pH 的关系图知,在 pH 为 5.6 时脱硫效果最佳, pH 增大,石灰石的溶解度减小,与
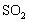 的反应变慢;温度升高,
的反应变慢;温度升高,
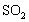 的溶解度减小。故答案为:石灰石的溶解度减小,减慢了与
SO
2
的反应; 温度升高SO
2
的溶解度小。
的溶解度减小。故答案为:石灰石的溶解度减小,减慢了与
SO
2
的反应; 温度升高SO
2
的溶解度小。
【练习 2 】以甲酸和碳酸钾为原料生产二甲酸钾,实验测得反应条件对产品回收率的影响如下:
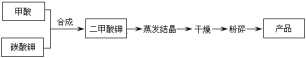
表 1 反应温度对产品回收率的影响
反应温度( ℃ )
20
30
40
50
60
70
80
产品回收率( % )
75. 6
78. 4
80. 6
82. 6
83. 1
82. 1
73. 7
② 实际生产二甲酸钾时应选择的最佳反应条件是反应温度应控制在 ____________℃~____________℃ ,由表 1 可知反应温度过高,反应回收率反而会降低,其原因可能是 ___________________________________________ 。
【答案】温度过高,甲酸挥发
【解析】从表 1 可看出,温度控制在 50℃~60℃ 二甲酸钾的产率较高,温度过高,反应回收率反而会降低,其原因可能是:甲酸易挥发,温度太高甲酸挥发了。
【练习 3 】实验室中用 FeSO 4 溶液与 NaOH 溶液制备 Fe(OH) 2 ,装置如图,请回答下列问题:
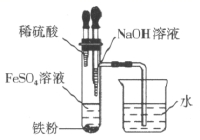
配制 NaOH 溶液时使用的蒸馏水通常要煮沸,其目的是 __________________________________ 。
【答案】除去水中溶解的氧气
【解析】硫酸亚铁易被氧化而变质,因此配制 NaOH 溶液时,应排除溶液中的氧气,可用加热溶液的方法除去溶解的氧气。
【练习 4 】四氯化锡用作媒染剂和有机合成上的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息数据如下:
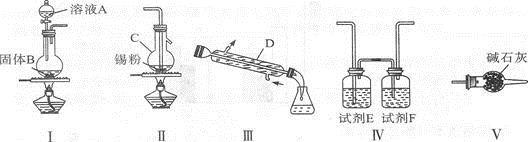
② 无水四氯化锡是无色易流动的液体,熔点 -33℃ ,沸点 114.1℃ 。
实验制得的 SnCl 4 中因溶解了 C1 2 而略显黄色,提纯 SnCl 4 的方法是 ________________ 。
【答案】加热蒸馏
【解析】由于 SnCl 4 的沸点 114.1℃ ,因此如果实验制得的 SnCl 4 中因溶解了 C1 2 而略显黄色,提纯 SnCl 4 的方法是加热蒸馏。
【练习 5 】白云石的主要成份是 CaCO 3 ·MgCO 3 ,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现 Ca 2+ 、 Mg 2+ 的分离。碳化反应是放热反应,化学方程式如下: Ca(OH) 2 +Mg(OH) 2 +3CO 2
 CaCO
3
+Mg(HCO
3
)
2
+H
2
O。完成下列填空:
CaCO
3
+Mg(HCO
3
)
2
+H
2
O。完成下列填空:
碳化温度保持在 50~60℃ 。温度偏高不利于碳化反应,原因是 __________________ 、 __________________ 。温度偏低也不利于碳化反应,原因是 ___________________________ 。
【答案】二氧化碳的溶解度小;碳酸氢镁分解,反应速率较小。
【解析】该反应为放热反应,而且是可逆的,当温度过高时,平衡逆反应方向移动,二氧化碳的溶解度减小,导致钙镁离子的分离减弱, Mg(HCO 3 ) 2 是易分解,温度过高就分解了,温度过低,反应速率太小,导致得到产物消耗的时间太长,不利于碳化反应,故答案为:二氧化碳的溶解度小、碳酸氢镁分解;反应速率较小。
5.除去热不稳定的杂质,如 NH 4 HCO 3 、 NH4(CO 3 ) 2 、 KMnO 4 、 NH 4 C1等物质
【练习 1 】物质的分离与提纯是化学的重点,请根据下列实验目的,分别选择相应的操作和实验装置。下列为操作:
a.蒸馏 b .结晶法 c .加适量水,过滤 d .加热(或灼烧) e .加适量盐酸,蒸发 f .萃取分液 g .分液 h .升华
下列为实验装置:
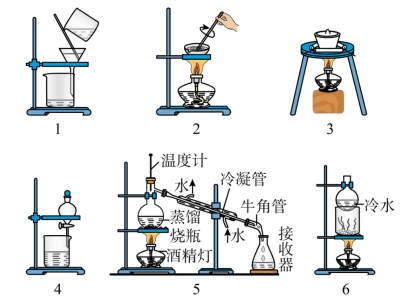
( 1 )除去氯化钠晶体中的碳酸钠: ______ 、 ______ (分别填操作序号及实验装置图编号,下同)。
( 2 )除去碳酸钙中的氯化钠: _______ 、 ______ 。
( 3 )分离乙酸(沸点 118℃ )和乙酸乙酯(沸点 77.1℃ )的混合液(两者互溶): ______ 、 ______ 。
( 4 )从溴水中提取溴: _______ 、 _______ 。
( 5 )除去氧化钙中的碳酸钙: _______ 、 _______ 。
( 6 )分离固体食盐和碘的方法: _______ 、 _______ 。
【答案】 e 2 c 1 a 5 f 4 d 3 h 6
【解析】
( 1 )碳酸钠与盐酸反应生成 NaCl ,则加适量盐酸,蒸发可分离,对应于装置 2 ,故答案为 e ; 2 ;
( 2 )碳酸钙不溶于水,氯化钠晶体溶于水,则选择过滤法可分离,对应于装置 1 ,故答案为 c ; 1 ;
( 3 )二者互溶,但沸点不同,则选择蒸馏法分离,对应于装置 5 ,故答案为 a ; 5 ;
( 4 )溴不易溶于水,易溶于有机溶剂,则选择萃取、分液法分离,对应于装置 4 ,故答案为 f ; 4 ;
( 5 )碳酸钙高温分解生成氧化钙,则选择加热分解法除杂,对应于装置 3 ,故答案为 d ; 3 ;
( 6 )碘容易升华,则选择升华法分离固体食盐和碘,对应于装置 6 ,故答案为 h ; 6 。
二.降低温度
1.防止某物质在高温时会分解(或溶解)
【练习 1 】电解精炼铜的阳极泥中主要含 Ag 、 Au 等贵重金属。以下是从精炼铜的阳极泥中回收银、金的流程图:
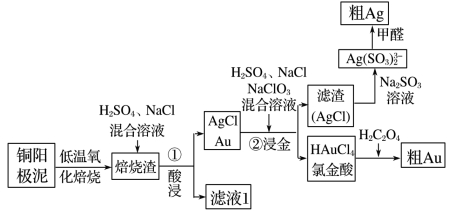
铜阳极泥氧化时,采用 “ 低温焙烧 ” 而不采用 “ 高温焙烧 ” 的原因是 _______ ______________。
【答案】低温焙烧时, Ag 与氧气转化为 Ag 2 O,高温时,氧化银分解又生成 Ag 和氧气;故答案为:高温焙烧时,生成的 Ag 2 O又分解为 Ag 和 O 2 (或 2Ag 2 O
 4Ag+
O
2
↑)。
4Ag+
O
2
↑)。
【练习 2 】【 2018 北京卷】 磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分为 Ca 5 (PO 4 ) 3 (OH),还含有 Ca 5 (PO 4 ) 3 F和有机碳等。溶解度: Ca 5 (PO 4 ) 3 (OH)<CaSO 4 ·0.5H 2 O
( 1 ) H 2 O 2 将粗磷酸中的有机碳氧化为 CO 2 脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。 80℃ 后脱除率变化的原因: ____________________ 。
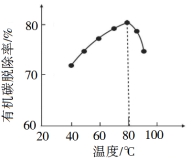
【答案】图示是相同投料比、相同反应时间,不同温度下的有机碳脱除率, 80℃ 前温度升高反应速率加快,相同
 时间内有机碳脱除率增大;
80℃
后温度升高,
H
2
O
2
分解速率大,
H
2
O
2
浓度显著降低,反应速率减慢,相同条件下有机碳脱除率减小。
时间内有机碳脱除率增大;
80℃
后温度升高,
H
2
O
2
分解速率大,
H
2
O
2
浓度显著降低,反应速率减慢,相同条件下有机碳脱除率减小。
【练习 3 】一种从铜阳极泥 ( 主要含有铜、银、金、少量的镍 ) 中分离提取多种金属元素的工艺流程如下:
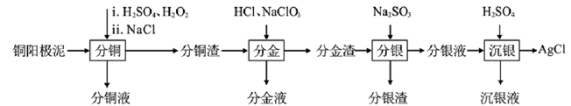
“分铜 ” 时,如果反应温度过高,会有明显的放出气体现象,原因是 ____________________________ 。
【答案】温度过高, H 2 O 2 分解放出氧气。
【练习 5 】钛铁矿主要成分为 FeTiO 3 (含有少量 MgO 、 SiO 2 等杂质), Li 4 Ti 5 O 12 和 LiFePO 4 都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:
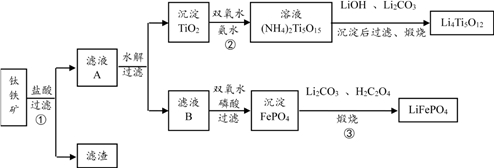
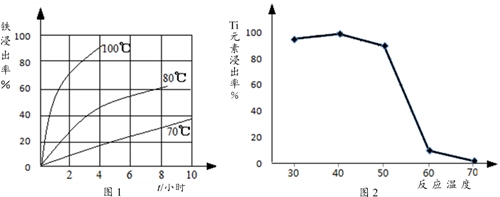
过程 ② 中固体 TiO 2 与双氧水、*水氨**反应转化成 (NH 4 ) 2 Ti 5 O 15 溶液时, Ti 元素的浸出率与反应温度的关系如图 2 所示,反应温度过高时, Ti 元素浸出率下降的原因是 ___________________________________________________ 。
【答案】温度过高,双氧水分解与氨气逸出导致 Ti 元素浸出率下降。
【练习 6 】工业上以软锰矿 ( 主要成分是 MnO 2 ,含有 SiO 2 、 Fe 2 O 3 等少量杂质 ) 为主要原料制备高性能的磁性材料碳酸锰 (MnCO 3 )。其工业流程如下:
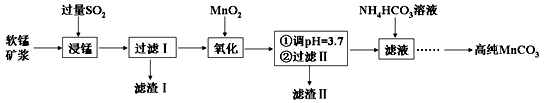
( 1 ) “ 浸锰 ” 反应中往往有副产物 MnS 2 O 6 生成,温度对 “ 浸锰 ” 反应的影响如右图所示,为减少 MnS 2 O 6 的生成, “ 浸锰 ” 的适宜温度是 ___________________________ 。
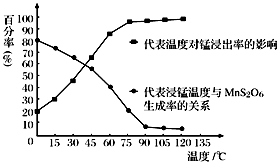
( 2 )向过滤 Ⅱ 所得的滤液中加入 NH 4 HCO 3 溶液时温度控制在 30-35℃ ,温度不宜太高的原因是 ___________________________________________________________________ 。
【答案】( 1 ) 90℃ 。( 2 )铵盐受热分解,向过滤所得的滤液中加入碳酸氢铵溶液,温度控制在 30-35℃ 的原因是防止 NH 4 HCO 3 受热分解,提高原料的利用率;
2.使化学平衡向着放热方向移动
【练习 1 】乙酸苯酚酯制备: 将
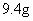 苯酚溶解在
苯酚溶解在
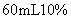 的氢氧化钠溶液中,加入
30g
碎冰块,然后加入
的氢氧化钠溶液中,加入
30g
碎冰块,然后加入
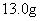 乙酸酐,搅拌
乙酸酐,搅拌
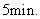 将反应后混合物倾入分液漏斗中,加入约
4mL
将反应后混合物倾入分液漏斗中,加入约
4mL
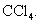 将有机相用试剂
X
和水洗涤然后无水
将有机相用试剂
X
和水洗涤然后无水
 干燥,蒸馏收集
干燥,蒸馏收集
 馏分.
馏分.
① 用碎冰块代替水可能的原因是: ______________________________________ .
【答案】该反应是放热反应,碎冰温度低有利于酯的生成
【解析】 ① 碎冰温度低有利于酯的生成,故答案为:该反应是放热反应,碎冰温度低有利于酯的生成。
3.使某个沸点高的产物液化,使其与其他物质分离
【练习 1 】石墨在材料领域有重要应用。某初级石墨中含 SiO 2 ( 7.8% )、 Al 2 O 3 (5.1%)、 Fe 2 O 3 (3.1%)和 MgO(0.5%) 等杂质。设计的提纯和综合应用流程如下:
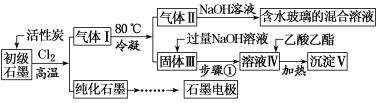
(注: SiCl 4 的沸点是 57.6ºC ,金属氯化物的沸点均高于 150ºC )
向反应器中通入 Cl 2 前,需通一段时间的 N 2 。高温反应后,石墨中的氧化物杂质均转变为相应氯化物。 80℃ 冷凝的目的是: _____________________ 。 ② 由活性炭得到气体 Ⅱ 的化学反应方程式为: _____________________ 。
【答案】高温下, Si 元素转化成 SiCl 4 ,铁元素转化成 FeCl 3 , Mg 元素转化成 MgCl 2 , Al 元素转化成 AlCl 3 , SiCl 4 沸点是 57.6℃ , MgCl 2 、 FeCl 3 、 AlCl 3 沸点均高于 150℃ ,加热到 1500℃ , MgCl 2 、 FeCl 3 、 AlCl 3 、 SiCl 4 全部转化成气体 I , 80℃ 冷凝, SiCl 4 还是气体,而 MgCl 2 、 FeCl 3 、 AlCl 3 状态是固体,便于与 SiCl 4 分开。
4.降低晶体的溶解度,减少损失。
【练习 1 】碳酸锂广泛应用于化工、冶金等行业.工业上利用锂辉石( Li 2 Al 2 Si 4 O x )制备碳酸锂的流程如图:
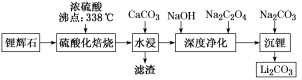
已知:碳酸锂的溶解度为( g/L )
温度
0
10
20
30
40
50
60
80
100
Li 2 CO 3
1. 54
1. 43
1. 33
1. 25
1. 17
1. 08
1. 01
0. 85
0. 72
( 1 )硫酸化焙烧温度控制在 250℃ ﹣ 300℃ 之间,主要原因是 __________________________________ ;焙烧中硫酸用量控制在理论用量的 l15% 左右,硫酸加入过多的副作用是 _________________________ 。
( 2 ) “ 沉锂 ” 需要在 95℃ 以上进行,主要原因是 _______________________ ,过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有 _____________ 和 ______________ 。
【答案】( 1 )硫酸化焙烧温度控制在 250℃ ﹣ 300℃ 之间,主要原因是温度低于 250℃ ,反应速率较慢,温度高于 300℃ ,硫酸挥发较多;焙烧中硫酸用量控制在理论用量的 l15% 左右,硫酸加入过多的副作用是后续中还需要除去过量的硫酸,增加后续杂质的处理量、增加后续中和酸的负担。
(2) 温度越高,碳酸锂溶解度降低,减少碳酸锂溶解,可以增加产率;溶液中硫酸钠不反应,使用碳酸钠要过量,少量碳酸锂溶解在溶液中,过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂。过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂。所以 “ 沉锂 ” 需要在 95℃ 以上进行,主要原因是温度越高,碳酸锂溶解度降低,可以增加产率;过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂。
【练习 2 】某废旧电池材料的主要成分为钴酸锂 (LiCoO 2 ),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到 Co 2 O 3 和锂盐。
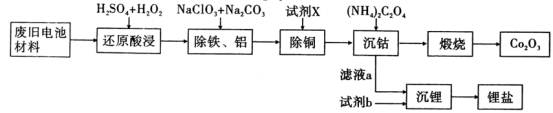
已知: CoC 2 O 4 ·2H 2 O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的 C 2 O 4 2- 离子生成 Co(C 2 O 4 ) n 2(n- 1) - 而溶解。
( 4 ) “ 沉钴 ” 过程中, (NH 4 ) 2 C 2 O 4 的加入量 ( 图 a) 、沉淀反应的温度 ( 图 b) 与钴的沉淀率关系如图所示:
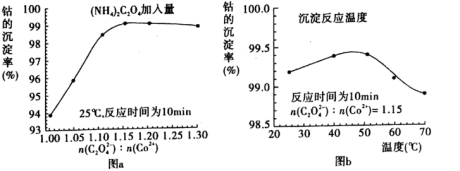
① 随 n(C 2 O 4 2- ): N(Co 2+ )比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因 ________________________ 。
② 沉淀反应时间为 10 min ,温度在 50℃ 以上时,随温度升高而钴的沉淀率下降的可能原因是 _______________________________________________________________________________________________ 。
【答案】 ① 过量的 C 2 O 4 2- 与 Co 2+ 反应生成 Co(C 2 O 4 ) n 2(n-1)- 而溶解 ② 它的溶解度随温度升高而逐渐增大
【解析】 ① 随 n(C 2 O 4 2- ): N(Co 2+ )比值的增加,过量的 C 2 O 4 2- 与 Co 2+ 反应生成 Co(C 2 O 4 ) n 2(n-1)- 而溶解,钴的沉淀率先逐渐增大后又逐渐减小;
② 沉淀反应时间为 10 min ,温度在 50℃ 以上时,溶解度随温度升高而逐渐增大。
5.减少能源成本,降低对设备的要求
【练习 1 】目前常用的工业生产纯碱的方法是 “ 联合制碱法(侯氏制碱法) ”
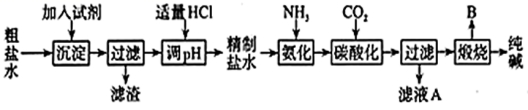
世界上最早工业生产碳酸钠的方法是 “ 路布兰法 ” ,其流程如下:
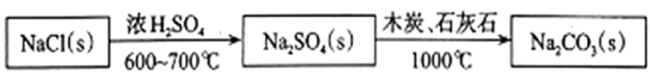
与 “ 路布兰法 ” 相比, “ 联合制碱法 ’ 的优点之一是 _________________________ 。
【答案】原料利用率高,反应所需温度低,耗能少
【解析】据流程可知:路布兰法是利用食盐晶体和浓硫酸在 600°C 到 700°C 下反应生成硫酸钠和氯化氢,再利用 C 与石灰石和硫酸钠在 1000°C 生成碳酸钠;侯德榜研究出联合制碱法为在饱和的氯化钠溶液中直接通入氨气和 CO 2 ,得到氯化铵和碳酸氢钠晶体,并利用碳酸氢钠的分解制得纯碱,
 在
270℃
时就完全分解,分解产生的二氧化碳还可以循环利用,故联合制碱法反应所需温度低,耗能少、提高了原料利用率。
在
270℃
时就完全分解,分解产生的二氧化碳还可以循环利用,故联合制碱法反应所需温度低,耗能少、提高了原料利用率。
三.控制温度(用水浴或油浴控温)
1 . 防止某种物质温度过高时会分解或挥发
【 2019 江苏】 实验室以工业废渣 ( 主要含 CaSO 4 ·2H 2 O, 还含少量 SiO 2 、 Al 2 O 3 、 Fe 2 O 3 ) 为原料制取轻质 CaCO 3 和 (NH 4 ) 2 SO 4 晶体 , 其实验流程如下 :
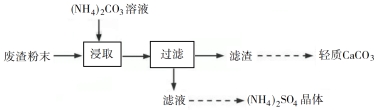
( 1 )废渣浸取在如图所示的装置中进行。控制反应温度在 60~70 ℃ ,搅拌,反应 3 小时。温度过高将会导致 CaSO 4 的转化率下降,其原因是 ;保持温度、反应时间、反应物和溶剂的量不变,实验中提高 CaSO 4 转化率的操作有 。
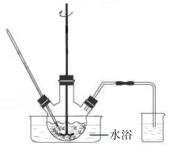
【答案】由于铵盐具有不稳定性,受热易分解,所以温度过高,( NH 4 ) 2 CO 3 分解,从而使 CaSO 4 转化率下降;由于浸取过程中的反应属于固体与溶液的反应(或发生沉淀的转化),保持温度、反应时间、反应物和溶剂的量不变,提高 CaSO 4 转化率即提高反应速率,结合外界条件对化学反应速率的影响,实验过程中提高 CaSO 4 转化率的操作为加快搅拌速率(即增大接触面积,加快反应速率,提高浸取率)。
2 . 控制固体的溶解与结晶
【习题 1 】 【 2017 新课标 3 卷】 重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为 FeO·Cr 2 O 3 ,还含有硅、铝等杂质。制备流程如图所示:
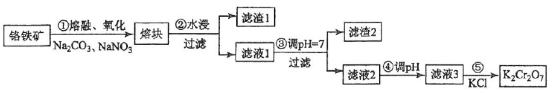
有关物质的溶解度如图所示。向 “ 滤液 3” 中加
 入适量
KCl
,蒸发浓缩,冷却结晶,过滤得到
K
2
Cr
2
O
7
固体。冷却到
___________
(填标号)得到的
K
2
Cr
2
O
7
固体产品最多。
入适量
KCl
,蒸发浓缩,冷却结晶,过滤得到
K
2
Cr
2
O
7
固体。冷却到
___________
(填标号)得到的
K
2
Cr
2
O
7
固体产品最多。
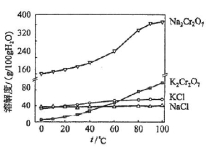
a. 80℃ b. 60℃ c. 40℃ d. 10℃
【答案】 d
【解析】首先分析图像特点, Na 2 Cr 2 O 7 溶解度最大, NaCl 溶解度最小且随温度变化很小, K 2 Cr 2 O 7 的溶解度在高温下大,但低温下较小,即随温度变化最大;然后分析反应特点 2KCl+Na 2 Cr 2 O 7 =K 2 Cr 2 O 7 ↓ +2NaCl的反应类型为复分解反应;再结合操作条件 “ 蒸发浓缩,冷却结晶,过滤 ” ,得出结论加热蒸发过程中,随着水分的蒸发,平衡向右进行;最后根据条件冷却可知,要保证重铬酸钾溶解度最小,因此温度为 10℃ 。
3. 使催化剂的活性达到最好
【习题 1 】 【 2016 全国卷 Ⅱ27】 以丙烯、氨、氧气为原料 , 在催化剂存在下生成丙烯腈 (C 3 H 3 N) 和副产物丙烯醛 (C 3 H 4 O) 的热化学方程式如下 :
① C 3 H 6 (g)+NH 3 (g)+
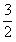
 O
2
(g)
O
2
(g)
 C
3
H
3
N(g)+3H
2
O(g)
Δ
H=-515 kJ·mol
-1
C
3
H
3
N(g)+3H
2
O(g)
Δ
H=-515 kJ·mol
-1
② C 3 H 6 (g)+O 2 (g)
 C
3
H
4
O(g)+H
2
O(g)
Δ
H=-353 kJ·mol
-1
C
3
H
4
O(g)+H
2
O(g)
Δ
H=-353 kJ·mol
-1
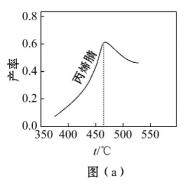
图 (a) 为丙烯腈产率与反应温度的关系曲线, 最高产率对应的温度为 460℃ 。低于 460℃ 时,丙烯腈的产率 (填 “ 是 ” 或 “ 不是 ”) 对应温度下的平衡产率,判断理由是 _____ ___ ;高于 460° 时,丙烯腈产率降低的可能原因是 (双选,填标号 ) 。
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大
【答案】 A 、 C
【解析】因为该反应为放热反应,平衡产率应随温度升高而降低,反应刚开始进行,尚未达到平衡状态, 460℃ 以前是建立平衡的过程,所以低于 460℃ 时,丙烯腈的产率不是对应温度下的平衡产率;高于 460℃ 时,丙烯腈产率降低。催化剂在一定温度范围内活性较高,若温度过高,活性降低, A 正确;平衡常数的大小不影响产率, B 错误;根据题意,副产物有丙烯醛,副反应增多导致产率下降, C 正确;反应活化能的大小不影响平衡, D 错误
4 . 防止副反应的发生
【练习 1 】 【 2018 江苏】 以 Cl 2 、 NaOH 、 (NH 2 ) 2 CO(尿素)和 SO 2 为原料可制备 N 2 H 4 ·H 2 O(水合肼)和无水 Na 2 SO 3 ,其主要实验流程如下:
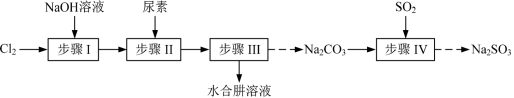
已知: ① Cl 2 +2OH −
 ClO
−
+Cl
−
+H
2
O是放热反应。
②
N
2
H
4
·H
2
O沸点约
118 ℃
,具有强还原性,能与
NaClO
剧烈反应生成
N
2
。
ClO
−
+Cl
−
+H
2
O是放热反应。
②
N
2
H
4
·H
2
O沸点约
118 ℃
,具有强还原性,能与
NaClO
剧烈反应生成
N
2
。
( 1 )步骤 Ⅰ 制备 NaClO 溶液时,若温度超过 40 ℃ , Cl 2 与 NaOH 溶液反应生成 NaClO 3 和 NaCl ,其离子方程式为 ____________________________________ ;实验中控制温度除用冰水浴外,还需采取的措施是 ____________________________________ 。
【答案】温度超过 40℃ , Cl 2 与 NaOH 溶液发生歧化反应生成 NaClO 3 、 NaCl 和 H 2 O,反应的化学方程式为 3Cl 2 +6NaOH
 5NaCl+NaClO
3
+3H
2
O,离子方程式为
3Cl
2
+6OH
-
5NaCl+NaClO
3
+3H
2
O,离子方程式为
3Cl
2
+6OH
-
 5Cl
-
+ClO
3
-
+3H
2
O。由于
Cl
2
与
NaOH
溶液的反应为放热反应,为了减少
NaClO
3
的生成,应控制温度不超过
40℃
、减慢反应速率;实验中控制温度除用冰水浴外,还需采取的措
5Cl
-
+ClO
3
-
+3H
2
O。由于
Cl
2
与
NaOH
溶液的反应为放热反应,为了减少
NaClO
3
的生成,应控制温度不超过
40℃
、减慢反应速率;实验中控制温度除用冰水浴外,还需采取的措
 施是:缓慢通入
Cl
2
。
施是:缓慢通入
Cl
2
。
【练习 2 】硒 (Se) 和铜 (Cu) 在生产生活中有广泛的应用。硒可以用作光敏材料、电解锰行业的催化剂,也是动物体必需的营养元素和对植物有益的营养元素等。氯化亚铜 (CuCl) 广泛应用于化工、印染、电镀等行业。 CuCl 难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜 ( 主要成分是 Cu 和少量 CuO) 为原料,采用硝酸铵氧化分解技术生产 CuCl 的工艺过程如下所示:
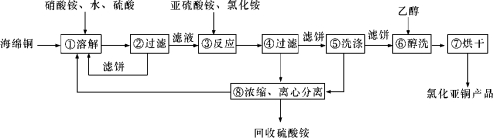
氯化亚铜产率与温度、溶液 pH 关系如下图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响 CuCl 产率的原因是 ____________________________________ ;温度过高、 pH 过大也会影响 CuCl 产率的原因是 _______________________________ 。
【答案】据图分析,流程化生产氯化亚铜的过程中,温度过低影响 CuCl 产率的原因是温度过低反应速率慢;温度过高、 pH 过大也会影响 CuCl 产率的原因是温度过高、 pH 过大,容易向 CuO 和 Cu 2 O转化,且温度过高,铵盐 ( 氯化铵,亚硫酸铵 ) 易受热分解;
【练习 3 】呋喃 (
 )为无色液体,沸点为
32 ℃
,难溶于水,主要用于有机合成或用作溶剂,工业上可用呋喃甲醛制备呋喃。某兴趣小组设计实验探究其制备方法,实验原理及实验步骤如图:
)为无色液体,沸点为
32 ℃
,难溶于水,主要用于有机合成或用作溶剂,工业上可用呋喃甲醛制备呋喃。某兴趣小组设计实验探究其制备方法,实验原理及实验步骤如图:
① 2
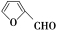 +NaOH→
+NaOH→
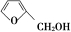 +
+
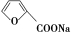 ΔH<0
ΔH<0
②
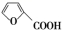
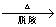

实验步骤:
① 取一定量的氢氧化钠溶液于烧杯中,在不断搅拌下,慢慢滴加 4.8 g 呋喃甲醛,控制反应温度在 8~12℃ 。滴加完毕后继续在上述温度下搅拌 20min ,反应完全后得黄色浆状物,在搅拌下加入少量的水使固体完全溶解。然后用*醚乙**萃取,分液。
② 取水层液体,加入盐酸,搅拌、过滤、提纯、干燥,得到呋喃甲酸。
③ 将制得的呋喃甲酸加入如图装置 ( 部分装置省略 ) 中进行脱羧处理,得到呋喃 1.1 g 。
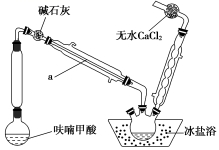
( 2 )步骤 ① 的关键是控制温度在 8~12 ℃ ,采取的最好措施是磁力搅拌、 ___________________ ;简述步骤 ① 中温度不能过高或过低的原因是 ___________________________ 。
【答案】( 2 )将烧杯置于冷水浴中 温度过低,反应速率太慢,温度过高,呋喃甲酸钠产率较低
【解析】控制温度在 8~12 ℃ ,需将烧杯置于冷水浴中;温度过低,反应速率太慢,温度过高,副产物增多,呋喃甲酸钠产率较低,故答案为:温度过低,反应速率太慢,温度过高,呋喃甲酸钠产率较低。
【习题 4 】 【 2017 新课标 2 卷】 *烯丁**是一种重要的化工原料,可由丁烷催化脱氢制备。正丁烷( C 4 H 10 )脱氢制 1- *烯丁**( C 4 H 8 )的热化学方程式如下: ① C 4 H 10 (g)= C 4 H 8 (g)+H 2 (g) Δ H 1 =+123kJ·mol −1
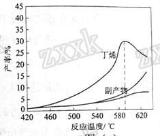
图( c )为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。*烯丁**产率在 590℃ 之前随温度升高而增大的原因可能是 ___________ 、 ____________ ; 590℃ 之后,*烯丁**产率快速降低的主要原因可能是 _____________ 。
【答案】升高温度有利于反应向吸热方向进行;温度升高反应速率加快;*烯丁**高温裂解生成短链烃类
【解析】根据图 (c) , 590℃ 之前,温度升高时反应速率加快,生成的*烯丁**会更多,同时由于反应 ① 是吸热反应,升高温度平衡正向移动,平衡体系中会含有更多的*烯丁**。而温度超过 590℃ 时,由于丁烷高温会裂解生成短链烃类,所以参加反应 ① 的丁烷也就相应减少。
5.蒸馏分离物质
【练习 1 】实验室可用环己醇制备环己酮,使用的氧化剂可以是次氯酸钠、重铬酸钾等。

已知:环己醇沸点: 160.8℃ ,微溶于水;
环己酮沸点: 155.6℃ ,微溶于水;
醋酸沸点 117.9℃ ,和水以任意比例互溶。
用如图对粗产品进行精制,蒸馏收集 _____________℃ 的馏分。
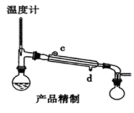
【答案】 155.6
【解析】环己酮的沸点: 155.6℃ ,所以收集 155.6℃ 的馏分。
【练习 2 】以环己醇制备环己烯:
密度( g/cm 3 )
熔点( ℃ )
沸点( ℃ )
溶解性
环己醇
0.96
25
161
能溶于水
环己烯
0.81
- 103
83
难溶于水
收集产品时,控制的温度应在 ________________ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是 _______
A.蒸馏时从 70℃ 开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
【答案】 83ºC C
【解析】因为环己烯的沸点为 83℃ ,所以控制的温度应在 83℃ 左右;
A.蒸馏时从 70℃ 开始收集产品,则产品的质量高, A 错误;
B.环己醇实际用量多了,会使产品的量增加, B 错误;
C.制备粗品时环己醇随产品一起蒸出,会使生成的环乙烯量减少, C 正确。
6 . 趁热过滤:减少因降温而析出的溶质的量
【练习 1 】实验室通常是在 NH 3 和 NH 4 Cl存在条件下,以活性炭为催化剂,用 H 2 O 2 氧化 CoCl 2 溶液来制备三氯化六氨合钴 [Co(NH 3 ) 6 ]Cl 3 ,该反应属于大量放热的反应。某小组用如图所示装置制备 [Co(NH 3 ) 6 ]Cl 3 ,实验步骤如下:
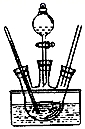
Ⅰ.称取研细的 CoCl 2 •6H 2 O10.0g和 NH 4 Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入 25mL 浓*水氨**和适量活性炭粉末,逐滴加入 5mL30% 的 H 2 O 2 溶液。
Ⅱ.用水浴将混合物加热至 60℃ ,恒温 20 分钟,然后用冰水浴冷却,充分结晶后过滤。
Ⅲ.将沉淀溶于热的盐酸中,趁热过滤,滤液中加适量浓盐酸并冷却结晶。
Ⅳ.过滤、用乙醇洗涤晶体并在 105℃ 条件下烘干。
( 5 )步骤 Ⅲ 中趁热过滤的主要目的是 __________________________________________ 。
【答案】除去活性炭并防止产品析出
【解析】( 5 )步骤 Ⅲ 中,若过滤时间长,滤液温度降低多, [Co(NH 3 ) 6 ]Cl 3 会在过滤过程中结晶析出,所以需趁热过滤,主要目的是除去活性炭并防止产品析出;为获得更多的产品,可利用同离子效应,降低产品的溶解度,由此得出滤液中加适量浓盐酸的主要目的是增大氯离子浓度,有利于析出 [Co(NH 3 ) 6 ]Cl 3 。
【练习 2 】将上述粗产品冷却后加入 40ml
 的氢氧化钠水溶液,再加
90ml
水,加热活性炭脱色,
趁热过滤
、冷却。
的氢氧化钠水溶液,再加
90ml
水,加热活性炭脱色,
趁热过滤
、冷却。
趁热过滤的目的 ____________________________ 。
【答案】防止肉桂酸钠结晶而析出堵塞漏斗
【解析】温度低,肉桂酸钠的溶解度降低,会结晶析出晶体,所以趁热过滤的目的是防止肉桂酸钠结晶而析出堵塞漏斗。
7 . 该温度下反应的结果已经较好,不需要继续变温
【练习 1 】钛酸锂电池应用广泛, 电池放电后负极材料主要含有 Li 4 Ti 5 O 12 、 铝箔及少量Fe , 可通过下列工艺流程回收钛、 锂。回答下列问题:
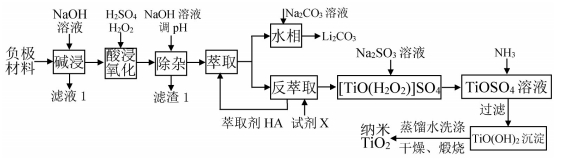
萃取时, 温度对萃取率的影响如图所示。由图分析知实验时选择在常温下进行即可, 理由是__ 。
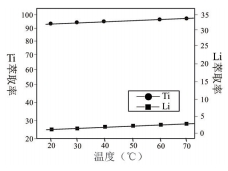
【答案】由温度对萃取率的影响图可知,常温下钛的萃取率已经比较高 (90% 以上 ) ,温度升高对萃取率的增加幅度很小,所以不必升温,实验时选择在常温下进行即可,
【练习 2 】高铁酸钾 (K 2 FeO 4 )是新型多功能水处理剂。图 1 为不同的温度下,不同质量浓度的 Fe(NO 3 ) 3 对 K 2 FeO 4 生成率的影响。
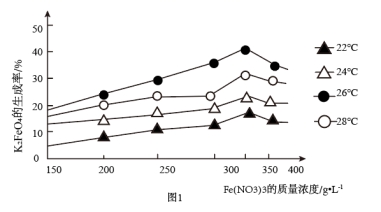
工业生产中最佳温度为 _____________________ 。
【答案】 26℃
【解析】 26℃ 摄氏度时,温度是最佳的。
【综合练习 1 】工业上以石煤 ( 主要成分为 V 2 O 3 ,含有少量 SiO 2 、 P 2 O 5 等杂质 ) 为原料制备钒的主要流程如图:
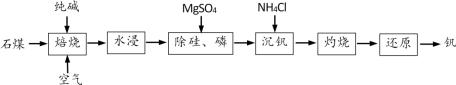
已知: ① NH 4 VO 3 难溶于水。 ② K sp (MgSiO 3 )=2.4×10 -5 , K sp [Mg 3 (PO 4 ) 2 ]=2.7×10 -27 。
( 1 )焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将 V 2 O 3 转化为 NaVO 3 的化学方程式为 ________________________________________________ 。
( 2 )除硅、磷:
① 用 MgSO 4 溶液除硅、磷时, Si 、 P 会形成 Mg 3 (PO 4 ) 2 、 MgSiO 3 沉淀。若沉淀后溶液中 c(PO
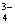 )=1.0×10
-8
mol•L
-1
,则
c(SiO
)=1.0×10
-8
mol•L
-1
,则
c(SiO
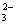 )=____________mol•L
-1
。
)=____________mol•L
-1
。
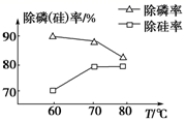
② 如图所示,随着温度升高,除磷率下降,其原因是 Mg 3 (PO 4 ) 2 溶解度增大、 ___________________________ ;随着温度升高,除硅率升高,其原因是 ______________________________ 。
( 3 )沉钒:此过程反应温度需控制在 50℃ 左右,温度不能过高的原因为 _____________________ 。
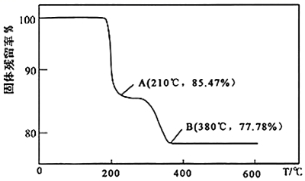
( 4 )灼烧:在灼烧 NH 4 VO 3 的过程中,固体的残留率 (
 ×100%)随温度变化的曲线如图所示,则
A~B
段发生反应的方程式为
____________________________________
。
×100%)随温度变化的曲线如图所示,则
A~B
段发生反应的方程式为
____________________________________
。
【答案】( 1 ) Na 2 CO 3 +O 2 +V 2 O 3
 2NaVO
3
+CO
2
2NaVO
3
+CO
2
( 2 ) ① 0.08 ② 促进 Mg 2+ 水解生成 Mg(OH) 2 ;促进
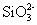 水解生成硅酸沉淀 促进SiO
水解生成硅酸沉淀 促进SiO
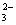 水解生成硅酸沉淀
水解生成硅酸沉淀
( 3 ) NH 4 Cl受热会分解
( 4 ) 2HVO 3
 V
2
O
5
+H
2
O
V
2
O
5
+H
2
O
【分析】
根据已知信息,流程第一步焙烧时 V 2 O 3 、 SiO 2 、 P 2 O 5 依次转化为 NaVO 3 、 Na 2 SiO 3 、 Na 3 PO 4 ,第三步加入 MgSO 4 生成 MgSiO 3 、 Mg 3 (PO 4 ) 2 沉淀, NaVO 3 进入后续步骤,在第四步生成 NH 4 VO 3 沉淀,再经过灼烧、还原得到钒单质。
【解析】
( 1 )依据 V 2 O 3 反应生成 NaVO 3 , V 元素化合价升高,需要氧化剂,故空气中 O 2 要参与反应,即 V 2 O 3 + Na 2 CO 3 +O 2
 2NaVO
3
+CO
2
。
2NaVO
3
+CO
2
。
( 2 ) ① K sp [Mg 3 (PO 4 ) 2 ]=
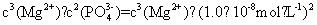 =2.7×10
-27
,解之得
=2.7×10
-27
,解之得
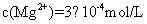 ,由
K
sp
(MgSiO
3
)=
,由
K
sp
(MgSiO
3
)=
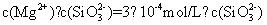 =2.4×10
-5
,解得
=2.4×10
-5
,解得
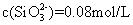 。
。
②
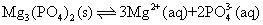 ,升温促进促进
Mg
2+
水解,导致沉淀溶解平衡右移,故除磷率下降;
,升温促进促进
Mg
2+
水解,导致沉淀溶解平衡右移,故除磷率下降;
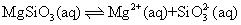 ,升温促进
,升温促进
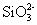 水解成
H
2
SiO
3
,沉淀溶解平衡右移,但
H
2
SiO
3
是沉淀,故除硅率升高。
水解成
H
2
SiO
3
,沉淀溶解平衡右移,但
H
2
SiO
3
是沉淀,故除硅率升高。
( 3 ) NH 4 Cl受热易分解,故温度不能过高。
( 4 )设 NH 4 VO 3 为 1mol ,即 117g ,起始到 A 点失去质量 =117g×(1-85.47%) ≈ 17g ,结合铵盐受热分解一般产生 NH 3 ,故推测 A 物质为 HVO 3 ,酸分解一般产生氧化物和水,故推测 B 点为 VO x ,根据 V 元素守恒 n(VO x )=1mol,则 (51+16x)g/mol×1mol=117g×77.78% ,解得 x=2.5 ,故 B 点为: VO 2.5 ,即 V 2 O 5 ,所以 A 到 B 段方程式为: 2HVO 3
 V
2
O
5
+H
2
O。
V
2
O
5
+H
2
O。
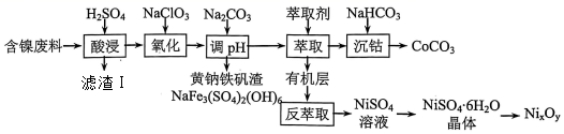
【综合练习 2 】实验室以含镍废料 ( 主要成分为 NiO ,含少量 FeO 、 Fe 2 O 3 、 CoO 、 BaO 和 SiO 2 )为原料制备 Ni x O y 和碳酸钴 (CoCO 3 )的工艺流程如图。
请回答以下问题:
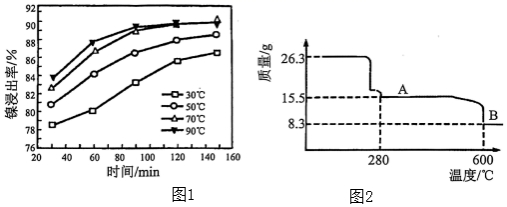
( 1 ) “ 滤渣 Ⅰ” 主要成分是 ___________ , “ 酸浸 ” 过程中镍的浸出率与温度和时间的关系如图 1 所示,酸浸的最佳温度和时间是 ___________ 。
( 4 )资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
温度
低于 30.8℃
30.8℃~ 53.8℃
53.8℃~ 280℃
高于 280℃
晶体形态
NiSO 4 •7H 2 O
NiSO 4 •6H 2 O
多种结晶水合物
NiSO 4
从 NiSO 4 溶液获得稳定的 NiSO 4 •6H 2 O晶体的操作依次是蒸发浓缩、 _____________________________ 。
( 5 ) NiSO 4 •6H 2 O晶体煅烧时剩余固体质量与温度变化曲线如图 2 ,该曲线中 B 段所表示氧化物的化学式为 _________________ 。
【答案】( 1 ) SiO 2 、 BaSO 4 70 ℃和 120 min
( 4 )冷却至 30.8℃ ~ 53.8℃ 之间时结晶、过滤、洗涤、干燥
( 5 ) Ni 2 O 3
【解析】
( 1 )由上述分析可知, “ 滤渣 I" 主要成分为 SiO 2 、 BaSO 4 ;由图 1 可知酸浸时温度越低,镍浸出率越高越好。由图示可知酸浸的最佳温度和时间是 70℃ 和 120 min ;
( 4 )从 NiSO 4 溶液获得 NiSO 4 ·6H 2 O晶体的操作依次是蒸发浓缩、冷却至 30.8℃ ~ 53.8℃ 之间时结晶、过滤、洗涤、干燥得到 NiSO 4 ·6H 2 O晶体;
( 5 ) 26.3 g NiSO 4 ·6H 2 O晶体的物质的量为 n(NiSO 4 ·6H 2 O)=
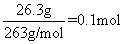 ,由图可知
0.1 mol NiSO
4
·6H
2
O晶体中含有
Ni
的物质的量为
0.1 mo1
,其质量为
m(Ni)=5.9 g
,晶体受热分解失去结晶水,再分解生成
Ni
x
O
y
,其质量为
8.3 g
,则其中含有
O
的质量为
m(O)=8.3 g-5.9 g=2.4 g
,所以
n(O) =
,由图可知
0.1 mol NiSO
4
·6H
2
O晶体中含有
Ni
的物质的量为
0.1 mo1
,其质量为
m(Ni)=5.9 g
,晶体受热分解失去结晶水,再分解生成
Ni
x
O
y
,其质量为
8.3 g
,则其中含有
O
的质量为
m(O)=8.3 g-5.9 g=2.4 g
,所以
n(O) =
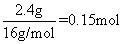 ,即
x
:
y=0.1 mol:0.15 mol=2:3
,
B
点氧化物的化学式为
Ni
2
O
3
。
,即
x
:
y=0.1 mol:0.15 mol=2:3
,
B
点氧化物的化学式为
Ni
2
O
3
。