轴向型脊椎关节炎是一种慢性炎性疾病,主要累及骶髂关节和脊柱,因炎症导致慢性腰痛和乏力。该疾病包括x线和非x线axSpA。在美国,Taltz(Ixekizumab)是第一种人类化白细胞介素(IL)-17A拮抗剂疗法,被批准用于治疗有客观炎症征象的成人活动性非X线性脊柱炎(NR-axSpA)。该疗法现在适用于治疗所有类型的axSpA,包括强直性脊柱炎(AS),或x线axSpA和nr-axSpA。
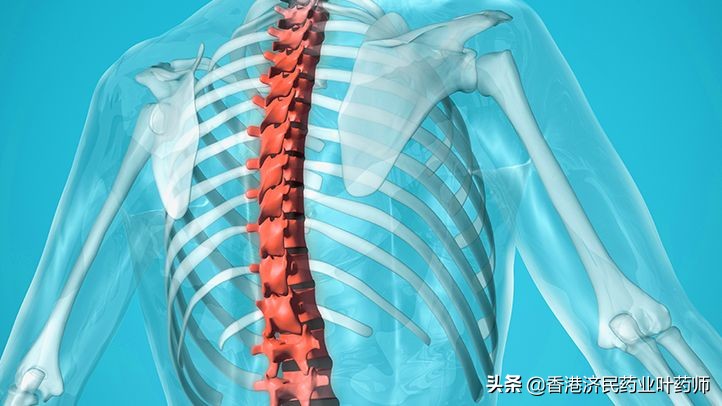
轴向型脊椎关节炎体征和症状
美国约有230万人使用axSpA,其中50%的人使用nr-axSpA。该病以骶髂关节结构损伤为特征,X线片上对X线axSpA患者有识别。非x线axSpA患者的x线照片未明确显示结构损伤,因此通常无法诊断。
疾病的恶化会对关节和脊柱造成更多的伤害,导致更严重的疾病,称为强直性脊柱炎。大约30%的nr-axSpA患者在2至30年内罹患强直性脊柱炎。
该病最常见的症状是背痛,其他症状包括虚弱、关节僵硬或肿胀、手指肿胀和脚跟疼痛。

Taltz批准
2016年,Taltz获得了美国食品药品监督管理局(FDA)对治疗6岁及以上中度至重度斑块型银屑病患者的初始批准。在美国,它还被批准用于治疗axSpA射线照相术和银屑病关节炎。
2016年11月,礼来公司与托里制药在日本推出该药物,用于治疗寻常型银屑病、关节型银屑病、脓疱型银屑病和银屑病性红皮病病。
2019年7月,该公司向美国FDA提交了Taltz的补充生物制品许可证申请(sBLA),以治疗成年nr-axSpA患者。该药物于2020年6月获得批准。
Taltz在欧洲可用于治疗斑块型银屑病和银屑病关节炎。2020年4月,欧洲药品管理局(EMA)人用药品委员会(CHMP)对治疗放射影像学axSpA和nr-axSpA的药物的营销授权通过了肯定意见。
在加拿大,Taltz已被批准用于axSpA、斑块型银屑病和银屑病关节炎的放射治疗。
注:以上信息截止2020年。
Taltz的作用机制
Ixekizumab是一种通过重组DNA技术在重组哺乳动物细胞系中产生的人源化IgG4单克隆抗体。它选择性地与IL-17A细胞因子结合,并阻断其与IL-17受体的相互作用,IL-17受体是体内负责炎性和免疫反应的天然细胞因子。这会抑制体内提醒免疫细胞的细胞因子和趋化因子的释放。
Taltz (ixekizumab)
Taltz的临床研究
FDA批准Taltz治疗nr-axSpA是基于一项为期52周、多中心、随机、双盲、安慰剂对照的III期临床研究COAST-X的结果。
本研究评估了该药物的安全性和有效性,主要目标是改善患者nr-axSpA的体征和症状,属于脊椎关节炎国际协会40 (ASAS40)反应评估。
在这项研究中,304名患者被随机分配接受每四周或两周一次的80mg Taltz治疗或安慰剂治疗。在第16周,每四周接受talz治疗的患者中有35%的患者,每两周接受talz治疗的患者中有40%的患者出现ASAS40应答,而接受安慰剂治疗的患者中只有19%出现此现象。
在第52周,30%的患者每四周接受一次talz治疗,31%的患者每两周接受一次talz治疗,这两个比例在接受安慰剂治疗的患者中为13%。
结果显示该药物的安全性概况与其他已批准条件下先前报告的数据一致。
临床试验期间在患者中观察到的一些常见副作用有注射部位反应、上呼吸道感染、恶心和真菌感染。
注:本文旨在介绍医药健康研究,不作任何用药依据,具体用药指引,请咨询主治医师。