专题五 化学计算
类型一 有关化学式的计算
【方法技巧】 以AmBn为例,设A、B两种元素的相对原子质量分别为a、b,则
AmBn的相对分子质量=ma+nb。
A、B元素的原子个数比=m∶n。
A、B元素的质量比=ma∶nb。
A元素的质量分数=eq \f(ma,ma+nb)×100%。
例1 (2016·内江)中国科学家屠呦呦因创制了新型抗疟药——青蒿素和双氢青蒿素,挽救了全球数百万人的生命,获得了2015年诺贝尔生理学或医学奖。青蒿素的化学式为C15H22O5。
(1)青蒿素含有________种元素,它属于__________(填"无机物"或"有机物")。
(2)青蒿素中各元素的质量比为____________(最简整数比)。
(3)青蒿素中碳元素的质量分数为__________(计算结果精确到0.1%)。
例2 如图为某市加碘低钠盐的标签:

(1)根据包装袋上所要求的食用和储存方法,可以推测KIO3可能的化学性质为__________________。
(2)KIO3中钾、碘、氧三种元素的质量比为__________。
(3)KIO3中碘元素的质量分数为__________(结果精确到0.1%)。
(4)根据资料卡片,该市实行新标准后,每千克食用盐中至少加了__________mg的碘酸钾。
例3 (2016·*安泰**改编)α-丙氨酸是合成蛋白质的基础物质之一,其分子结构如图所示(注"—"表示原子之间相互连接),试计算:
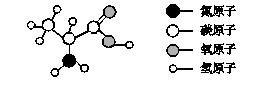
(1)α-丙氨酸的化学式为__________,相对分子质量为__________。
(2)α-丙氨酸中碳、氢、氧元素的原子个数比为__________。
(3)17.8 g α-丙氨酸中含氮元素的质量为__________g。
类型二 有关化学方程式的综合计算
中考中有关化学方程式的计算通常与图像、图表、实验或溶液中溶质质量分数的计算相结合,题目较为综合。尤其需要注意的是:求反应后所得溶液中溶质的质量分数时,应先分别求出溶质的质量和溶液的质量。计算溶质的质量时应注意分析原物质中是否含有该物质。计算所得溶液的质量时应注意减去生成的沉淀、气体的质量和不溶性杂质的质量,即反应后所得溶液的质量=加入容器中所有物质的质量-生成沉淀的质量-生成气体的质量-不溶性杂质的质量。
题型一 文字叙述类
【方法技巧】 该类计算一般以文字叙述的形式给出发生的反应及反应物、生成物的质量信息,答题时应注意读取、理解题目叙述中隐含的信息,找出反应物、生成物之间的质量关系,然后按步骤答题。
例4 (2016·雅安)取氯酸钾和二氧化锰的混合物13 g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质量为8.2 g,将剩余固体加入一定量的水中,充分搅拌后过滤,滤液是10%的氯化钾溶液(假设溶液无损失),计算:
(1)生成氧气的质量;
(2)参加反应的氯酸钾的质量;(写出计算过程)
(3)氯化钾溶液的质量。(写出计算过程)
题型二 表格数据类
【方法技巧】 表格数据类计算题,一般有三种形式:①随着加入某一反应物的质量增加,另一反应物的质量不断减少直至不再改变;②随着加入某一反应物的质量增加,产物的质量不断增大直至不再改变;③随着时间的推移,某一反应物的质量不断减少或某一生成物的质量不断增大直至不再改变。答题时要找出恰好完全反应的点,判断反应物的过量情况或加入一定量的某一反应物消耗另一种反应物的量。分析时,注意利用质量守恒定律分析生成的沉淀、气体的质量,进而进行计算。
例5 某化学兴趣小组使用右图所示装置,对某种铁铜合金的成分进行测量。先取足量稀硫酸于烧杯中,再向其中加入14.0 g合金样品开始计时,并将电子天平的读数记录在下表中。
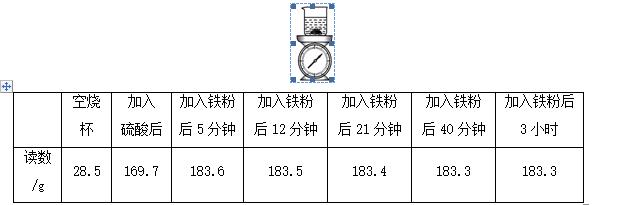
请回答下列问题:
(1)根据电子天平读数和时间的关系分析,该反应进行过程中,氢气的产生速度有什么特点?
(2)完全反应后,所得溶液中盐的质量分数为多少?
(3)合金中铁元素的质量分数为多少?
例6 (2016·黔南州)小芳同学采用如下方法测定石灰石中碳酸钙的质量分数:取该石灰石样品10 g,把40 g稀盐酸分四次加入,实验过程所得数据如表(石灰石样品中含有的二氧化硅等杂质不溶于水也不与稀盐酸反应)
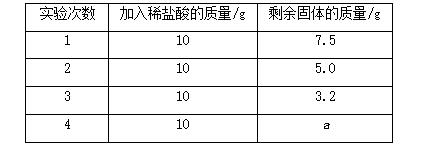
根据实验数据计算:
(1)表中a的数值为__________;
(2)样品中碳酸钙的质量分数是__________;
(3)求盐酸中溶质的质量分数。
题型三 坐标图像类
【方法技巧】 坐标图像类计算题的主要特点是数据要经过分析坐标图像后才能获得,必须结合数学知识,而且要理清题目中涉及的化学反应,可能需要判断所涉及的反应的先后顺序,再结合图像分析每段图像对应的化学反应,弄清楚"起点""转折点""终点"的化学含义,确定相关物质的质量。
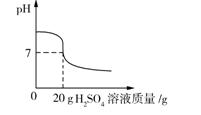
例7 (2015·深圳)某小组欲用4.9%的稀H2SO4测一瓶标签破损的NaOH溶液的质量分数。
(1)从一瓶标签模糊的NaOH溶液里取出几滴后向________(填写溶液名称)里滴加,呈红色。
(2)取10 g NaOH溶液样品,并与4.9%的稀硫酸溶液混合。由图可得,完全反应时,所用稀硫酸溶液中溶质的质量为__________。
(3)求NaOH溶液样品中溶质的质量分数。
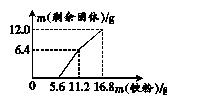
例8 (2016·梅州)现有FeCl3和CuCl2的混合溶液195.2 g,向其中加入铁粉,反应的先后顺序为:2FeCl3+Fe=== 3FeCl2、CuCl2+Fe=== FeCl2+Cu。加入铁粉质量与反应后溶液中剩余固体质量的关系如图所示。
(1)m(剩余固体)>6.4 g时,剩余固体的成分是__________(填化学式),此剩余固体加入盐酸,发生反应的化学方程式为____________________________。
(2)原FeCl3和CuCl2的混合溶液中FeCl3的质量为__________g。
(3)求当加入11.2 g铁粉时,反应后所得溶液中FeCl2的质量分数。(写出计算过程)
题型四 图表结合类
【方法技巧】 图表结合类计算题主要是在一道计算题中增加考查方式,要掌握解上述表格和图像类计算题的方法技巧。值得注意的是该类题目在图表结合时,往往会有承上启下的过程,需要考生有较强的分析能力,知道每一个环节研究的对象是原来样品中的某物质还是经过反应后得到的产物(继续实验),否则很容易失分。
例9 (2015·东营)在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂。他们对该试剂进行了定量实验分析:称取试剂19.8 g放入锥形瓶中,加入30.2 g的水,充分振荡,再向锥形瓶中依次滴加25 g盐酸充分反应。测得部分数据与图像如下。请根据有关信息回答问题。
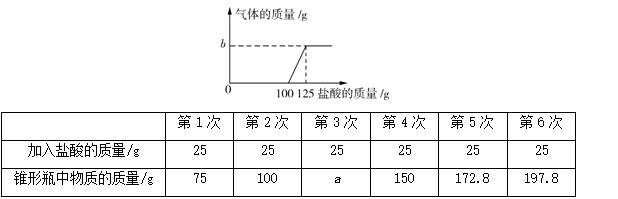
(1)a的数值为__________,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图像作出你的分析)_______________________________________
________________________________________________________________________。
(2)b的数值为____________。计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数)。
题型五 结合实验类
【方法技巧】 该类题目的特点是在实验探究的基础上(一般以实验装置图呈现)对某个化学问题进行分析,也结合定量(数据、表格、图像)更严谨、更综合地分析,该类题目要求认真审题,充分挖掘题目所给的信息,首先弄明白实验的目的,然后顺着实验步骤推理得出实验结论,根据已知条件,找到解题的突破口,再按照题目设问求解,将实验结论转化为计算条件,充分利用质量守恒定律,尤其关注每一个等量关系。
例10 (2014·广东)同学们做甲、乙两个中和反应实验的探究(见下图)。
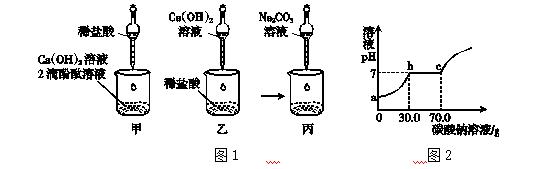
(1)甲实验恰好中和,则该溶液中的溶质是__________(填化学式)。
(2)取乙反应后的溶液60.0 g,滴加质量分数26.5%的Na2CO3溶液(见丙图),溶液pH的变化如图2所示。则与CaCl2反应的碳酸钠溶液的质量为__________g;请计算该溶液中CaCl2的溶质质量分数(写出计算过程,精确到0.1%)。
(3)根据计算所得数据在图3中画出产生沉淀的曲线。
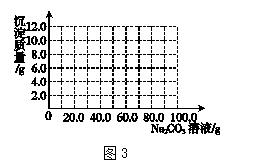
(4)乙组的中和反应实验设计存在的不足是_________________________。
例11 (2012·广东)甲、乙两同学用氧化铜做了如下实验,请回答有关问题:
甲同学:取40 g氧化铜与足量稀硫酸充分反应后得蓝色溶液。
(1)甲同学所得溶液中使溶液显蓝色的溶质的化学式为__________。
(2)溶液中含硫酸铜的质量是多少?写出计算过程。
乙同学:将五份含6 g炭粉和40 g氧化铜的混合物,分别放入密闭的容器中隔绝空气加强热。在不同的反应时间里收集到如下数据:
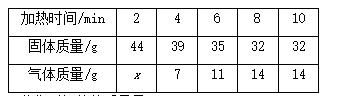
(3)①加热2 min收集到气体的质量是__________g。
②混合固体在加热过程中产生的反应有:CuO+Ceq \o(=====,\s\up7(高温)) Cu+CO↑、2CuO+Ceq \o(=====,\s\up7(高温)) 2Cu+CO2↑,还可能发生反应的化学方程式为__________________________________(写一个);加热8 min后容器中的气体的化学式为__________。