
第一作者:Bingyu Lu
通讯作者:Wurigumula Bao, Ying Shirley Meng
通讯单位:加州大学圣地亚哥分校,芝加哥大学
【研究背景】
随着高性能电动汽车和个人便携式设备需求的快速增长,锂(Li)金属由于其高比容量和低电化学电位,已成为开发高能量密度可充电电池负极材料的热门候选者。尽管已经进行了广泛的研究以延长锂金属负极的循环寿命,但金属锂在高能量密度电池中带来的潜在安全隐患仍然是其大规模商业化之前的最大障碍之一。20世纪80年代,锂金属电池首次尝试商业化,但以失败告终,当时报告了多起电池着火的案例。从那时起,使用锂金属作为高能电池负极材料的安全问题从未停止过。其中,电池级别的安全隐患取决于每个电池组件的反应性以及它们之间的相互作用。至于商业化锂离子电池,利用加速速率量热法(ARC)和X射线衍射法(XRD),Dahn等人发现锂化石墨(Li0.81C6)在低至90℃的温度下开始与电解液分解。Amine等人应用原位同步辐射XRD和质谱(MS)研究了稳健SEI在保护锂化石墨免受热分解中的作用。根据目前的文献,可以得出结论,锂化石墨(Li-Gr)在材料水平上远非安全稳定的材料,但它可以通过适当的工程和优化在最先进的电池组中实现。
作为一种高活性碱金属,Li一直被认为对实际电池不安全,已经进行了各种尝试来设计安全的可充电锂金属电池。1995年,Aurbach及其同事展示了AA尺寸的Li||LiMnO电池可以承受短路和过充电测试。然而,电池安全性受到循环数的严重影响。最近,人们提出了具有不易燃溶剂的新型电解质作为防止电池着火的方法。阻燃局部高浓度电解质(LHCE)也已使用不易燃的溶剂或稀释剂开发,例如磷酸三甲酯或HFE等。尽管这些工作集中在防止电池着火上,但目前尚不清楚锂金属在自然界中的活性如何,更不用说在类似充电状态下与其他负极材料进行直接比较。
【成果简介】
在此, 美国加州大学圣地亚哥分校孟颖教授和芝加哥大学Wurigumula Bao 利用差示扫描量热法(DSC)与原位傅里叶变换红外光谱(FTIR)相结合, 定量比较了两种不同电解液中Li-Gr,Li-Si和锂金属(电沉积Li)的反应性,通过精确调整电沉积过程中的外部堆叠压力,进一步探讨了Li形貌对反应性的影响 。研究发现, 电解液组成、Li沉积形貌、控制非活性Li和正极稳定性 等所有电池成分在调节锂沉积的反应性方面起着至关重要的作用 。通过优化这些因素,锂金属全电池在高达400°C时没有表现出明显的热反应。在设计良好的系统中,锂沉积金属的热响应可以与Li-Gr和Li-Si的热响应具有相同的幅度。此外,还分析了正极对锂金属反应性的影响。这项研究确定了控制锂金属反应性的关键参数,对推进锂金属电池的设计和制造至关重要。
相关研究成果以“ Key Parameters in Determining the Reactivity of Lithium Metal Battery ”为题发表在 ACS Energy Lett. 上。
【核心内容】
人们普遍认为,当组装在电池中时,原始石墨和硅比锂金属安全得多。然而,在实际应用中,电池主要处于负极锂化的充电状态,其化学稳定性明显降低。因此,锂金属的反应性应与Li-Gr和Li-Si的反应性进行比较,而不是原始的反应性。需要做更多的工作来确定控制电池系统中锂金属反应性的关键参数,并为安全的锂金属电池(LMB)提供设计原则。有多种方法可以定义不同卷轴下的金属反应性。例如,当(1)金属在氧化反应过程中引起较大的负生成焓 ΔHf ,或(2)在氧化或水化过程中需要较小的升华能和电离能时,金属被认为是高度反应性的。由于带电状态下的负极充满了要释放的电子,它们也会与水和氧发生剧烈的反应,定量比较不同负极材料在良好控制的电池系统中的反应性是很重要的。
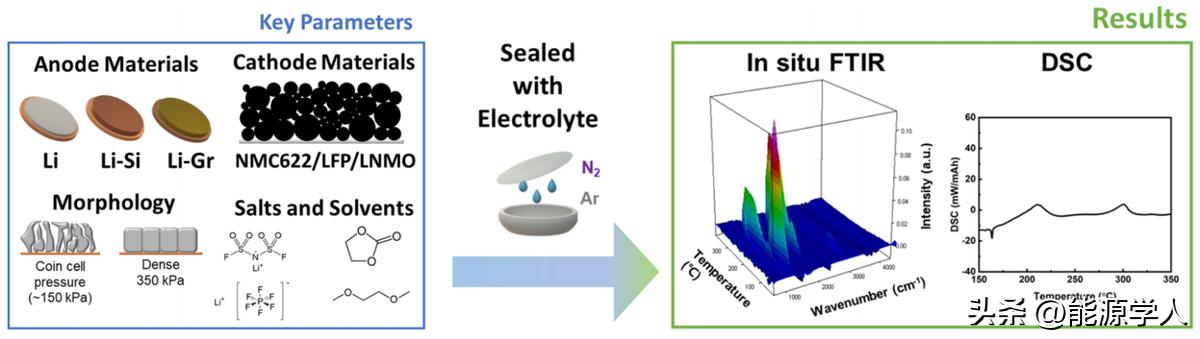
图1. 样品制备和实验工艺的原理图。
图2显示了在普通碳酸酯电解液和局部高浓电解液中Li-Gr,Li-Si和沉积锂的DSC曲线,在Li-Gr和Li-Si中,大多数吸热峰与电解液溶剂(如DEC和EC)的蒸发有关(图2a)。当加热至400℃时,Li-Gr和Li-Si样品中没有明显的放热峰。然而,当碳酸盐中的沉积锂在DSC测量期间被加热时,两个放热峰分别与DEC和EC溶剂的蒸发重叠(图2c)。当Li在180℃左右熔化时,出现尖锐的吸热峰。放热反应可能是由熔化的Li与剩余的EC溶剂和LiPF6快速反应引起的。图2d显示了LHCE电解质中沉积锂的DSC曲线。DME和TTE溶剂大多在100℃之前蒸发,由于其蒸发点低,而不是与Li反应。在图2d中,在180℃左右也显示出一个尖锐的Li熔点,这表明Li在加热过程中大部分被熔化而不是氧化。Li完全熔化后可以观察到一个小的氧化峰,这与电解质液的分解有关。
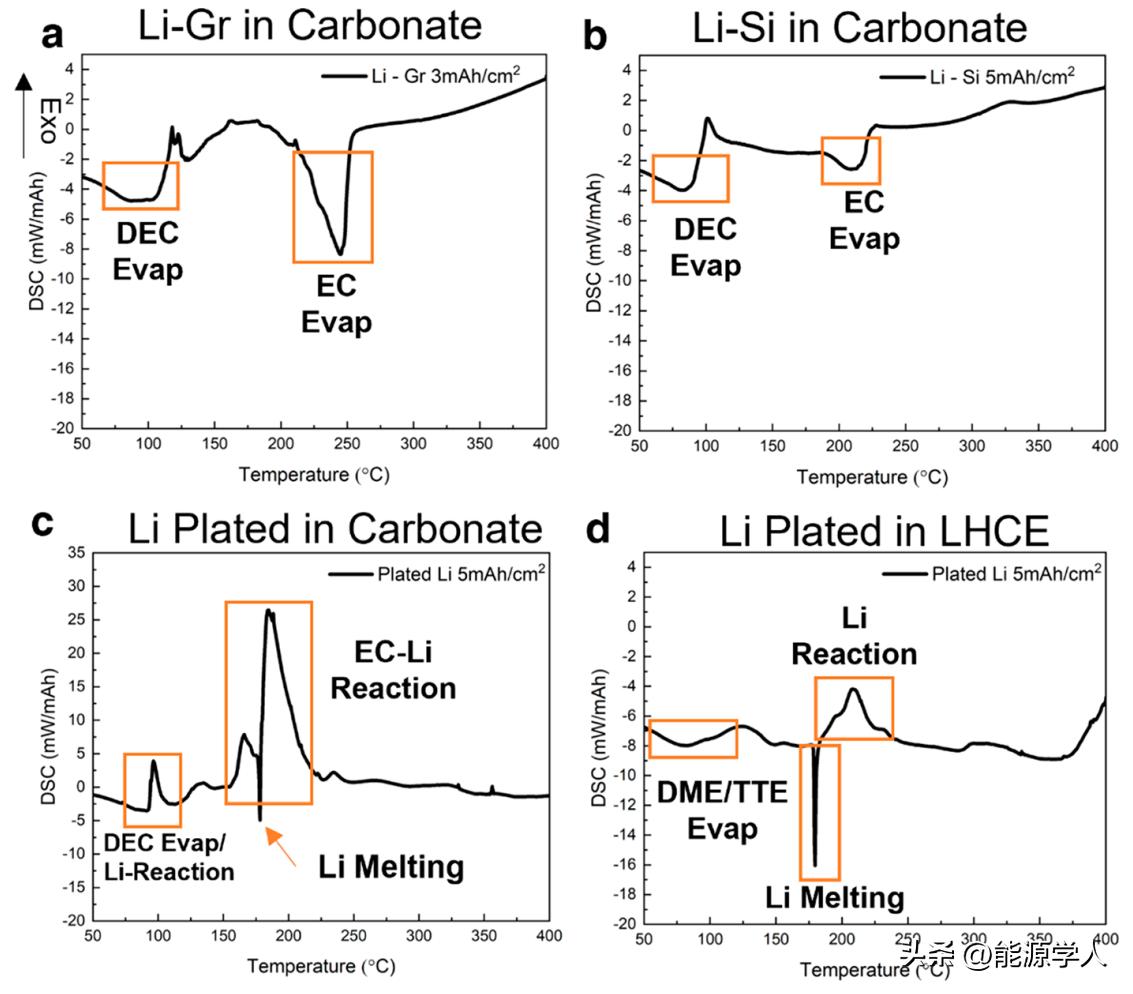
图2. LHCE中三种不同负极的DSC测试。
图3a-c显示了循环10次后锂化石墨负极的DSC曲线和形貌,与第一循环充电态石墨样品类似,大多数DSC峰与电解液溶剂的蒸发有关。同时,如图3b,c所示,石墨表面似乎有一些SEI积累,层状表面形貌在循环10次后消失,小的放热峰(约100和230℃)可能与溶剂蒸发过程中Li-Gr电极的氧化有关。在循环10次后Li-Si负极中也发现了类似的趋势(图3d-f),在同一温度范围内也发现了两个放热峰(约100和230℃),SEI积累在Si表面上也很明显。总体而言,锂化硅和石墨的反应性相对较低,在加热过程中没有观察到大的放热峰。图3g显示了循环10次后LHCE电解液中沉积锂的DSC曲线,如插入的图像和SEM图像所示(图3h,i),由于LHCE的优越性能,沉积的Li仍然有光泽。
此外,大多数电解液溶剂在Li熔点之前蒸发。因此,LHCE中Li的热响应仍然相对较低,与Li-Gr和Li-Si情况相同。然而,对于碳酸盐中的电镀锂,电极表面积聚了大量的苔藓状锂(图3k,l和图3j的插图)。 由于碳酸酯电解液的低库仑效率(CE),电极上积累了大量的纳米级非活性Li,这些纳米尺寸的非活性Li的积累最终在加热过程中引起了DSC曲线的变化。这些发现与Aurbach及其同事提出的评论相对应,即循环数在电池安全中起着至关重要的作用,非活性Li随着循环数的增加不断积累。
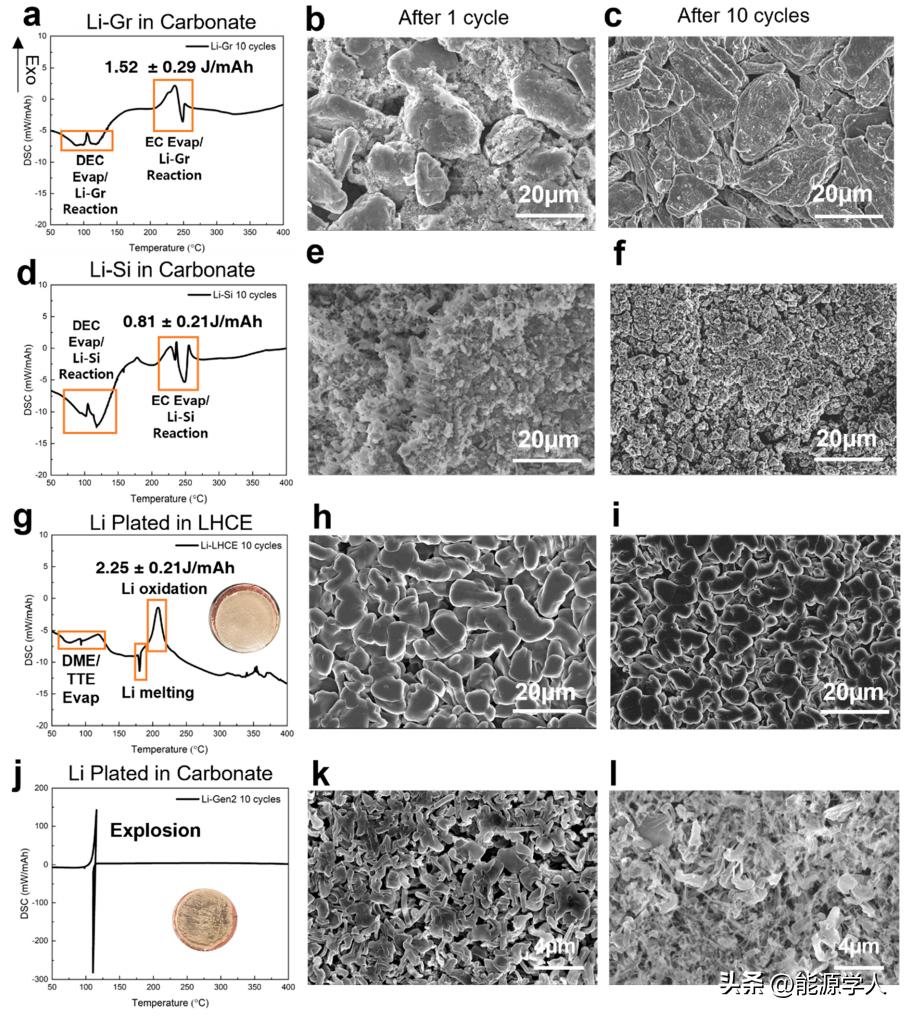
图3. 循环10圈后三种不同负极的SEM图像。
此外,原位FTIR用于追踪金属锂DSC过程中的气体逸出,以研究电解液对沉积锂的影响。图4a,c显示了碳酸酯电解液中气体的FTIR光谱。在130℃之前,大多数峰与DEC的蒸发有关。光谱有两个主峰,分别位于1268和1771 cm-1,分别表示DEC分子上的O-C-O对称拉伸和C=O拉伸。与碳酸酯电解液相反,由于TTE和DME的低沸点,LHCE电解液中的溶剂在120℃之前蒸发(图4b,d)。因此,Li的氧化主要是由残余有机成分和电解液盐引起的,原始LHCE的DSC也证实了这一观察结果。 迄今为止的结果证实, 电解液溶剂是锂金属电池热不稳定的主要原因 。然而, 未来的电解质设计不仅要研究溶剂的阻燃特性,还需要关注电解液盐的热稳定性,因为盐的分解导致FSI-阴离子中的S-N键断裂形成FSO2N·自由基,还会氧化熔融的Li,与脱锂的正极相互作用,最终引起热量甚至火灾的发生。
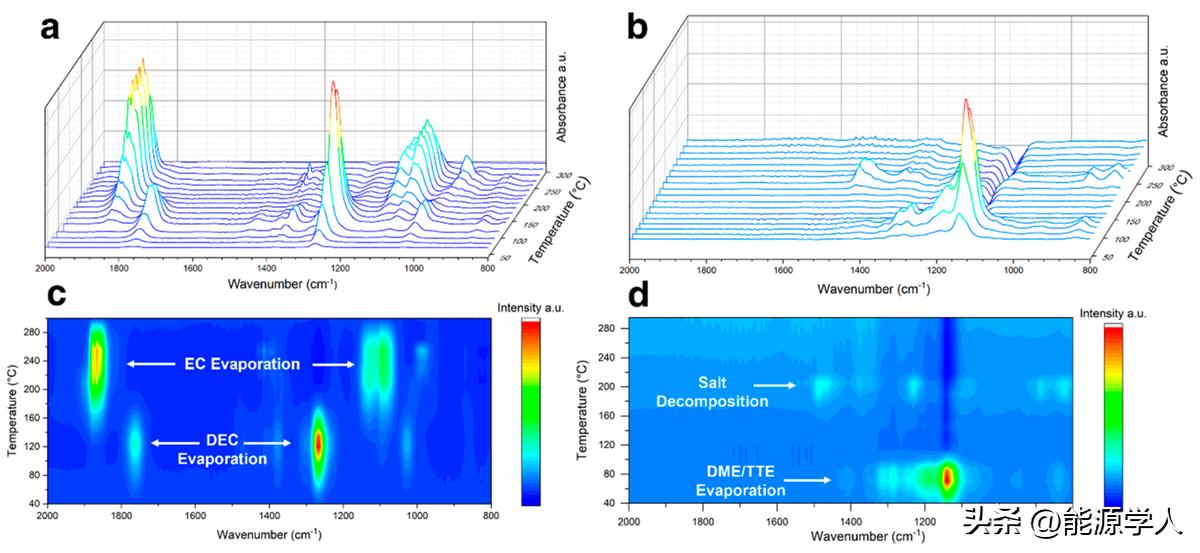
图4. 不同温度下在碳酸酯电解液和LHCE电解液中沉积锂的原位FTIR光谱。
作者还研究了Li形貌对Li反应性的影响, 即使使用以产生Li枝晶而闻名的碳酸酯电解液,在不同的压力下,沉积的Li也可以实现接近100%的致密形貌 。随着形貌的改善,Li孔隙率明显降低,如图5e所示。沉积锂显示出相对缓慢的氧化过程,而不是如图5d所示的突然热量释放。结果表明, 电解液和Li形貌在控制Li反应性方面均起关键作用。Li的大部分氧化发生在Li和电解液之间,如果Li可以沉积成接近100%致密的形貌,则可以明显减小Li与电解液之间的接触表面积,从而使电解液对Li金属的氧化也可以在很大程度上减慢。
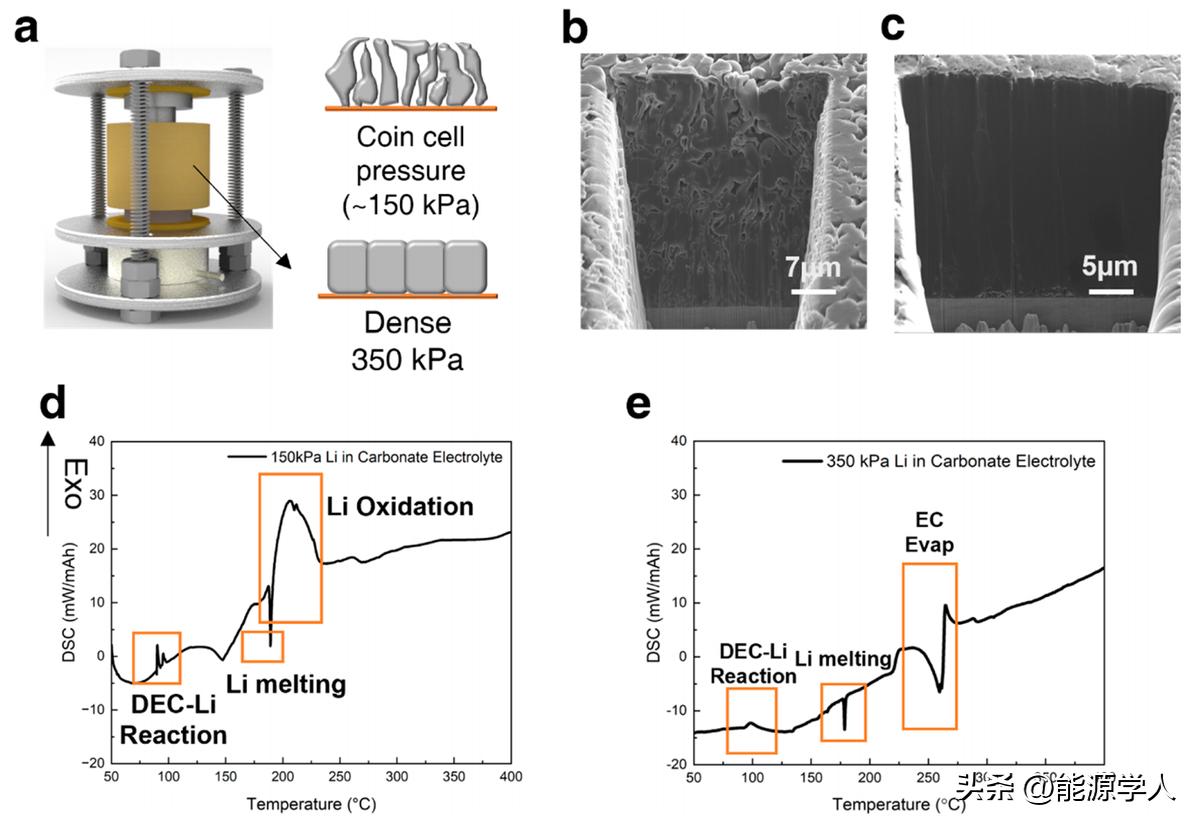
图5. 不同压力下锂沉积的差异。
还分析了锂金属全电池的反应性,图6a显示了带有电解液和隔膜的脱锂NMC622的DSC曲线。结果显示,脱锂的NMC622在220和300°C左右分解,释放出O2。除此之外,在220°C左右也观察到LiFSI盐的分解,这与NMC622的分解重叠。当脱锂的NMC622与沉积锂偶联时,从分解的正极和LiFSI盐释放的氧气将与Li剧烈反应并引起大量的热量释放(图6b)。即使优化了Li形貌和电解液,O2仍然不利于全电池水平的安全性。
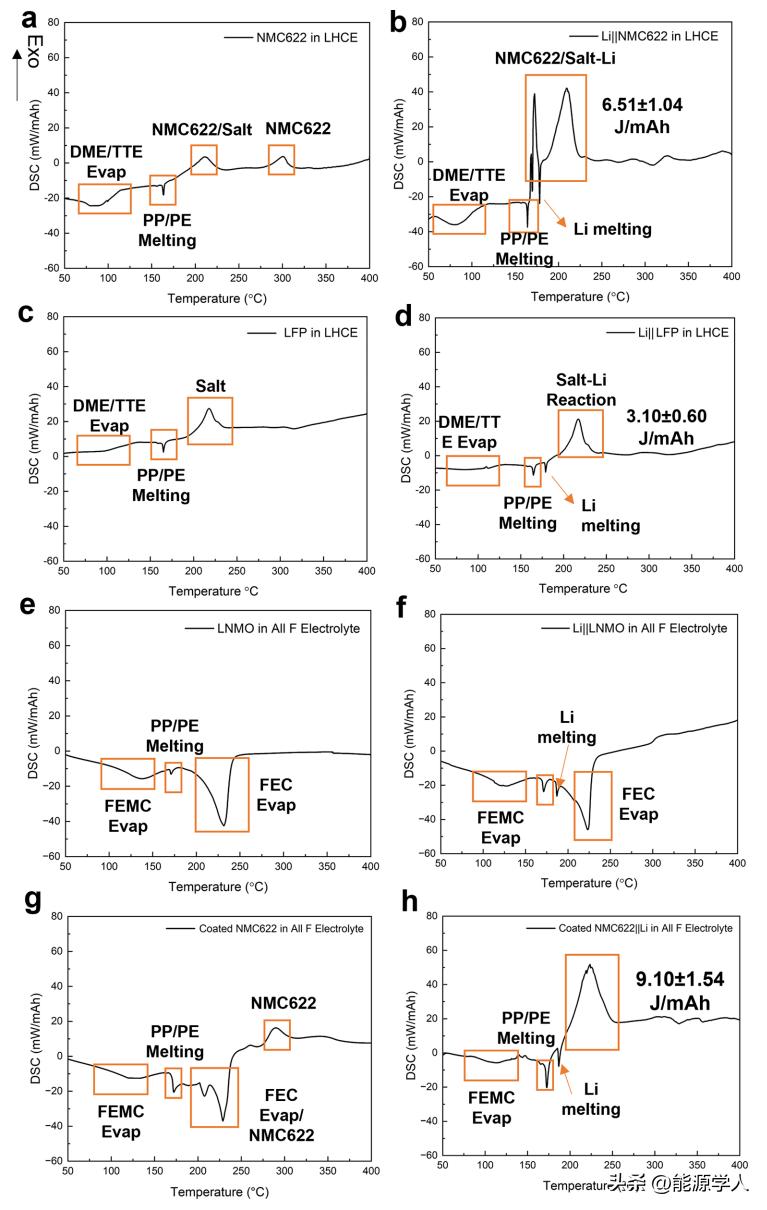
图6. 正极材料的DSC曲线。
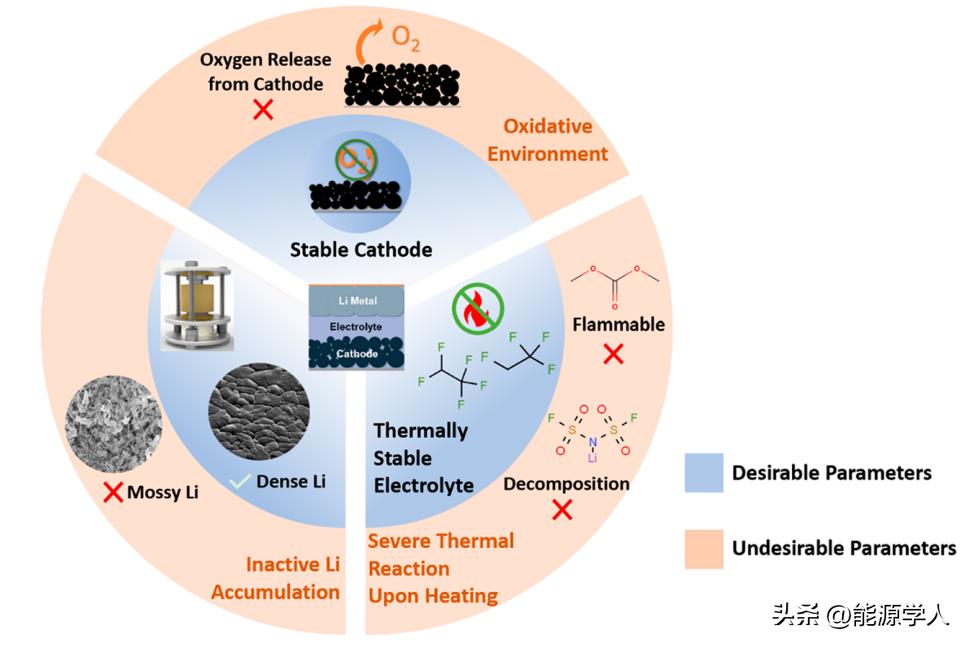
图7. 控制锂金属电池反应性的关键参数:内环表示锂金属负极的优化条件,而外环表示未优化条件。
【结论展望】
综上所述,本文使用DSC和原位FTIR技术比较了Li-Gr,Li-Si和沉积Li的反应性。研究发现,电池中沉积锂的反应性与其形貌和电解液组成高度相关(图7)。凭借致密的形态和新型电解质,电池中沉积锂的反应性可以大幅抑制到与Li-Gr和Li-S负极相同的水平。因此,将Li沉积致密的形态以最小化其表面积并利用热稳定的电解液,这对Li金属电池的安全循环至关重要。此外,使用锂金属负极时,正极热分解的串扰影响可能会造成安全隐患。通过改用热稳定性更高的正极材料,如LFP和LNMO,可以大大提高锂金属全电池的热稳定性。此外,电解液盐的分解也必须严格控制。最后,循环次数和电池环境对锂金属反应性有影响。即使在延长周期后,控制非活性Li和Li形貌的积累也很重要。本工作发现的控制锂金属反应性的关键参数可应用于未来实用锂金属全电池锂金属负极的研究。
【文献信息】
Bingyu Lu, Diyi Cheng, Bhagath Sreenarayanan, Weikang Li, Bhargav Bhamwala, Wurigumula Bao,* Ying Shirley Meng*, Key Parameters in Determining the Reactivity of Lithium Metal Battery , , 2023, ACS Energy Lett. , https://doi.org/10.1021/acsenergylett.3c01001