导读:
锂电池是一次性电池,锂离子电池是可充电循环电池,锂离子电池与锂电池的原理。
相同之处是:两种电池都采用了一种能使锂离子嵌入和脱出的金属氧化物或硫化物作为正极,采用一种有机溶剂-无机盐体系作为电解质。
不同之处是:在锂离子电池中采用可使锂离子嵌入和脱出的碳材料代替纯锂作为负极。
正文:
锂离子电池正极材料工作原理
锂离子电池的正极是整个电池中可嵌脱锂离子的来源,其基本要求包括:
①放电反应应该有较负的吉布斯自由能较高的放电电压。
②基体结构的分子量要低并且能够插入大量的Li+高质量比容量。
③主体结构的Li+扩散和电子迁移速度必须快高功率密度。
④Li+嵌入与脱出可逆,嵌脱过程中主体结构的变化要小长循环寿命。
⑤化学稳定性要好,无毒,性价比高。
⑥材料的制备容易。
正极材料的选取首先要考虑其是否具有合适的电位,而电位取决于锂在正极材料中的电化学势μC,即从正极材料晶格中脱出锂离子的能量及从正极晶格中转移出电子能量的总和,前者即为晶格中锂位的位能,后者则与晶格体系的电子功函密切相关,这两者又相互作用。
位能是决定μC的最主要因素,其次是锂离子之间的相互作用。
氧化还原电对导带底部与阴离子p轨道间的距离从本质上限制了正极材料的电极电位。
正极材料电位不仅与氧化还原电对元素原子的价态相关,而且与该原子同最近邻原子的共价键成分相关,氧化还原电对所处的离子环境影响该电对的共价键成分从而影响材料的电极电位。
例如,Fe3+/Fe2+电对在不同磷酸盐体系中由于磷原子在不同晶体结构中对铁原子具有不同的诱导作用,使得该电对在不同的磷酸盐体系中具有不同的费米能级,即各种磷酸盐材料具有不同的电极电位正极材料的反应机理有两类: 固溶体类型和两相反应类型。
①固溶体反应
锂离子嵌入脱出时没有新相生成,正极材料晶体结构类型不发生变化,但晶格参数有所变化。随着锂离子的嵌入电池电压逐步减小,放电曲线呈S形,
(a)所示。以MO2+Li++e-LiMO2为例,其电极电位可表达如下。
式中 ——标准电极电位; R——理想气体常数; T——热力学温度; F——法拉第常数; y——材料晶体结构中锂含量; by——嵌入晶体结构中Li+的相互作用。
(a)均一固相反应;
(b)两相反应
②两相反应
锂离子嵌入/脱出时有新相生成,正极材料晶体结构发生变化伴随第二相生成,电池电压在两相共存区保持不变,放电后期电池电压随着活性物质消耗急剧减小,放电曲线呈L形。
(b)所示。以MO2+Li++e-LiMO2为例,电极电位表达式如下。
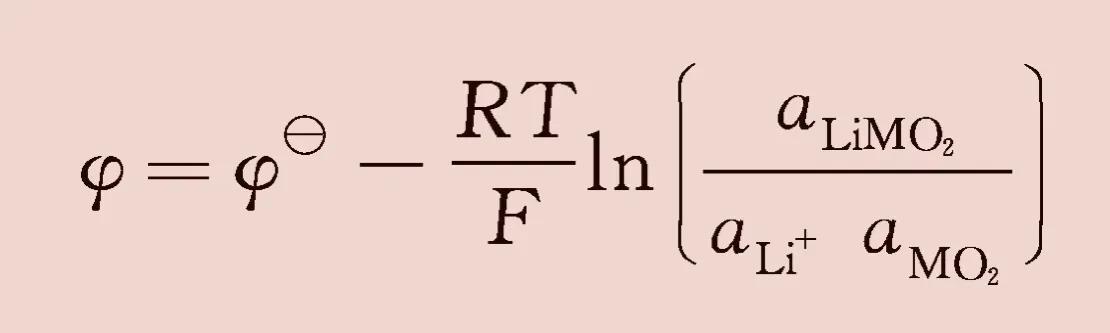
式中,a表示各种物质的活度。 锂离子电池正极材料的研究已有半个世纪历史,到目前为止,据称已有二百余种锂离子电池正极材料。
但真正可以实用的,也是人们研究最多的,是具有固溶体反应行为的过渡金属氧化物和具有两相反应行为的磷酸盐。
常见的真正实际有生产的,也是将要讨论的正极材料,包括钴酸锂、镍钴锰三元、NCA材料、锰酸锂和磷酸铁锂等。
1、钴酸锂
LiCoO2是第一种锂离子电池的正极材料,在40年的发展过程中,虽然有一些改性和提高,但基本上可以认为它是最成熟的锂离子电池正极材料。
该材料具有放电平台高、比容量较高(140mA·h/g左右)、循环性能好、合成工艺简单等优点。
目前它仍是锂离子电池,特别是小型锂离子电池的最佳选择。但该材料中钴元素毒性较大,价格昂贵,同时制作大型动力电池时安全性难以得到保证。
LiCoO2属于α-NaFeO2的结构,在氧离子(O2-)形成的立方密堆积框架结构中,CoO2和Li层交替连续排列形成空间群,Li和Co都是八面体配位。
LiCoO2中Co3+的3d电子以低自旋形式存在,3d轨道中六个电子全部占据t2g轨道,eg轨道全空。在充电过程中,当脱锂量小于0.5时,材料没有相变,脱锂是一种固溶体行为。
同时Co3+被氧化为Co4+,伴随着从t2g轨道中脱出电子。随着锂离子的脱出,相邻CoO2层之间的静电排斥力增大,使得c轴增长。在脱锂量达到0.5时,会发生六方—单斜的相转变,这意味着,锂的排列从有序变为无序。
如果再进一步充电,由于钴的t2g轨道与氧的2p轨道有重叠,此时锂离子脱出时会造成氧离子的2p轨道同时脱出电子,导致氧离子脱离晶格被氧化为氧气。
研究发现随着锂离子脱出量的增加,钴在电解液中的溶解量增加,严重影响LiCoO2的循环稳定性及LiCoO2电池的安全性能。
所以LiCoO2 的充电截止电压一般为4.2V,过高的充电截止电压,或者说过多的锂离子脱出,不仅会破坏LiCoO2的结构,也会带来安全问题。
所以LiCoO2的实际可逆容量仅为理论容量的一半左右。 LiCoO2应用的另一个问题是钴的资源问题。
钴在地壳中的丰度仅为0.0025%,大规模使用已经造成了钴的稀缺和价格上涨。
2、镍酸锂
由于Co的资源问题,人们最初试图开发镍酸锂(LiNiO2)来替代钴酸锂。与钴酸锂相比,锂镍氧系正极材料的实际比容量高,原材料价格低廉而且来源广泛。但人们很快就发现LiNiO2制备困难,并且热稳定性差,存在较大的安全隐患。
与Co3+相比,Ni3+多一个核外电子,Ni3+的3d电子以低自旋的形式排布,这一方面使得LiNiO2可参与电化学反应的电子数增多,实际比容量提高。
另一方面其中有一个电子要占据能量较高的eg轨道,导致Ni—O键没有Co—O键稳定,降低了LiNiO2的电化学及热稳定性能
由于Ni2+较难氧化为Ni3+,较难合成化学计量比的LiNiO2,所以LiNiO2一般在氧气气氛下合成。
另外,由于Li+与Ni2+半径相近,Ni2+容易进入Li+的3a位,形成不具有电化学活性的立方“岩盐磁畴”相,降低了LiNiO2实际放电比容量,并且进入3a 位的Ni2+在脱锂后期被氧化为半径更小的Ni3+/Ni4+导致附近晶格结构塌陷,阻碍Li+的正常可逆脱嵌,严重影响LiNiO2的电化学性能。
研究人员一直试图对LiNiO2进行改性以得到比容量更高的材料体系。
有研究人员发现在层状氧化物锂盐中,钴、镍、锰三种元素可以以任意比例无限互溶,利用这一特性,可以制备诸如:
LiNi1-xCoxO2、
LiNi1-xMnxO2、
LiNi1-x-yCoxMnyO2
等固溶体材料。其中NMC三元材料在降低材料成本的同时,结合了钴酸锂优良的循环性能,镍酸锂较高的放电容量和锰酸锂优异的安全性能,三者的协同效应使得该材料具有优良的电化学性能。
常见的三元材料主要有:
Li[Ni1/3Co 1/3Mn1/3]O2、Li[Ni0.4Co0.2Mn0.4]O2、Li[Ni0.5Co0.2Mn0.3]O2
等等,这一系列材料中,三种过渡金属离子的组成比例对材料的电化学性能和热稳定性有着显著的影响。
可以比较明显的看到,随着镍含量的增加,虽然材料的容量增加了,但其循环稳定性下降,功率性能变差,同时热稳定性降低。
NMC系列三元材料的组成与性能比较
由LiNi1-xCoxO2掺Al发展而来的
Li[Ni0.8Co0.15Al0.05]O2
(NCA)材料,也可以看成是LiNiO2、LiCoO2和LiAlO2的固溶体。
相对于LiCoO2材料,NCA材料在大大减少了Co的用量之后,尽管其放电电压平台要低0.1~0.2V,但容量可以达到180~210mA·h/g,综合在能量密度上仍比LiCoO2有所提高。
同时由于Al的引入,提高了材料的热力学稳定性。因此被认为是一种比较稳定的高容量正极材料。
3、锰酸锂
锰酸锂(LiMn2O4)
具有较高的氧化电位,其热稳定性能比钴酸锂和镍酸锂好,耐过充。LiMn2O4为标准的立方尖晶石结构,属于Fd3m空间群,该结构中锂属于四面体配位,过渡金属元素锰是八面体配位。
其尖晶石结构为锂离子的嵌入/脱出提供了良好的通道,有利于大电流充放电。
LiMn2O4的理论容量为148mA·h/g,实际容量达到120mA·h/g左右。LixMn2O4的主要电化学反应发生在4V附近,对应的x值为0<x<1,在这个范围内,材料保持立方对称,Li+脱出/嵌入没有引起非常明显的体积膨胀或收缩。
因此,在3.5~4.5V电压范围,LiMn2O4具有较好的循环寿命。而在更低的电压平台3V附近,对应的x值为1<x<2,Jahn-Tell效应导致材料从立方晶系向四方晶系发生转变,即c/a值发生了较大的变化,晶体结构发生严重扭曲。晶体结构的扭曲使得材料承受微应力,导致循环时容量会迅速衰减。
因此LiMn2O4的应用研究主要在4V区域内。 尖晶石LiMn2O4具有工作电压高、安全性好、性价比高和环境友好等优点,但是在高温循环过程中,由于锰的溶解、Jahn-Teller效应和电解液的分解等问题导致容量衰减特别严重。
4、磷酸铁锂
磷酸铁锂 LITHIUM IRO
磷酸铁锂 化学式: FeLiO4P
磷化工行业分析:
从零到磷酸铁锂,磷酸铁锂属于磷酸盐的一种,是目前磷化工产业链中景气度最高的细分品类。
中文名:磷酸铁锂
英文名:LITHIUM IRON
LiFePO4中的阳离子排列不同于层状LiCoO2和尖晶石LiMn2O4。
Fe2+处于氧八面体的4c位,Li+处于氧八面体的4a位。聚阴离子结构热稳定性较好,但是八面体结构的FeO6被四面体结构中的O原子分开而未能形成连续的FeO6网络,导致LiFePO4的电子电导率较差。
室温下:
LiFePO4的电子电导率为10-10~10-9S/cm。
远远低于LiCoO2(约10-3S/cm)
和LiMn2O4(2×10-5~5×10-5S/cm)
第一性原理计算表明Li沿着非线性的方向移动能量最低。
理论离子扩散系数高达10-8~10-7cm2/s,但是与二维和三维隧道不同,一维隧道容易被堵塞而阻止锂离子迁移,因此离子扩散系数远远低于理论值。
通过各种方法测得的离子扩散系数为10-15~10-12cm2/s。低电导率以及离子迁移数导致LiFePO4的倍率性能非常差,科研工作者建立了大量动力学模型试图解释。
LiFePO4充放电动力学原理,如核收缩模型、Domino-cascade模型、亚稳态分离模型等等。
学术界以及产业界通常采用掺杂、包覆和颗粒纳米化等手段来改善LiFePO4的导电性能。
如通过Mg2+、Al3+、Ti4+、Zr4+
Nb5+、W6+等阳离子掺杂制造阳离子缺陷和空位来提高材料的导电性。
另外,碳材料具有导电性好和比表面积大等特点,因此,通过碳包覆可以提高LiFePO4与电解液接触面积以及构建碳导电网络。
同时,碳还原性强,高温烧结制备LiFePO4过程中碳源的加入可以提高还原气氛,避免材料合成过程中Fe2+氧化成Fe3+,因此碳包覆可以大大改善LiFePO4的导电性。
导电金属Cu、Ag、Au和Pt等粉体的掺入也可以提高材料的导电性。具有金属导电能力的Fe2P。
NiP和Co2P等磷化物包覆同样可以明显提高材料的导电性。而颗粒纳米化则可以大大缩短Li+的迁移路径,从而改善其导电性能。