
陈培松
2019年底在湖北省武汉市暴发的新型冠状病毒肺炎正对我国人民健康造成巨大威胁[1]。2020年1月12日,世界卫生组织正式将引起武汉肺炎疫情的新型冠状病毒命名为2019新型冠状病毒(2019 new coronavirus,2019-nCoV)[2]。新型冠状病毒是一种从未在人类中发现的新型冠状病毒,传播迅速,传染性强,人群普遍易感。然而,新型冠状病毒引起的肺炎尚无特异性治疗方案[3]。目前,新型冠状病毒已被国家卫生健康委员会纳入《中华人民共和国传染病防治法》规定的乙类传染病,并按甲类传染病预防和控制。截至2020年2月1日20:00时,全中国已有11889例确诊患者,17988例疑似患者(信息来自国家卫生健康委员会官方网站)[4]。目前,实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction, qPCR)是筛查和诊断新型冠状病毒的重要手段[5]。但是由于新型冠状病毒肺炎标本存在极强的传染性,使得实验室检测的工作人员处于极大的危险中[6]。因此,需要投入大量的防护装备和采取一系列的措施去降低感染风险。同时,实验室检测人员也遭受巨大的心理压力。根据现行的新型冠状病毒诊疗指南,新型冠状病毒在56 ℃ 30 min和75%的酒精处理下,会被灭活[7]。虽然目前实验室检测标本前,会采用对标本的灭活步骤,但不能明确标本灭活处理后是否会对后续的检测结果造成影响。因此,本研究比较了56 ℃ 30 min和75%的酒精标本灭活处理,对后续新型冠状病毒核酸qPCR检测的影响,为有效减低实验室传播风险,预防控制医疗机构新型冠状病毒肺炎感染,保护实验室检测人员的安全提供新策略。
材料与方法
一、材料
1.标本来源:
2020年1月22号至2020年1月28号,研究者收集中山大学附属第一医院两例冠状病毒qPCR核酸检测阳性患者的咽拭子标本。两位患者均有在武汉的停留史,在我院发热门诊就诊,最终由广东省疾病预防控制中心确诊为2019新型冠状病毒感染。
2.试剂与仪器:
半自动核酸提取仪及配套核酸提取试剂:Smart32(达安基因公司),核酸提取试剂(DA0623,达安基因公司)。ABI7500荧光定量PCR仪购自美国Thermofisher公司。
二、方法
1.标本处理及灭活:
用1 ml的生理盐水洗涤咽拭子标本,然后进行以下操作:(1)取100 μl咽拭子洗脱液+300 μl的生理盐水。(2)取100 μl咽拭子洗脱液加300 μl无水乙醇,形成75%乙醇终浓度的处理环境,然后室温放置30 min。(3)取100 μl咽拭子洗脱液+300 μl的生理盐水,然后水浴箱56 ℃温育30 min。将以上处理好的咽拭子洗脱液按照1:2,1:4,1:8,1:16,1:32的比例进行稀释,分别对其进行核酸提取,之后进行qPCR核酸检测。
2.核酸提取和qPCR反应:
核酸提取使用达安基因的smart32全自动核酸提取仪及配套的提取试剂(DA06 23),每个样本需要200 μl的咽拭子洗脱液。qPCR使用达安基因qPCR检测试剂(DA5070),按照试剂说明书进行操作,反应体系使用PCR反应液A 17 μl+ PCR反应液B 3 μl+ 5 μl核酸提取液。序列的来源参考BetaCoV/Wuhan/IVDC-HB-01/2019|EPI_ISL_402119,引物和探针设计的范围位于ORF1ab:20700-21000 bp。在ABI 7500型荧光定量PCR仪上进行2019-nCoV qPCR核酸检测,反应条件如下:50 ℃ 15 min→95 ℃ 15 min→94 ℃ 15 s, 55 ℃ 45 s(40个循环),所有检测均进行3次重复,取平均循环阈值(cycling threshold,CT)进行计算。
三、统计学分析
采用Graphpad Prism软件(Version8.0)进行统计学分析。应用Spearman相关系数对不同处理的标本CT值进行相关性分析,并采用Bland-Altman图对CT值一致性进行分析。P<0.05为差异有统计学意义。
结果一、未灭活处理与灭活处理后不同稀释浓度样本的qPCR结果比较
对不同浓度的标本进行检测,发现使用56 ℃ 30 min和75%的乙醇灭活处理后qPCR的结果与未经灭活处理的标本的结果相近,见表1。标本1和2的标准扩增曲线见图1。

表1
未灭活处理与灭活处理后样本的qPCR结果
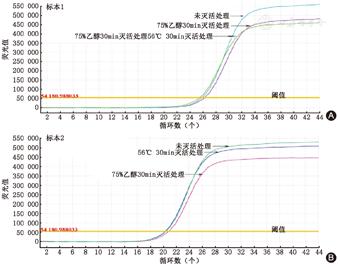
图1
未灭活处理与灭活处理后的两个样品的典型扩增图
二、未灭活处理与灭活处理后不同稀释浓度样本的qPCR结果的相关性及一致性分析
56 ℃ 30 min和75%乙醇处理和没有灭活处理的标本结果相关性明显,其Spearman相关系数均为r=0.996(P<0.001),见图2。同时,Bland-Altman分析结果显示见图3,56 ℃ 30 min和75%乙醇处理和没有灭活处理的标本结果具有良好的一致性。

图2
未灭活处理与灭活处理结果的相关性分析
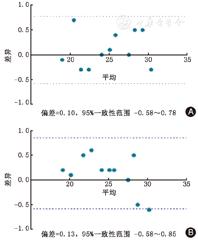
图3
未灭活处理与灭活处理结果Bland-Altman分析
讨论
新型冠状病毒肺炎作为突发公共卫生事件,传播迅速广泛,传染性强,然而其并无特异性治疗方法,给全世界人民的生命健康带来巨大威胁[8]。新型冠状病毒预防和控制的重点主要在早发现、早诊断、早隔离、早治疗[9]。新型冠状病毒主要通过飞沫、接触以及呼吸道气溶胶近距离传播。人体感染新型冠状病毒后可引起发热、乏力、干咳及呼吸困难等症状,部分患者症状较轻,并无发热现象,但少量患者可出现急性呼吸窘迫综合征、难以纠正的代谢性酸中毒及出凝血功能障碍[10]。新型冠状病毒对热敏感,56 ℃ 30 min、*醚乙**、75%乙醇、含氯消毒剂、过氧乙酸和三氯甲烷等脂溶剂均可有效灭活病毒[11]。
通过qPCR对新型冠状病毒核酸检测是感染确诊的主要方法。新型冠状病毒的强传染性让实验操作者处于极大的危险和心理压力中。如何降低新型冠状病毒在实验室传播的可能性,最大程度保护实验室人员,是当下急需解决的问题。这对于在全国范围内广泛开展新型冠状病毒核酸检测,诊断和隔离感染者,有着重要作用。本研究通过对比灭活处理与灭活处理后样本的qPCR结果发现,56 ℃ 30 min和75%乙醇处理和没有灭活处理的标本结果具有明显的相关性且一致性良好。这提示使用56 ℃ 30 min和75%乙醇对咽拭子标本进行新型冠状病毒灭活处理,对后续新型冠状病毒核酸qPCR检测无明显的影响,为保护实验室检测人员的安全提供了新策略。而且56 ℃加热和75%乙醇灭活在大多实验室均具备该实验条件,对检测的成本也无明显影响。在今后的新型冠状病毒核酸检测中,可考虑先对咽拭子标本先进行56 ℃ 30 min或75%乙醇预处理,然后再进行qPCR检测,将大大降低实验室操作人员感染新型冠状病毒几率。
本研究的局限性在于:(1)我院阳性咽拭子标本较少,只能够对仅有的两个阳性标本进行验证。(2)在检测的两个阳性标本,CT值均比较高(未稀释时,分别为19和24),对于某些CT值偏低的标本,是否存在同样的相关性,仍需要进一步探讨。(3)研究者的实验结果完成比较早(1月24号完成),当时普遍使用的是不带内参的单通道试剂,如若能结合内参基因,N基因,ORF基因一起分析会提供更详细的验证信息。(4)本研究仅比较了一个厂家的试剂,是否其他厂家的试剂也是如此,仍需更多的数据支持。
考虑到本研究结果存在以上的局限性,在此呼吁全国同行共同关注和参与新型冠状病毒的灭活后检测验证,群策群力,共同推动灭活后的新策略。
参考文献[1]HuiDS, I AzharE, MadaniTA, et al. The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health - The latest 2019 novel coronavirus outbreak in Wuhan, China[J]. Int J Infect Dis, 2020,91:264-266. DOI: 10.1016/j.ijid.2020.01.009.[2]ZhuN, ZhangD, WangW, et al. A Novel Coronavirus from Patients with Pneumonia in China, 2019[J]. N Engl J Med,2020. DOI: 10.1056/NEJMoa2001017.[3]LancetT. Emerging understandings of 2019-nCoV[J]. Lancet, 2020,395(10221):311. DOI:10.1016/S0140-6736(20)30186-0.[4]www.nhc.gov.cn[5]李太生,曹玮,翁利, 等. 北京协和医院关于"新型冠状病毒感染的肺炎"诊疗建议方案(V2.0)[J].协和医学杂志,2020:1-5.[6]靳英辉,蔡林,程真顺,等. 新型冠状病毒(2019-nCoV)感染的肺炎诊疗快速建议指南(标准版)[J]. 解放军医学杂志,2020,45(1):1-20.[7]华中科技大学同济医学院附属同济医院救治医疗专家组. 新型冠状病毒感染的肺炎诊疗快速指南(第三版)[J].医药导报,2020:1-9.[8]*京大南**学南海研究协同创新中心执行主任*京大南**学国际关系研究院院长朱锋. 新冠病毒,人类共同的敌人[N]. 环球时报,2020-01-31(007).[9]魏秋华,任哲. 2019新型冠状病毒感染的肺炎疫源地消毒措施[J].中国消毒学杂志,2020 (1):1-4.[10]HuangC, WangY, LiX, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China[J]. Lancet, 2020,DOI: 10.1016/S0140-6736(20)30183-5.[11]王琛,王旋. 新型冠状病毒感染的流行、医院感染及心理预防[J].全科护理,18(3):1-2.
(此文为转载)