
文|北秋农事
编辑|北秋农事
«——【·前言·】——»
鞘枯病(ShB)是由水稻根瘤菌引起的三大病害之一。它在整个生育期对水稻造成危害,主要侵染叶片、鞘和穗部,最终导致整株植株枯萎和倒伏。
一种严重的ShB可使水稻产量减少约50%。目前,控制这种疾病的主要方法是使用杀菌剂,因为缺乏对ShB具有抗性的品种。

然而,杀菌剂并不环保,因为它们会直接影响其他微生物,而且它们的使用也会增加种植成本。
因此,有必要分离抗性水稻品种并了解其防御机制,以开发对ShB的抗性。
先前的研究表明,几丁质酶、ȕ-1、3-葡聚糖酶或多聚半乳糖醛酸酶抑制蛋白(OsPGIP1)的过表达导致水稻对茄枯病菌的抗性增强。
乙烯合成酶OsACS2的过表达促进了水稻对稻瘟病和白叶枯病的抗性。广谱抗性2 (BROAD-SPECTRUM RESISTANCE2, BSR2)基因的过表达使拟南芥和水稻对茄枯病菌产生抗性。

此外,水杨酸依赖性免疫有助于水稻和短茅对茄枯病菌的抗性。
此外,糖最终会被输出转运蛋白11基因的突变和松散植物结构1 (LPA1)/不确定结构域14 (IDD14)的过表达可以显著保护水稻免受ShB。
IDD13与LPA1相互作用,通过激活PIN1a增强对ShB的抗性。
IDD包含两个C2H2和两个C2HC锌指基序,IDD基因在植物中具有多种生物学功能。以前的研究报道ID1控制玉米和水稻的开花时间。
MAGPIE/ AtIDD3和JACKDAW/AtIDD10调控根细胞的命运,ENHYDROUS/ AtIDD1调控种子成熟,AtIDD8调节植物发育。
AtIDD14、AtIDD15和AtIDD16通过促进拟南芥生长素的生物合成和运输协同调节侧枝器官形态发生和向地性,LPA1/IDD14调控茎部向地性和椎板关节角度。

结果
1.RAVL1直接激活IDD3
我们之前发现,RAVL1负调控水稻对ShB的防御机制, LPA1/IDD14保护水稻对ShB的防御机制。
此外,RNA-seq结果显示,另一个IDD成员IDD3受RAVL1调控。
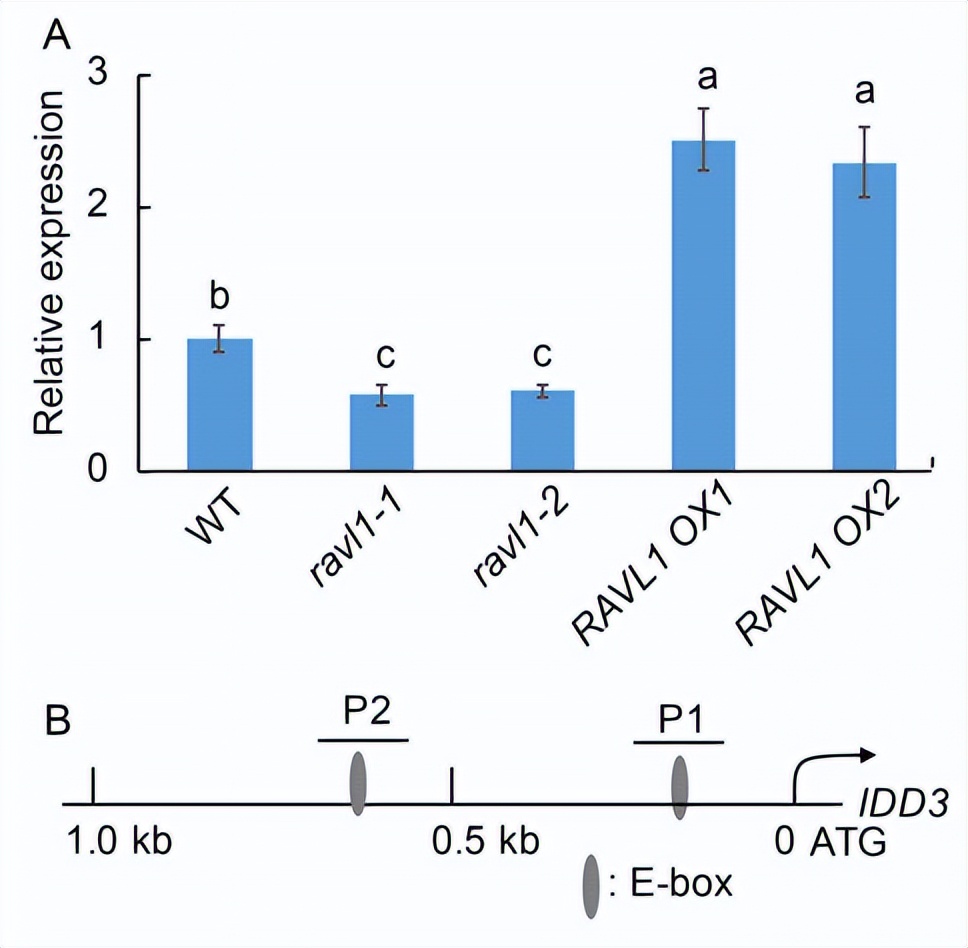
在本研究中,qRT-PCR结果显示,与野生型(WT)相比,IDD3在ravl1突变体(ravl1-1和ravl1-2)中表达下调,而在ravl1过表达植物(ravl1 OX-1和ravl1 OX-2)中表达上调(图1-A)。

启动子序列分析发现,两个E-box基序出现在IDD3启动子1.0 kb内,这两个基序是推测的RAVL1结合序列(图1 b)。
利用35S:GFP和35S:RAVL1:GFP转基因植物越伤组织进行的染色质免疫沉淀(ChIP)实验结果显示,RAVL1的沉淀富集了IDD3启动子的P1区,而不是P2区(图1-C)。
通过酵母单杂交实验证实了该结合实验的结果,结果表明,只有在IDD3 (mpIDD3) P1区域的E-box启动子没有突变的情况下,RAVL1才能激活1.0 kb的IDD3 (pIDD3)(图1-D)。
2.IDD3的表达模式及其转录活性
我们分析了IDD3在叶片、茎、节、花和根中的表达模式。在所有组织中都检测到IDD3 mRNA,在淋巴结和花中表达较低(图2-A)。

接下来,我们利用由3.0 kb内源IDD3启动子驱动的GUS转基因植物,研究了IDD3在植物中的表达模式。
GUS基因在叶片脉管系统、节、花、侧根原基和初生根脉管系统中的表达检测(图2-B)。然后,利用茄茄AG1-IA接种的叶片RNA进行qRT-PCR检测IDD3的表达是否对ShB有响应。
结果显示,IDD3在接种后24和72 h (hpi)表达增强,而在48 hpi时表达被抑制(图2-C)。
我们对IDD3和ID1进行了序列比对。分析表明,IDD3和ID1在ID结构域高度保守。然而,它们具有不同的c端区域(图3-A)。

由于ID1是已知的转录因子,我们使用酵母单杂交系统检测了IDD3的转录活性。在转录激活实验中,将表达GAL4 DNA结合域(BD)的载体与酵母中全长IDD3编码区、n端ID结构域或c端区域融合。
3.IDD3负向调控水稻对ShB的防御
我们检测了idd3突变体(idd3-1和idd3-2)和idd3过表达体(idd3 OX1和idd3 OX),以评估idd3在水稻抗ShB防御机制中的作用。
将t - DNA插入IDD3位点的第二个内含子(图4-A),qRT-PCR结果证实,idd3突变体是敲除突变体,与WT植株相比,idd3过基因体中idd3的表达显著高表达(图4-B)。
接种番茄红霉的结果显示,idd3突变体与WT对ShB的反应相似。然而,与WT相比,idd3过表达者对番茄红霉感染表现出更敏感的症状(图4-C)。

在WT中,大约41.5%的叶面积被病变覆盖,而IDD3 -1中为42.2%,IDD3 -2中为40.9%,IDD3 - OX1中为54.9%,IDD3 - OX2中为55.7%(图4-D)。
与WT植株相比,idd3突变体对ShB的反应没有显著差异,这表明idd3和其他IDD成员可能在功能上是冗余的。
由于IDD14/LPA1抑制植物与IDD14/LPA1相似,表现出更大的板关节角,IDD3抑制系是通过超人抑制域X (SRDX)基序序列与IDD3的c端融合而产生的。
3.IDD3正调控BR生物合成和信号基因
RAVL1是BR稳态的上游调控因子。因此,我们研究了IDD3在调节BR相关基因表达中的作用。

我们分析了IDD3抑制因子和过表达因子中BR受体基因BRI1和生物合成基因D2和D11的表达。
qRT-PCR分析结果显示,与WT植株相比,IDD3抑制因子BRI1、D2和D11的表达下调,而IDD3过表达因子BRI1、D2和D11的表达上调(图6-A)。
启动子序列分析显示,推测的IDD蛋白结合基序(TTTGTCC /G)位于D2和D11启动子1.0 kb以内(图6-B)。
利用35S:GFP和35S:IDD3:GFP转基因植物愈伤组织的ChIP实验结果显示,IDD3不与D2和D11启动子区域的推测基序结合(图6-C)。


讨论
稻瘟病是一种严重危害水稻产量的主要病害。然而,宿主的抗性机制尚不清楚。我们之前的研究发现,RAVL1通过激活BR和乙烯信号通路来修饰水稻对ShB的防御机制。
结果表明,BR和乙烯信号通路分别负向和正向调节水稻对ShB的防御。然而,RAVL1调控水稻抗ShB的具体机制尚不清楚。
有趣的是,我们发现了另一个IDD成员IDD3,受RAVL1正调控,这是通过RAVL1突变体和过表达体证实的。

RAVL1是一种转录激活因子,通过结合E-box元件激活下游基因。进一步分析发现IDD3启动子区域包含E-box元素。
通过ChIP实验、酵母单杂交实验和瞬时实验证实了RAVL1与IDD3启动子区域的结合亲和力。
结果表明,RAVL1结合到含有一个E-box元件的P1区域,而没有结合到含有一个E-box元件的P2区域,这表明RAVL1通过启动子结合直接激活了IDD3。
接下来,我们发现,IDD3在24和72 hpi时表达增强,而在48 hpi时表达抑制,这表明鸢尾蓟马与IDD3转录之间存在复杂的调控机制。
因此,未来的研究可能包括测试蛋白质水平。结果表明,两株idd3突变株对ShB的反应与WT株无显著差异。

IDD3定位于IDD3- gfp转基因植物根部的细胞核中,我们的分析表明它在酵母细胞中具有转录活性,这证实了IDD3可能是一种转录激活剂。
SRDX与LPA1的融合起到抑制因子的作用。因此,IDD3的抑制因子IDD3- SRDX被生成,以解决IDD3是否与其他转录因子在功能上冗余以调节下游基因表达。
接种结果表明,与野生型植株相比,IDD3抑制物对ShB的敏感性较低。由此产生IDD3过表达子,并分析其对ShB的反应进一步验证。
结果表明,IDD3过表达者较WT型植株更易感染ShB。这些结果表明IDD3负向调控水稻对ShB的防御。


方法
1.植物生长与茄蚜AG1-IA接种
野生型(WT)选用粳稻品种东金、IDD3 -1 (PFG_3A-09378)、IDD3 -2 (PFG_3A-14411)、IDD3GFP过表达者(IDD3 OX)、RAVL1- 1、RAVL1- 1和RAVL1- GFP过表达者(RAVL1 OX)植株,在沈阳农业大学温室23℃ - 30℃环境下生长。
从主分蘖的第二个最年轻的叶片上剪下一块10厘米长的叶片,放在湿润的滤纸上,放在培养皿中(直径36厘米,高度,2.5厘米)。
每个重复由6个叶片组成,为了完全随机设计,我们每行使用4个重复。取定植的马铃薯葡萄糖琼脂(PDA)块(直径7 mm)放置于每片叶片的背面。

叶片在连续光照下于25℃培养箱中培养72 h,滤纸用无菌水保持湿润。72h后,使用Image J软件(美国国立卫生研究院)测量每个叶片内病变的尺寸(长×宽),并使用Eizenga(2002)和Prasad和Eizenga(2008)的方法计算病变面积的百分比。
接下来,将1个月大的野生型植株接种茄茄AG1-IA,在0、24、48和72 hpi后采集叶片,分析茄茄AG1-IA感染介导的IDD基因表达。
2.质粒构建
将IDD3开放阅读框(ORF)序列扩增并克隆到pCAMBIA1302二元载体的BglII和SpeI限制性内切酶位点,生成IDD3- gfp过表达转基因植株。

本研究将IDD3编码序列n端融合到GFP编码序列,将IDD3 ORF序列n端融合到SRDX基序序列,生成pGA1611二值载体中的IDD3阻遏子构建体。
3.Transactivation化验
对含有lacZ和HIS3报告基因的酵母菌PJ69-4A进行了转激活试验。
使用pGBT9载体,将编码GAL4 DNA结合域的DNA融合到以下IDD3 DN*片A**段:完整的ORF,编码前212个氨基酸的5ƍ-cDNA,或编码213-495个氨基酸的3ƍ-cDNA。3ƍ-AtNAC1片段编码143-324氨基酸的肽,作为阳性对照。
这些构建体或空载体(pGBT9)分别导入酵母细胞。酵母转化体在合成dropout (SD)/Trp-和SD/His-plates上生长。表S1提供了用于克隆IDD3 cDN*片A**段的引物。

4.染色质免疫沉淀(ChIP)测定
从表达35S:GFP、35S:RAVL1:GFP或35S:IDD3:GFP的转基因植株中收集水稻愈伤组织(8 g)进行ChIP实验。
ChIP测定和随后的ChIP- pcr测定按照先前描述的方案进行,表S1提供了用于ChIP-PCR检测的引物。
5.瞬时表达试验
在瞬时表达实验中,将效应质粒(35S:RAVL1)和报告质粒(pIDD3或突变启动子mpIDD3)以及内控质粒(35S:LUC)共转化到拟南芥原生质体细胞中。
GUS活性分析采用Xuan(2013)的方法进行。使用荧光素酶测定试剂盒(Promega, USA)评估荧光素酶测定。

实验重复三次,并按照先前描述的方案进行聚乙二醇(PEG)介导的转化和荧光素酶活性测定。表S1提供了用于瞬时表达试验的引物列表。
6.酵母单杂交分析
将IDD3启动子(正常或E-box突变)的1.0 kb片段克隆到pHISi载体中。接下来,将RAVL1 ORF序列克隆到pGAD424载体中。
将构建的pGAD424- ravl1或pGAD424空载体转化到酵母菌株(YM4271)中,在缺乏Leu或Leu和His的合成dropout培养基(SD)上监测酵母细胞的生长情况。

参考文献:
- Tong H H, Chen H Q. 2019.近40年我国水稻改良品种分析. Chin J Rice Sci, 33(6): 523–531.(in Chinese with English abstract)
- Eizenga G C, Lee F N, Rutger J N. 2002.水稻抗纹枯病品种筛选. Plant Dis, 86(7): 808– 812.
- Feurtado J A, Huang D Q, Wicki-Stordeur L, Hemstock L E, Potentier M S, Tsang E W T, Cutler A J. 2011.拟南芥C2H2锌指不确定域1/ENHYDROUS通过调节种子成熟过程中的光和激素信号来促进种子的萌发. Plant Cell, 23(5): 1772–1794.
- Liu J M, Li D P, Hu Y B, Xuan Y H. 2018.抑制叶肉细胞中OsSWEET11的功能可提高水稻对纹枯病的抗性. Mol Plant Pathol, 19(9): 2149–2161.
- Helliwell E E, Wang Q, Yang Y N. 2013.诱变乙烯转基因水稻对稻瘟病菌和茄根丝核菌表现出广谱的抗病性. Plant Biotechnol J, 11(1): 33–42.