中文名:谷氨酸
英文名:glutamic acid
别 名:2-氨基戊二酸
化学名:2-Aminopentanedioic acid
分子式:C5H9NO4
CAS号:617-65-2 L 56-86-0 D isomer: 6893-26-1
分子量:147.1293
外观:鳞片状或粉末状晶体
熔点:199 °C (390 °F; 472 K)
沸 点:333.78 ℃
等电点:
水溶性:7.5g/L(20 ℃)

Skeletal formula of L-phenylalanine骨架结构式

ball-and-stick model球棍模型

space-filling model空间结构模型
谷氨酸(符号Glu或E)是一种α-氨基酸,几乎所有生物在蛋白质的生物合成中都使用它。它是人类的非必需营养素,这意味着人体可以合成足够的谷氨酸。它也是脊椎动物神经系统中最丰富的兴奋性神经递质。它是在GABA能神经元中合成抑制性γ-氨基丁酸(GABA)的前体。
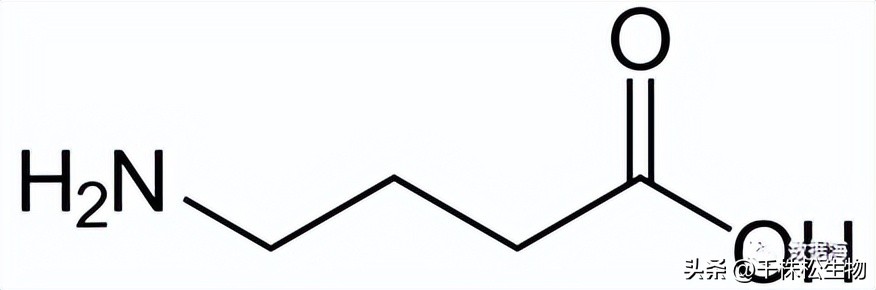
γ-氨基丁酸(GABA)
其分子式为C5H9NO4。谷氨酸以三种光学异构形式存在;右旋L-型通常由谷蛋白水解或从甜菜糖生产的废水以及发酵获得。其分子结构可以理想化为HOOC−CH(NH2)−(CH2)2−COOH,具有两个羧基−COOH和一个氨基−NH2。然而,在固态和弱酸性水溶液中,分子呈电中性的两性离子结构- OOC - CH(NH+3) - (CH2)2 - COOH。它由密码子GAA或GAG编码。
谷氨酸可以从第二个羧基上失去一个质子形成共轭碱,即单负离子谷氨酸−OOC−CH(NH+3)−(CH2)2−COO−。这种形式的化合物普遍存在于中性溶液中。谷氨酸神经递质在神经激活中起主要作用。这种阴离子创造了食物的鲜味,存在于谷氨酸调味剂中,如味精。在欧洲,它被归类为食品添加剂E620。在高碱性溶液中,双负阴离子−OOC−CH(NH2)−(CH2)2−COO−普遍存在。与谷氨酸相对应的自由基叫做谷氨酰。
谷氨酸离子化
当谷氨酸溶解在水中时,氨基(-NH2)可能获得一个质子(H+),和/或羧基可能失去质子,这取决于介质的酸度(acidity)。
在足够酸性的环境中,氨基获得一个质子,分子变成一个带单正电荷的阳离子,HOOC−CH(NH3+)-(CH2)2−COOH。
在pH值在2.5 ~ 4.1之间时,靠近胺的羧酸一般会失去一个质子,酸变成中性两性离子- OOC-CH(NH3+)-(CH2)2-COOH。这也是化合物在晶体固体状态下的形式。质子化状态的变化是渐进的;这两种形式在pH 2.10时浓度相等。
在更高的pH值下,另一个羧酸基失去了它的质子,酸几乎完全以谷氨酸阴离子- OOC-CH(NH3+)-(CH2)2- COO -的形式存在,总体上带一个负电荷。质子化状态的变化发生在pH为4.07时。在生理pH范围内(7.35-7.45),两种羧酸均缺乏质子的这种形式占主导地位。
在更高的pH值下,氨基失去额外的质子,普遍存在双负离子−OOC−CH(NH2)−(CH2)2−COO−。质子化状态的变化发生在pH值9.47时。
光学异构体
靠近氨基的碳原子是手性的(与四个不同的基团相连)。谷氨酸可以以三种光学异构体的形式存在,包括右旋L-型、D(-)和L(+)。L型是自然界中最广泛存在的一种,但D型出现在一些特殊的环境中,如细菌的荚膜和细菌的细胞壁(细菌可以用谷氨酸消旋酶从L型中制造D型)和哺乳动物的肝脏。
历史
尽管谷氨酸和其他氨基酸自然存在于许多食物中,但它们对风味的贡献直到20世纪初才被科学证实。1866年,德国化学家卡尔·海因里希·里特豪森(Karl Heinrich Ritthausen)发现并确认了这种物质,他用硫酸处理小麦面筋(它因此而得名)。1908年,日本东京帝国大学(Tokyo Imperial University)的池田菊苗(Kikunae Ikeda)发现,大量海带汤蒸发后留下的棕色晶体是谷氨酸。当品尝这些晶体时,他重现了他在许多食物中发现的那种难以言说但不可否认的味道,尤其是在海藻中。池田教授将这种味道称为鲜味。然后,他申请了一项批量生产谷氨酸结晶盐(味精)的专利。
工业合成
谷氨酸的生产规模是所有氨基酸中最大的,2006年估计年产量约为150万吨。20世纪50年代,化学合成被糖和氨的有氧发酵所取代,谷氨酸棒杆菌(也称为黄短杆菌)是生产中使用最广泛的生物体。可以通过浓缩和结晶来实现分离和纯化;谷氨酸也作为盐酸盐被广泛使用。
功能及用途
新陈代谢
谷氨酸是细胞代谢的关键化合物。在人体内,膳食蛋白质通过消化被分解为氨基酸,作为体内其他功能的代谢燃料。氨基酸降解的一个关键过程是转氨化,在此过程中,氨基酸的氨基转移到α-ketoacid,通常由转氨酶催化。这种反应可以概括为:
R1-amino acid + R2-α-ketoacid ⇌ R1-α-ketoacid + R2-amino acid
一种非常常见的α-酮酸是α-酮戊二酸,它是柠檬酸循环的中间体。α-酮戊二酸的转氨反应生成谷氨酸。由此产生的α-酮酸产品往往是一个有用的,也可以作为燃料或作为进一步代谢过程的底物。举例如下:
Alanine + α-ketoglutarate ⇌ pyruvate + glutamate
Aspartate + α-ketoglutarate ⇌ oxaloacetate + glutamate
*酮丙**酸(pyruvate)和草酰乙酸(oxaloacetate)都是细胞代谢的关键组成部分,作为糖酵解、糖异生和柠檬酸循环等基本过程的底物或中间体作出贡献。
谷氨酸在身体处理过剩或废物氮方面也起着重要作用。谷氨酸在谷氨酸脱氢酶的催化下发生脱氨反应,具体如下:
glutamate + H2O + NADP+ → α-ketoglutarate + NADPH + NH3 + H+
氨(作为铵)然后主要以尿素的形式排出体外,尿素在肝脏中合成。因此,转氨作用可以与脱氨作用相联系,有效地允许氨基酸胺基中的氮通过谷氨酸作为中间体被除去,最终以尿素的形式排出体外。
谷氨酸也是一种神经递质(见下文),这使它成为大脑中最丰富的分子之一。被称为胶质瘤或胶质母细胞瘤的恶性脑瘤利用这一现象,利用谷氨酸作为能量来源,特别是当这些肿瘤由于IDH1基因的突变而更加依赖谷氨酸时。
神经递质
谷氨酸是脊椎动物神经系统中含量最丰富的兴奋性神经递质。在化学突触中,谷氨酸被储存在囊泡中。神经冲动促使突触前细胞释放谷氨酸。谷氨酸作用于离子性和代谢性(G蛋白偶联)受体。在相反的突触后细胞中,谷氨酸受体,如NMDA受体或AMPA受体,与谷氨酸结合并被激活。由于其在突触可塑性中的作用,谷氨酸参与了大脑中的学习和记忆等认知功能。被称为长期增强的可塑性形式发生在海马体、新皮层和大脑其他部分的谷氨酸突触上。谷氨酸不仅作为点对点的传递器,还通过突触间的溢出串音,即从相邻突触释放的谷氨酸总和产生突触外信号/体积传输。此外,正如马克·马特森(Mark Mattson)最初描述的那样,谷氨酸在大脑发育过程中调节生长锥和突触发生中发挥着重要作用。
脑非突触谷氨酸传导电路
果蝇(Drosophila)大脑中的细胞外谷氨酸已被发现调节突触后谷氨酸受体集群,通过一个涉及受体脱敏的过程。在胶质细胞中表达的一种基因积极地将谷氨酸转运到细胞外空间,而在伏隔核刺激II型代谢谷氨酸受体中,该基因被发现降低了细胞外谷氨酸水平。这就提出了一种可能性,即这种细胞外的谷氨酸作为更大的稳态系统的一部分,发挥着“内分泌样”的作用。
GABA前体
谷氨酸还作为在GABA能神经元中合成抑制性γ -氨基丁酸(GABA)的前体。该反应由谷氨酸脱羧酶(GAD)催化,GAD在小脑和胰腺中含量最多。僵人综合征是一种由抗GAD抗体引起的神经系统疾病,导致GABA合成减少,因此,运动功能受损,如肌肉僵硬和痉挛。由于胰腺中含有丰富的GAD,直接造成胰腺的免疫破坏,从而导致糖尿病的发生。
增味剂
谷氨酸是蛋白质的组成成分,存在于含有蛋白质的食物中,但只有当它以非结合形式存在时,才能尝到它的味道。大量的游离谷氨酸存在于各种各样的食物中,包括奶酪和酱油,谷氨酸负责鲜味,这是人类味觉的五种基本味道之一。谷氨酸常以钠盐的形式被用作食品添加剂和风味增强剂,即味精。
植物生长
Auxigro是一种含有30%谷氨酸的植物生长制剂。
核磁共振
近年来,关于剩余偶极耦合(RDC)在核磁共振波谱(NMR)中的应用进行了大量的研究。一种谷氨酸衍生物,聚-γ-苄基-谷氨酸(PBLG),经常被用作校准介质,以控制所观察到的偶极相互作用的规模。
药理学
药物苯环己哌啶(通常被称为PCP或“天使粉”)在NMDA受体上非竞争性拮抗谷氨酸。由于同样的原因,右美沙芬和氯胺酮也有很强的解离和致幻作用。急性输注药物LY354740(也被称为eglumagad,代谢性谷氨酸受体2和3的激动剂)导致育亨宾诱导的bonnet猕猴(辐射猕猴)应激反应的显著降低;与未治疗的对照组相比,这些动物长期口服LY354740显著降低了基线皮质醇水平(约50%)。LY354740也被证明对人肾上腺皮质细胞的代谢性谷氨酸受体3 (GRM3)起作用,下调醛固酮合成酶、CYP11B1和肾上腺类固醇(即醛固酮和皮质醇)的产生。谷氨酸不能轻易通过血脑屏障,而是通过高亲和力运输系统进行运输。它也可以转化为谷氨酰胺。