在阅读此文前,诚邀您请点点右上方的“关注”,既方便您进行讨论与分享,还能及时阅读最新内容,感谢您的支持。
鸡白痢沙门菌是一种可引起各日龄鸡感染的传染性病原菌,对雏鸡危害尤其严重,该菌既可垂直传播又可水平传播,在动物体内很难清除,甚至可以使动物终生带菌,无法根除,造成持续性感染。
对鸡白痢沙门菌病的防治,传统方法主要以药物和检疫淘汰鸡为主,但药物的过度使用不仅导致细菌耐药性的增加,同时也造成了药物残留问题,对公共卫生健康的威胁也越来越大。

疫苗接种是一种较好的防治措施,基因缺失疫苗是利用基因工程方法敲除致病菌的毒力基因,在减弱其毒力的同时不影响其免疫原性,因此该类疫苗是未来疫苗的研究方向。
鸡白痢沙门菌cya基因编码合成环化腺苷酸酶,其crp基因编码环腺苷酸(cAMP)受体蛋白,是沙门菌的重要毒力调节基因。
研究证明,鼠伤寒沙门菌、猪霍乱沙门菌cya、crp基因缺失株的毒力明显降低,且保留了良好的免疫原性。
鸡白痢沙门菌仅crp基因缺失株有相关报道[5],而对cya基因单缺失株、crp/cya基因双缺失株尚无相关研究报道。
因此,本实验利用重组自杀性质粒介导的同源重组技术构建鸡白痢沙门菌C79-13株的cya基因单缺失株及crp、cya基因双缺失株,并分析其生物学特性、毒力及免疫保护率,为鸡白痢沙门菌基因缺失疫苗的研发提供参考依据。

材料与方法
主要实验材料
自杀性质粒p RE112、p Bluescriptsk (+)大肠杆菌χ7213、鸡白痢沙门菌C79-13株、鸡白痢沙门菌crp基因单缺失株C79-13Δcrp (简称Δcrp)均由本实验室保存;1日龄健康罗曼雏鸡购自洛阳白元种鸡场,雏鸡经平板凝集试验检测鸡白痢抗体为阴性;限制性内切酶、DNA Marker均购自上海碧云天生物技术有限公司;质粒小量提取试剂盒、凝胶回收试剂盒、二氨基庚二酸(DAP)均购自北京鼎国昌盛生物技术有限责任公司;氯霉素、氨苄青霉素购自上海碧云天生物技术有限公司。

引物的设计与合成
根据GenBank中的鸡白痢沙门菌C79-13株(AE008859)基因序列设计相关引物,引物均由上海生工生物工程技术服务有限公司合成。
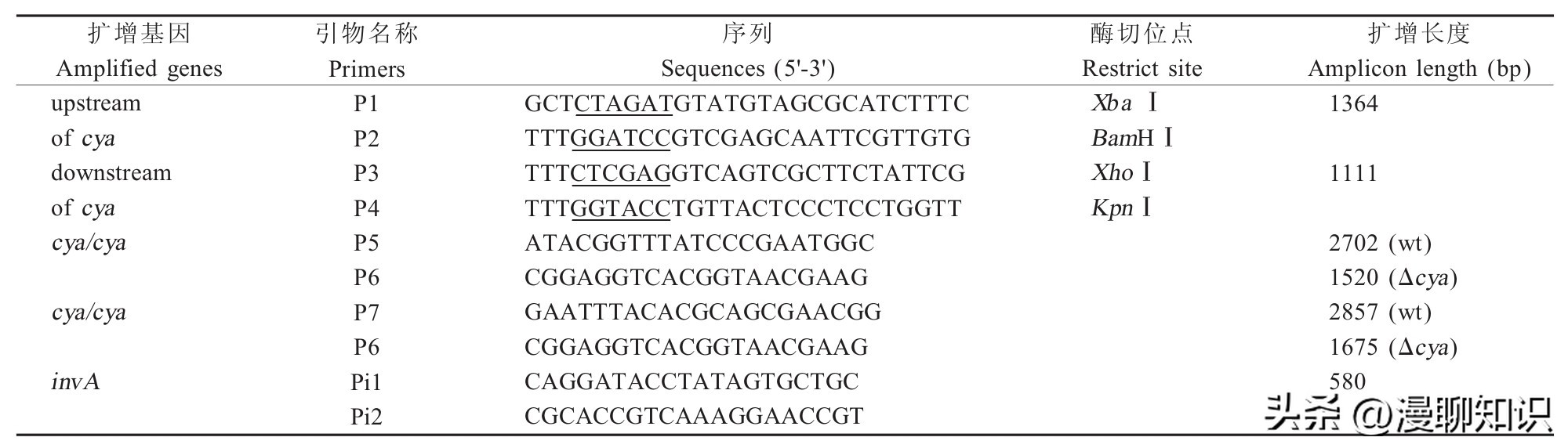
表1 PCR扩增所需引物
重组自杀性质粒p REΔcya的构建及鉴定
以提取的鸡白痢沙门菌C79-13株基因组为模板,利用引物P1/P2、P3/P4分别经PCR扩增cya基因上(cya1)、下(cya2)游同源臂,回收后分别克隆至中间载体p BluescriptSK(+)中构建重组质粒p SKΔcya,经PCR及测序鉴定正确后,利用XbaⅠ和KpnⅠ双酶切p SKΔcya,回收融合片段cya (cya1+cya2)并克隆至自杀性质粒p RE112中,构建缺失1 182 bp cya基因片段的重组自杀性质粒p REΔcya,并分别经各双酶切鉴定后由上海生工生物工程技术服务有限公司测序。

鸡白痢沙门菌缺失菌株Δcya和ΔcrpΔcya的构建与鉴定
以鸡白痢沙门菌C79-13ΔcrpΔcya缺失株的构建为例,通过自杀性质粒介导的同源重组技术,经两步重组法筛选出基因缺失株。
将p REΔcya转化大肠杆菌χ7213,构建重组菌p REΔcya/χ7213并作为供体菌,Δcrp为受体菌,参照其他文献进行接合转移试验,12 h后取适量菌液涂布于含氯霉素和10%蔗糖的LB固体平板并于37℃培养,筛选获得一次重组菌,并采用引物P5/P6经PCR鉴定,将鉴定正确的一次重组菌在含10%蔗糖且无抗性无NaCl的LB (NB)液体培养基中于37℃过夜培养后10倍倍比稀释,涂布LB固体培养基,于37℃过夜培养后挑取白色细小菌落接种于含氯霉素的LB固体培养基,12 h后挑取单菌落提取基因组,获得二次重组菌,分别利用引物P5/P6以及P7/P6经PCR鉴定,PCR产物由上海生工生物工程技术服务有限公司测序鉴定。
正确的菌株即为crp和cya基因双缺失株C79-13ΔcrpΔcya (简称ΔcrpΔcya)。
缺失株C79-13Δcya (简称Δcya)的构建则是将C79-13做为受体菌,其余步骤均相同。
构建的缺失株Δcya利用P6/P7引物经PCR和测序鉴定。
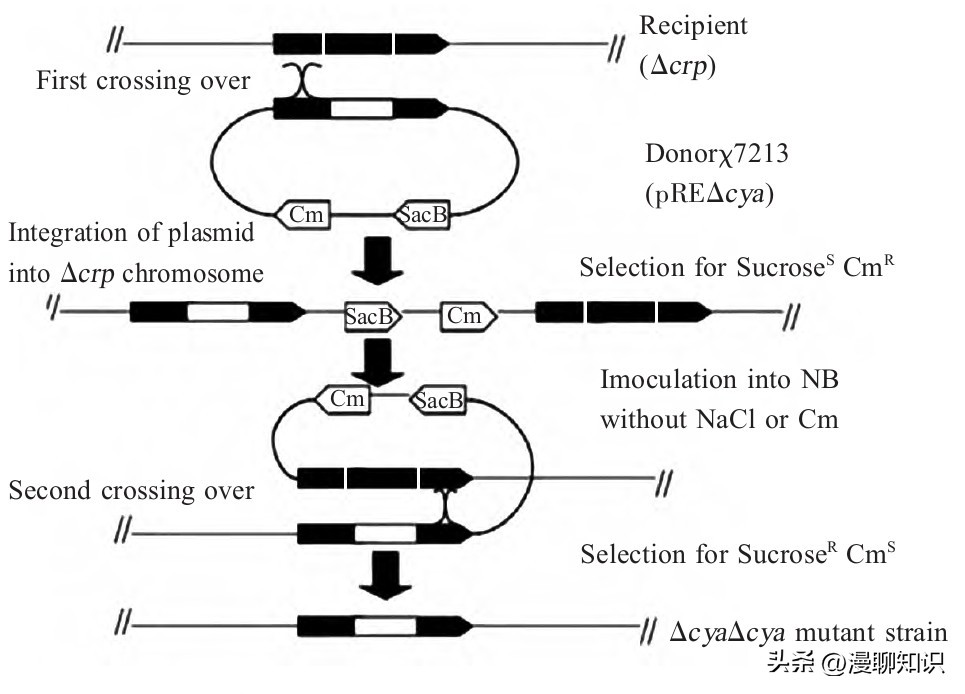
图1 缺失株ΔcrpΔcya的构建策略
各缺失株的血清型及生化特性鉴定
参照文献,利用玻片凝集试验鉴定缺失株Δcya、Δcrp、ΔcrpΔcya及亲本菌株C79-13的血清型;同时将缺失株Δcya、Δcrp、ΔcrpΔcya与亲本菌株C79-13分别接种至葡萄糖、乳糖、麦芽糖等细菌微量生化反应管,检测各菌株的生化特性。
各缺失株的遗传稳定性鉴定
将缺失株ΔcrpΔcya、Δcya分别在LB液体培养基中连续传代培养,并挑取第10、20、30、40、50、60代的单菌落,利用P6/P7引物经PCR检测cya基因,鉴定各缺失株的遗传稳定性。
各缺失株生长曲线的测定
将缺失株ΔcrpΔcya、Δcya、Δcrp及亲本株C79-13分别接种于LB培养基致终浓度为106cfu/mL,继续于37℃培养,每间隔1 h取菌涂板,共计16 h,通过计算固体培养基每小时的菌数绘制各菌株的生长曲线。

各缺失株生物被膜(BF)形成能力的测定
将亲本菌株C79-13,缺失株ΔcrpΔcya、Δcya、Δcrp分别于37℃培养并调节至106cfu/mL,将各菌液加入96孔细胞培养板,28℃培养72 h后,用PBS将96孔板洗3次,并在37℃干燥30 min,再加入结晶紫(100μL/孔)孵育30 min后,每孔添加100μL无水乙醇,测量OD570nm值。
每个菌株设置3个重复。
根据各菌株OD570nm值分析各缺失菌株BF的形成能力。

各缺失株对雏鸡半数致死量(LD50)的测定
将130只1日龄雏鸡,随机均分为13组,并将鸡白痢沙门菌C79-13、Δcya、Δcrp及ΔcrpΔcya在LB液体培养基中37℃过夜培养,根据本研究室前期试验结果,将各菌株分别以表3的剂量经腹腔注射感染雏鸡,同时设置PBS阴性对照组,观察21 d直至无雏鸡死亡,根据Bliss法计算各株菌对雏鸡的LD50,同时采用引物pi1/pi2从感染组各死亡雏鸡肝脏分离的细菌中经PCR鉴定。

各缺失株对雏鸡的免疫保护率试验
将40只1日龄雏鸡,随机均分为4组,10只/组。
分别为Δcrp、Δcya、ΔcrpΔcya免疫组以及PBS对照组,参考文献各组雏鸡均分别灌服107cfu/mL的各菌液,每只100μL,7 d后再以同样剂量与方式灌服一次,对照组以PBS代替菌液经同样的处理,每次接种前12 h对雏鸡禁食禁水,并按200μL/只灌喂10%NaHCO3溶液中和胃酸。
二免后7 d各组雏鸡均以5.0×108cfu/mL经腹腔注射亲本菌株C79-13进行攻毒,500μL/只,在42 d的观察期内观察并记录各组鸡的发病及死亡情况。
并计算各菌株对雏鸡的免疫保护率。
免疫保护率=(对照组鸡死亡数-接种鸡死亡数)/对照组鸡死亡数×100%。

重组自杀性质粒p REΔcya的鉴定结果
对构建的重组自杀性质粒p REΔcya经KpnⅠ、XbaⅠ双酶切鉴定,结果显示,出现5 173 bp和2 475 bp两条目的条带;经KpnⅠ、XhoⅠ双酶切鉴定结果显示,出现6 537 bp和1 111 bp两条目的条带;经Bam HⅠ、XbaⅠ双酶切鉴定结果显示,出现6 284 bp和1 364 bp两条目的条带,均与预期一致。
测序结果显示,插入的基因缺失了1 182 bp的基因片段,且该片段确为cya基因。
表明正确构建重组自杀性质粒p REΔcya。
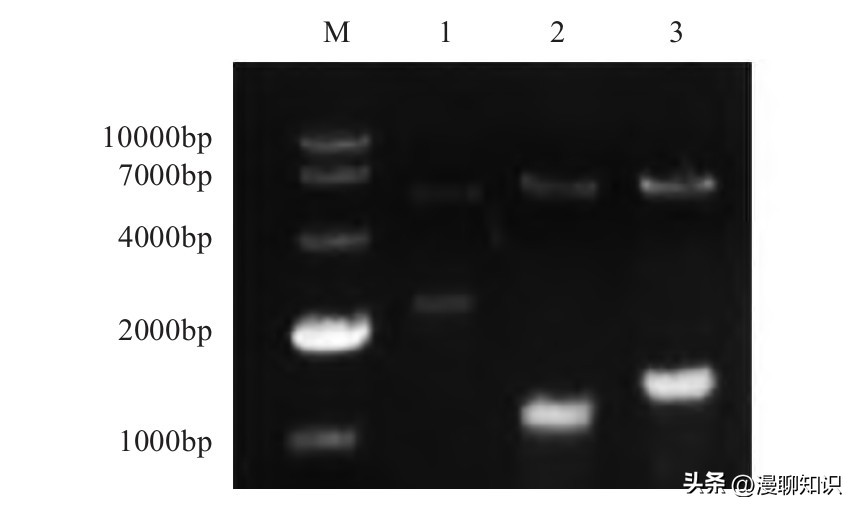
图2 重组自杀性质粒pREΔcya的酶切鉴定结果
M:DL10000 DNA Marker;1:p REΔcya/KpnⅠ+XbaⅠ;2:p REΔcya/KpnⅠ+XhoⅠ;3:pREΔcya/Bam HⅠ+XbaⅠ
各缺失株的构建及鉴定结果
以重组菌p REΔcya/χ7213作为供体菌,Δcrp为受体菌,通过接合转移试验将重组自杀性质粒p REΔcya/χ7213转入Δcrp中,过夜培养后,涂布在含氯霉素和蔗糖的LB固体培养基中继续过夜培养,获得一次重组菌并利用引物P5/P6经PCR鉴定。
结果显示,Δcrp出现约2 700 bp的目的片段,一次重组菌出现约2 700 bp、1 500 bp的两条目的片段。
将一次重组菌在NB培养基中过夜培养后,涂布LB固体培养基,过夜培养后再经含氯霉素的LB固体培养基筛选,12 h后挑取单菌落即为二次重组菌并采用P5/P6引物经PCR鉴定。
结果显示,Δcrp扩增出约2 700 bp的目的条带,二次重组菌出现约1 500 bp的目的片段。

进一步采用引物P6/P7经PCR鉴定该二次重组菌,结果显示出现约1 500 bp的片段,Δcrp出现约2 800 bp的片段,而p REΔcya/χ7213未扩增到任何条带。
测序结果显示,该重组菌确实缺失了321 bp和1 182 bp的基因片段,且分别为crp基因与cya基因片段。
均与预期相符,表明正确构建双基因缺失株ΔcrpΔcya。
以C79-13株为受体菌,大肠杆菌p REΔcya/χ7213为供体菌,按照构建ΔcrpΔcya的方法构建缺失株Δcya,并利用P6/P7引物经PCR鉴定,结果显示,获得约1 600 bp的目的片段,与预期相符。
测序结果显示,该缺失株缺失了1 182 bp的片段且确为cya基因片段。
表明,正确构建缺失株Δcya。

各缺失株的血清型及生化特性鉴定结果
血清型鉴定结果显示,Δcya、ΔcrpΔcya株与亲本菌株C79-13的血清型相比未发生变化,仍为O9型。
生化鉴定结果显示,Δcya、Δcrp、ΔcrpΔcya的生化特性与亲本株C79-13并不完全一致。
与亲本菌株C79-13相比,Δcya、Δcrp、ΔcyaΔcrp仅保留了发酵半乳糖、山梨醇的能力,而失去了发酵鼠李糖、葡萄糖、麦芽糖等糖类的能力。
表明crp、cya基因缺失后显著影响鸡白痢沙门菌的生化特性。

各缺失株遗传稳定性的鉴定结果
将各缺失株分别在LB培养基上连续培养60代,每隔10代采用P6/P7引物分别对各cya基因缺失株均经PCR和测序鉴定。
结果显示,均得到了1 575 bp的目的片段,亲本菌株C79-13扩增出2 857 bp的片段,表明各cya基因缺失株均能够稳定传代。
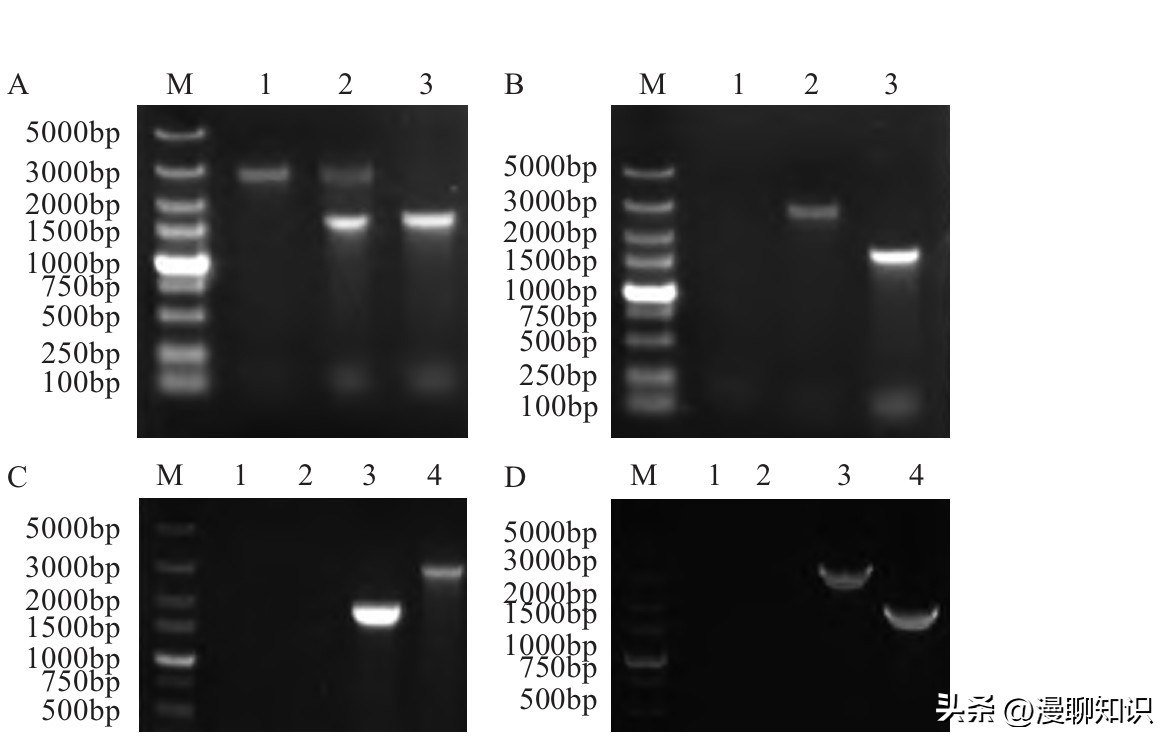
图3 缺失株ΔcrpΔcya(A、B、C)及Δcya (D)的PCR鉴定结果
A:p5/p6 PCR鉴定一次重组菌:M:DL5000分子质量标准;1:Δcrp;2:一次重组菌;3:p REΔcya/χ7213;B:p5/p6 PCR鉴定二次重组菌ΔcrpΔcya:M:DL5000分子质量标准;1:ddH2O;2:Δcrp;3:ΔcrpΔcya;C:p7/p6 PCR鉴定二次重组菌ΔcrpΔcrp:M:DL5000分子质量标准;1:ddH2O;2:p REΔcya/χ7213;3:ΔcrpΔcya;4:Δcrp D:p7/p6 PCR鉴定Δcya缺失菌株:M:DL5000分子质量标准;1:ddH2O;2:pREΔcya/χ7213;3:C79-13株;4:Δcya
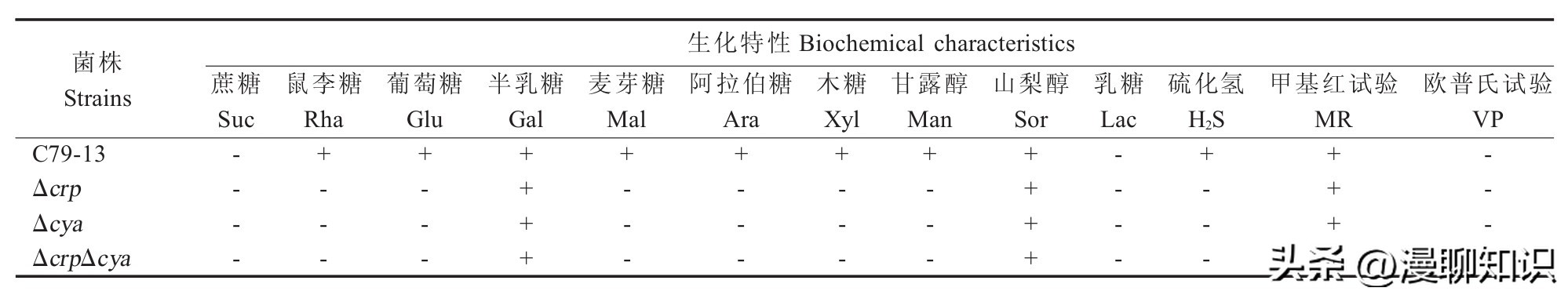
表2 各菌株生化特性的鉴定结果
各缺失株生长曲线的测定
将初始浓度均为106cfu/mL的Δcya、Δcrp和ΔcrpΔcya及亲本菌株C79-13转接至LB液体培养基震荡培养,每隔1 h取菌液平板计数,绘制生长曲线,结果显示,各缺失株的生长速度较亲本菌株相比均显著降低,尤其ΔcrpΔcya株的生长速度极显著下降(P<0.01),而Δcya与Δcrp的生长速度则无明显差异,表明crp、cya基因缺失后均对鸡白痢沙门菌的生长有一定的抑制作用。

各缺失株BF形成能力的测定结果
利用微量结晶紫法通过测定C79-13、Δcya、Δcrp及ΔcrpΔcya株的OD570nm值,分析各菌株BF的形成能力。
结果显示,与亲本株相比,各基因缺失株BF的形成能力均极显著降低(P<0.01),其中双基因缺失株BF的形成能力更低。
表明cya、crp基因均参与鸡白痢沙门菌BF的形成。
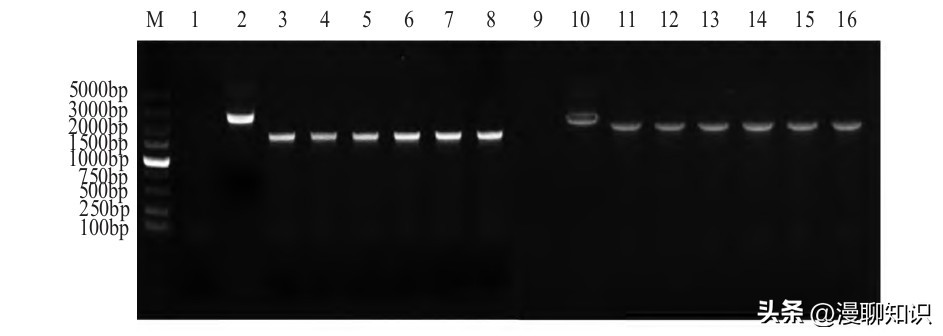
图4 cya基因缺失株的遗传稳定性鉴定结果
M:DL5000分子质量标准;1:ddH2O;2:Δcrp;3~8:ΔcrpΔcya第10、20、30、40、50、60代的扩增结果;9:C79-13株;10~16:Δcya第10、20、30、40、50、60代的扩增结果
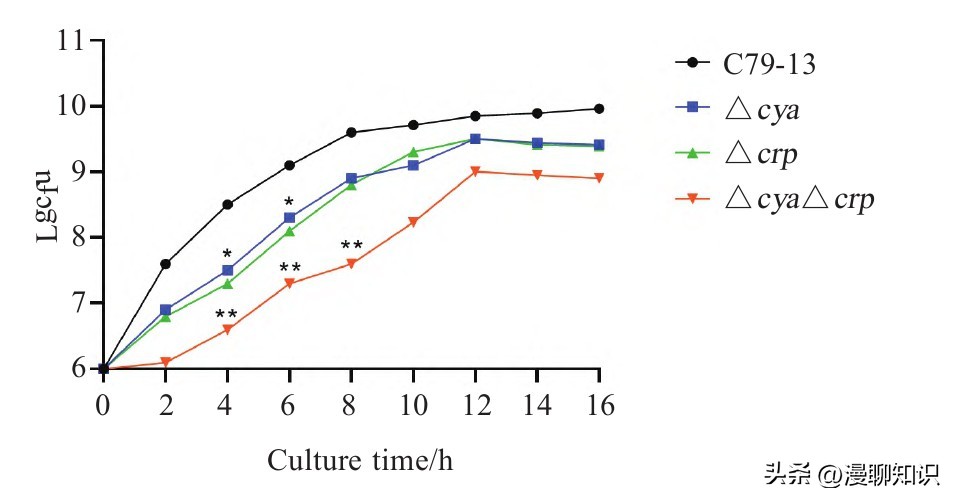
图5 各缺失株的生长曲线
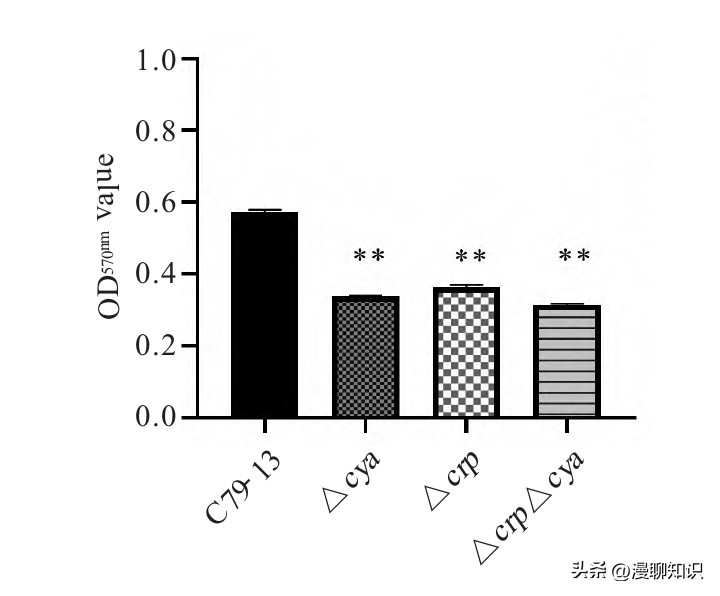
图6 各菌株BF形成能力的测定结果
各缺失株对雏鸡LD50的测定结果
将不同剂量的C79-13、Δcya、Δcrp、ΔcrpΔcya分别感染雏鸡后,雏鸡均不同程度死亡,而PBS对照组雏鸡均健活。
采用引物pi1/pi2经PCR均可以从感染组各死亡雏鸡肝脏分离的细菌中扩增出目的条带,表明,雏鸡确是由鸡白痢沙门菌感染引起死亡。
经Bliss法计算LD50,结果显示C79-13的LD50为2.46×106cfu/mL、Δcrp的LD50为1.41×1010cfu/mL、Δcya的LD50为2.84×109cfu/mL、ΔcrpΔcya的LD50为2.51×1011cfu/mL。
与亲本菌株相比,Δcrp的LD50升高约5.7×103倍、Δcya的LD50升高约1.1×103倍、ΔcrpΔcya的LD50升高约1×105倍,各缺失株毒力均明显下降,尤其是ΔcrpΔcya双缺失株毒力下降最多。
表明crp、cya基因与沙门菌对鸡的毒力密切相关。
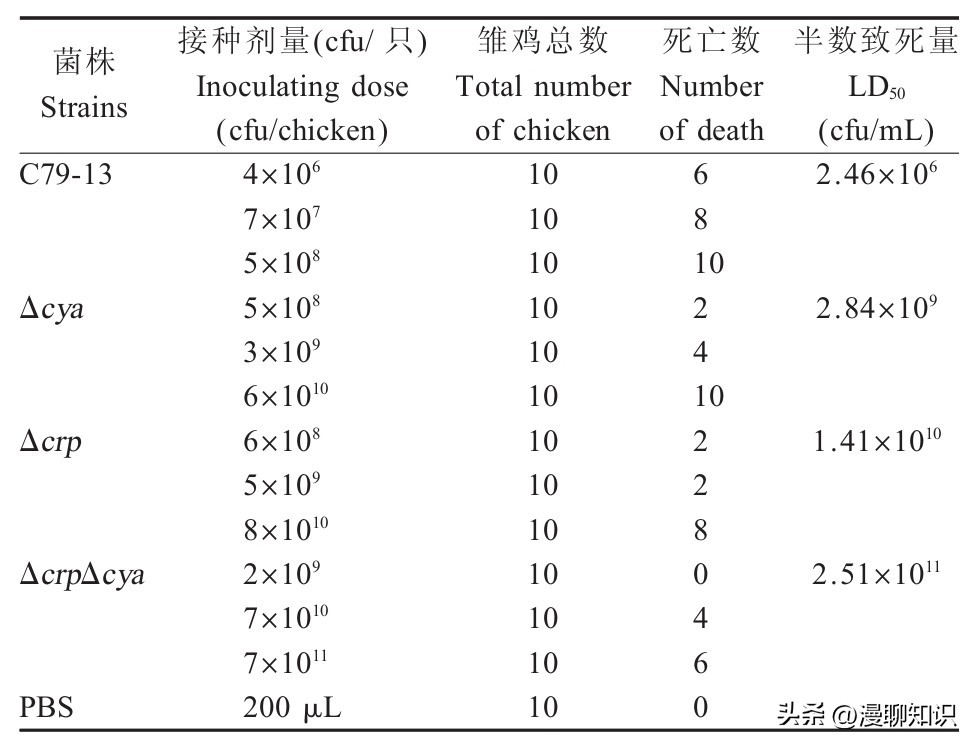
表3 各菌株对雏鸡毒力的测定结果
各缺失株对雏鸡免疫保护率的试验结果
各菌株均按107cfu/mL免疫雏鸡,在二免后一周利用亲本菌株C79-13攻毒,在42 d的观察期内观察并记录各组鸡的发病及死亡情况,并计算各菌株对雏鸡的免疫保护率。
结果显示:PBS对照组雏鸡攻毒后均出现腹泻症状,且在42 d内全部死亡。
而3个实验组的雏鸡攻毒后出现精神沉郁症状,且有部分鸡死亡。
Δcrp、Δcya、ΔcrpΔcya对雏鸡免疫保护率分别为80%(8/10)、60%(6/10)、50%(5/10)。
表明3株缺失菌中Δcrp的免疫保护效果相对较好,而cya基因缺失后反而降低了菌株的免疫保护效力。

随着分子生物学技术的迅速发展,以及对沙门菌致病机理的深入研究,科研人员开展了各种沙门菌疫苗的研究,其中利用基因工程技术将强毒株相关毒力基因敲除后构建的沙门菌新型减毒活疫苗,安全性好、毒力不易返强。
该类疫苗毒力减弱的同时保留了免疫原性,可以刺激机体产生全面的免疫应答,是相对理想的疫苗。
目前常使用基因重组技术构建含目的菌同源基因片段的重组自杀性质粒,将其转入受体菌后利用宿主的重组系统以及重组序列,经两步法最终完成同源重组,该技术可以直接对宿主的基因进行特殊修饰,已经广泛应用于革兰氏阴性菌的基因工程研究。

目前高效自杀性载体系统和Red同源重组系统均可以直接对革兰氏阴性菌的染色体处理及修饰,其中自杀性载体系统在染色体中不保留目的基因以外的其他片段,而Red同源重组系统对重组菌PCR融合产物的纯度要求较高,并且在敲除目的基因时会残留FLP重组酶作用(FRT)位点。
因此,本研究选择利用重组自杀性质粒介导的同源重组技术分别敲除或者同时敲除鸡白痢沙门菌的crp、cya基因,并构建相应的基因缺失菌株Δcya和ΔcrpΔcya。
cya和crp基因均为研究较为深入的鸡白痢沙门菌毒力相关基因,分别编码腺苷酸环化酶和cAMP受体蛋白,可参与该菌多种基因的表达,并能够调节其氨基酸、碳水化合物的利用以及菌毛、鞭毛及外膜蛋白的合成,与细菌的生理活动与物质代谢密切相关。
缺失crp基因阻断了细菌在哺乳动物体内摄取cAMP的唯一途径,缺失cya基因则使细菌失去了生成cAMP的能力,使其无法生成cAMP导致细菌在宿主体内不能正常生存。

为了探究缺失crp/cya基因后对C79-13株的影响,本研究构建了cya单缺失株以及双缺失株,对亲本菌株及各缺失菌株生物学特性的比较分析发现,与C79-13株相比,各缺失株的血清型均无变化,但其生化特性发生了一些改变,失去了发酵鼠李糖、葡萄糖、麦芽糖等糖类的能力,但保留了发酵山梨醇、半乳糖的能力,说明crp、cya基因的缺失会在一定程度上损伤细菌对碳源的利用能力,其参与碳水化合物和氨基酸代谢等的基因表达以及菌毛与鞭毛相关基因的表达受到影响,可能会降低细菌的新陈代谢水平。
与亲本菌株相比,缺失菌株的生长速度明显降低,其中双基因缺失菌株ΔcrpΔcya的生长速度最慢,而Δcya与Δcrp相比生长速度无明显差异,说明由于crp、cya基因的缺失损伤了细菌利用外源碳源的能力,进一步降低了其营养代谢的水平,从而极大影响了鸡白痢沙门菌的生长性能;在BF形成能力的测定中发现,分别缺失cya及crp基因后菌株BF的形成能力与亲本菌株相比显著降低,且双基因缺失株BF的形成能力更低。

BF是细菌在自然界中存在的主要形式之一,是其于有害环境中产生的藻酸盐多糖、纤维蛋白、脂质蛋白等,使细菌相互粘附或附着于物体表面而形成的膜状物,是防止细菌受到外界恶劣环境影响的一种结构,能够提高细菌逃避宿主免疫反应的能力,增强细菌对抗生素、消毒剂等外界环境的抵抗力,进而造成细菌的持续反复感染,结合以上试验表明,作为毒力调节基因的crp、cya对鸡白痢沙门菌BF的形成是必需的,BF形成能力的降低有可能导致细菌毒力的下降。
为了评价基因缺失菌株对雏鸡的毒力即感染性,本实验室在前期预试验中发现亲本菌株的致病性较强,但基因缺失株对雏鸡的致病性降低,其中双基因缺失株对雏鸡的致病性最弱,将缺失株与亲本株以同样的剂量感染并未造成雏鸡死亡,导致无法评价沙门菌对雏鸡的毒力。

因此本研究先将各菌株10倍倍比稀释涂板计数后再选合适的稀释度接种(接种剂量以实际计数为准),即将细菌培养达对数生长期后,按预试验的结果将C79-13、Δcrp、Δcya、ΔcrpΔcya分别稀释为107cfu/mL、109cfu/mL、109cfu/mL、1010cfu/mL,并分别选择各菌相邻的两个浓度共3个浓度感染雏鸡后发现,各缺失菌株的毒力明显降低,与亲本菌株相比,Δcya的LD50升高约1.1×103倍,Δcrp的LD50升高约5.7×103倍,而ΔcrpΔcya的LD50升高约1.0×105倍,表明crp、cya基因均与鸡白痢沙门菌的毒力密切相关,二者的单一缺失和同时缺失均能够降低沙门菌的毒力,尤其同时缺失二者后极大降低了该菌的毒力。

也印证了上述基因缺失株BF形成能力的降低有可能致其毒力下降的推测。
在此基础上进行的攻毒保护试验结果显示:Δcrp、Δcya、ΔcrpΔcya免疫后雏鸡获得的攻毒保护率分别为80%、60%、50%,通过该试验可见虽然双基因缺失株ΔcrpΔcya毒力最低,有良好的安全性,但其免疫保护率却最低,推测可能是由于crp、cya基因的缺失导致无法很好的激发雏鸡的免疫应答。
Δcrp的免疫保护效果最佳,因此该菌株有望作为一种沙门菌基因缺失疫苗的候选菌株。
综上所述,本研究结果表明crp和cya基因与鸡白痢沙门菌的生长代谢、毒力有一定的相关性,且缺失株Δcrp有较好的免疫保护效果,为鸡白痢沙门菌基因缺失疫苗及沙门菌病的防控提供了借鉴与参考。
《鸡白痢沙门菌htrA基因缺失株的构建及其相关生物学特性研究》
《5株鼠伤寒沙门菌基因缺失株的生物学特性比较》
《减毒鸡白痢沙门氏菌Δcrp C79-13株的构建及其对雏鸡的免疫活性》
《鼠伤寒沙门氏菌SL1344株ΔcrpΔcya缺失株的构建及其生物学特性初步研究》