Anal. Chem. | 基于金属-有机框架限制效应的类过氧化物酶仿生纳米酶用于生物传感
**今条头日**上无法显示上标、下标,欲获得更好的阅读体验请前往微信公众号。
*前往“纳米酶Nanozymes”公众号,了解有关纳米酶的最新消息!
*本文首发于“纳米酶Nanozymes”公众号,2022年7月1日
*编辑:俞纪元
背景介绍
天然酶具有独特的三维结构,是一种重要的生物催化剂,一般在温和的条件下对特定底物表现出较高的催化效率。然而,天然酶也存在一些明显的缺点,例如成本高、纯化过程复杂、在恶劣环境中稳定性差等等。作为其替代物,仿生纳米酶通过模拟天然酶活性位点的结构,在许多领域显示出良好的应用前景,并且在催化活性和稳定性方面优于天然酶。本文探讨的是一种基于多肽或蛋白质的纳米酶。多肽或蛋白质在空间中折叠产生丰富的结合位点,构造疏水的微环境,可以调节纳米酶的活性。尽管该纳米酶的前景光明,但在其研究过程中仍存在一些挑战。例如,由于这种基于蛋白质的纳米酶与天然酶的化学成分相似,它在恶劣条件下也表现出较差的稳定性和耐受性。因此,寻找一种合理调节多肽或蛋白质基仿生纳米酶的催化活性和稳定性的方法是亟待解决的问题。
金属-有机骨架(MOFs )由金属离子和有机连接物组装而成,具有可变的多孔网络结构和超高的比表面积。与典型的多孔材料相比,MOFs在蛋白质保护和生物催化方面,尤其是在酶或纳米酶方面,显示出了良好的应用前景。因此,作者提出了一种新的构造方法,将氯化血红素(Hemin)/牛血清白蛋白(BSA)共组装在ZIF-8骨架中,通过限域效应实现类过氧化物酶的活性调控(示意图A)。
Hemin@BSA的结构类似于辣根过氧化物酶(HRP),其中BSA像口袋一样包住作为活性辅因子的血红素,同时为底物构建一个疏水的空间。由于限域效应,有多孔内腔的ZIF-8被看作是Hemin@BSA的理想外层,不仅可以加速底物的反应,而且可以显著增强其类过氧化氢酶的活性。此外,用ZIF-8包裹Hemin@BSA可以通过快速结晶形成一层保护壳来防止Hemin@BSA在恶劣中的分解。

示意图 A Hemin@BSA及Hemin@BSA@ZIF-8的制备及应用。
Hemin@BSA@ZIF-8的类过氧化物酶活性以及稳定性都比Hemin@BSA更好,目前已经成功应用于小分子超灵敏光敏平台的开发。此外,和抗体结合的Hemin@BSA@ZIF-8可以被用在一种改进的间接竞争酶联免疫吸附实验(ELISA)中BPA(牛血清白蛋白)的分析。Hemin@BSA@ZIF-8还被引入基于纸或凝胶的生物传感平台,该平台可以与智能手机同步,进行实时比色法检测H2O2和葡萄糖(示意图B)。
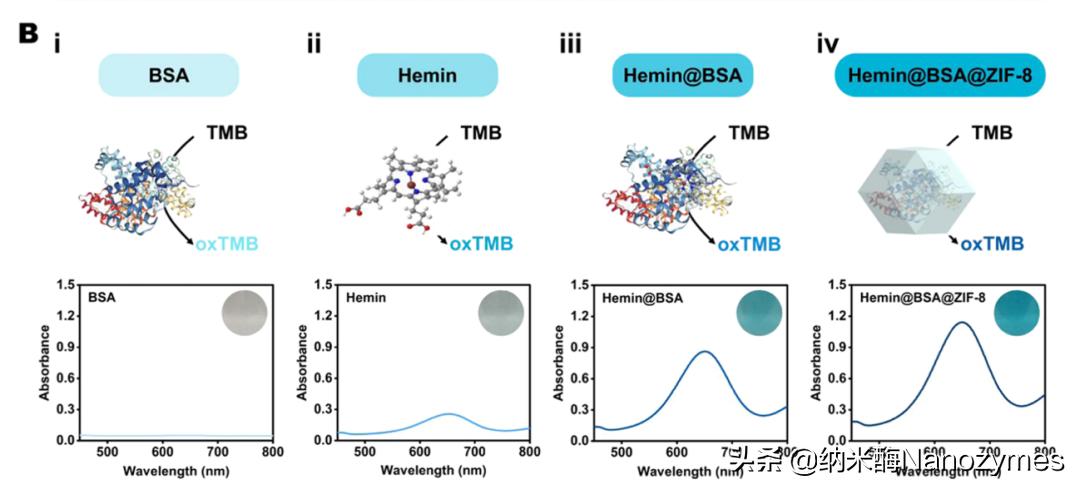
示意图 B 对不同物质的机理描述及相应的紫外光谱分析。
从左到右的组分为(i)BSA;(ii)血红素(Hemin);(iii)Hemin@BSA及(iv)Hemin@BSA@ZIF-8。
Hemin@BSA和Hemin@BSA@ZIF-8的制备与表征
在Hemin@BSA制备过程中,可以通过调整Hemin/BSA的比例进行Hemin@BSA的结构优化。Hemin@BSA的分子直径在30-50 nm之间(图1A)。使用傅里叶变换红外光谱(FTIR)研究了Hemin@BSA的共组装反应。图1E表明Hemin和BSA的吸收峰值分别在 ~1699 cm−1和~1653 cm−1,这可能是氨基酸中羧基的拉伸震动造成的。图1E同时指出,Hemin@BSA在1011 cm−1处有一个明显的吸收峰,这要归因于C−N键在BSA中的吡咯环或咪唑环拉伸振动。而且,Hemin和BSA组合后,所有吸收带的峰位都出现了明显的偏移,说明血红素和BSA之间确实存在共价键。可以这样认为:Hemin@BSA可能受到共价键、π-共轭相互作用和氨基酸氢键的共同影响。

图1 Hemin@BSA@ZIF-8纳米颗粒的制备与表征。
Hemin@BSA@ZIF-8具有与ZIF-8类似的典型菱形十二面体结构(图1B),表明封装Hemin@BSA对ZIF-8的晶体形成没有影响。此外,在ZIF-8内部可以看到一些光滑均匀的球形颗粒,说明生物矿化方法可以将Hemin@BSA嵌入ZIF-8的内腔中。这一观察结果与图1C中元素映射图像的结果一致。从图1C的HAADF-STEM图像可以看出,Fe元素均匀分布在C、N、O、Zn元素的中间,并没有Hemin@BSA分布在Hemin@BSA@ZIF-8表面上。图1D表明Hemin@BSA是被包裹在ZIF-8中,而不是处于简单的物理吸附状态。XRD图像中,Hemin@BSA@ZIF-8是以ZIF-8的晶体形式观察到的,Hemin@BSA@ZIF-8的所有的衍射峰可以与模拟的ZIF-8的标准结构相匹配(所有位置用黑点标记)。此外,图1E中FTIR图像也可以证明这一点。图1F中的N 1s光谱表明,一个N=C在398.6 eV处的结合峰和N-C在399.3 eV的处结合能是吡咯环或咪唑环造成的。基于Fe 2p区域的特定结合能差值(ΔE)为13.1 eV,结合708 eV和 722.2 eV 处的拟合峰可以确定纳米酶中氯化血红素的Fe(III)的价态。
Hemin@BSA和Hemin@BSA@ZIF-8类过氧化物酶活性
如图2A所示,使用TMB、APTS和OPD三种不同的底物,通过比色法来检测Hemin@BSA和Hemin@BSA@ZIF-8类过氧化氢酶的活性。图2B是TMB溶液分别加入BSA、Hemin以及Hemin@BSA与H2O2混合溶液之后的紫外光谱。从曲线a可以看出,加入BSA后并没有发生颜色变化,证明BSA仅用作结合,与Hemin@BSA的催化活性没有直接关系。BSA与氯化血红素组装后(曲线c),吸光度比纯氯化血红素(曲线b)更高,同时溶液颜色变为蓝色。这说明BSA与Hemin的共价相互作用具有良好的催化性能。 接下来,研究者以TMB和H2O2混合溶液为底物,如图2C所示分别加入BSA(a)、ZIF-8(b)、ZIF-8/BSA(c)、Hemin@ZIF-8(d)和Hemin@BSA@ZIF-8(e),观察它们的吸收光谱。显而易见,曲线e所代表的溶液对底物的催化性能最为良好。当Hemin、BSA、ZIF-8分别加入底物中时,紫外光谱无明显变化,表明催化中心主要取决于Hemin@BSA和ZIF-8的催化剂组合。如图2D,通过限域效应精确调节特定区域基底的大小/形状,引入ZIF-8后Hemin@BSA的类过氧化物酶性能得到增强。
研究者接着通过比较试验对Hemin,Hemin@BSA, 和Hemin@BSA@ZIF-8的类过氧化物酶活性进行比较。首先,计算处理后Hemin、Hemin@BSA、Hemin@BSA@ZIF-8的溶液对应不同底物的吸光度,如图2E所示。Hemin@BSA添加到底物之后吸光度比纯Hemin有大幅度提升,对应TMB、ABTS、OPD分别为3.55倍,2.98倍和2.08倍。在图2B、C进行的实验中,我们已经知道Hemin@BSA@ZIF-8光谱吸收峰值大于纯的Hemin@BSA。对应TMB、ABTS和OPD吸光度最终分别提高了1.29倍、1.22倍和1.25倍,表明Hemin@BSA@ZIF-8相比Hemin@BSA有进一步优化,并且直观地证明了这种纳米酶对各种底物都有显著的催化活性。
随后,进行了稳态动力学实验,以进一步评估Hemin、Hemin@BSA和Hemin@BSA@ZIF-8的类过氧化物酶性质,实验所用底物为 8 mM H2O2 和0.4 mM TMB。评估参数为Michaelis−Menten constant (Km) 和 maximum initial velocity (Vmax)。Km越低说明纳米酶和相应底物的亲和力越高。如图2F所示,Hemin@BSA@ZIF-8的Km低于Hemin和Hemin@BSA,说明ZIF-8的包封有利于提高该纳米酶与底物之间的结合亲和力。此外,Hemin@BSA@ZIF-8相较其他两组Vmax明显增加,说明ZIF-8的限域效应有助于底物交换,进一步促进催化过程的反应速率。图2G是TMB比色系统中的吸光度随时间变化的曲线,也证实了这一发现。由此,我们可以得出结论:Hemin@BSA@ZIF-8作为仿生纳米酶,与Hemin和Hemin@BSA相比,具有优异的类过氧化物酶催化活性。其中ZIF-8的增强效应对催化性能起着重要的调节作用。
研究者还进一步比较了Hemin@BSA和Hemin@BSA@ZIF-8的性质。图2H的底物是0至40mM范围内的不同H2O2浓度,检测Hemin@BSA和Hemin@BSA@ZIF-8的吸光度。对于两种物质,紫外线-可见光吸收峰dou 随着H2O2浓度增加逐渐增大。在650 nm处,吸光度与H2O2浓度之间获得了良好的相关曲线。同样条件下,Hemin@BSA@ZIF-8吸光度更高。放置35天后,Hemin@BSA的活性降低了60%,而Hemin@BSA@ZIF-8的活性为第一天的88%。ZIF-8封装在保持催化剂稳定性方面发挥着重要作用。
为了评估Hemin@BSA和Hemin@BSA@ZIF-8在微扰条件下的表现,研究者设计了一系列模拟的恶劣环境,分别是胰蛋白酶、二甲基甲酰胺(DMF)、95°C和95°C时DMF存在的环境。可以用TMB溶液的颜色作为参考(图2J,K)。孵化一段时间后,Hemin@BSA相比Hemin@BSA@ZIF-8吸光度略有下降(图2K)。相比于Hemin@BSA,Hemin@BSA@ZIF-8更能耐受恶劣环境对其催化活性的干扰,尤其是在高温和DMF环境下。没有ZIF-8的保护时,细胞内的催化活性损失最高可达到58.8%。毫无疑问,ZIF-8在防止活性物质在恶劣环境中受损方面具有不可忽视的作用。

图2 Hemin@BSA和Hemin@BSA@ZIF-8类过氧化物酶样活性比较。
应用
BPA是一种常见的内分泌干扰物,广泛应用于以婴儿用品为代表的各种消费品。Hemin@BSA@ZIF-8与抗体结合(Hemin@BSA@ZIF-8@Ab)可以代替HRP用于间接ELISA比色法检测BPA(图3A)。在抗原稀释8000倍、抗体稀释4倍的情况下观测的结果最理想,450 nm处的色度信号强度随着BPA浓度的增加而逐渐增加(图3B),并且在1-729ng/mL的检测范围内线性关系良好,检测极限如图3C所示为0.546 ng/mL。相比较而言,用Hemin@BSA@Ab检测一系列BPA浓度,最终LOD为2.61 ng/mL,比基于Hemin@BSA@ZIF-8@Ab的灵敏度低约4.78倍。

图3 基于Hemin@BSA@ZIF-8的新型ELISA比色法检测BPA示意图及观测结果。
此外,这项研究还可以用于H2O2和葡萄糖检测的纸基和凝胶基传感器。如图4,通过将Hemin@BSA@ZIF-8和TMB溶液浸入滤纸来构建纸的传感器。为了避免Hemin@BSA@ZIF-8失活,需要将试纸转移到冷冻干燥容器中进行冻干处理。从SEM图像(图4)可以看出,在滤纸的纤维结构上发现了许多规则的ZIF-8颗粒,证实了这种制备方法的可行性。

图4 基于Hemin@BSA@ZIF-8的纸张传感器,用于H2O2和葡萄糖的比色检测原理图。
总结Conclusion
这项工作设计了一种简单的仿生纳米酶(Hemin@BSA@ZIF-8)。由于限域效应,ZIF-8外层能明显提高Hemin@BSA类过氧化物酶活性。ZIF-8的刚性结构也能提高其在恶劣环境下的耐受性。用Hemin@BSA@ZIF-8作为探针,对H2O2、葡萄糖和BPA的检测获得了令人满意的分析性能。此外,Hemin@BSA@ZIF-8还可以用于基于纸张或凝胶的智能传感器,数据与手机端同步,实现对目标的实时测定。
往期推荐
01
大学化学 | 纳米酶在抗肿瘤治疗中的应用
02
ACS Nano | 类中性粒细胞膜包被纳米酶治疗缺血性脑损伤
03
Chem. Eng. J. | 含氧缺陷功能化的五氧化二钒纳米片电极用于仿生催化
04
JACS | 基于过氧化氢置换纳米氧化铈表面DNA的策略
撰稿:俞纪元
审阅:赵婧媛
编辑:俞纪元
原文链接:https://pubs.acs.org/doi/10.1021/acs.analchem.2c00058