1月9日,FDA批准Blueprint Medicines公司Ayvakit (avapritinib)上市,用于治疗携带血小板源性生长因子受体 α(PDGFRA)基因18外显子突变的不可手术或转移性成人胃肠道间质瘤(GIST)患者,其中也包括D842V 位点突变这种最常见的18外显子跳跃突变类型。
Avapritinib是一种口服的、具有高活性高选择性的KIT及PDGFRα*制剂抑**。具有KIT及PDGFRα突变(包括KIT D816V、PDGFRα D842V 和KIT 外显子17突变)的多种疾病对标准疗法响应很差,缺乏有效的治疗方式,avapritinib针对以上突变在临床前均表现了很好的活性。
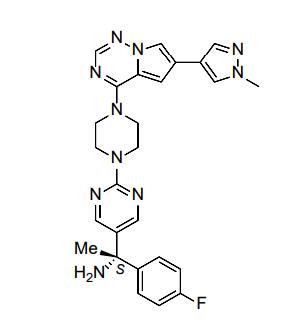
Avapritinib结构式
GIST是一类起源于胃肠道间叶组织的肿瘤,占消化道间叶肿瘤的大部分。GIST 可以发生于消化道的任何部位,以胃和小肠最为常见,分子机制是编码酪氨酸激酶受体蛋白基因 KIT(CD117) 或血小板源性生长因子受体 α(PDGFRα) 基因激活突变所致。大约6%的新确诊患者携带PDGFA外显子18突变。
FDA此次批准主要基于43例携带PDGFRα 外显子 18 突变的开放标签、多中心、单臂I期临床研究(代号NAVIGATOR)的数据,其中38例患者携带PDGFRA D842V突变。患者接受avapritinib 300或400mg每日1次治疗,直至疾病进展或出现不可耐受毒性。
结果显示,患者的总应答率(ORR)达到了84%,其中完全应答为7%,PDGFRA D842V突变突变患者的ORR更高一些,达到了89%,完全应答为8%。
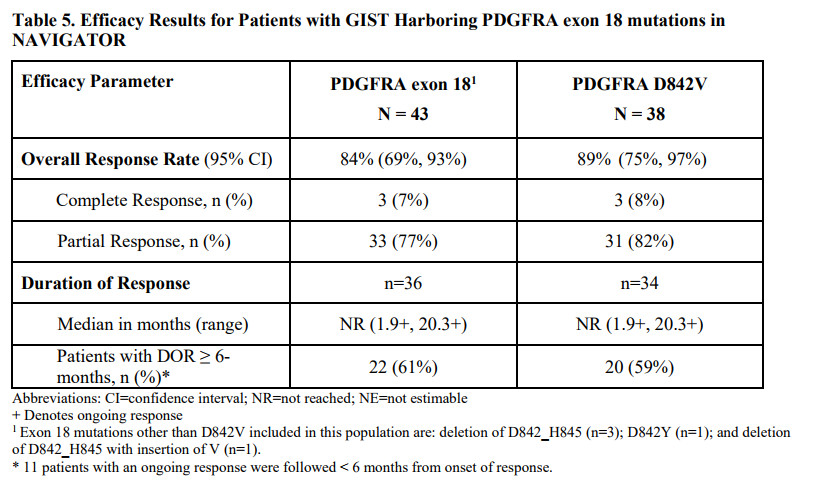
来源:FDA Label
安全性方面,avapritinib治疗最常见的不良反应包括水肿、恶心、疲劳、认知功能损伤、呕吐、食欲下降、腹泻等。
2017年6月,avapritinib获美国食品和药物管理局(FDA)授予的突破性疗法认定,用于治疗携带PDGFRα D842V突变的不可切除或转移性胃肠道间质瘤患者。此前,avapritinib已获FDA授予的孤儿药资格和快速审批资格,以及欧盟委员会授予的孤儿药资格。
Blueprint Medicines还在开发avapritinib用于晚期系统性肥大细胞增生症的适应症,目前处于II期阶段。
2018年6月4日,基石药业和Blueprint Medicines宣布达成独家合作及授权许可协议,获得3款药物在中国大陆及香港、澳门和台湾地区的临床开发与商业化权利,avapritinib正是其中之一。avapritinib目前在国内的III期研究正在进行,评估BLU-285与瑞戈非尼治疗胃肠道间质瘤的疗效和安全性差异,第1例患者已于2019年6月25日入组。