研究背景


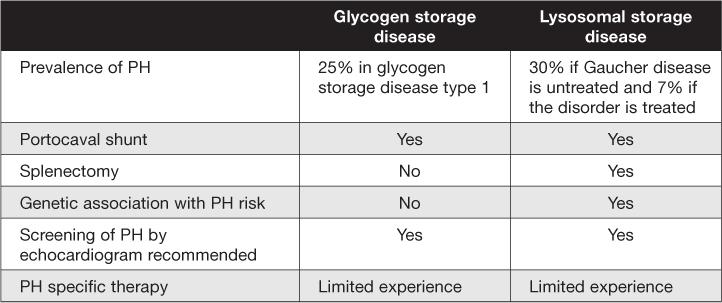
第六届世界肺动脉高压研讨会建议在所有形式的前顶冠前肺动脉高压(PH)的定义中,将肺血管阻力≥3 Wood单位与平均肺动脉压力<20 mmHg相关联。自1998年以来,第5组在“直接影响肺血管的疾病”到2003年的“杂项”之间经历了重大变化,直到最近的更新中,该组中包括了多种病理生理过程。作为这个异质性群体的一部分,代谢性疾病被认为在与PH相关的主要病理生理机制中起着一定作用。其中包括肝糖原贮积病和高氏病。甲状腺疾病虽然没有被明确纳入世界研讨会的分类中,但已经描述了多种与PH相关的机制,因此在本综述中也将进行讨论。我们将描述这些代谢性与PH相关的疾病的流行病学、发病机制和治疗(下表)。
代谢疾病都有哪些?
糖原贮积病:
糖原贮积病是由糖原代谢的遗传变异引起的,导致糖原在各种器官中沉积,主要是肝脏和肾脏。有11种不同类型的糖原贮积病,根据酶缺乏和临床表现的不同而变化。有与糖原贮积病1型(冯·吉尔克病)和2型(庞贝病)相关的肺动脉高压病例报告。在各种糖原贮积病中,主要在糖原贮积病1型中被描述为肺动脉高压。
1)糖原贮积病1型
糖原贮积病1型是由葡萄糖-6-磷酸酶酶缺乏(GSD 1a)或葡萄糖-6-磷酸酶微粒体转运蛋白缺乏(GSD 1b)引起的。这种情况通常在婴儿期诊断,表现为进食间低血糖。据估计,大约25%的糖原贮积病患者可能是1型。糖原贮积病1a的发病率为每10万人中1例。到目前为止,糖原贮积病中肺动脉高压的发病率尚不清楚,只有报道了11例糖原贮积病1型合并肺动脉高压的患者。其中,5例伴有可能诱发肺动脉高压的其他疾病,包括门体分流、心房间隔缺损和遗传性出血性毛细血管扩张症。
有人假设与糖原贮积病1型相关的肺动脉高压患者具有与第6届世界肺动脉高压研讨会第1组肺动脉高压(PAH)类似的特征,因为他们体内血清素水平升高,血清素是一种血管收缩胺,它既是肺血管收缩剂,也是血小板中的血管平滑肌细胞生长因子。
根据这一假设,Humbert等人收集了13例糖原贮积病1a患者、1例糖原贮积病1a合并严重肺动脉高压患者和16例严重肺动脉高压患者的血浆血清素水平。有趣的是,糖原贮积病1a合并肺动脉高压患者的血浆血清素水平显著升高(113.4 nmol/L),而仅有严重肺动脉高压(38.8 ± 7.3 nmol/L)或糖原贮积病1a(36.8 ± 11.5 nmol/L)的病例血浆血清素水平较低。这一发现引起了在这一人群中考虑针对肺动脉高压的治疗的思考。Ueno等人对一名17岁的患者进行了单一疗法的西地那非治疗,患者出现晕厥,诊断为低心输出量的右心衰竭,经过3周治疗后,患者的血流动力学和生物标志物得到了改善。
针对这些人群建议定期进行心脏超声心动图筛查肺动脉高压。已知报道的糖原贮积病1型和肺动脉高压的病例是在10岁以上的儿童中。因此,可以根据10岁及以上糖原贮积病患者的指南进行筛查计划和定期心脏超声心动图检查。
2)糖原贮积病2型
Li等人描述了一例16岁女孩的糖原贮积病2型并发肺动脉高压的病例。该患者存在严重的呼吸肌无力,导致肺功能受损和呼吸衰竭。她的肺动脉收缩压为65 mmHg,慢性呼吸性酸中毒,pH值为7.3,Pco2为83 mmHg。他们推测,严重的肌无力导致肺功能受损和呼吸衰竭可能是引发肺动脉高压的原因。我们的研究小组之前已经描述了高碳酸血症如何直接导致肺血管收缩和血管重构的机制,包括通过增加氢离子浓度和交感神经系统的激活。
溶酶体贮积病(高氏病)
高氏病是一种常染色体隐性遗传疾病,其特征是溶酶体贮积病,即酶葡糖脑苷酰酶的缺乏。因此,巨噬细胞-单核细胞系统和器官(主要是骨髓、肝脏和脾脏)中会积聚葡糖脑苷酰。与罕见的婴儿或急性型(2型)相比,成年或慢性型(1型)高氏病的发病率更高。
高登氏病(Gaucher病)的肺动脉高压(PH)形成机制有以下几个方面:首先,由于糖脂酶缺乏,Glucocerebroside在肺间质(以间隔增厚表现)沉积增加,导致肺组织微循环受损。其次,由于肺泡毛细血管阻塞和致命的骨髓小栓子形成,血管病变进一步加剧。高登细胞已在肺实质、血管内腔、淋巴分布的斑片浸润、肺泡内浸润和间质空间(围支气管、围血管和间隔)中被发现。肺毛细血管的普遍受累表明该疾病具有全身性质。有趣的是,高登病1型与孤立性PH有关,但在肺实质中没有高登细胞的存在。
高登病还通过间接机制促进肺血管疾病的发展,因为它与脾切除和肝脏疾病有关,这两者都会导致PH的发生。脾切除后,由于骨髓梗死和外骨髓造血引起的巨核细胞对毛细血管的加固,可能发生血栓栓塞。此外,高登病患者脾切除与严重和危及生命的PH密切相关。Mistry等人的研究发现,所有严重PH(右室收缩压力50-130 mmHg)的患者均无脾功能,而右室收缩压力<50 mm Hg的患者只有31%(比值比28.8,95%置信区间1.6-531.6,P <0.001)。
脾脏作为主要的细胞储存库被切除后,单核巨噬细胞向其他组织(如肝脏、骨骼肌和肺)迁移,从而导致血管壁的持续重塑。BMPR2和ALK1的遗传关联未被证明是高登病1型的修饰因子。肝脏受累在高登病中很常见,其严重程度和临床意义呈广泛范围,从无症状到肝硬化不等。门脉高压可以导致肺动脉高压,而在肝硬化生理学中常见的高动力循环可导致PH,因为右室心输出量增加。
未接受治疗的高登病1型患者中PH的发生率为30%,而接受酶替代治疗的病例中可以降至7%。个体可能由于肺血管阻力升高和肝肺综合征而发展为PH。Elstein等人对134名高登病1型成年患者进行了研究,发现其中7%的病例有PH,他们建议对接受和未接受酶替代治疗的所有患者进行常规心脏超声监测。发展PH的危险因素包括女性、脾切除、血管紧张素转换酶1基因多态性、酸性β-葡糖苷酶基因突变、不良酶替代治疗依从性和阳性家族史(即有PH的兄弟姐妹)。高登病的严重程度与PH的严重程度并不相关。与发展PH的危险因素类似,特定的突变(如GBA基因非N370S突变)、有相似表型的阳性家族史(如ACE 1等位基因)和雌性性别或脾切除史等表观遗传修饰因子可以预测PH的严重程度。
酶替代治疗已被证明是治疗高登病1型的安全有效方法,目前已成为标准治疗。有关高登病患者并发PH的文献报道了酶替代治疗和PH靶向治疗的使用。少数文献报道了高登病1型患者因PH和肺实质疾病需要肺移植的情况,这些患者多为女性,之前曾接受脾切除。首例接受肺移植的高登病1型患者为10岁患者,患有广泛的间质性肺疾病,并通过支气管肺泡灌洗检查发现高登细胞。随后,Goobie等人和de Boer等人报道了两例高登病1型女性患者,患有严重PH和脾切除史,接受了酶替代治疗和PH靶向治疗(包括博生坦、西地那非和前列地尔)。
这些患者接受了双侧肺移植手术,术后肺组织显示出与肺动脉高压一致的肺血管改变,但未见高登细胞。认为这与术前使用imiglucerase有关。然而,其他作者也显示,酶替代治疗可能导致PH稍微恶化,尽管影响似乎很小。Goitein等人报道了8例高登病患者肺部明显病变的临床表现,其中2例接受酶替代治疗的成年患者在超声心动图估计的压力基础上显示出新发或加重的PH。目前尚不清楚这一结果的临床意义,但估计的肺动脉收缩压力增加大约为5 mmHg到10 mmHg。高分辨率计算机断层扫描和胸部X线显示出异常的肺结构,尽管使用了酶替代治疗,但无法阐明其潜在机制。
甲状腺疾病
甲状腺功能紊乱在PH患者中并不罕见,常常与突然恶化有关。PH患者中甲状腺疾病的患病率较高,约为20%至35%。甲状腺刺激素与肺动脉压力以及游离甲状腺素与肺动脉压力之间存在相关性。甲状腺功能异常的生理效应与PH患者的不良预后有关。
回顾性研究表明甲状腺疾病与PH的诊断或治疗之间存在关联,且有几份病例报告描述了PH与甲状腺疾病之间的关系。有一些病例系列研究表明PH与甲状腺功能亢进症、甲状腺功能减退症或甲状腺抗体升高之间存在关联。Zuhur等人描述了Graves病患者中35%患者、多结节性甲状腺肿患者中36%患者和甲状腺功能减退症患者中13.5%患者出现较高的肺血管阻力。
自身免疫过程与PH之间存在联系,有趣的是,甲状腺疾病也可以由自身免疫过程引发。在对63名PH患者进行的一项观察性研究中,49%的患者显示出同时存在的自身免疫性甲状腺疾病证据,研究人员发现PH患者中抗甲状腺球蛋白和抗甲状腺过氧化物酶抗体的患病率较高。PH的诊断或治疗与自身免疫性甲状腺疾病的时间顺序无关。重要的是,25%的患者有一级亲属患有自身免疫性甲状腺疾病。Yanai-Landau等人还发现40名PH患者中有30%的患者携带抗甲状腺球蛋白抗体。对于这种关联尚无明确的解释。此外,甲状腺疾病患者中也发现了成人和儿童PH患者的骨形态发生蛋白受体2突变。
除了自身免疫过程外,甲状腺疾病还可能增加儿茶酚胺敏感性,增强内源性肺血管扩张剂,降低肺动脉顺应性,减少血管收缩剂,并产生可能导致PH的高心输出状态。其中一些提出的机制得到了在甲状腺正常状态恢复后肺血管阻力降低的支持。甲状腺激素影响血管细胞和组织的生长和成熟,影响细胞膜和内质网对钙ATP酶以及细胞膜通量的影响,从而影响平滑肌细胞。特定的甲状腺方案,如甲巯咪唑,通过甲状腺细胞的直接抑制作用、T辅助细胞和T抑制细胞比例的改变以及分泌血管活性物质的细胞,诱导免疫调节作用。
除了个别报告外,目前没有明确证据表明针对甲状腺疾病的PH靶向治疗的有效性。使用抗甲状腺药物、放射性碘、手术或这些疗法的组合已经证明可以降低或正常化肺动脉平均压。一项观察性研究显示,164名术前平均肺动脉收缩压为39 mmHg的患者在接受抗甲状腺药物、放射性碘和手术治疗后,平均术后压力可降至30 mmHg。使用PH靶向治疗也已经在甲状腺功能障碍和PH的病例中得到描述。Menon等人描述了6例甲状腺功能亢进和自身免疫性甲状腺肿患者,其中5例接受静脉前列环素(依前列醇)治疗,1例接受口服前列环素受体激动剂(塞来西洛)。这些作者得出结论,靶向前列环素通路可能是发展症状性甲状腺疾病的潜在风险因素,因为患者出现了Graves病、Hashimoto病和甲状腺毒症。
前列环素类药物治疗PH的副作用之一是甲状腺功能亢进,这已经在使用依前列醇、曲前列醇和塞来西洛的研究中得到证实。在事件驱动的III期试验Prostacyclin (PGI2) Receptor Agonist In Pulmonary Arterial Hypertension (GRIPHON)研究中,使用塞来西洛的治疗组(N = 574)中有8名患者出现甲状腺功能亢进,而安慰剂组(N = 582)中没有患者出现。其他研究报道,接受依前列醇治疗的已有PH的成年患者中,甲状腺刺激免疫球蛋白阴性的甲状腺功能亢进的患病率为6.7%。
研究结论
目前可用的数据表明,糖原贮积病和高酶病是重要的代谢性疾病,已经证明具有增加PH风险,并作为第6次世界PH研讨会分类中的5组。甲状腺疾病虽然没有被纳入5组分类,但其患病率较高,并通过各种机制与PH相关。这些疾病中PH的真实发病率通常不为人知,尽管研究表明PH可能很常见。治疗的指导依赖于个别病例报告、系列病例和观察性研究,但总体治疗方向是治疗潜在的基础疾病。
参考文献
Estefania Oliveros, Anjali Vaidya; Metabolic Disorders of Pulmonary Hypertension. Advances in Pulmonary Hypertension 1 April 2021; 20 (2): 35–39. doi: https://doi.org/10.21693/1933-088X-20.2.35