2.1 原子和分子
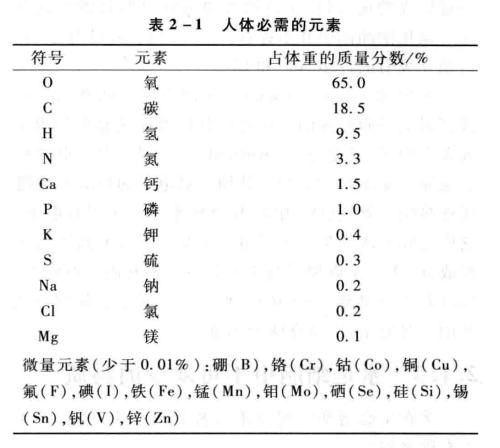
1.生命需要多种元素
元素是具有相同核电荷数的一类原子的总称。
3种亚原子颗粒(或称基本粒子)。
这3种基本粒子是质子( proton)、电子( electron)和中子( neutron)。质子带正电荷,电子带负电荷,中子则不带电荷。质子与电子的电荷大小相等,符号相反。中子的质量与质子的相等。
每一种元素的原子中,亚原子颗粒的数目不等。但每一种原子中,质子的数目是该原子所特有的。这一数目称为该原子的原子序数。例如,氢的原子序数是1 ,氦的是2。碳原子核中有6个质子,所以其原子序数是6。
每一种原子中,质子的数目与电子的数目总是相等的。但中子的数目则可能有变化。质子数和电子数都相同,但中子数不同的原子称为同位素( isotope), 因为它们在周期表中的位置相同。
例如碳元素就有3种同位素:C-12, C-13, C-14。它们都各有6个质子和6个电子,但中子数不同,分别为6、7和8。12C和13C为稳定性同位素,就是说它们的原子核不会发生变化。14C为放射性同位素( radioactive isotope ),因为其原子核会自行衰变,产生粒子和能量。
放射性同位素对生物是有害的,但在生物学研究和医学中有许多用途:
生物体对于含有放射性同位素的化合物照样吸收,和非放射性的一样。放射性极易用照相底片或计数器检测出来,所以可以利用放射性同位素显示某种原子在生物体内的来踪去迹。这种技术称为同位素示踪。例如,生物学家要了解二氧化碳在光合作用中的变化,便14CO2引入植物体内,看14C的变化途径。结果发现首先出现的是一种三碳的化合物。由此查明了CO2转变为糖的全过程。
放射性同位素也可用于疾病的诊断。例如对于肾病患者,可以将极少量的放射性示踪物注入血液内,观察放射性化合物在尿中出现的情况。这种诊断所用的放射性化合物量极少,所用的放射性同位素又是极易衰变的,所以对人体无害。
2.化合物由元素组成
原子的各种基本粒子中,决定其化学性质的是电子。电子所带的能量多少不等,距离原子核越远,电子所带的能量越多。原子中的电子存在于不同的能级,或称电子层。原子序数不同,原子中的电子层的数目也不等。最内的电子层中最多只能有2个电子,其外层中则可以有8个电子。最外层中的电子数决定着原子的化学特性。
生物体内最主要的4种原子是H,C,N和О,它们的最外层轨道都没有填满,所以都可以与别的原子发生反应。
原子的电子的共用或得失,也就是化学键的形成而形成化合物。化学键基本上有两类:离子键和共价键。
离子键:两个电荷符号相反的离子彼此吸引,形成离子键( ionic bond)。例如,钠原子和氯原子形成氯化钠,所形成的化合物(例如NaCl)是电中性的。氯化钠是一种盐,盐都是由离子键形成的化合物。氯化钠晶体中并不存在一个一个的 NaCl分子,只是相互吸引的许多Na+和Cl-。
共价键( covalent bond)是由两个原子间共用一对或多对电子而形成的。这种由共价键连接起来的两个或多个原子,就是分子(molecule)。氢气(H2)中的两个氢原子是由两个氢原子共用一对电子而形成的单键所连接的。水(H2O)则为两个氢原子分别与氧共用一对电子,所以有两个单键。
3.水是细胞不可缺少的物质
第一,水是极性分子。水是由两个氢原子和一个氧原子组成的,氢和氧共同争夺电子,形成共价键,但是氢和氧拉住电子的能力稍有不同。一个原子拉住共用电子的力量称其为电负性( electronegativity) ,拉住电子的力量越大,电负性越强。氧是元素中电负性最强的一种,氧吸引共用电子对的力量比氢大得多,结果共用电子对离氧原子近得多。水分子中的氧略带一点负电荷,氢略带一点正电荷。水是一个极性分子(polar molecule)。
第二,水分子之间会形成氢键。水分子的极性使得它们之间相互作用。略带负电荷的一端(O)与略带正电荷的一端(H)相互吸引,形成一个较弱的键——氢键(hydrogen bond)。其结果,每个水分子可以通过氢键与另外4个水分子连接。水分子的极性和它们之间氢键的形成使得水分子具有许多特性,因而液态水成为生命在地球上存在和发展的主要环境。
第三,液态水中的水分子具有内聚力。在瞬息之间,每个水分子都与无数个别的水分子相结合,彼此“黏合”在一起,这种内聚力( cohesion force)比任何其他液体中的都强。水的内聚力对生命极其重要,例如 ,参天大树,水分能从地下深处的根中上运到叶中,就是因为有这种内聚力使之形成连续不断的水柱而被拉上去。水分子之间的内聚力也使水的表面张力极大,使水的表面上好像覆盖了一层看不见的薄膜。正因为如此,密度比水大的昆虫才有可能在水面上爬行。
第四,水分子之间的氢键使水能缓和温度的变化。加热时,水的温度上升得慢。这是因为水分子间有氢键,热能必须先将氢键破坏才能使水分子运动得快些,温度才会上升。相反,当水冷却时,又会形成更多的氢键,这时就会有热能被释放出来,使冷却过程变慢。
沿海的气候较内陆温和,冷热变化较小,原因就在于水分子间的氢键。同样,它也使海洋的温度变化不大,适于海洋生物的存活。
氢键也使水分不易蒸发,使水的沸点高达100℃ ,这使地球上能保持着大量的液态水,利于生命的存在和发展。水分的蒸发也起冷却作用,出汗使陆生哺乳动物在夏季不致过热,人在剧烈运动时出汗也是调节体温的一种方式。
第五,冰比水轻。固态的密度小于液态的密度,这是水的独一无二的特性。
第六,水是极好的溶剂。由于水是极性分子,所以带有极性的分子也非常容易溶于水中。例如将食盐晶体放在水中,其中的Na+便吸引水分子中带负电荷的一端,使水分子将其包围;而CI- 则吸引其带正电荷的另一端,也使水分子将其包围。这样, NaCI 就溶于水中了。事实上,许多带有极性的分子都易溶于水,这种特性,使水在所有细胞内,在血液和植物的汁液内,都成为生命所需要的各种各样物质的良好溶剂。
第七,水还有一个重要特性,就是能够电离。在生物体内的大部分水溶液中,水分子是不电离的,但有一些水分子则电离成氢离子(H+)和羟离子(OH-)。凡是产生H+的化合物就是酸,产生OH-的化合物就是碱。
细胞中pH的微小变化都可能是有害的。生物体内的液体中有缓冲剂( buffer ),它们能抵抗 pH的变化,即当pH 高时,它们产生H+;而当pH低时,它们又能产生OH-去中和H+。但缓冲剂的缓冲能力是有限的,当环境中的pH 变化太大时,缓冲剂就无能为力,生物体也自然会受到伤害。
酸雨来源于矿物燃料(煤、石油、天然气)的燃烧。燃料中的硫和氮经燃烧变成了氧化物,这些氧化物与空气中的水蒸气形成硫酸和硝酸,随水降落到地上就成了酸雨。酸雨的pH可达2~3,有时酸雾的 pH可达1.7。酸雨可能酸化土壤,影响动植物的生长和人体的健康。严重的问题是海洋的酸化。
4.化学反应使原子重组
生命现象的特点之一就是新陈代谢( metabolism),新陈代谢包括无数的化学反应。这些化学反应使生物体内的众多物质千变万化。
化学反应并不能创造或破坏原子,它只能将原子重新组合。所以化学反应是破坏已有的化学键,形成新的化学键。
2.2 组成细胞的生物大分子
1.碳是组成细胞中各种大分子的基础
碳原子有着不同寻常的特性,就是能够形成非常大的各种各样的分子。活的生物体内含碳化合物的量仅次于水。除一氧化碳、二氧化碳和碳酸盐等少数简单化合物外,含碳化合物统称为有机化合物。
可以把所有的有机化合物都看作是由烃衍生而来的。除去碳原子和氢原子外,有机化合物还可以有别的原子,其中最常见的是氧和氮。而且参加化学反应的往往是这些原子组成的原子团,这类原子团称为功能团( functional group)。
在组成细胞的分子中最为重要的功能团有4种:羟基(—OH)、羰基(>CO),羧基( —COOH)和氨基(—NH2)。
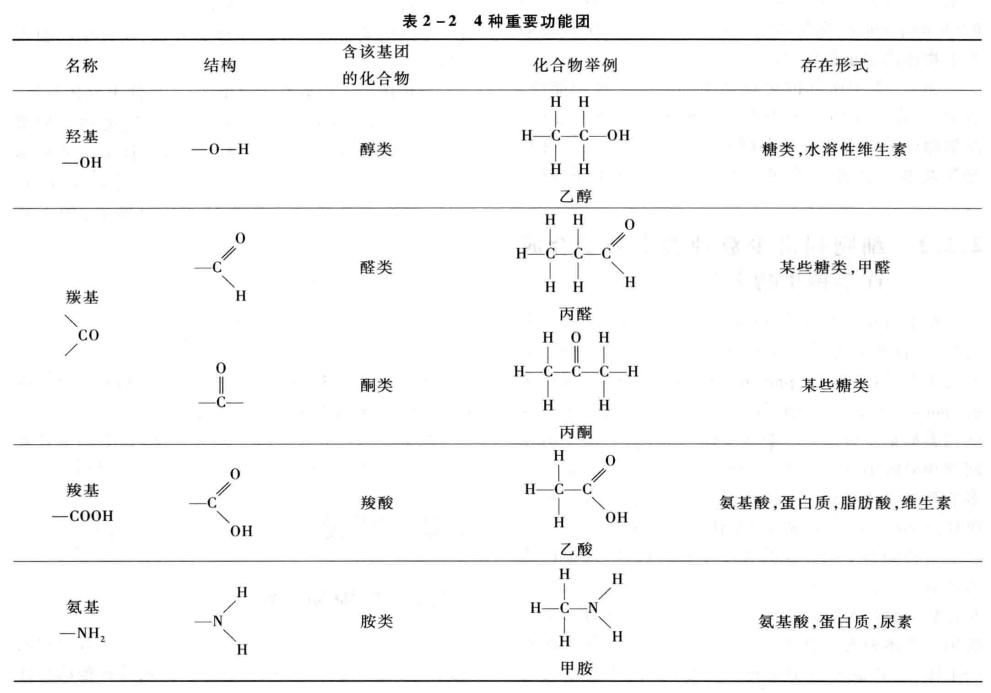
这4种功能团有一个共同特点,就是都有极性,因为其中的氧原子或氮原子都有很强的电负性,能够吸引电子。因此,所有含有这些基团的化合物都是亲水的( hydrophilic ) ,都是水溶性的。这是这些化合物能在生物体内起重要作用的必要条件。许多生物分子中含有两种或更多种功能团。
2.细胞利用少数种类小分子合成许多种生物大分子
生物大分子可分为4大类:蛋白质( protein) 、核酸( nucleic acid) 、多糖( polysaccharide)和脂质( lipid)。
细胞将单体组成多聚体的方式是:脱水合成( dehydration synthesis)。所有的单体都有氢原子(H)和羟基(—OH),每加上一个单体,便有一个H和一个—OH形成了水(HOH),产生一个新的共价键,这便是脱水合成。
生物体内不仅要合成多聚体,还要使多聚体分解。例如,生物所摄取的食物往往是大分子,要将它们吸收,必须先将它们分解为单体。将多聚体分解为单体的反应恰是脱水合成的逆反应,即水解反应( hydrolysis )。水解就是加入一个水分子使键断裂。
2.3 糖类
1.单糖和双糖
- 最常见的单糖是葡萄糖(醛糖)和果糖(酮糖),果糖比葡萄糖甜得多。
存在于生物体内的单糖还有由3.4、5和7个碳原子组成的,分别称为丙糖( triose)、丁糖( tetrose),戊糖( pentose)和庚糖( heptose)。其中戊糖尤其重要,因为它们是组成核酸的成分。
- 双糖在细胞中是由两个单糖通过脱水作用合成的。
麦芽糖=葡萄糖+葡萄糖。
麦芽糖存在于萌发中的禾谷类子粒中,例如,用于制作啤酒的大麦芽中就有麦芽糖。
蔗糖=葡萄糖+果糖。
最常见的双糖为蔗糖( sucrose),植物汁液中的糖主要是蔗糖,它是植物体内运送的主要养分。食用的蔗糖就是由甘蔗茎或甜菜根制取的。
- 甜度:果糖>蔗糖>葡萄糖
2.多糖
多糖是由数百至数千个单糖通过脱水合成而形成的多聚体。这些多聚体有许多种,最重要的有3种:淀粉( starch),糖原( glycogen)和纤维素( cellulose)。
- 淀粉:贮存在植物根和其他部分中,由葡萄糖的单体聚合而成。它是很长的分子,由于连接葡萄糖单位的键形成一定的角度,所以其长链卷曲成螺旋。淀粉的螺旋可能无分支或有分支。
- 糖原是人和其他动物体内贮藏的多糖。糖原的结构和淀粉一样,也形成螺旋,不过分支更多。人体内的糖原贮存在肝细胞和肌细胞中,在需要时,这两种细胞就会将糖原水解成葡萄糖。人的消化系统也能消化食物中的糖原颗粒。
- 植物的细胞壁中有许多种多糖,起着保护细胞和支持植物体的作用。其中最重要的多糖是纤维素。纤维素是地球上最丰富的有机化合物,它形成微原纤维( microfibril) ,存在于细胞壁中。微原纤维形成坚固的壁保护着细胞,是木材的主要成分。纤维素也和淀粉及糖原一样,是葡萄糖的多聚体,但又与淀粉和糖原不同,其中连接单体的键方向不同,它们形成不分支的链,而不发生卷曲。这些相互平行的链彼此由氢键联系,数千条合在一起,像电缆一样,形成原纤维的一部分。在木材中,一层一层的原纤维与其他类型的多聚体结合在一起,形成坚固的支持物,支持着高耸的大树。
纤维素不能被动物消化管中的酶所水解,这对于维持消化系统的健康极为有益,但它不是养分。有些动物如牛、马或白蚁,能消化纤维素,因为它们的消化管中寄生着能水解纤维素的微生物。
2.4 脂质
1.脂肪是脂质中主要的贮能分子
脂质包括多种多样的分子,其特点是主要由碳和氢两种元素以非极性的共价键组成。由于这些分子是非极性的,所以和水不能相容,因此是疏水的( hydro-phobic)。
脂质中最常见的是脂肪( fat),脂肪是由甘油和脂肪酸通过脱水合成而形成的。
脂肪分子中甘油的3个羟基通常为3个脂肪酸所酯化,所以脂肪=甘油三酯=三酰甘油。
有双键的脂肪酸称为不饱和脂肪酸(unsaturated fatty acid ) ,没有双键的则称为饱和脂肪酸( saturated fatty acid)。双键的存在使得碳链弯曲,占的空间较大,所以含有双键的脂肪在常温下是液态,因为其分子不能排列得太紧密。
脂肪中有多个碳氢链,所以是含能量较多的分子。1 g 脂肪中所贮存的能量约为1 g 淀粉的两倍。
动物的脂肪中不饱和脂肪酸很少,植物油中则较多。膳食中饱和的脂肪太多会引起动脉粥样硬化,因为脂肪和胆固醇均会在血管内壁上沉积而形成斑块,这样就会妨碍血流,产生心血管疾病。
2.磷脂、蜡和类固醇都是脂质
脂肪只是脂质中的一类,另外还有3类重要的脂质,它们是磷脂( phospholipid)、类固醇(steroid)和蜡(wax )。
- 磷脂是细胞膜的重要组分,其结构与脂肪类似,不过分子中只有两个脂肪酸,另外一个酸是磷酸。磷脂是非常重要的生物分子,将在有关生物膜的部分中讨论。
- 蜡也是酯,是由一些长链的醇与长链脂肪酸形成的酯。它们的疏水性比脂肪的更强,所以可保护生物体的表面。例如,苹果、梨的表皮上都有一层蜡,可以保护这些果实,避免干燥。动物的表面也有蜡,例如,昆虫就有蜡保护着其躯体,避免干燥。
- 类固醇是一类不同的脂质。它们的特点是碳链折成4个环,3个六元环和1个五元环。胆固醇是细胞膜的重要成分,也是动物体内合成其他类固醇的原料。动物的雌、雄性激素都是类固醇。
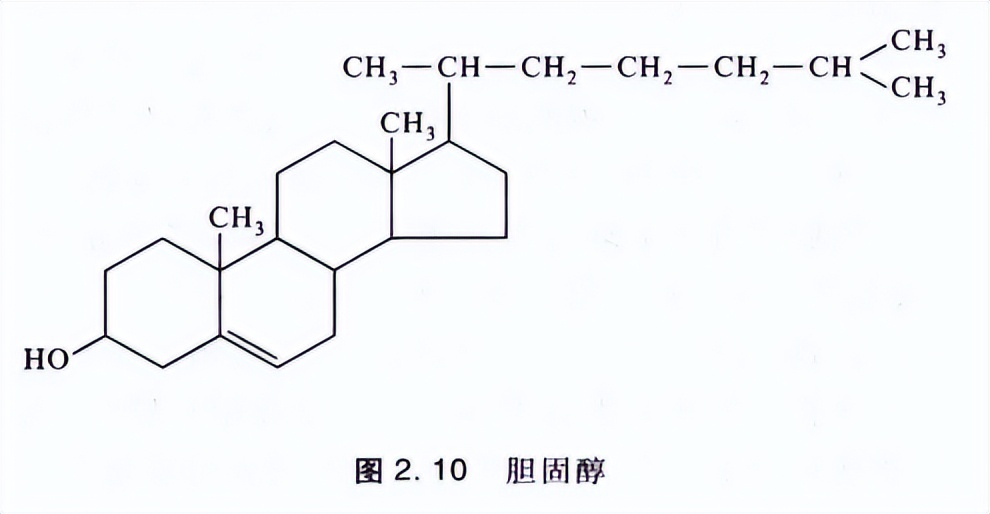
- 有一些类固醇药物称为促蛋白合成类固醇( anabolic steroid),是人工合成的类似雄性激素的药物。它能促进肌肉发达,增强体力,常为一些运动员所服用。这些药物有许多严重的副作用,对运动员身心两方面都有严重影响,为许多体育组织所禁用。
2.5 蛋白质
1.蛋白质为生命活动所必需
蛋白质是由氨基酸组成的多聚体,是重要的生物分子.细胞、组织和机体的结构都与蛋白质有关,生物体内的每一项活动都有蛋白质参与。
根据蛋白质在机体内的功能,可将其分为7大类:
(1 )结构蛋白
例如,哺乳动物的毛、发、肌腱和韧带,蚕和蜘蛛的丝等都是由专门的蛋白质组成的。
(2)收缩蛋白
收缩蛋白与结构蛋白共同起作用,例如,肌肉的运动就需要收缩蛋白与肌腱共同起作用。
(3)贮藏蛋白
例如,卵清蛋白
(4)防御蛋白
例如,抗体
(5)转运蛋白
负责物质转运的蛋白质,例如,血红蛋白
(6)信号蛋白
信号蛋白是将信号从一个细胞传送到另一个细胞的蛋白质。例如,某些激素
(7)酶
酶大概是生物体内最重要的蛋白质。它们是生物催化剂,催化体内的每一个化学反应。酶促进化学反应的进行,但本身并不在反应中发生变化。实际上细胞中所有的化学反应都是由酶促进和调节的。
综上所述,无论是生物体的结构,还是每一种生命活动,都离不开蛋白质。
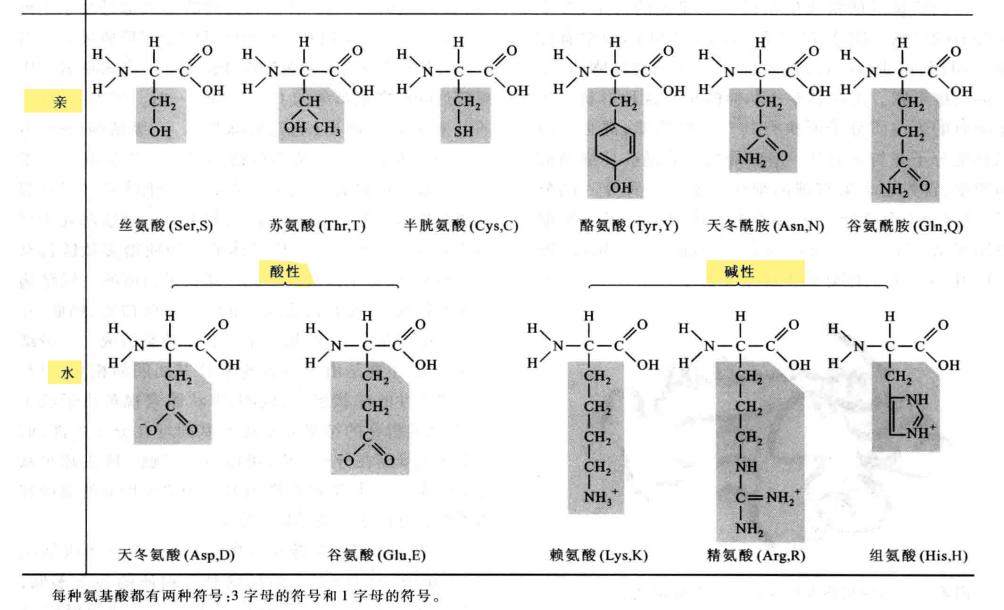
2.蛋白质仅由20种氨基酸组成
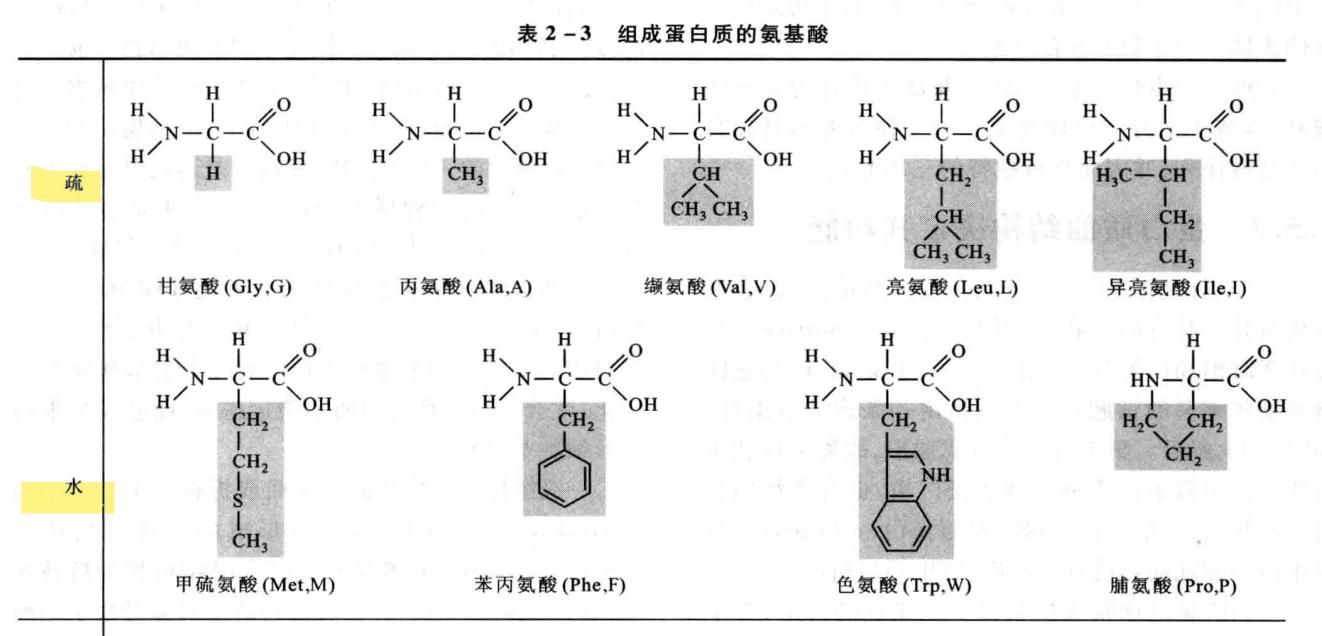
3.蛋白质的结构决定其功能
蛋白质的变性( denaturation)就是指多肽链松开,失去了其专一的三维形状,因而也就失去了其功能。
- 多肽链中氨基酸的排列顺序就是 一级结构( primary structure)。
- 一级结构中部分肽链的卷曲或折叠产生二级结构( secondary structure)。卷曲所形成的二级结构称为α螺旋(α - helix) ,折叠所形成的二级结构称为折叠片( pleated sheet)。这两种二级结构的形成都是由于距离一定的一N-H基团和—C=О基团之间形成氢键。
- 三级结构( tertiarystructure)表示的是一条多肽链的总的三维形状。三维形状一般都可以大致说是球状的或纤维状的。三级结构的形成,主要是由于多肽链中R基团间的相互作用,某些极性的R基团之间形成的氢键和离子键也有助于三级结构的维持。
- 由两条或多条肽链组成的蛋白质具有四级结构( quaternary structure)。组成这种蛋白质的各个多肽,称为亚基( subunit),四级结构是由各亚基之间形成的键所维持的。
2.6 核酸
1.核酸由核苷酸组成
核酸( nucleic acid)也是多聚体。
有两类核酸:脱氧核糖核酸(deoxyribonucleic acid, DNA)和核糖核酸(ribonucleic acid, RNA)。
DNA 和 RNA都是多聚体,组成它们的单体是核苷酸( nucleotide) 。核苷酸由3个部分组成。
第一部分是戊糖, DNA中戊糖是脱氧核糖( deoxyribose ); RNA 中的戊糖是核糖( ribose)。
第二部分是磷酸基团,连在戊糖的一端。
第三部分是含氮碱基,连在戊糖的另一端是含氮碱基( nitrogenous base )。DNA 中的含氮碱基有4种,即腺嘌呤( adenine , A ) ,胸腺嘧啶( thymine, T),胞嘧啶( cytosine , C)和鸟嘌呤( guanine,G)。RNA中的也是A,C和G,但T被尿嘧啶( uracil ,U)所替代。
2.DNA双螺旋
B型—DNA双螺旋模型的特点如下 :
(1)多核苷酸链的两个螺旋围绕着一个共同的轴旋转,为右手螺旋。
(2)多核苷酸链是通过磷酸和戊糖的3’,5'碳相连而成的。因此,长链的两端是不同的,一端是与3'碳相连的羟基(3'C—OH),另一端是与5'碳相连的磷酸基团(5'C——PO4)。双螺旋的多核苷酸长链一条是从3'到5',另一条方向相反,是从5'到3'。
(3)嘌呤碱和嘧啶碱在双螺旋内部,而磷酸根和核糖则在外部。碱基的平面与轴相垂直,糖的平面又与碱基的平面几乎相垂直。
(4)螺旋的直径约为2 nm,相邻碱基之间相距0.34 nm并沿轴旋转 36°。因此,整个旋转每隔10个碱基之后,即相距3.4 nm之后又转回原位置。
(5)两条链是由碱基对之间的氢键连在一起的,腺嘌呤(A)总是与胸腺嘧啶(T)配对,鸟嘌呤(G)总是与胞嘧啶(C)配对。A -T之间有2个氢键,G-C之间有3个氢键。
(6)多核苷酸中碱基的序列不受任何限制。碱基对的准确序列携带着遗传信息。
碱基配对的专一性是DNA 双螺旋中最重要的问题。沃森和克里克之所以断定A必须与T配对,G必须与C配对,有两个根据:①氢键的形成;②空间的排列。双螺旋中两个碱基之间的距离是10.8 nm,如果两个都是嘌呤碱,就放不下,而如果两个都是嘧啶碱,又有多余空间,只有一个嘌呤碱和一个嘧啶碱才正好合适。何况A-T之间又正好形成2个氢链,而G-C之间又正好形成3个氢链。
1950年,Chargaff发现不同物种的DNA中碱基的组成,发现A 与T之比以及G与C之比总是接近于1.0,沃森和克里克的模型正好说明了Chargaff 的发现。