文|墨归客
编辑|墨归客
前言
PLC-δ1 的结构由四个结构域组成:PH 结构域、EF-hand 结构域、催化结构域和 C2 结构域,另一方面,bPLC 折叠成类似于 PLC-δ1 催化结构域的单结构域结构,bPLC 和 PLC-δ1 的催化结构域都属于称为 (βα)8 桶或 TIM 桶的大型结构超家族。
然而,这些 PI-PLC 中的 TIM 桶折叠是扭曲的,而不是处于理想的构象,这种变形被认为是为了适应酶对接磷脂膜的空间要求,并允许磷脂头部基团进入活性位点或在催化后释放产物。
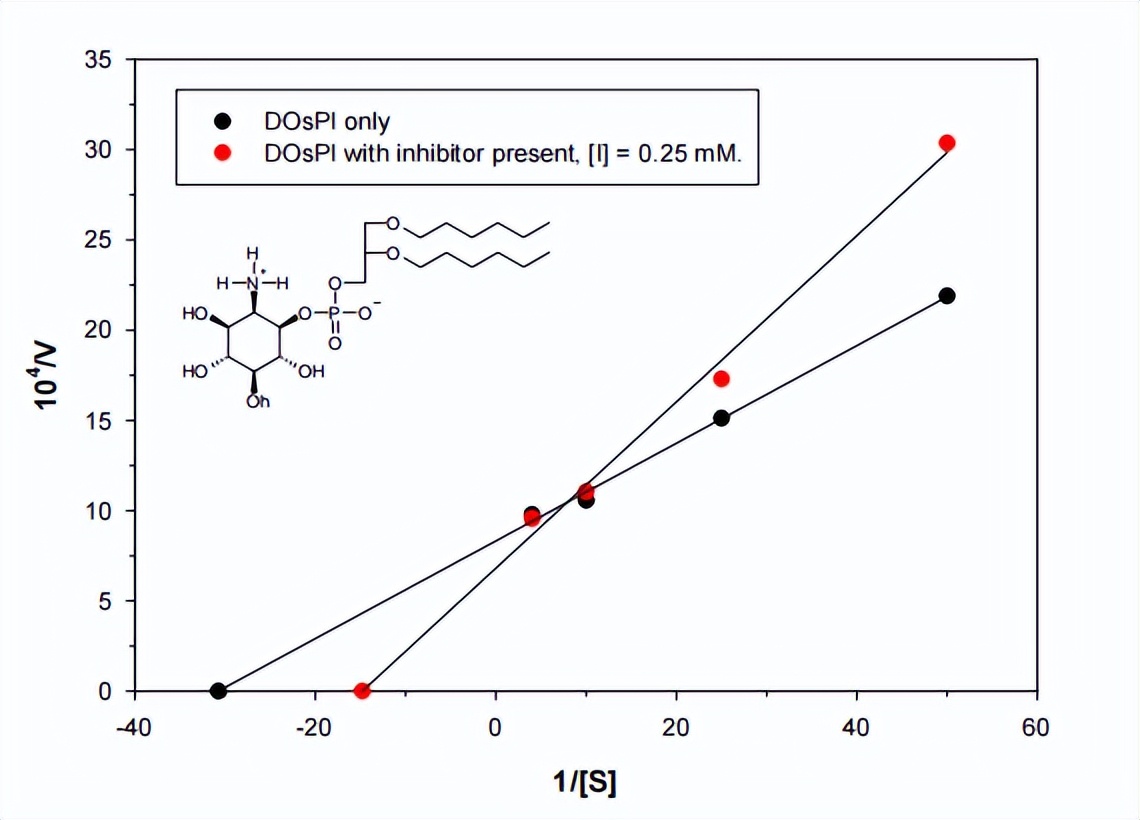
当 bPLC 的结构和 PLC-δ1 的催化结构域叠加时,发现它们的 N 端半部分(称为 X 区域)显示出极好的匹配,这些 X 区域对应于特定残基(bPLC 中的 1 至 163 和 PLC-δ1 中的 299 至 440),尽管这些区域之间的序列同一性低至 11%,但 104 个等效 Cα 位置的均方根 (rms) 偏差接近 1.8 Å,对酶活性很重要的催化残基也位于该区域内。
值得注意的是,催化组氨酸残基(PLC-δ1 中的 His311/His356 和 bPLC 中的 His32/His82)和阳性部分(PLC-δ1 中的 Ca2+ 和 bPLC 中的精氨酸侧链)之间的空间排列存在惊人的相似性。
与保守的 N 端一半相反,TIM 桶的 C 端一半(称为 Y 区)没有表现出明显的保守性,在 PLC-δ1 中,Y 区域主要通过表面螺旋与邻近的 C2 结构域进行重要接触,这个掩埋界面占催化域总表面积的 9%。
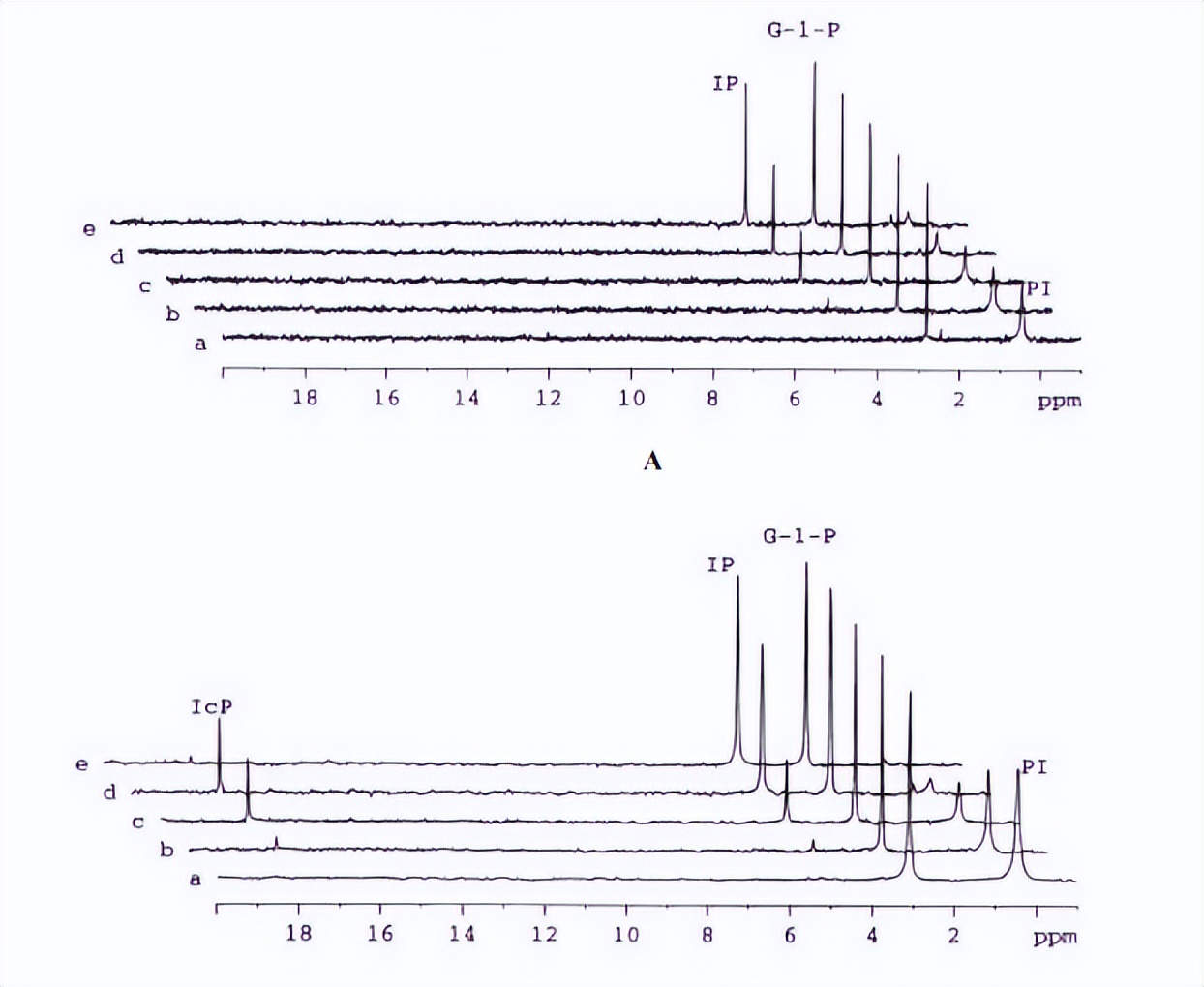
特异性磷脂酶在磷脂酰肌醇中的研究
对磷脂酰肌醇特异性磷脂酶 C (PI-PLC) 的各种研究积累的信息导致提出了涉及一般碱/酸催化的顺序催化机制,该反应分两步进行:生成环状磷酸二酯中间体的磷酸转移步骤和生成无环肌醇磷酸产物的磷酸水解酶步骤,由于第二步的速度较慢,细菌酶(例如 btPLC)主要产生环状中间体,相比之下,真核 PI-PLC 主要生产无环肌醇磷酸盐作为主要产品。
细菌和真核生物 PI-PLC 都利用通用酸和通用碱机制进行催化,然而,它们使用不同的残基来完成一般酸和碱的作用,在 btPLC 中,由 Asp274 和 His32 组成的催化二元组作为通用碱基,His32 去质子化肌醇环的 2-OH 基团,然后攻击磷酸中心。
在研究过程中涉及 Arg69、Asp33 和 His82 的催化三联体参与降低 2-OH 基团的 pKa,通过与磷酸基团的亲 S 氧相互作用稳定带负电荷的过渡态,并质子化离去的甘油二酯( DAG)组。

在真核 PI-PLC(例如 PLC-δ1)中,两个保守的组氨酸残基 His311 和 His356 起着重要作用,建议 His356 的功能类似于 btPLC 的 His82,在第一步中质子化离开的 DAG 基团, 然而,His311 的具体功能尚不完全清楚,His311 突变为亮氨酸显着降低酶活性,表明其参与一般碱催化(类似于 His32)或稳定过渡态。
PLC-δ1 利用 Ca2+ 作为 btPLC 中 Arg69 的对应物,Ca2+ 与各种氨基酸配位,包括 Asn312、Asp343、Glu341、Glu390,以及水分子和肌醇磷酸 3 (InsP3) 的 2-OH 基团,Glu341 被认为是使肌醇环的 2-OH 基团质子化的通用碱基,然而,关于羧基是否可以在与金属离子配位时接受质子的争论仍然存在。
PI-PLC 的顺序催化机制涉及一般酸和碱催化,特定残基发挥这些作用,关键残基在催化机制中的精确功能仍然是一个活跃的研究领域,从这些研究中积累的知识揭示了金属非依赖性细菌 PI-PLC 和 Ca2+ 依赖性真核 PI-PLC 之间的显着催化差异。
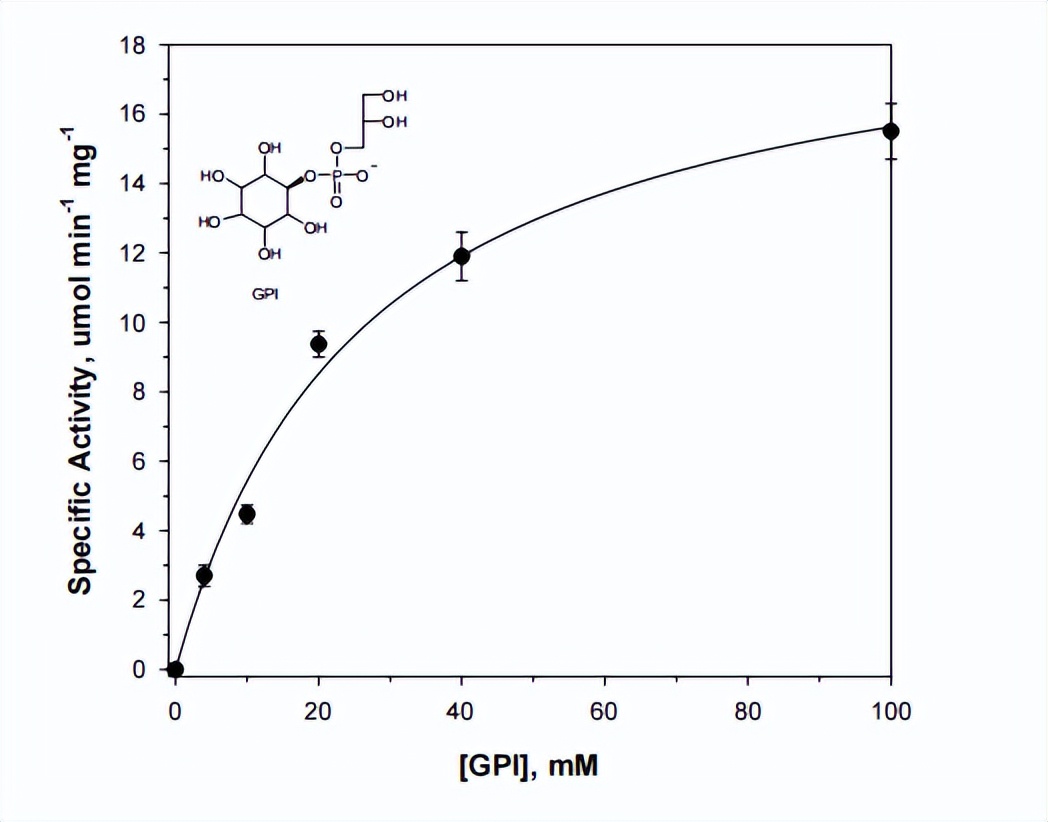
一个主要区别是利用精氨酸残基的细菌 PI-PLC 已经进化为仅催化两步反应的第一步,另一方面,依赖于 Ca2+ 辅助因子的真核 PI-PLC 已经进化为催化连续的两步反应。
哺乳动物 PI-PLC在环状磷酸中催化的反应
在哺乳动物 PI-PLC 催化的反应中,观察到在生成 IP3 的同时会形成少量环状磷酸中间体,特别是在磷酸肌醇高周转率的细胞中, 最初,这种环状中间体受到的关注较少,因为它被认为是第二信使生成的副产品,而且它的细胞水平通常太低而无法激活 IP3 受体。
然而,在某些细胞中,例如人乳腺癌细胞系,环磷酸盐是磷酸肌醇裂解的主要产物,几种潜在的含肌醇的第二信使,包括肌醇磷酸聚糖和前列腺素-肌醇结合物,都含有 1,2-环磷酸残基。

哺乳动物和细菌 PI-PLC 都被提议采用一般酸和一般碱机制来催化磷脂酰肌醇 (PI) 的水解,然而,它们的催化位点表现出显着差异,大鼠 PI-PLC-δ1 中的钙离子与蜡样芽孢杆菌 PI-PLC 中的精氨酸侧链之间的空间排列存在显着相似性, 蜡样芽孢杆菌 PI-PLC (bPI-PLC) 与苏云金芽孢杆菌 PI-PLC (btPLC) 的区别仅在于 8 个非保守氨基酸。
结构数据以及立体化学和诱变研究的结果都表明,这两个位置相似的带正电实体发挥着类似的催化作用,它们通过与磷酸二酯部分的 pro-S 氧相互作用稳定磷酰基转移反应的过渡态,并促进肌醇环 2-OH 基团的去质子化,然而,目前尚不清楚 Ca2+ 与 Arg 的使用如何导致哺乳动物和细菌酶之间底物特异性和产物特征(环状与非环状产物的比率)的差异。
其他研究小组已努力将 Ca2+ 非依赖性 PI-PLC 设计成 Ca2+ 依赖性酶,反之亦然,但这些尝试迄今尚未成功,例如,bPI-PLC (R69D/K115E) 的双突变体在 Ca2+ 存在或不存在的情况下,均未显示可检测的催化活性,尽管已正确折叠。

有人提出,哺乳动物 PI-PLC 中的 Ca2+ 结合位点可能具有严格的空间和电子要求,相反,消除哺乳动物 PI-PLC 对 Ca2+ 依赖性的努力也失败了,因为即使在突变带负电荷的钙结合残基(E390K、E343R 或 E390K/E343R)后,钙亲和力也没有降低。
在之前的研究中,有人提出钙在 PI-PLC 中的作用不仅限于提供正电荷,还涉及通过与过渡态的额外相互作用进行空间加速催化。
磷脂酰肌醇在硫代磷酸酯的活性
btPLC 通过 R69D 突变成功转化为金属依赖性酶,动力学数据表明 Ca2+ 的存在显着激活了该突变体的催化活性,NMR 光谱结构数据表明,Ca2+ 的存在对于将突变体催化位点的微环境恢复为野生型 (WT) 酶的微环境至关重要,磷脂酰肌醇的硫代磷酸酯类似物的 RP- 和 SP- 异构体用于研究 Ca2+ 在催化中的作用,立体化学研究结果表明。
在 Ca2+ 存在的情况下,R69D 突变体对 DPPsI 的 RP 异构体表现出高特异性,与 WT btPLC 相比,RP/SP 立体选择性比高 5 倍。

在构建显示 Ca2+ 激活的突变体时,该设计基于哺乳动物 PI-PLC-δ1 (mPI-PLC) 中钙离子空间排列与芽孢杆菌 PI-PLC (bPI) 中精氨酸侧链的相似性-PLC),晶体学数据还显示,bPI-PLC 的 Arg69 与三个酸性残基(Asp33、Asp67 和 Glu117)形成氢键。
这三个酸性残基占据的位置与协调 mPI-PLC 中的钙离子的 Asn312、Glu341、Asp343 和 Glu390 的位置相似. 通过消除 Arg69 的正电荷同时保留 Asp33、Asp67 和 Glu117 的负电荷,提出了金属结合位点的初步蓝图。
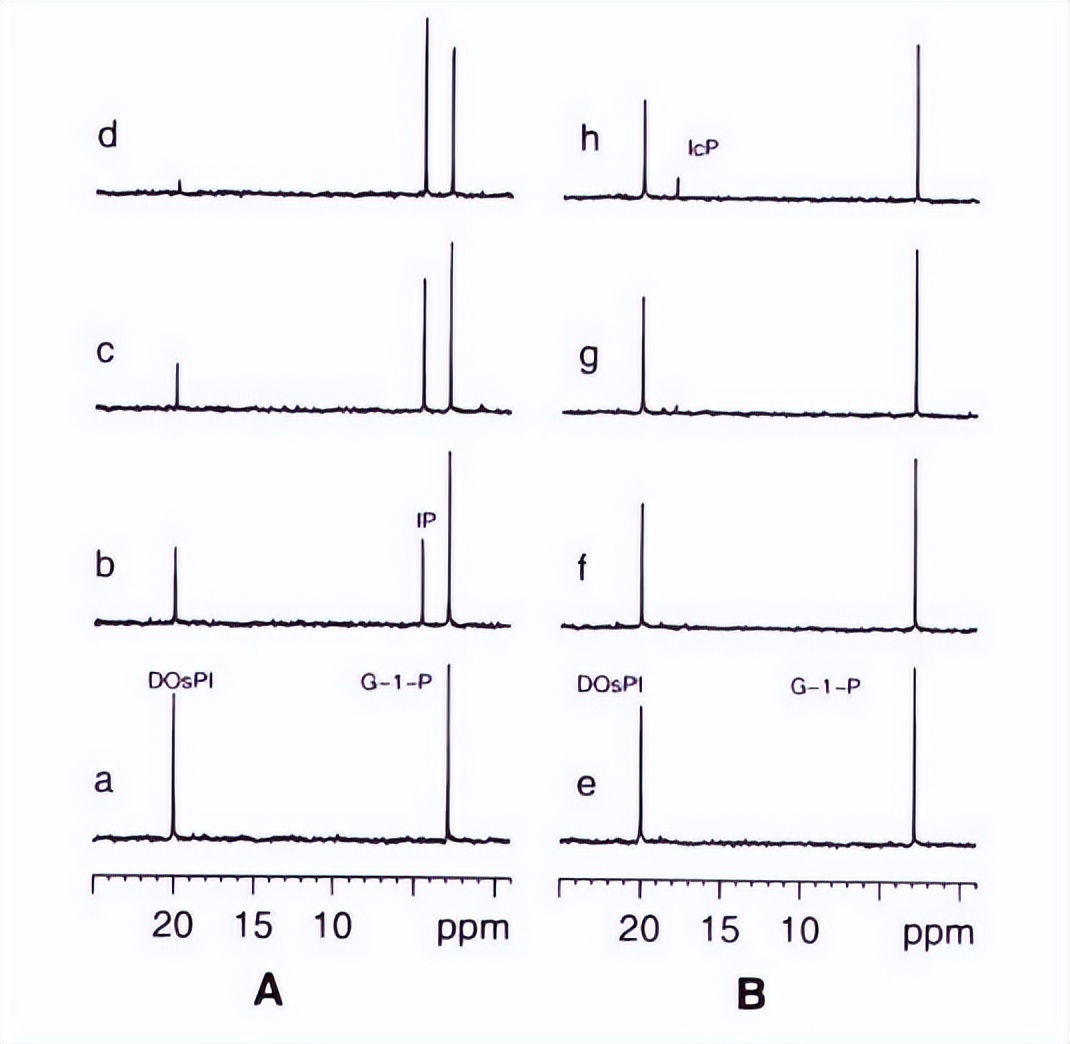
构建了几个突变体,包括 R69D、R69E、R69G、R69A、R69C 和 R69N,并通过测量 IcP 的形成在稳态条件下评估它们被 Ca2+ 激活,野生型 (WT) 酶和各种突变体在将 PI 转化为 IcP 时的活性,无论是否存在浓度为 0.1 mM 和 1 mM 的 Ca2+ 离子。
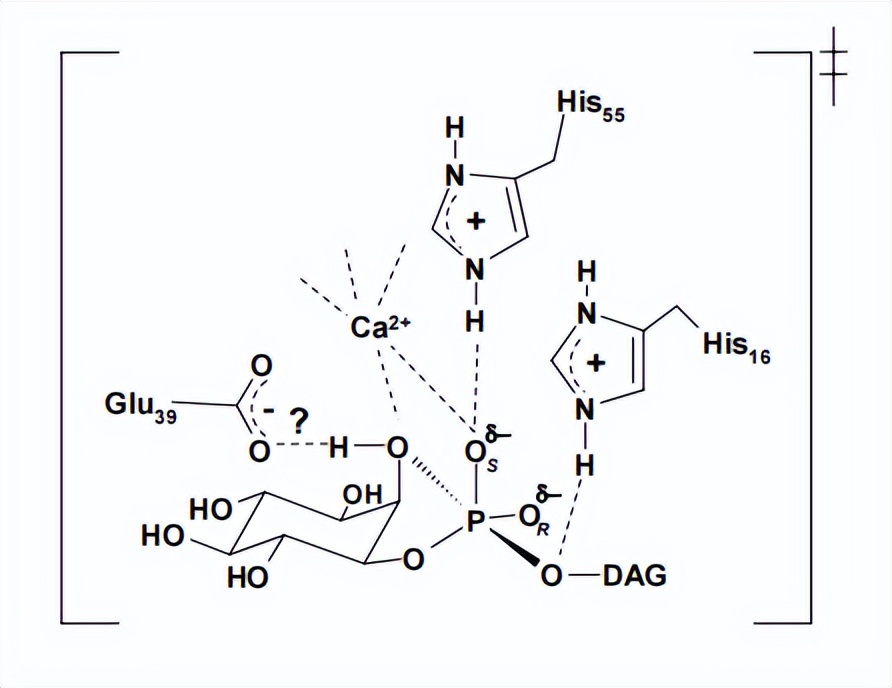
R69E 突变体是无活性的 (0.044 U/mg),并且未显示被任何测试的二价金属离子(包括 Ca2+)激活,相比之下,R69D 突变体显示出相对活性 (0.29 U/mg),并且在添加 Ca2+ 后可以进一步激活大约 30 倍,还构建了 R69G、R69A、R69C 和 R69N 突变体,但它们均未显示被 Ca2+ 激活。
在确认 R69D 突变体的 Ca2+ 活化特性后,进一步研究了该突变体的金属离子特异性,检测了碱土金属离子对 R69D 的激活,突变体表现出不同程度的 Mg2+、Ca2+ 和 Sr2+ 激活,这些金属离子对 R69D 的增强活性遵循相对于金属离子浓度的饱和动力学,然而,Ba2+ 在浓度高达 1 mM 时不会激活或抑制 R69D。
不同碱土金属离子的活化程度,R69D 与 Mg2+、Ca2+ 和 Sr2+ 的复合物在饱和底物浓度 (2 mM) 下的最大速度分别为 10.2 ± 0.2、12.0 ± 0.3 和 2.7 ± 0.3 U/mg,对应于 35 倍、41 倍, 和 9 倍激活。

相比之下,Ca2+ 对 mPI-PLC 的激活发生在较低浓度(钙的表观解离常数:Kd_app = 1.3 µM),而 Mg2+ 即使在浓度高达 5 mM 时也不会激活 mPI-PLC,进一步分析揭示了活化程度与金属离子的 Kd_app 之间存在粗略的相关性: Ca2+ 和 Mg2+ 表现出良好的结合和活化,Sr2+ 表现出中间性质,而 Ba2+ 与突变体结合但未能激活它。
Kd_app(和 Ki_app)值与离子半径大致相关:Mg2+ (0.66 Å) < Ca2+ (0.99 Å) < Sr2+ (1.12 Å) < Ba2+ (1.35 Å),在这些离子中,Ca2+ 最适合结合位点,在没有结构信息的情况下,Mg2+ 和 Ca2+ 的不同催化作用的确切原因仍不清楚。
然而,怀疑配体供体原子可能不容易形成明确定义的八面体几何形状,有利于 Mg2+ 在位置 69 处精氨酸到天冬氨酸的突变, 相反,这种配位球可能有利于 Ca2+,它形成更松散的复合物,具有更高的和可变的配位数,缺乏方向性和表现出可变的键长。

与碱土金属离子相反,过渡金属离子 Co2+、Mn2+ 和 Cd2+ 在与 R69D 突变体相互作用时表现出不同的活性与金属离子浓度曲线,这些过渡金属离子在低浓度下增加了突变体的活性,在 Cd2+、Mn2+ 和 Co2+ 的浓度分别为 25 µM、50 µM 和 100 µM 时观察到最大活化,Cd2+ 的最大激活小于 7 倍,Mn2+ 约为 14 倍,Co2+ 约为 18 倍。
然而,金属离子浓度的进一步增加导致酶活性的抑制, 尽管即使在 Mn2+ 和 Co2+ 的浓度为 1 mM 时,该活性仍高于背景水平,Cd2+ 表现出更强的抑制作用,而 Zn2+ 在浓度低于 1 mM 时完全消除酶活性,还检查了碱性(一价)金属离子对 R69D 活性的影响。
钠离子在二价金属离子中的特异性
Na+、K+ 和 Cs+ 不激活突变体,而 Li+ 在饱和浓度下导致 5 倍激活,这些单价金属离子均不抑制 Ca2+ 诱导的 R69D 活性,因此,通过 EDTA 和 HEPES 缓冲液引入的测定系统中存在的钠离子与前面描述的二价金属离子引起的激活和抑制作用无关,由于 Li+ 的激活是温和的,不太可能是由于与 R69D 活性位点的特异性结合,因此没有进一步调查这种激活的确切原因。

Li+、Na+、K+、Cs+、Mg2+、Ca2+、Sr2+、Ba2+、Mn2+均表现出轻微的活化作用,活化水平不超过30%,另一方面,Co2+、Cd2+、Ni2+ 和 Zn2+ 会显着抑制酶活性,正如 15N-1H HSQC 实验(在本文后面的部分中描述)所表明的, 某些金属离子的轻微活化作用背后的机制不太可能归因于与 WT 酶的特异性结合,先前在其他研究中观察到的某些二价离子的抑制作用可归因于这些离子在活性位点或附近的非特异性结合。
在该研究中,利用异核核磁共振波谱研究了酶中 R69D 突变引起的潜在变化,分析揭示了 15N-1H HSQC 光谱的主链酰胺区域和精氨酸侧链 (εNH) 区域中信号位置和强度的变化,如果没有完整的 NMR 分配,则无法完全解释主链酰胺区域的变化,但在精氨酸区域观察到的变化提供了宝贵的见解,以下是精氨酸区域的变化具有信息性的原因:
分子量为 35 kDa 的野生型 (WT) 酶包含总共 9 个精氨酸残基,每个残基在 15N-1H HSQC 光谱的精氨酸区域中贡献不同的信号。
基于 WT 酶和相应丙氨酸突变体的光谱(未发表的结果)之间的比较,分配了三个精氨酸信号(Arg69、Arg71 和 Arg163)。
Arg71 和 Arg163 位于靠近活性位点的位置,而其余的精氨酸残基则位于距离活性位点较远的位置,R69D 突变导致 NMR 光谱精氨酸区域发生可检测到的变化,表明对活性位点周围的结构环境有潜在影响。

总结
这项研究的主要结果表明,R69D突变体是一种对钙离子(Ca2+)激活敏感的磷脂酶C(PI-PLC)变体,该突变体通过改变活性位点附近的结构环境,展现了与野生型酶不同的金属离子激活特性,另外,碱土金属离子对其也具有激活效应,而过渡金属离子则呈浓度依赖性的激活和抑制效应,这些发现为进一步研究磷脂酶C的催化机制和金属离子调控提供了重要的结构证据。
参考文献
【1】《SG 环状和非环状肌醇磷酸盐由磷脂酶》
【2】《抗生素链霉菌的两种不同的磷脂酰肌醇特异性磷脂酶》
【3】《蜡样芽孢杆菌的磷脂酰肌醇特异性磷脂酶》
【4】《哺乳动物磷酸肌醇特异性磷脂酶 C delta 的晶体结构》
【5】《蜡样芽孢杆菌和苏云金芽孢杆菌》