微流控芯片是20世纪90年代在分析化学领域发展起来的,它以微管道网络为结构特征,以生命科学为主要应用对象,并开始在分析化学、生命科学及生物医学器件等领域发挥愈来愈重要的作用。
在蛋白质分析技术中,蛋白质芯片是一种高通量、微型化和自动化的新型分析手段。目前蛋白质芯片主要分两种:一种类似于 DNA 芯片,即在固相支持物表面高密度排列的探针蛋白点阵,可特异地捕获样品中的靶蛋白,然后通过检测器对靶蛋白进行定性或定量分析;另一种就是微流控电泳芯片,通过在玻璃片或硅片上设置各种微泵、微阀、微电泳以及微流路,可将生化实验室的分析功能浓缩固化在蛋白质芯片上,然后在电场作用下,样品中的蛋白质通过芯片上的孔道分离开来,经喷雾直接进入质谱仪中进行检测,以确定样品中蛋白质的分子量及种类。

国外团队开发的由玻璃片为基底制作的微流体电泳芯片,采用光刻技术对所设计的流路进行刻蚀,在微通道里加入待测样品和检测试剂,电渗流泵首先用于样品的输送以及与反应试剂的混合,反应后的溶液进入芯片上的电泳分离通道。为了满足高通量分析的需要,在芯片上并行制作许多电泳通道结构。尽管微流体式芯片仍处在研制阶段,但其潜在优势十分明显:(1) 由于微流体芯片中蛋白质吸附表面增大,分析敏感度高;(2) 微通道可提高电泳分离的速度,减少检测所需时间;(3) 微流体芯片耗样少、成本低,可重复多次使用。
另外有团队利用一种三维微流控体系将复杂的生物样品布设于一基板表面,形成特定的图案并进行检测。该装置由具有特定通道图案的上层的PDMS 板和底层的PDMS 膜经封合而成。他们将具有螺旋形通道体系的三维微流控装置固定在一个聚苯乙烯底板表面,在两个通道内分别加入用FITC 标记的BSA及纤维素原蛋白 (磷酸缓冲液中),使这两种蛋白吸附在聚苯乙烯底板表面约45min,由于BSA的浓度比纤维素原蛋白大约10倍,所以其荧光图像较强。
蛋白质芯片将为生物化学和分子生物学提供强有力的分析工具。相对于DNA芯片,蛋白质芯片的研究进展显得相对滞后,主要原因是:(1) 芯片材料表面的修饰方法尚不成熟 ; (2) 样品制备和标记操作过于繁琐;(3) 信号检测灵敏度低,如低拷贝蛋白质的检测和难溶蛋白的检测精度更加难以保证,因此需要研制和开发高度集成化样品制备及检测仪器。这些问题不仅为蛋白质芯片技术增加了难度,同时也是蛋白质芯片能否从实验室推向临床应用的关键所在。
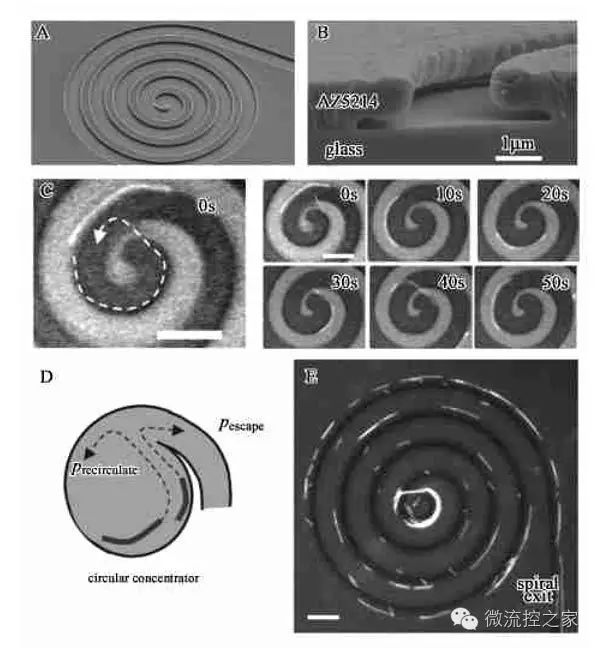
最近,又有团队制作出一种具有螺旋形通道网络的微流控芯片,可使微管沿着覆盖有驱动蛋白的螺旋轨道运动并对其进行实时监测和浓缩,称之为动力蛋白“绕行”。
在细胞中,动力蛋白在物质运输及细胞组分构建等方面起着十分关键的作用。活性生物运输分子如驱动蛋白不仅被用在细胞体系中运输纳米尺度的物质颗粒,而且还可用于组装及定位细胞结构 ,它利用ATP水解所释放的能量沿着微管向其正极运输小泡。因此掌握并控制这些动力蛋白的运动情况对于构建生物纳米材料是十分重要的。在微通道上覆盖一层驱动蛋白,并在蛋白溶液中加入ATP,因此用荧光标记的微管可在驱动蛋白的作用下,利用 ATP 水解所释放出的能量沿着轨道滑行。由于控制动力蛋白的运动十分关键,因此必须设计出最为适合的轨道。他们首先设计了3种不同形状的通道网络即十字交叉形、三角交叉形以及螺旋形。结果表明,微管在前两种轨道中运动时会陷于拐角处而无法持续前行;而在螺旋形轨道中,微管能够一直沿着通道运动并最终浓缩聚集于螺旋中央。
微流控装置的用途广泛,但目前流行的微流控装置最大的不足之处是它们需要大量辅助的外部设备,体积庞大且成本很高 ,这就极大地限制了它的应用。克服这些困难的一个途径就是将所需试剂装配并存储于微流控体系内部 ,真正实现“lab-on-a- chip”。
最近研制出的一种全新微流控装置,可以控制某种功能蛋白从脱水的无活性状态恢复至其功能状态。具体做法是在微通道壁旁做了一个储藏室,在体系封合之前,往该室中装上浓缩的海藻糖及葡聚糖溶液,溶液中含有需要的化学试剂,如β半乳糖苷酶 (βgalactosidase)。当这种含有βgal的糖溶液凝固以后,形成一种储藏母体,然后将体系封合。这样,β半乳糖苷酶就处于脱水的无活性状态。RBG( resorufinβgalactoside) 作为β半乳糖苷酶的底物,本身不发荧光,但是当它被β半乳糖苷酶分解后,所得产物为半乳糖荧光染料试卤灵 (resorufin)。

该分解反应是一个一步完成的简单酶促反应,其动力学曲线符合米氏方程,因此可以通过检测荧光强度来检测酶活力。当8.2μM的RBG溶液流过微通道并进入穴中时,可使葡聚糖母体溶解并释放出β半乳糖苷酶。该酶在溶液中从脱水的无活性状态转化为活性状态,并催化RBG分解,生成荧光产物试卤灵,通过检测荧光强度可以测得β半乳糖苷酶的活力。
结果表明,在整个实验过程中,储存室中的酶仍然保持着30%~80%的初始活力。酶活力之所以有如此大的浮动,可能源于所加酶溶液的体积不一致(150±75nL)。同时还比较了在其他条件相同的情况下,圆柱形与方形储存室对酶活力的影响,结果表明,用圆柱形储存室时酶活力较高,并且释放平稳,效果较佳。