一,分类方法的应用
1.分类可以帮助我们更好地认识物质的性质,找出各类物质之间的关系

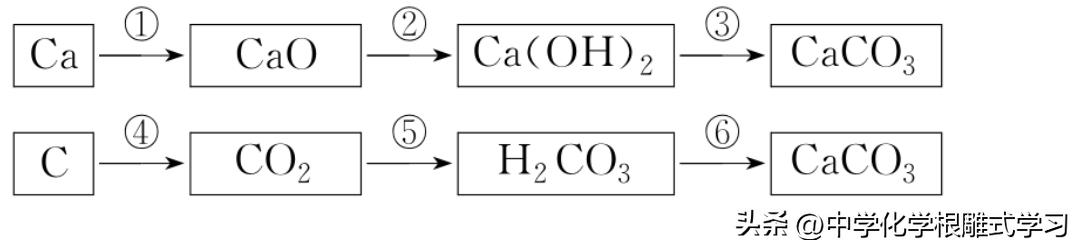
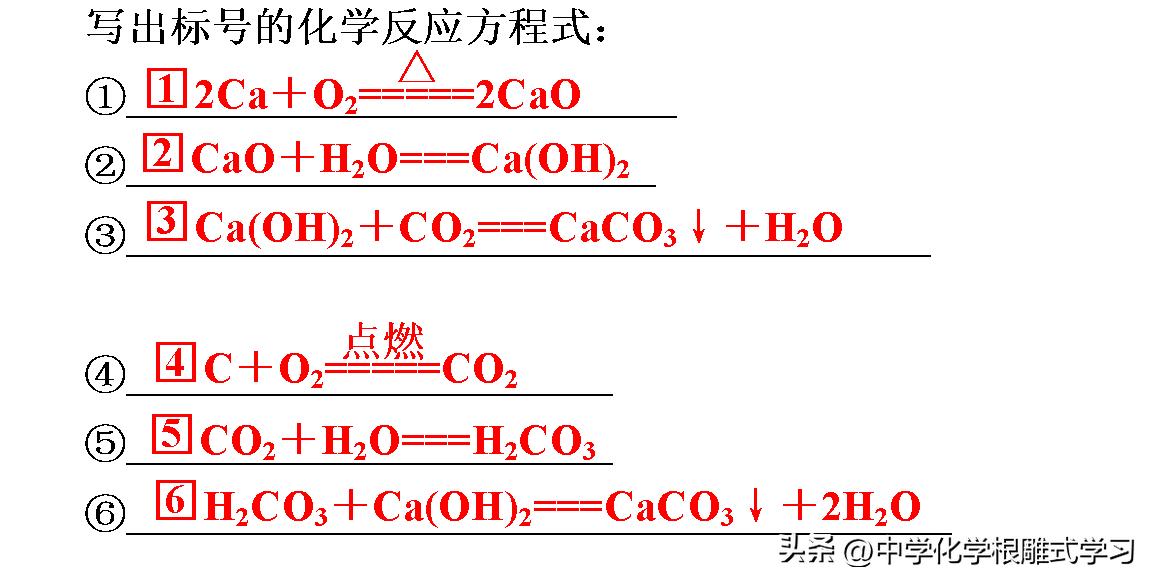
二,各类物质的化学通性
1,金属单质(以铁为例)

(1)金属单质和氧气反应生成金属氧化物,属于化合反应。
(2)金属和酸反应生成盐和氢气,通常为置换反应。
(3)金属和盐溶液反应生成新盐和新金属,通常为置换反应。
2,氧化物(以二氧化碳、氧化钙为例)
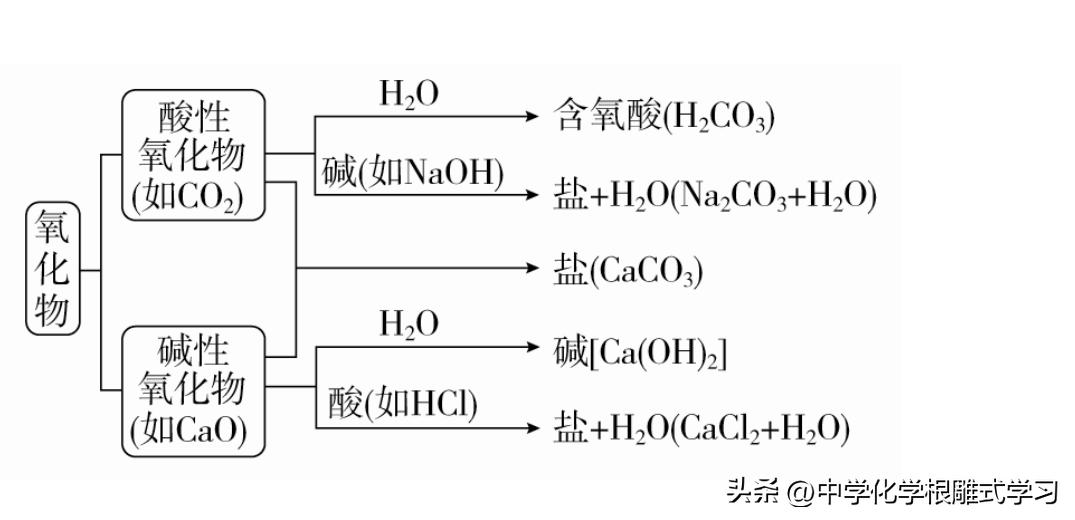
(1)碱性氧化物和对应碱之间可以相互转化,一些碱性氧化物和水反应生成碱,一些难溶性碱受热分解生成碱性氧化物和水,碱性氧化物可以和酸反应生成盐和水。
(2)酸性氧化物和对应酸之间可以相互转化,一些酸性氧化物和水反应生成酸,一些不稳定性酸受热分解生成酸性氧化物和水,酸性氧化物可以和碱反应生成盐和水。
(3)酸性氧化物和碱性氧化物反应生成含氧酸盐。
3,酸(以稀盐酸为例)
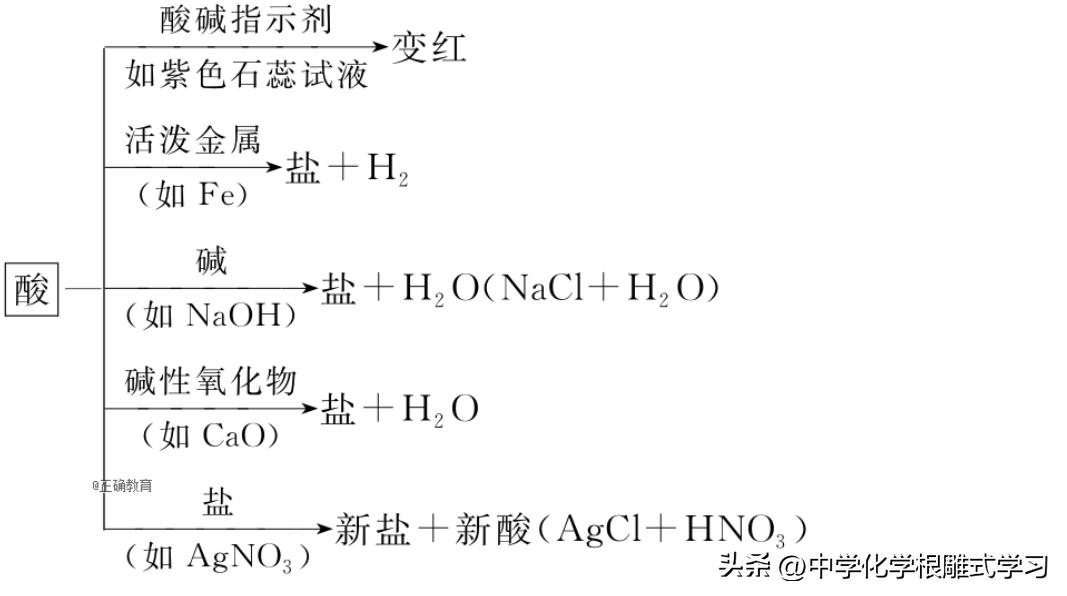
(1)酸可以使紫色石蕊试液变红,遇无色酚酞试液不变色。
(2)酸和活泼金属反应生成盐和水,属于置换反应。
(3)酸和碱性氧化物反应生成盐和水,化合价不变。
(4)酸和碱发生中和反应生成盐和水。
(5)酸和盐反应生成新酸和新盐。
4,碱[以氢氧化钙为例]
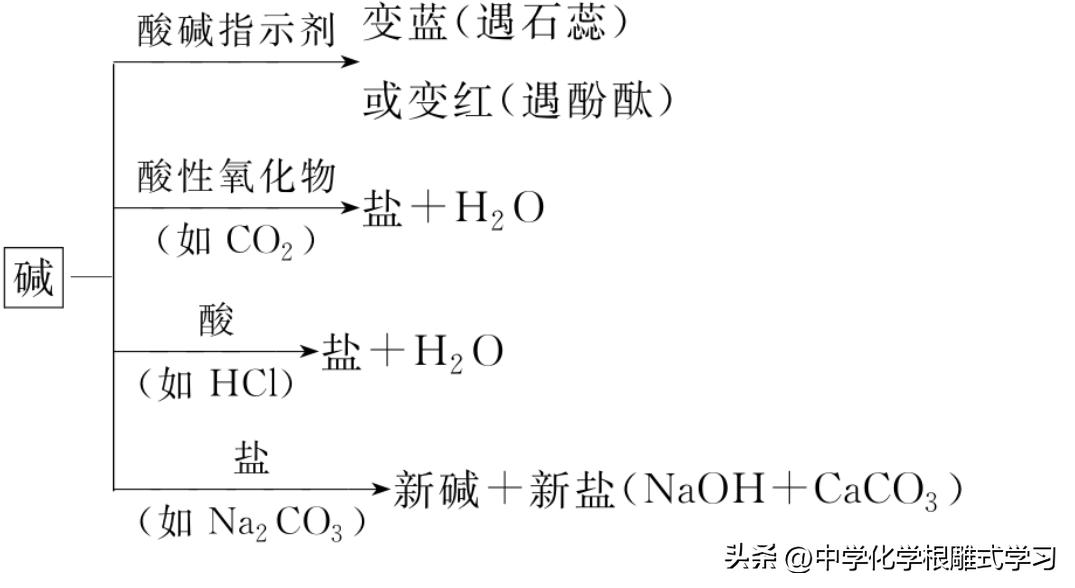
(1)碱可以使紫色石蕊试液变蓝,遇无色酚酞试液变红色。
(2)碱和非金属反应,通常是歧化反应。
(3)碱和酸性氧化物反应生成盐和水,化合价不变。
(4)碱和酸发生中和反应生成盐和水。
(5)碱和盐反应生成新碱和新盐。
5,盐的性质

酸碱盐之间的反应通常是复分解反应,交换成分,化合价保持不变。
1,复分解反应完成的条件:能生成沉淀或气体或水。
2,金属间发生置换反应的条件:金属活动性顺序表中强的置换弱的。
(1)判断金属与酸反应时:金属必须排在氢前面;酸不能用硝酸、浓硫酸等强氧化性酸。
(2)判断金属与盐反应时:必须同时满足“排在前面的金属”和“可溶性盐”两个条件。
内容总结
1.常见的分类方法有交叉分类法和树状分类法。
2.物质可分为纯净物和混合物,纯净物又分为单质和化合物,常见的化合物有氧化物、酸、碱、盐等等。
3.常见的四种基本反应类型为化合反应、分解反应、置换反应和复分解反应。
4.非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物。金属氧化物不一定是碱性氧化物,碱性氧化物一定是金属氧化物等等。



视频加载中...