专注中考教学研究,分享中考理化教学资源,发布最新中考资讯,构建化学学科专业交流平台。



抗击新冠疫情的重要防护用品——口罩
题目
目前,口罩是抗击新冠疫情的重要防护用品已成为国际共识。自疫情爆发以来,我国已向世界各国捐赠和出口口罩一百多亿只,彰显了中国的大国情怀和国际担当。
(1)普通医用口罩由内、中、外三层构成,口罩外层具有防水作用,可阻断部分病毒通过飞沫传播。戴过的口罩内层会变得潮湿,将其晾干的过程中,水发生的物态变化是 ,该过程 热。
(2)口罩中间层——熔喷布始终带有静电,则熔喷布属于 (填“导体”或“绝缘体”)。当不带电的病毒靠近熔喷布外表面时,会被熔喷布 (填“吸附”或“排斥”),使病毒不能通过熔喷布从而阻断病毒的传播。若制作熔喷布的高压设备输出的电压为22kV,该电压为家庭电路电压的 倍。
(3)在熔喷布的生产环节——熔融挤压时,熔喷布受到的压强为5×105Pa,约为 个标准大气压。若某规格的熔喷布密度为0.9×103kg/m3,1m2熔喷布的质量为25g,则该熔喷布的厚度为 m(结果保留1位有效数字)。1吨该规格的熔喷布大约可以制造普通医用口罩(单层熔喷布) (填“15”“40”或“120”)万个。
解析
(1)戴过的口罩内层会变得潮湿,将其晾干的过程中,水由液态变成气态,是汽化现象,汽化吸热;
(2)熔喷布始终带有静电,不易导电,因此是绝缘体;
由于带电体能够吸引不带电的轻小物体,所以当不带电的病毒靠近熔喷布外表面时,会被熔喷布吸附,使病毒不能通过熔喷布从而阻断病毒的传播;
答案
(1)汽化;吸;
(2)绝缘体;吸附;100;
(3)5;3×10﹣5;120。
题目
宏宏发现氢氧化钠溶液忘记盖瓶盖。对于该溶液是否变质,宏宏等同学进行了探究,请你一起完成下列实验报告。
(1)【提出问题1】该溶液是否变质?
【实验探究1】

(2)【提出问题2】该溶液变质程度怎样?
猜想一:已完全变质,该溶液中溶质只含Na2CO3。
猜想二:部分变质,该溶液中溶质含有 。
【查阅资料】氯化钡溶液呈中性。
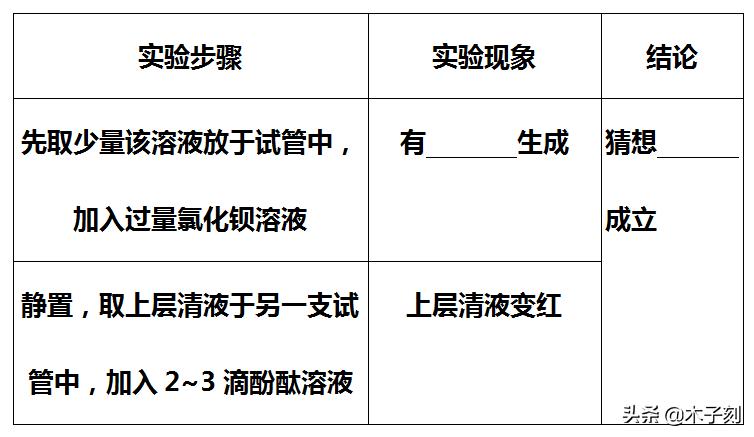
【实验探究2】
(3)【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体。
【实验探究3】为得到纯净的氢氧化钠固体,同学们取该样品并设计了如图实验方案。
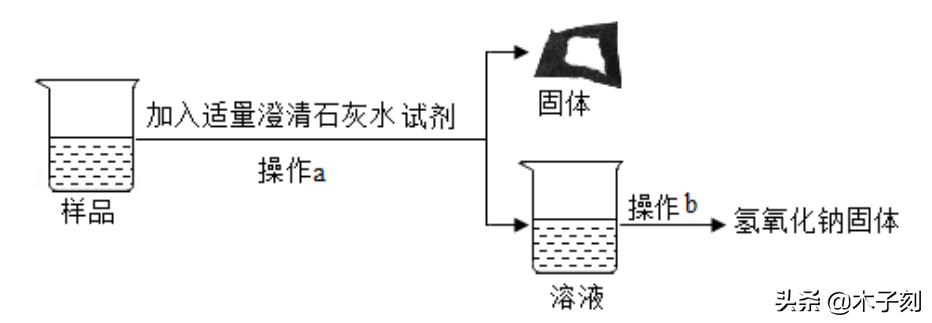
请回答下列问题:
①操作a和操作b中都需用到玻璃棒,其中操作a中玻璃棒的作用为 。
②根据实验流程可知,最终所得氢氧化钠固体质量 (填“大于”“小于”或“等于”)变质后样品中氢氧化钠的质量。
(4)【反思交流】在【实验探究2】中加入过量的氯化钡溶液的目的是 。

解析
(1)【提出问题1】由于氢氧化钠易于空气中二氧化碳反应生成了碳酸钠,碳酸钠能与酸反应生成了二氧化碳气体,所以
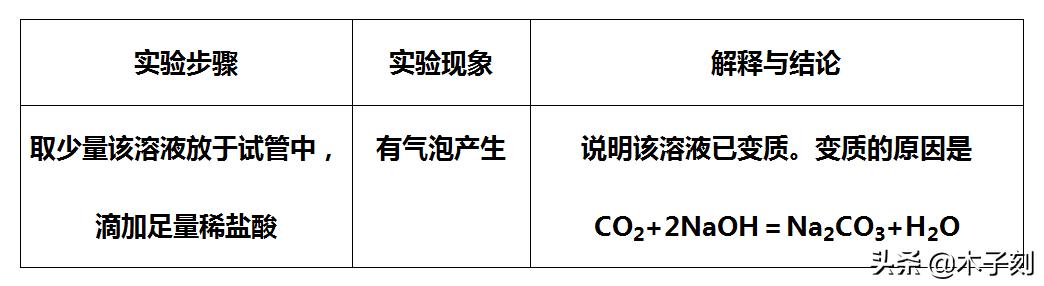
【实验探究1】如下:
(2)【提出问题2】若氢氧化钠全部变质,则溶液中只有碳酸钠,若部分变质,溶液中是碳酸钠和氢氧化钠的混合物,所以猜想二是:该溶液中溶质含有NaOH、Na2CO3;
【实验探究2】要探究溶液中是否含有氢氧化钠,应将碳酸钠除干净,所以实验如下:

【实验探究3】①操作a和操作b中都需用到玻璃棒,其中操作a能将固液分开,操作是过滤,玻璃棒的作用为引流。②根据实验流程和反应的方程式:CO2+2NaOH=Na2CO3+H2O、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH可知,最终所得氢氧化钠固体质量大于变质后样品中氢氧化钠的质量。
(4)【反思交流】在【实验探究2】氧探究是否含有含有氢氧化钠,应将碳酸钠除去,碳酸钠能与氯化钡反应,所以与中加入过量的氯化钡溶液的目的是检验并将碳酸钠完全除去。

参考答案
(1)【提出问题1】气泡
CO2+2NaOH=Na2CO3+H2O
(2)【提出猜想】NaOH、Na2CO3
【实验探究2】白色沉淀 二
(3)【提出问题3】①引流 ②大于
(4)【反思交流】检验并将碳酸钠完全除去。

题目
今年新冠病毒肺炎肆虐全球,医用口罩成为急需品。某化学兴趣小组对制作医用口罩的材料进行了科学探究。
探究一:口罩材料能燃烧吗?是什么样的材料制造的?
【实验1】取样,点燃,产生火焰,冒黑烟,有特殊气味;燃烧过程中熔化滴落的液体能拉成丝,冷却后的灰烬坚硬、不易碾碎。
【结论1】口罩材料能燃烧,其材料是 (选填“天然纤维”或“合成纤维”)。
探究二:口罩材料的组成元素是什么?
【查阅资料】
(1)无水硫酸铜是白色固体,遇水变蓝色。
(2)碱石灰的成分是氢氧化钠和氧化钙的混合物,在本实验中用作吸收空气中的二氧化碳。
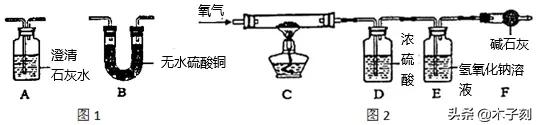
【实验2】将口罩燃烧后的气体通入如图1中的装置,气体通入装置的连接顺序是 (填“AB”或“BA”)。实验时观察到A装置中的现象是 ,B装置中的现象是 。
【结论2】口罩的材料中一定含有碳、氢元素,可能含有氧元素。
【实验3】为了确定材料的组成中是否有氧元素,同学们称取2.1g剪碎的样品放入玻璃管中,通入充足的氧气,加热(实验装置如图2所示)。充分反应后,燃烧产物被完全吸收,D装置增重2.7g,E装置增重6.6g。
【结论3】口罩材料中一定 (填“有”或“没有”)氧元素;口罩材料中碳元素和氢元素的质量比为 。
【反思拓展】
(1)E中发生反应的方程式是 。
(2)实验3的操作中,通入足量的氧气使样品完全燃烧,停止加热后,还要继续通入氧气,其目的是 (填字母)。
a.防止浓硫酸倒吸
b.将燃烧产生的气体排入D、E中完全吸收
c.使样品完全燃烧
(3)若没有F装置,则会导致 元素的测定结果偏大。
解析
探究一:【结论1】口罩材料能燃烧,燃烧过程中熔化滴落的液体能拉成丝,冷却后的灰烬坚硬、不易碾碎,说明其材料是合成纤维。
探究二:【实验2】将口罩燃烧后的气体通入如图1中的装置,气体通入装置的连接顺序是BA,如果顺序颠倒,则不能检验是否生成水;实验时观察到A装置中的现象是澄清石灰水变浑浊,说明反应生成了二氧化碳,B装置中的现象是白色固体变蓝色,说明反应生成了水。

【反思拓展】
(1)E中氢氧化钠和二氧化碳反应生成碳酸钠和水,发生反应的方程式是:2NaOH+CO2═Na2CO3+H2O。
(2)实验3的操作中,通入足量的氧气使样品完全燃烧,停止加热后,还要继续通入氧气,其目的是将燃烧产生的气体排入D、E中完全吸收。
(3)若没有F装置,空气中的二氧化碳会进入E装置,则会导致碳元素的测定结果偏大。

参考答案
合成纤维 BA 澄清石灰水变浑浊
白色固体变蓝色 没有 6﹕1
2NaOH+CO2═Na2CO3+H2O b 碳