慢性病毒感染和癌症中的CD8 T细胞功能耗竭已得到充分描述,但不同的PD-1+CD8+T细胞群体对抗PD-1治疗的反应不同,证明了存在巨大的异质性(Blackburn et al, 2008; Paley et al, 2012)。例如,部分耗竭的PD-1+CTLA-4+ CD8+浸润T细胞与PD-1应答相关(Daud et al, 2016)。与效应T细胞和TEM细胞相比,耗竭的PD-1 + CD8 + T细胞显示出不同的染色质谱图(Pauken et al, 2016; Sen et al, 2016),而这些表观遗传不同的T细胞状态影响耗竭的PD-1 + T细胞是否可以重新编程,以避免最终衰竭和功能障碍(Philip et al, 2017)。
对PD-1/PD-L1阻断后扩增的特定CD8+ T细胞亚群的评估发现了一个独特的CD8+ PD-1+ T细胞亚群,该亚群具有滤泡辅助性T细胞、CD8记忆前体和干细胞的特征(Im et al, 2016),并且类似于CXCR5+ CD8+滤泡T细胞(He et al, 2016; Leong et al, 2016; Utzschneider et al, 2016)。最近使用质谱细胞分析技术对肿瘤浸润T细胞进行了分析,揭示了PD-1和CTLA-4阻断的不同作用机制,表明PD-1阻断重新激活了CD8+ T细胞应答,而CTLA-4阻断导致表达共刺激配体ICOS的Th1-样CD4+细胞扩增(Wei et al, 2017)。
替代性共抑制免疫检查点(如CTLA-4、TIM- 3、LAG-3和VISTA)的表达与PD-1阻断治疗耐药相关(Thommen et al, 2015; Koyama et al, 2016b),使用LAG-3+ PD-1 (Woo et al, 2012)和TIM-3+ PD-1 (Sakuishi et al, 2010)的联合检查点阻断已在临床前模型中证明改善了应答。虽然这些研究提示PD-1+ CD8+T细胞的不同亚群发挥着关键作用,但需要进一步研究来确定如何靶向特定的CD8和CD4 T细胞亚群,以克服原发性和获得性耐药。
不依赖PD-L1的免疫逃逸机制包括替代免疫检查点或共抑制受体、免疫抑制性细胞因子、免疫抑制性代谢物和免疫抑制性细胞(Pitt et al, 2016; O’Donnell et al, 2017; Sharma et al, 2017)。在临床前模型中,影响ICI疗效的免疫抑制细胞类型包括Tregs, MDSCs, Th2 CD4+T细胞和M2-极化的肿瘤相关巨噬细胞(Pitt et al, 2016; O’Donnell et al, 2017; Sharma et al, 2017)。
这些细胞类型主要通过释放细胞因子、趋化因子和其他可溶性介质,单独和共同促进具有免疫抑制性的TME,从而防止抗肿瘤细胞毒性和Th1-导向的T细胞活性(Pitt et al, 2016; Sharma et al, 2017)。实验证明,去除这些免疫抑制细胞类型(例如MDSCs和Tregs)可增强抗肿瘤免疫应答,克服固有耐药性(Highfill et al, 2014; Ngiow et al, 2015)。髓系细胞和癌细胞来源的吲哚胺-2,3-双加氧酶(IDO)将色氨酸分解代谢为具有免疫抑制作用的犬尿氨酸(Platten et al, 2014)。
有趣的是,另一种免疫抑制酶精氨酸酶1 (arginase 1)最近被证明可以配合IDO通路抑制树突状细胞功能(Mondanelli et al, 2017)。最近,肿瘤相关巨噬细胞被证明以FcgR-依赖的方式从PD-1+CD8+ T细胞中去除抗PD-1抗体,从而直接限制PD-1阻断(Arlauckas et al, 2017)。也有新的数据表明,额外的代谢(如葡萄糖消耗、乳酸生成和胆固醇代谢)和炎症途径(如环氧化酶-2/前列腺素E2)可以同时影响肿瘤细胞和免疫细胞(Pitt et al, 2016)。
T细胞记忆形成受损
最令人信服的ICI成功的临床证据与长期、持久临床获益的潜力相关。因此,虽然ICI可能暂时重新激活CTLs以加强肿瘤控制,但如果TEM细胞的形成受损,那么临床应答可能会减弱,导致获得性耐药或停止治疗后疾病复发。肿瘤内TEM对PD-1阻断反应的扩增已经被证实,并且在对治疗有反应的患者中更明显(Ribas et al, 2016b),提示TEM细胞在抗PD-1作用和临床应答中发挥关键作用(O’Donnell et al, 2017)。PD-1阻断后TEM扩增的细胞和分子机制尚不完全清楚,然而,最近的研究已经确定了与初始、急性效应细胞、记忆和耗竭T细胞状态相关的不同转录程序(Pauken et al, 2016; Sen et al, 2016)。
越来越多的证据表明,T细胞衰竭与表观遗传变化有关,这些变化促进了不同于效应或记忆CD8 T细胞的转录图谱(Sen et al, 2016)。重要的是,这些表观遗传变化似乎限制了PD-1阻断后CD8 T细胞功能的持久性(Pauken et al, 2016)。如果肿瘤抗原持续存在(如肿瘤负荷较高的患者),记忆T细胞应答的重新获得可能会受到限制(Huang et al, 2017),这表明未来可能需要增强现有的新T细胞应答或初始新T细胞群,以产生持久的抗肿瘤T细胞记忆。
总结和未来方向
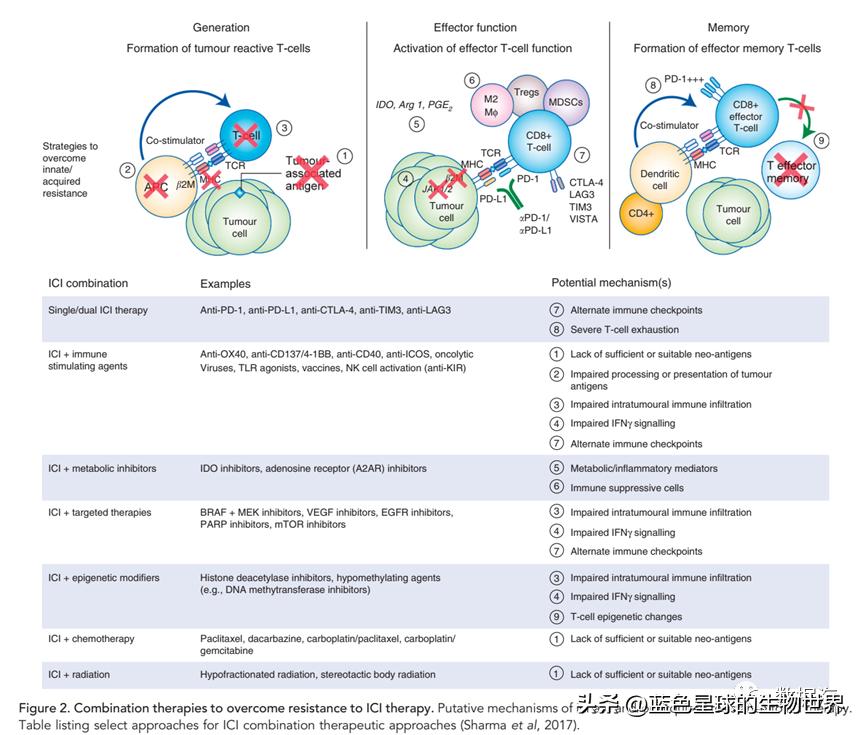
将免疫治疗药物与靶向药物、细胞毒性化疗和/或放疗联合应用的几项临床试验正在进行中,所有试验的目的都是让更多患者获得长期的疾病控制(Buque et al, 2015) (图2)。通过靶向TME内假定的免疫逃逸机制来克服先天耐药的联合治疗正处于不同的开发阶段(Spranger and Gajewski, 2013; Smyth et al, 2016)。癌症疫苗(Ott et al, 2017; Sahin et al, 2017)显示出作为个体化癌症免疫治疗手段和潜在增强免疫记忆的前景。目前正在开展更多研究工作,以确定与ICI耐药和应答相关的生物标志物,同时对新型免疫调节剂以及免疫调节剂和ICI与其它癌症疗法的新型联合应用进行早期临床试验(Mahoney et al, 2015)。
迄今为止,精准医学基本上等同于利用肿瘤的分子和大部分基因组特征来给予特异性靶向小分子和生物制剂;然而,新型和功能性的精准医疗平台可能为个性化患者或患者群体提供更多的选择(Friedman et al, 2015)。随着对免疫检查点*制剂抑**的反应和耐药机制的进一步阐明,分子和功能技术可以并且应该整合起来开发新的精准免疫肿瘤平台。此外,开发用于评估ICI治疗应答和耐药性的功能检测方法以及新型组合可能需要生物工程专业知识来适当模拟肿瘤自身免疫微环境(Hirt et al, 2014)。短期内,复合生物标志物(例如CD8 T-cell abundance tumoural/stromal PD- L1 staining)可能会取代单一生物标志物(例如PD- L1 staining),而下一代分子和/或功能诊断方法正在开发中。最终,我们预期这些精准治疗方法将用于确定特定疗法或治疗组合,以优化个体患者的临床疗效和临床应答的持久性。