摘要
本方案介绍了如何使用pull-down实验分析蛋白之间可能存在相互作用的一个例子(Sauer et al., 2013)。将感兴趣的诱饵蛋白(在本例中是拟南芥的MTV1)融合GST标签并在细菌中表达。接着通过GST标签与谷胱甘肽结合的琼脂糖珠基质结合,将诱饵蛋白分离出来。清洗去除细菌裂解液中提取的非特异性结合蛋白。将天然的植物蛋白提取液通过基质,诱饵GST-MTV1和猎物蛋白之间就会发生结合。再次清洗去除非特异性结合的蛋白质。最后,将诱饵和猎物蛋白质从珠子中释放出来。使用免疫印迹分析识别与GST-MTV1结合的蛋白质。此外,需要同时分析单独由GST标签组成的阴性对照,以排除猎物蛋白与GST-MTV1诱饵结合是由GST标签引起的可能性。
关键词 :pull-down、相互作用、网格蛋白、 MTV1(mtv1)、EPSIN(epsin)
材料与试剂
1. 含表达重组GST-MTV1融合蛋白(诱饵)质粒的BL21大肠杆菌
注:本例中,将MTV1编码序列克隆到一个修饰过的pGEX-2T质粒( General Electric Company ,目录号:28-9546-53)上,载体构建采用Gateway的方法。
2. 仅表达GST标签的BL21大肠杆菌作为阴性对照
3. MS培养基混合维生素和MES缓冲液(Duchefa Biochemie BV,目录号:M0255.0010)
4. 谷胱甘肽琼脂糖(Sigma-Aldrich,目录号:G4510)
5. 完全*制剂抑**(不含EDTA)(Roche Diagnostics,目录号:11 873 580 001)
6. 苯甲基磺酰氟(PMSF)(如Sigma-Aldrich,目录号:P7626)
7. Triton X-100(Sigma-Aldrich,目录号:T8787)
8. 羧苄青霉素(Sigma-Aldrich,目录号:C9231)
9. 异丙基β-D-1-硫代半乳糖苷(IPTG)(Sigma-Aldrich,目录号:I6758)
注:应配制成1M的原液,在-20℃下保存。
10. 十二烷基硫酸钠(SDS)(Sigma-Aldrich,目录号:L3771,或任何其他供应商)
注:可制备20%(重量/体积)的水溶液,并在121℃下高压灭菌15min。
11. 甘油(Sigma-Aldrich,目录号:G5516,或任何其他供应商)
12. Tris(羟甲基)氨基甲烷(Tris)(Sigma-Aldrich,目录号:252859,或任何其他供应商)
13. 酵母膏(Sigma-Aldrich,目录号:Y1625,或任何其他供应商)
14. 色氨酸(Sigma-Aldrich,目录号:95039,或任何其他供应商)
15. Anti-GST多克隆抗体(选配)(Carl Roth,目录号:3998)
16. Anti-CHC单克隆抗体(可选)(BD Biosciences,目录号:610499)
17. 液氮
18. NaCl(任何供应商)
19. KCl(任何供应商)
20. Na2HPO4(任何供应商)
21. KH2PO4(任何供应商)
22. β-硫基乙醇
23. 液体培养6-8天的拟南芥幼苗
24. MS培养基(见配方)
25. PBS(见配方)
26. 洗涤液(见配方)
27. 提取缓冲液(见配方)
28. 上样缓冲液(见配方)
29. LB培养基(见配方)
设备
1. 1.5和2mL标准反应管的微离心机(任何制造商)
注:无论是冷藏或位于4℃的冷室,应能达到16000 ×g。
2. 用于50mL离心管的冷冻离心机(任何制造商)
注:应能达到4℃和3000 ×g。
3. 超声发生装置(微型音调类型)
注:我们使用B. Braun的labsonic已经不再生产了。但是任何适合于小体积(2-5mL)的尖端式超声器设备都可以用于实验,例如与MS3超声管耦合的UP100H设备(Hielscher超声技术)。
4. Poly-Prep色谱柱(Bio-Rad Laboratories,目录号:731-1550)
5. 锥形烧瓶
6. 纸巾
7. 1.5mL小型离心机,能够支持16000 ×g (任何供应商)
8. 50mL聚丙烯锥型离心管(任何供应商)
9. 0.20µm滤膜(如Minisart®, Sartorious,目录号:17597)加上兼容的5mL注射器
10. 37℃震荡培养箱培养细菌(任何供应商)
11. 25℃摇床或室温下的摇床(任何供应商)
12. 立式圆筒形混合机(任何供应商)
13. 能够在600nm处测量光密度的分光光度计(任何供应商)
14. 研钵和研棒(直径约10cm)(任何供应商)
步骤
1. 提前规划
表达GST-MTV1和GST蛋白的细菌培养沉淀物可在-80℃下保存数周,因此可提前制备。植物提取物在实际pull-down实验当天优先制备。得到这些植物材料需要8-10天(从种子消毒到收获)。Pull-down实验可以在一天内完成。
2. 细菌中的蛋白质表达
(1)将GST-MTV1(诱饵)和GST(阴性对照)表达菌的单个菌落(或保存的甘油菌种),在10mL LB中过夜培养,并选择适当的抗生素(在本例中,抗生素为100μg/mL羧苄青霉素)。使用50mL离心管,在37℃震荡培养箱中培养,转速至少为200rpm。离心管道不应完全封闭,以允许气体交换。
(2)次日,准备两个锥型烧瓶(体积500mL),每个烧瓶中加入150mL LB+100μg/mL羧苄青霉素,接着,分别加入MTV1-GST和GST预培养物。在25℃的摇床中培养、转速至少200rpm,直到OD600值达到0.6。细菌在25℃下生长有助于产生可溶性的蛋白质。
(3)为了诱导GST-MTV1和GST的表达,添加IPTG至最终浓度为1mM,在25℃下继续培养3-4h。
(4)将每种培养物放入3个50mL的离心管中,在4℃、3000 ×g 的条件下离心5min。
(5)弃掉上清液,用冷的PBS重悬沉淀物,然后如上所示再次离心。
(6)弃掉上清液,将沉淀物储存在-80℃。沉淀物可以储存几个星期。在一个pull-down实验中,只使用其中一个沉淀物(对应于50mL的细菌培养)。
3. 从细菌中提取蛋白质
(1)取GST-MTV1和GST沉淀物(对应50mL细菌培养物),分别在2.5mL冷的提取缓冲液中重悬。
(2)使用超声破壁仪破坏细菌细胞,直到它们被溶解,呈现为不透明度降低和黏度增加。该操作必须在冰上进行,并且建议每隔一段时间进行超声一次(例如超声10s,然后在冰上放置10s,以此类推)。必须注意不要使用高强度的声波。如果检测到起泡或形成白色沉淀,则需要降低超声强度。
(3)将溶解的菌液转移到1.5mL离心管中,在4℃,16000 ×g 的条件下离心20min。
4. 重组谷胱甘肽琼脂糖珠
(1)重组谷胱甘肽琼脂糖珠。对于每个GST-MTV1和GST,称10mg干珠,并加入2mL洗涤缓冲液。让珠子膨胀10min,同时偶尔旋转。
(2)将浆液装入两个Poly-Prep柱上,将它们垂直放置在适当的支架上,让缓冲液通过底部开口通过重力排出。不要使用离心机或真空来增加流量。这适用于后续所有洗涤步骤。
(3)然后用10mL洗涤缓冲液清洗柱子,并通过重力排出。
5. 蛋白与谷胱甘肽珠结合
在离心的细菌裂解液中,取150μL上清液,与75μL样品装载缓冲液混合,煮沸5min,-20℃保存,作为对照。检查细菌裂解后的蛋白质表达和完整性,例如使用抗GST抗体进行免疫印迹分析。其余的上清装入色谱柱,一个用于GST-MTV1,一个用于GST。如果裂解液粘度过高,可以加入1-2mL提取缓冲液。关闭柱子里面和外面的出口,并将其放置在4°C的旋转轮上2h。将裂解液通过重力沥干,用10mL洗涤缓冲液在4℃下洗涤3次。
6. 植物提取物
(1)用纸巾将水培培养的拟南芥幼苗吸干。称取0.7g,然后转移到研钵中。
(2)加入液氮冷冻,然后用研棒磨成细粉。
(3)加入4mL提取缓冲液,慢慢解冻,然后进一步研磨。
(4)将样品转移到1.5mL的离心管中,在16000 ×g ,4℃条件下离心20min。
(5)将上清液通过0.20μm的过滤注射器进行过滤,将提取液冷藏。每个柱子需要1mL提取液。
7. Pull-down
(1)关闭柱子的出口。
(2)对于每根柱子,将1mL提取液与1mL提取缓冲液混合,并加入到洗涤柱中。
(3)关闭柱子的入口,并将其置于4℃的旋转轮上1.5h。
(4)然后打开柱子里面和外面的出口,并收集流出的混合液。
(5)将每个色谱柱中的流动液150μL与75μL的上样缓冲液混合,煮沸5min,保持在-20°C。这些样本是流动的,包含所有未结合的植物蛋白(通常还有一些细菌蛋白)。
(6)用10mL洗涤缓冲液在4℃条件下洗涤3次,通过重力沥干。
(7)珠子的体积现在约为100µL。关闭柱子的出口,在200µL洗涤缓冲液中重新悬浮珠子。
(8)取150μL的珠浆,加入75μL的样品上样缓冲液。将样品煮沸5min,用力混合,16000 ×g 离心5min。
(9)将上清液放入新管中,放在-20℃下保存。这些样品分别含有与GST-MTV1或GST结合的蛋白质以及诱饵蛋白本身的洗脱物。
(10)一般情况下,流动样品和洗脱液样品相邻装载在GST和GST-MTV1的免疫印迹上(见图1)。通常建议纠正流动和洗脱液中不同的蛋白含量,一个好的起始量是加载5µL流动液和20µL洗脱液,但这必须通过经验来确定。
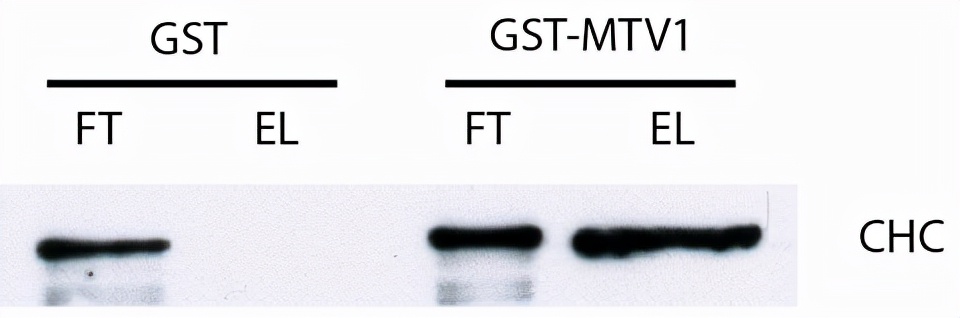
图1 免疫印迹显示抗网格蛋白重链(CHC)抗体的典型结果(约190kDA)。在GST和GST-MTV1的流动液(FT)中均检测到该蛋白,表明CHC在孵育过程中以相同的水平存在。洗涤后,只有GST-MTV1的洗脱液(EL)产生信号,表明CHC与MTV1特异性结合。在本印迹中,装载5µL FT样品和20µL EL样品以补偿不同的蛋白水平。
(11)在两种流动样品中都能检测到与GST-MTV1特异性结合的蛋白,但只在GST-MTV1洗脱样品中检测到。以网格蛋白重链(CHC)为例,可以使用一种商业抗CHC抗体检测(见图1)。
(12)在两种洗脱液样品中检测到的蛋白质与GST标签或谷胱甘肽-琼脂糖基质非特异性结合。这种情况会增加洗涤步骤的时间和数量,因此可以从步骤6开始使用不同的盐或洗涤液进行洗涤。
注:(1)该实验方法理论上可以用于任何一种可以融合到GST标签上的蛋白质。不过,可能需要针对每个特定情况进行优化。MTV1是一种易在大肠杆菌中表达的可溶性蛋白,不需要真核生物翻译后修饰,如糖基化。其他的蛋白质可能需要不同的表达和缓冲体系。
(2)PMSF是剧毒的,在水溶液中非常不稳定,所以制备时必须小心。常见的做法是在甲醇中制备200mM原液,在-20°C下可以储存至少半年。
(3)价格昂贵的羧苄青霉素可以用相同浓度的氨苄青霉素代替。但氨苄青霉素的稳定性较差,故首选羧苄青霉素。
(4)完全*制剂抑**以片状的形式出现,每片可以用于最终体积为50mL的缓冲液。如果需要更小的体积,片剂可以溶解在1mL水中,产生50×的原液,剩余原液可以在-20°C下保存几周,而不会急剧地失去活性。
配方
1. 水培培养的拟南芥幼苗
(1)200-300个拟南芥种子(我们使用Col-0系,也可以是任何株系、突变体或转基因株系)。在1.5mL离心管中用70%乙醇浸泡15min,偶尔涡旋。
(2)在超净工作台中,用1mL无菌水清洗种子5次。最后一次清洗后,将种子放在水中,盖紧离心管,在黑暗4°C 条件下放置2-3天进行分层。
(3)将分层后的种子放入装有100mL MS培养基的250mL锥型烧瓶中,在植物生长室中轻轻搅拌(如50rpm的摇床)。采用16h光照/8h黑暗,在24℃的生长条件下,生长6-8天。
2. MS培养基(1L)
2.45g MS培养基与维生素和MES缓冲液混合
10g蔗糖
添加无菌水至1L
用KOH将pH调至5.8
3. PBS(1L)
8g NaCl
0.2g KCl
1.44g Na2HPO4
0.24g KH2PO4
溶于800mL无菌水
用HCl将pH调至7.4
最后定容至1L
4. 清洗缓冲液
PBS
0.5% Triton X-100
0.5mM PMSF(由200mM PMSF甲醇原液制成)
5. 提取缓冲液
类似于清洗缓冲液,但添加了1×的完全*制剂抑**
6. 上样缓冲液(50mL)
15ml 20% SDS水溶液
15mL甘油
15mL 0.5M Tris溶液(pH=6.8)
1.25mL无菌水
少量溴酚蓝,刚好足以提供中等蓝色的颜色。
使用前,每925μL缓冲液中加入75μL β-巯基乙醇。
7. LB培养基(1L)
10g胰蛋白胨
5g酵母粉
10g NaCl
加入1L的无菌水
在121℃下高压灭菌15min
References:
Sauer, M., Delgadillo, M. O., Zouhar, J., Reynolds, G. D., Pennington, J. G., Jiang, L., Liljegren, S. J., Stierhof, Y. D., De Jaeger, G., Otegui, M. S., Bednarek, S. Y. and Rojo, E. (2013). MTV1 and MTV4 encode plant-specific ENTH and ARF GAP proteins that mediate clathrin-dependent trafficking of vacuolar cargo from the trans-Golgi network. Plant Cell 25(6): 2217-2235.
好文推荐
Co-IP与信号通路研究
转录因子研究套路(一)
基因功能研究的那些套路你知道多少?(下)
磷酸化/去磷酸化对蛋白功能的研究竟有这么大?
伯远生物可以提供以下技术服务
GST pull-down